- Ряд напряжений и химические свойства металлов
- Самая удобная и увлекательная подготовка к ЕГЭ
- Общая характеристика металлов главных подгрупп I±III групп в связи с их положением в Периодической системе химических элементов Д. И. Менделеева и особенностями строения их атомов
- Химические элементы — металлы
- Характеристика переходных элементов ± меди, цинка, хрома, железа по их положению в Периодической системе химических элементов Д. И. Менделеева и особенностям строения их атомов
- Общая характеристика неметаллов главных подгрупп IV±VII групп в связи с их положением в Периодической системе химических элементов Д. И. Менделеева и особенностями строения их атомов
- Химические элементы – неметаллы
- Свойства атомов элементов – неметаллов
- Задание №2 ЕГЭ по химии



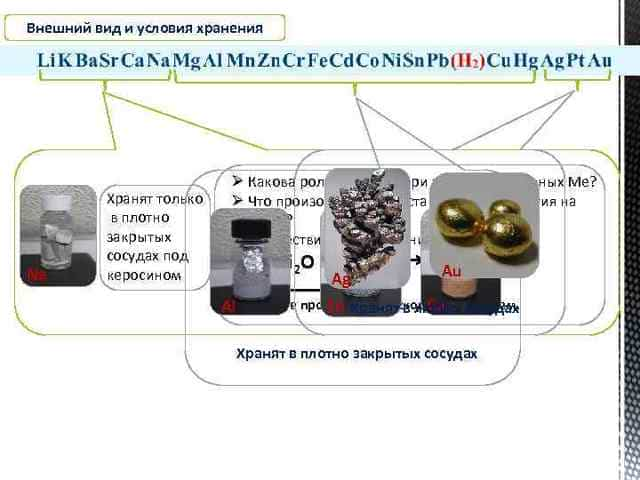

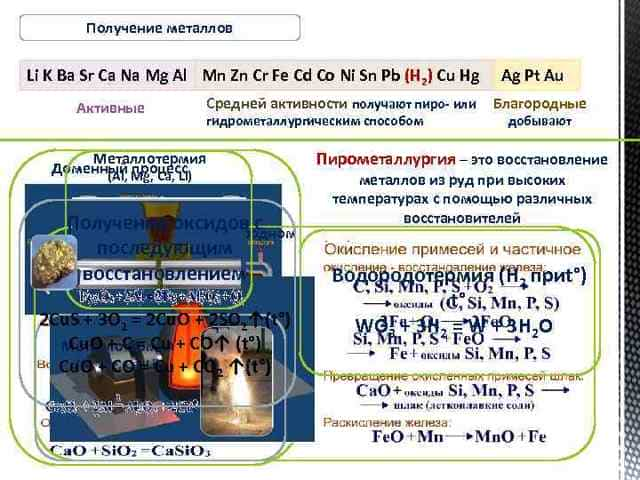
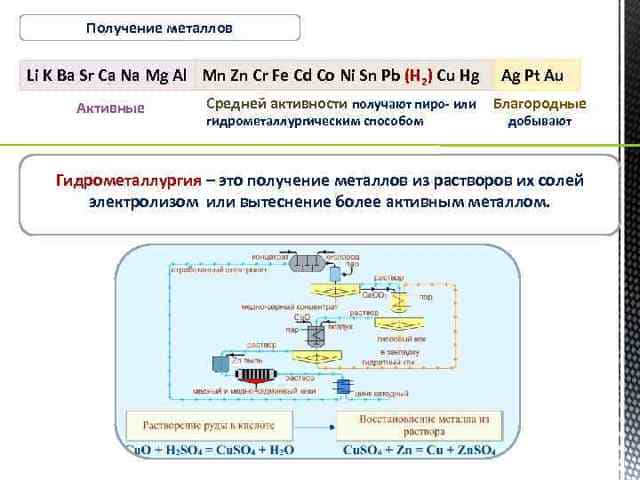
Химические свойства металлов Окисляются при комнатной температуре При обычных условиях взаимодействуют с водой с образованием щелочи и Н 2 ↑ При комн. t°окисл. только с поверх. Окисляются только при нагревании С водой взаимодействуют только при нагревании с образованием оксида и Н 2↑ Помни! 2 Al + 6 HOH → 2 Al(OH)3 + 3 H 2↑ (если снять оксидную пленку) При t° не окисл яются С водой не взаимодействуют Коррозионная устойчивость чистых металлов усиливается Из растворов кислот вытесняют водород (исключение HNO 3) Помни! Щелочные и щелочноземельные металлы в водных растворах взаимодействуют прежде всего с Н 2 О Из растворов кислот не вытесняют водород Взаимодействуют с серной кислотой (конц. ). В зависимости от условий и восстановительных свойств Ме образуются SO 2, S, H 2 S (Fe, Ni и некоторые металлы в H 2 SO 4 (конц. ) на холоду пассивируются). Не взаим одейст вуют
Химические свойства металлов Главная Взаимодействуют с разбавленной и концентрированной азотной кислотой и в зависимости от условий, восстановительных свойств металлов, концентрации кислоты образуются N 2, N 2 O, N 2 O 3, NO 2 u NH 3 (NH 4 NO 3).
Al, Fe, Cr в концентрированной азотной кислоте пассивируются.
С HNO 3 не реагиру ют С разбавленной H 2 SO 4 взаимодействуют с образованием Н 2 С раствором H 2 SO 4 не реагируют С HCl взаимодействуют с образованием Н 2 C HCl не реагируют Каждый впереди стоящий металл вытесняет все последующие металлы из растворов и расплавов их солей При электролизе сначала изменяется тот катион, металл которого находится правее в электрохимическом ряду напряжений металлов Примечание: среди закономерностей, связывающих ряд напряжений металлов и химические свойства Ме и их соединений, есть исключения из правил. Будьте внимательны, обратитесь к теории!
Соединения металлов Растворяются в Н 2 О с образованием щелочей Оксиды не растворяются в воде Оксиды При нагревании оксиды не разлагаются При t°разлагаются Гидроксиды разлагаются в воде Гидроксиды растворяются в воде Гидроксиды при t° не разлагаются Нитраты при t° разлагаются на нитриты и О 2 Cоли, образованные сильными кислотами не гидролизуются Cоли, образованные слабыми кислотами гидролизуются (среда щелочная). Гидроксиды не растворяются в воде Гидроксиды при t° разлагаются на воду и оксиды Соли Нитраты при t° разлагаются на оксид, NO 2 и О 2 При t° разлагаются на Ме, Н 2 О и О 2 Нитраты при t° разлагаются на Ме, NO 2 и О 2 Гидролиз солей Cоли, образованные сильными кислотами, гидролизуются с образованием кислой среды Существующие и растворимые соли, образованные слабыми кислотами, гидролизуются полностью
Электрохимический ряд напряжений металлов Проверь себя Ba + H 2 O → t° Fe + H 2 O → + Al + H 2 SO 4(р)→ Zn + Cu. SO 4 (р)→ + + Ba. O Ba(OH)2 H 2 + Ba. H 2 Fe(OH)2 Fe 2 O 3 Fe 3 O 4 H 2 S Zn. S Al 2(SO 4)3 Cu Al 2 S 3 Cu. O H 2 Zn. SO 4 t° Fe + O 2 → Na + O 2→ Fe 2 O 3 Fe 3 O 4 Fe. O Na. O 2 Na 2 O 2 Тренажер «Химические свойства металлов»
Проверь себя Тренажер «Химические свойства металлов» Укажите, какие из предложенных веществ реагируют с кальцием и напишите уравнения соответствующих реакций. Na. OH S Br 2 O 2 Na 2 O Са H 2 O K 2 SO 4 Zn N 2 Проверка Са +3 Са. О 2 = 22 Са. О 3 N 22 + Н 2 2 Са 2 Н 2 О Н Ca. S 2 Ca+++ Br 2 Са(ОН) Са + N = Ca. Н Са S = Ca. Br Ca
Электрохимический ряд напряжений металлов Проверь себя Теоретические тесты с выбором ответа 1. Коэффициент перед формулой восстановителя в реакции, схема которой Ca + HNO 3 (конц. ) → Ca(NO 3)2 + N 2↑+ H 2 O а) 5; б) 10; в) 1; г) 12; 2.
Коэффициент перед формулой окислителя в реакции, схема которой Zn + H 2 SO 4 (конц. ) → Zn. SO 4 + H 2 S↑ + H 2 O а) 1; б) 2; в) 4; г) 5; 3. В схеме превращений (1) (2) (3) (4) Al → Al(OH)3 → Al 2 O 3 → Al.
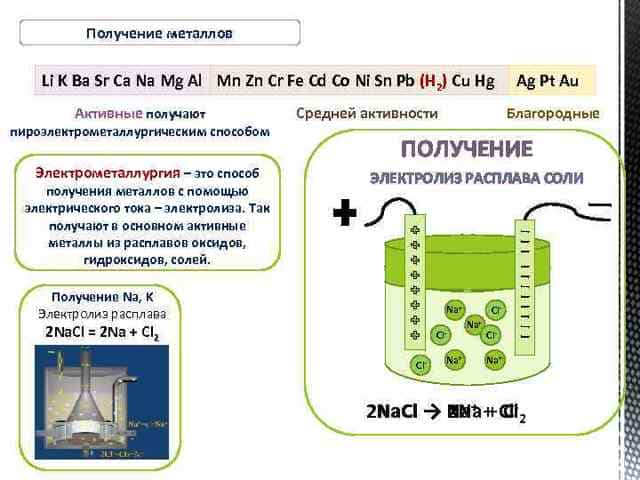
Cl 3 → Al требуется провести электролиз расплава для осуществления реакции на этапе: а) 4; б) 2; в) 3; г) 4; г) 1; 4. В схеме превращений из теста 3 требуется провести прокаливание для осуществления реакции на этапе: а) 1; б) 2; в) 3; г) 4; б) 2; 5.
При электролизе раствора Na. Cl образуются продукты а) Na; б) Na. OH; в) Cl 22; ; г) H 22; ; д) HCl; б) Na. OH; в) Cl г) H Проверка
С какими из веществ будут реагировать предложенные металлы при нормальных условиях? Na Na. Cl (р-р) ошибка Li 2 O молодец H 2 O K 2 SO 4(р-р) ошибка молодец O 2 ошибка SO 2 ошибка Na 2 SO 4 Fe.
SO 4 (р-р) молодец ошибка SO 3 H 2 SO 4 (р-р) молодец ошибка Ca Na. OH (р-р) ошибка Zn молодец Fe. Cl 2 (р-р) молодец HCl Al 2(SO 3)3 ошибка Al 2 S 3 ошибка H 2 O ошибка SO 2 Cu H 2 SO 4 (конц) молодец ошибка HCl ошибка Ca.
O ошибка O 2 ошибка P 2 O 5 Ag. NO 3 (р-р) молодец Mg
ВОПРОСЫ: К можно получить электролизом Более сильным восстановителем, чем К будет Более сильным окислителем будет ион Щелочную среду при гидролизе образует раствор соли Роль Al в алюминотермии ОТВЕТЫ: раствора KCl раствора КNO 3 расплава KCl р-ва смеси КCl u Mg. Cl 2 Li Sr Na Ca Cu 2+ Li 1+ Mg 2+ Au 3+ Na. Cl Al 2(SO 4)3 K 2 CO 3 Al 2 S 3 катализатор восстановитель окислитель не знаю Шаблон теста взят из презентации Гальцевой О. Н. (п. Анна, Воронежской обл. )
Ряд напряжений и химические свойства металлов
Изучая курс общей и неорганической химии мы с вами упустили очень важную тему, на который постоянно ссылаемся при изучении свойств простых веществ и их соединений, но ни разу не пояснили что это такое и почему именно так, а не иначе.
Речь сегодня пойдет про ряд напряжений и химические свойства металлов. Понять, что в заданиях ЕГЭ по химии нет прямого вопроса по этой теме, но без знания и понимая электрохимического ряда вы не сможете ответить на многие вопросы правильно.
Давайте разбираться вместе
Вы наверняка знаете, что атомы типичных металлов могут отдавать электроны (не принимать, а только отдавать, они – доноры). Поэтому металлы в виде простых веществ в химических реакциях играют роль восстановителей. В случае действия сильных окислителей и при соблюдении определенных условий (к примеру нагревании) практически любой металл может быть окислен до положительной степени окисления.
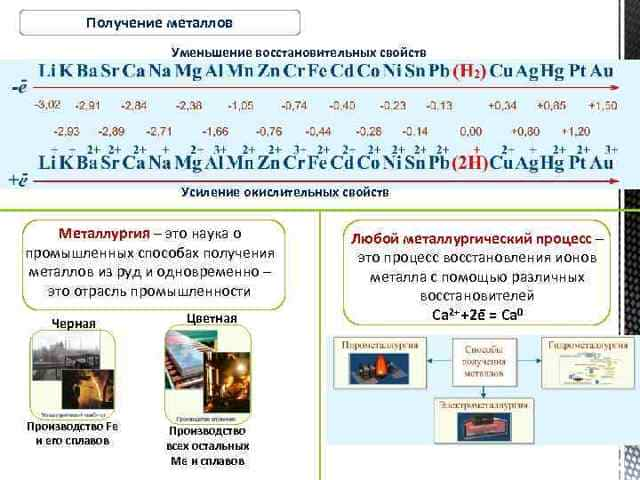
Различная восстановительная способность металлов дает возможность разместить их в так называемый ряд напряжений и как его еще называют электрохимический ряд металлов.
В этом ряду металлы располагаются в порядке уменьшения их восстановительных свойств и возрастания окислительных свойств соответствующих гидратированных катионов (посмотрите внимательно на таблицу, которые есть в любом справочнике)
Таким образом, мы видим, что в ряду напряжений слева располагаются металлы, которые вступая в реакцию с водными растворами будут проявлять сильные восстановительные свойства. Напротив, ионы, которые образуются при окислении этих металлов, будут проявлять слабые окислительные свойства. Поэтому такие металлы легко окисляются, а отвечающие им ионы трудно восстанавливаются.
Расположение металла в ряду напряжений определяет процесс окисления металла с образованием гидратированного иона, соответствующего низшей устойчивой в водном растворе степени окисления данного металла.
Данный металл может восстанавливать из растворов их соей металлы, которые расположены справа от него в ряду напряжений. Иными словами, металл левее вытесняет из солей металл, который находится правее него.
Металлы, расположенные в электрохимическом ряду правее водорода, не могут замещать его в молекулах кислот. Эти металлы хоть и реагируют с кислотами, которые обладают сильными окислительными свойствами, но в ходе реакции выделения водорода не будет (вспоминайте предыдущую нашу статью, какие продукты реакции будут в этом случае?).
Металлы, которые у нас расположены в ряду напряжений слева от водорода, могут вступать в реакции замещения с кислотами, вытесняя из последних водород. При этом помним, что ЭДС на основании которого и устанавливается расположение металла и водорода в ряду, измеряется в строго определенных условиях.

От чего же зависит положение металла в ряд?
- От энергии ионизации атома металла.
- От энергии гидратации, получаемого иона.
- От заряда иона.
- От размеров иона.
Рассмотрим теперь кто у нас в ряду напряжений из щелочных металлов стоит первым? Правильно, литий, но почему не цезий? Ведь, по логике он электрон отдает намного быстрее, чем литий.
Но мы с вами вспоминаем правило выше, которое вы должны запомнить очень хорошо: ряд напряжений отражает процесс окисления металла с образованием гидратированного иона.
Чем лучше и быстрее протекает процесс окисления, тем левее будет находится металл в электрохимическом ряду.
Вернемся к нашему коварному литию. В его случае имеет значение высокая энергия гидратации иона.
Маленький размер приводит к притягиванию отрицательных концов полярных молекул воды гораздо сильнее, нежели у более «громоздкого» цезия, так как расстояние между центрами отрицательного и положительного зарядов в случае лития будет меньше. В итоге общий процесс (отдача электронов с последующей гидратацией полученного иона) энергетически более выгоден у лития чем у цезия.
Окисление металлов водой и раствором щелочей
Вытеснять водород из воды в состоянии только те металлы, которые стоят в ряду напряжений перед кадмием, но тут есть нюансы: ввиду ограничений кинетических порядков (образование нерастворимой в воде оксидной пленки тех же амфотерных металлов) при комнатной температуре в реакцию с водой вступают только щелочные и щелочноземельные металлы.
А вот металлы, располагающиеся правее в ряду, могут восстанавливать водород до воды при нагревании. К примеру магний, измельченный в порошок, реагирует с горячей водой, а алюминий, тоже в виде порошка реагирует с кипящей водой.
А такие металлы как цинк и алюминий могут восстанавливать водород даже из раствора щелочи:
2Al+2NaOH+ 6H2O=2Na[Al(OH)4]+3H2
По какому же принципу тот или иной металл растворяется в щелочи? Как это можно определить?
- Металл должен быть сильным восстановителем и окисляться ионами водорода даже в малых концентрациях последних, находящихся в растворе щелочей.
- Ион металла в степени окисления до которой он окисляется ионами водорода, образует в щелочном растворе растворимое соединение.
Мы должны всегда помнить, что восстановительные свойства металлов в одной и безводной среде могут отличаться. А значит и порядок расположения металлов исходя из их восстановительной способности отличается. К примеру, в безводной среде сильным восстановителем будет цезий, а в водной среде – литий.
Самая удобная и увлекательная подготовка к ЕГЭ
- Перечислим закономерности изменения свойств, проявляемые в пределах периодов:
- — металлические свойства уменьшаются;
- — неметаллические свойства усиливаются;
- — степень окисления элементов в высших оксидах возрастает от $+1$ до $+7$ ($+8$ для $Os$ и $Ru$);
- — степень окисления элементов в летучих водородных соединениях возрастает от $–4$ до $–1$;
- — оксиды от основных через амфотерные сменяются кислотными оксидами;
- — гидроксиды от щелочей через амфотерные сменяются кислотами.
Д. И. Менделеев в $1869$ г. сделал вывод — сформулировал Периодический закон, который звучит так:
Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от относительных атомных масс элементов.
Систематизируя химические элементы на основе их относительных атомных масс, Менделеев уделял большое внимание также свойствам элементов и образуемых ими веществ, распределяя элементы со сходными свойствами в вертикальные столбцы — группы.
Иногда, в нарушение выявленной им закономерности, Менделеев ставил более тяжелые элементы с меньшими значениями относительных атомных масс.
Например, он записал в свою таблицу кобальт перед никелем, теллур перед йодом, а когда были открыты инертные (благородные) газы, — аргон перед калием.
Такой порядок расположения Менделеев считал необходимым потому, что иначе эти элементы попали бы в группы несходных с ними по свойствам элементов, в частности щелочной металл калий попал бы в группу инертных газов, а инертный газ аргон — в группу щелочных металлов.
Д. И. Менделеев не мог объяснить эти исключения из общего правила, не мог объяснить и причину причину периодичности свойств элементов и образованных ими веществ. Однако он предвидел, что эта причина кроется в сложном строении атома, внутреннее строение которого в то время не было изучено.
В соответствии с современными представлениями о строении атома, основой классификации химических элементов являются заряды их атомных ядер, и современная формулировка периодического закона такова:
Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от зарядов их атомных ядер.
Периодичность в изменении свойств элементов объясняется периодической повторяемостью в строении внешних энергетических уровней их атомов.
Именно число энергетических уровней, общее число расположенных на них электронов и число электронов на внешнем уровне отражают принятую в Периодической системе символику, т.е.
раскрывают физический смысл номера периода, номера группы и порядкового номера элемента.
Строение атома позволяет объяснить и причины изменения металлических и неметаллических свойств элементов в периодах и группах.
Периодический закон и Периодическая система химических элементов Д. И.
Менделеева обобщают сведения о химических элементах и образованных ими веществах и объясняют периодичность в изменении их свойств и причину сходства свойств элементов одной и той же группы.
Эти два важнейших значения Периодического закона и Периодической системы дополняет еще одно, которое заключается в возможности прогнозировать, т.е. предсказывать, описывать свойства и указывать пути открытия новых химических элементов.
Общая характеристика металлов главных подгрупп I±III групп в связи с их положением в Периодической системе химических элементов Д. И. Менделеева и особенностями строения их атомов
Химические элементы — металлы
- Большинство химических элементов относят к металлам — $92$ из $114$ известных элементов.
- Все металлы, кроме ртути, в обычном состоянии — твердые вещества и имеют ряд общих свойств.
- Металлы — это ковкие, пластичные, тягучие вещества, имеющие металлический блеск и способны проводить тепло и электрический ток.
- Атомы элементов-металлов отдают электроны внешнего (а некоторые и предвнешнего) электронного слоя, превращаясь в положительные ионы.
- Это свойство атомов металлов, как вы знаете, определяется тем, что они имеют сравнительно большие радиусы и малое число электронов (в основном от $1$ до $3$ на внешнем слое).
- Исключение составляют лишь $6$ металлов: атомы германия, олова, свинца на внешнем слое имеют $4$ электрона, атомы сурьмы и висмута — $5$, атомы полония — $6$.
Для атомов металлов характерны небольшие значения электроотрицательности (от $0.7$ до $1.9$) и исключительно восстановительные свойства, т.е. способность отдавать электроны.
Вы уже знаете, что в Периодической системе химических элементов Д. И. Менделеева металлы находятся ниже диагонали бор — астат, а также выше ее, в побочных подгруппах. В периодах и главных подгруппах действуют известные вам закономерности в изменении металлических, а значит, восстановительных свойств атомов элементов.
Химические элементы, расположенные вблизи диагонали бор — астат ($Be, Al, Ti, Ge, Nb, Sb$), обладают двойственными свойствами: в одних своих соединениях ведут себя как металлы, в других проявляют свойства неметаллов.
В побочных подгруппах восстановительные свойства металлов с увеличением порядкового номера чаще всего уменьшаются.
Это можно объяснить тем, что на прочность связи валентных электронов с ядром у атомов этих металлов в большей степени влияет величина заряда ядра, а не радиус атома. Величина заряда ядра значительно увеличивается, притяжение электронов к ядру усиливается. Радиус атома при этом хотя и увеличивается, но не столь значительно, как у металлов главных подгрупп.
Простые вещества, образованные химическими элементами — металлами, и сложные металлосодержащие вещества играют важнейшую роль в минеральной и органической «жизни» Земли. Достаточно вспомнить, что атомы (ионы) элементов металлов являются составной частью соединений, определяющих обмен веществ в организме человека, животных.
Например, в крови человека найдено $76$ элементов, из них только $14$ не являются металлами. В организме человека некоторые элементы- металлы (кальций, калий, натрий, магний) присутствуют в большом количестве, т.е. являются макроэлементами.
А такие металлы, как хром, марганец, железо, кобальт, медь, цинк, молибден присутствуют в небольших количествах, т.е. это микроэлементы.
Особенности строения металлов главных подгрупп I–III групп.
Щелочные металлы — это металлы главной подгруппы I группы. Их атомы на внешнем энергетическом уровне имеют по одному электрону. Щелочные металлы — сильные восстановители. Их восстановительная способность и химическая активность возрастают с увеличением порядкового номера элемента (т.е. сверху вниз в Периодической таблице).
Все они обладают электронной проводимостью. Прочность связи между атомами щелочных металлов уменьшается с увеличением порядкового номера элемента. Также снижаются их температуры плавления и кипения. Щелочные металлы взаимодействуют со многими простыми веществами — окислителями.
В реакциях с водой они образуют растворимые в воде основания (щелочи).
Щелочноземельными элементами называются элементы главной подгруппы II группы. Атомы этих элементов содержат на внешнем энергетическом уровне по два электрона. Они являются восстановителями, имеют степень окисления $+2$.
В этой главной подгруппе соблюдаются общие закономерности в изменении физических и химических свойств, связанные с увеличением размера атомов по группе сверху вниз, также ослабевает и химическая связь между атомами.
С увеличением размера иона ослабевают кислотные и усиливаются основные свойства оксидов и гидроксидов.
Главную подгруппу III группы составляют элементы бор, алюминий, галлий, индий и таллий. Все элементы относятся к $p$-элементам.
На внешнем энергетическом уровне они имеют по три $(s^2p^1)$ электрона, чем объясняется сходство свойств. Степень окисления $+3$. Внутри группы с увеличением заряда ядра металлические свойства увеличиваются.
Бор — элемент-неметалл, а у алюминия уже металлические свойства. Все элементы образуют оксиды и гидроксиды.
Характеристика переходных элементов ± меди, цинка, хрома, железа по их положению в Периодической системе химических элементов Д. И. Менделеева и особенностям строения их атомов
Большинство элементов-металлов находится в побочных группах Периодической системы.
В четвертом периоде у атомов калия и кальция появляется четвертый электронный слой, заполняется $4s$-подуровень, так как он имеет меньшую энергию, чем $3d$-подуровень. $K, Ca — s$-элементы, входящие в главные подгруппы. У атомов от $Sc$ до $Zn$ заполняется электронами $3d$-подуровень.
Рассмотрим, какие силы действуют на электрон, который добавляется в атом при возрастании заряда ядра. С одной стороны, притяжение атомным ядром, что заставляет электрон занимать самый нижний свободный энергетический уровень. С другой стороны, отталкивание уже имеющимися электронами.
Когда на энергетическом уровне оказывается $8$ электронов (заняты $s-$ и $р-$орбитали), их общее отталкивающее действие так сильно, что следующий электрон попадает вместо расположенной по энергии ниже $d-$орбитали на более высокую $s-$орбиталь следующего уровня. Электронное строение внешних энергетических уровней у калия $…
3d^{0}4s^1$, у кальция — $…3d^{0}4s^2$.
Последующее прибавление еще одного электрона у скандия приводит к началу заполнения $3d$-орбитали вместо еще более высоких по энергии $4р$-орбиталей. Это оказывается энергетически выгоднее.
Заполнение $3d$-орбитали заканчивается у цинка, имеющего электронное строение $1s^{2}2s^{2}2p^{6}3s^{2}3p^{6}3d^{10}4s^2$. Следует отметить, что у элементов меди и хрома наблюдается явление «провала » электрона.
У атома меди десятый $d$-электрон перемещается на третий $3d$-подуровень.
Электронная формула меди $…3d^{10}4s^1$. У атома хрома на четвертом энергетическом уровне ($s$-орбиталь) должно быть $2$ электрона. Однако один из двух электронов переходит на третий энергетический уровень, на незаполненную $d$-орбиталь, его электронная формула $…3d^{5}4s^1$.
Таким образом, в отличие от элементов главных подгрупп, где происходит постепенное заполнение электронами атомных орбиталей внешнего уровня, у элементов побочных подгрупп заполняются $d$-орбитали предпоследнего энергетического уровня. Отсюда и название: $d$-элементы.
Все простые вещества, образованные элементами подгрупп Периодической системы, являются металлами.
Благодаря большему числу атомных орбиталей, чем у элементов-металлов главных подгрупп, атомы $d$-элементов образуют большое число химических связей между собой и потому создают более прочную кристаллическую решетку.
Она прочнее и механически, и по отношению к нагреванию. Поэтому металлы побочных подгрупп — самые прочные и тугоплавкие среди всех металлов.
Известно, если атом имеет более трех валентных электронов, то элемент проявляет переменную валентность. Это положение относится к большинству $d$-элементов. Максимальная их валентность, как у элементов главных подгрупп, равна номеру группы (хотя есть и исключения). Элементы с равным числом валентных электронов входят в группу под одним номером $(Fe, Co, Ni)$.
У $d$-элементов изменение свойств их оксидов и гидроксидов в пределах одного периода при движении слева направо, т.е. с увеличением их валентности, происходит от основных свойств через амфотерные к кислотным. Например, хром имеет валентности $+2, +3, +6$; а его оксиды: $CrO$ — основной, $Cr_{2}O_3$ — амфотерный, $CrO_3$ — кислотный.
Общая характеристика неметаллов главных подгрупп IV±VII групп в связи с их положением в Периодической системе химических элементов Д. И. Менделеева и особенностями строения их атомов
Химические элементы – неметаллы
Самой первой научной классификацией химических элементов было деление их на металлы и неметаллы. Эта классификация не утратила своей значимости и в настоящее время.
Неметаллы —это химические элементы, для атомов которых характерна способность принимать электроны до завершения внешнего слоя благодаря наличию, как правило, на внешнем электронном слое четырех и более электронов и малому радиусу атомов по сравнению с атомами металлов.
Это определение оставляет в стороне элементы VIII группы главной подгруппы — инертные, или благородные, газы, атомы которых имеют завершенный внешний электронный слой. Электронная конфигурация атомов этих элементов такова, что их нельзя отнести ни к металлам, ни к неметаллам.
Они являются теми объектами, которые разделяют элементы на металлы и неметаллы, занимая между ними пограничное положение. Инертные, или благородные, газы («благородство» выражается в инертности) иногда относят к неметаллам, но формально, по физическим признакам. Эти вещества сохраняют газообразное состояние вплоть до очень низких температур.
Так, гелий Не переходит в жидкое состояние при $t°= –268,9 °С$.
Инертность в химическом отношении у этих элементов относительна. Для ксенона и криптона известны соединения с фтором и кислородом: $KrF_2, XeF_2, XeF_4$ и др. Несомненно, в образовании этих соединений инертные газы выступали в роли восстановителей.
Из определения неметаллов следует, что для их атомов характерны высокие значения электроотрицательности. Она изменяется в пределах от $2$ до $4$. Неметаллы — это элементы главных подгрупп, преимущественно $р$-элементы, исключение составляет водород — s-элемент.
Все элементы-неметаллы (кроме водорода) занимают в Периодической системе химических элементов Д. И. Менделеева верхний правый угол, образуя треугольник, вершиной которого является фтор $F$, а основанием — диагональ $B — At$.
Однако следует особо остановиться на двойственном положении водорода в Периодической системе: в главных подгруппах I и VII групп. Это не случайно. С одной стороны, атом водорода, подобно атомам щелочных металлов, имеет на внешнем (и единственном для него) электронном слое один электрон (электронная конфигурация $1s^1$), который он способен отдавать, проявляя свойства восстановителя.
В большинстве своих соединений водород, как и щелочные металлы, проявляет степень окисления $+1$. Но отдача электрона атомом водорода происходит труднее, чем у атомов щелочных металлов.
С другой стороны, атому водорода, как и атомам галогенов, до завершения внешнего электронного слоя недостает одного электрона, поэтому атом водорода может принимать один электрон, проявляя свойства окислителя и характерную для галогена степень окисления — $1$ в гидридах (соединениях с металлами, подобных соединениям металлов с галогенами — галогенидам). Но присоединение одного электрона к атому водорода происходит труднее, чем у галогенов.
Свойства атомов элементов – неметаллов
У атомов неметаллов преобладают окислительные свойства, т.е. способность присоединять электроны. Эту способность характеризует значение электроотрицательности, которая закономерно изменяется в периодах и подгруппах.
Фтор — самый сильный окислитель, его атомы в химических реакциях не способны отдавать электроны, т.е. проявлять восстановительные свойства.
Конфигурация внешнего электронного слоя.
| В периоде: — заряд ядра увеличивается; — радиус атома уменьшается; — число электронов на внешнем слое увеличивается; — электроотрицательность увеличивается; — окислительные свойства усиливаются; — неметаллические свойства усиливаются. | В главной подгруппе: — заряд ядра увеличивается; — радиус атома увеличивается; — число электронов на внешнем слое не изменяется; — электроотрицательность уменьшается; — окислительные свойства ослабевают; — неметаллические свойства ослабевают. |
Другие неметаллы могут проявлять восстановительные свойства, хотя и в значительно более слабой степени по сравнению с металлами; в периодах и подгруппах их восстановительная способность изменяется в обратном порядке по сравнению с окислительной.
Химических элементов-неметаллов всего $16$! Совсем немного, если учесть, что известно $114$ элементов. Два элемента-неметалла составляют $76%$ массы земной коры. Это кислород ($49%$) и кремний ($27%$). В атмосфере содержится $0.03%$ массы кислорода в земной коре. Неметаллы составляют $98.5%$ массы растений, $97.6%$ массы тела человека.
Неметаллы $C, H, O, N, S, Р$ — органогены, которые образуют важнейшие органические вещества живой клетки: белки, жиры, углеводы, нуклеиновые кислоты. В состав воздуха, которым мы дышим, входят простые и сложные вещества, также образованные элементами-неметаллами (кислород $О_2$, азот $N_2$, углекислый газ $СО_2$, водяные пары $Н_2О$ и др.).
Водород — главный элемент Вселенной. Многие космические объекты (газовые облака, звезды, в том числе и Солнце) более чем наполовину состоят из водорода. На Земле его, включая атмосферу, гидросферу и литосферу, только $0.88%$. Но это по массе, а атомная масса водорода очень мала. Поэтому небольшое содержание его только кажущееся, и из каждых $100$ атомов на Земле $17$ — атомы водорода.
Задание №2 ЕГЭ по химии
Закономерности изменения свойств.
Руслан Давыдов | Сайт: ege-rep.ru/blog/
Дмитрий Иванович Менделеев открыл периодический закон, согласно которому свойства элементов и образуемых ими изменяются периодически. Данное открытие было графически отображено в таблице Менделеева. По таблице очень хорошо и наглядно видно, как свойства элементов изменяются по периоду, после чего повторяются в следующем периоде.
Для решения задания №2 ЕГЭ по химии нам всего лишь нужно понять и запомнить, какие свойства элементов в каких направлениях изменяются и как.Всё это отображено на рисунке ниже.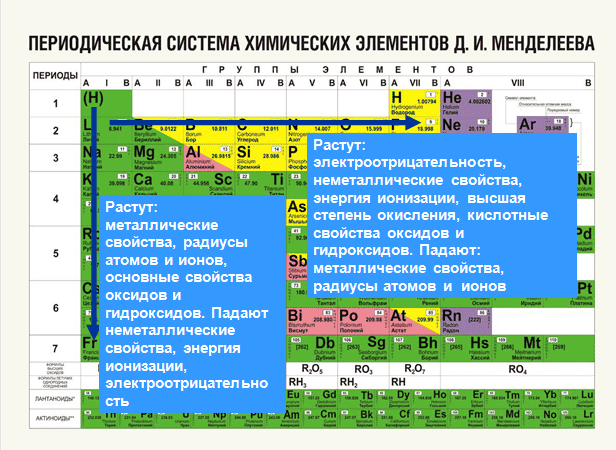 Слева направо растут электроотрицательность, неметаллические свойства, высшие степени окисления и т.д. А металлические свойства и радиусы уменьшаются.Сверху вниз наоборот: растут металлические свойства и радиусы атомов, а электроотрицательность падает. Высшая степень окисления, соответствующая количеству электронов на внешнем энергетическом уровне, в этом направлении не меняется.
Слева направо растут электроотрицательность, неметаллические свойства, высшие степени окисления и т.д. А металлические свойства и радиусы уменьшаются.Сверху вниз наоборот: растут металлические свойства и радиусы атомов, а электроотрицательность падает. Высшая степень окисления, соответствующая количеству электронов на внешнем энергетическом уровне, в этом направлении не меняется.
- Разберём на примерах.
- Пример 1. В ряду элементов Na→Mg→Al→Si
- Пример 2. В порядке усиления окислительных свойств элементы расположены в ряду:
- Пример 3. Валентность элементов в высшем оксиде увеличивается в ряду:
- Пример 4. В ряду элементов S→Se→Te
- Пример 5. В порядке ослабления основных свойств оксиды расположены в ряду:
А) уменьшаются радиусы атомов;Б) уменьшается число протонов в ядрах атомов;В) увеличивается число электронных слоёв в атомах;Г) уменьшается высшая степень окисления атомов;Если посмотреть в таблицу Менделеева, то мы увидим, что все элементы данного ряда находятся в одном периоде и перечислены в том порядке, как они стоят в таблице с лева направо. Что бы ответить на вопрос такого рода нужно просто знать несколько закономерностей изменений свойств в периодической таблице. Так слева направо по периоду металлические свойства падают, неметаллические растут, электроотрицательность растёт, энергия ионизации растёт, радиус атомов уменьшается. По группе сверху вниз металлические и восстановительные свойства растут, электроотрицательность падает, энергия ионизации уменьшается, радиус атомов растёт. Если вы были внимательны, то уже поняли, что в данном случае уменьшаются радиусы атомов. Ответ А.А. F→O→NБ. I→Br→ClВ. Cl→S→PГ. F→Cl→BrКак вы знаете, в периодической таблице Менделеева окислительные свойства растут слева направо по периоду и снизу вверх по группе. В варианте Б как раз приведены элементы одной группы в порядке снизу вверх. Значит Б подходит.А. Cl→Br→IБ. Cs→K→LiВ. Cl→S→PГ. Al→C→NВ высших оксидах элементы проявляют свою высшую степень окисления, которая будет совпадать с валентностью. А высшая степень окисления растёт слева направо по таблице. Смотрим: в первом и втором вариантах нам даны элементы, находящиеся в одних группах, там высшая степень окисления и соответственно валентность в оксидах не меняется. Cl→S→P – расположены справа налево, то есть у них наоборот валентность в высшем оксиде будет падать. А вот в ряду Al→C→N элементы расположены слева – направо, валентность в высшем оксиде увеличивается у них. Ответ: ГА) увеличивается кислотность водородных соединений;Б) увеличивается высшая степень окисления элементов;В) увеличивается валентность элементов в водородных соединениях;Г) уменьшается число электронов на внешнем уровне;Сразу смотрим на расположение этих элементов в таблице Менделеева. Сера, селен и теллур находятся в одной группе, одной подгруппе. Приведены в порядке сверху вниз. Смотрим еще раз на диаграмму выше. Сверху вниз в периодической таблице растут металлические свойства, растут радиусы, падает электроотрицательность, энергия ионизации и неметаллические свойства, количество электронов на внешнем уровне не меняется. Вариант Г сразу исключаем. Если число внешних электронов не меняется, то валентные возможности и высшая степень окисления тоже не меняется, Б и В — исключаем.Остаётся вариант А. Проверяем для порядка. По схеме Косселя сила безкислородных кислот возрастает с уменьшением степени окисления элемента и увеличением радиуса его иона. Степень окисления у всех трёх элементов одинаковая в водородных соединениях, а вот радиус сверху вниз растёт, значит и сила кислот растёт. Ответ – А.А. Na2O→K2O→Rb2OБ. Na2O→MgO→Al2O3В. BeO→BaO→CaO
Г. SO3→P2O5→SiO2
Основные свойства оксидов ослабевают синхронно с ослабление металлических свойств элементов их образующих. А Ме- свойства ослабевают слева направо или снизу вверх. Na, Mg и Al как раз располагаются слева направо. Ответ Б.
Выпускница 150-го лицея Калининского района Анастасия Карандашева набрала 300 баллов на ЕГЭ.
Средний тестовый балл по биологии в этом году — 50,16.






