- История элемента
- Нахождение в природе и получение
- Строение атома и структура
- Физические особенности
- Химические свойства
- Меры безопасности
- Сферы применения
- Значение для человека
- Полезные продукты
- Селен
- СТРУКТУРА
- СВОЙСТВА
- Запасы и добыча
- ПРОИСХОЖДЕНИЕ
- ПРИМЕНЕНИЕ
- КЛАССИФИКАЦИЯ
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
- Селен | это… Что такое Селен?
- История
- Происхождение названия
- Нахождение в природе
- Получение
- Физические свойства
- Химические свойства
- Применение
- Биологическая роль
- Изотопы
- См. также
- Примечания
- Селен
- Происхождение названия
- Нахождение в природе
- Получение
- Физические свойства
- Химические свойства
- Биологическая роль
- Токсичность
- Общий характер воздействия селена и его соединений
- Действие на кожу
- Изотопы

История элемента

Элемент был открыт Й. Я. Берцелиусом в 1817 году. Шведский химик и минералог проводил опыты с серной кислотой вместе с Я. Г. Ганом. Учёные обнаружили в веществе красновато-коричневый осадок с редечным запахом, который тогда служил определением присутствия теллура. Берцелиус решил исследовать осадок, надеясь обнаружить новый металл. После изучения этого явления он смог выявить неизвестное вещество, которое по свойствам напоминало теллур. Поскольку второй элемент был назван в честь Земли, химик назвал новый элемент Selenium (селен), что переводится с латинского «Луна».
В 1873 году Уиллоуби Смит доказал, что электрическое сопротивление элемента зависит от освещённости. Через несколько лет были разработаны первые продукты в виде ячеек на основе селена, которые использовали в фотофоне, созданном А. Г.
Беллом. С помощью химического элемента можно было изменять электропроводимость световых лучей, которые отражались от зеркала под влиянием звука. Полезное свойство селена позволило использовать его в разных измерителях освещённости.
В первой половине XX века начали производить выпрямители на основе этого элемента, которые заменили медно-закисные изделия. Полупроводниковые диоды широко использовали до 1970-х годов.
Когда начали происходить массовые отравления работников на селеновых заводах и животных, поедавших траву около этих предприятий, люди поняли, что химический элемент токсичен. В середине прошлого века учёные раскрыли биологическое значение вещества для живых организмов.
Нахождение в природе и получение

Неметалл в объёме 500 мг/т содержится в земной коре. Основные черты вещества можно определить по близкому отношению ионных радиусов селена и серы. С «лунным» элементом образуются 37 минералов, включая ашавалит, гуанахуатит, клаусталит, платинит, тиманнит и хастит. Селен в виде самородков встречается довольно редко. Его минералы можно найти чаще, но добывают материал в основном из сульфидов. В этих соединениях объём неметалла варьируется в пределах чисел 7−100 г/т. В морской воде концентрация вещества составляет 0,4 мкг/л.
Основным источником неметалла выступают шламы свинцовых камер и пыль, которая образуется при обжиге сульфидов с соответствующим веществом. Сырьё обрабатывают концентрированной серной кислотой с нитратом натрия.
В результате реакции образуется селенистая кислота с формулой H2SeO3 и в небольшом объёме селеновая кислота (H2SeO4).
Затем селенистую кислоту обрабатывают сернистым газом и получают элементарный селен и серную кислоту.
Чтобы очистить полученный осадок, его сжигают в кислороде, который насыщают парами азотной кислоты. В результате получается чистый диоксид селена.
В раствор SeO2 добавляют соляную кислоту, а затем пропускают через него сернистый газ, осаждая нужный элемент. Полученное вещество переплавляют, фильтруют через стеклоткань или активированный уголь.
Последняя стадия очистки элемента подразумевает дистилляцию в вакууме.
Строение атома и структура
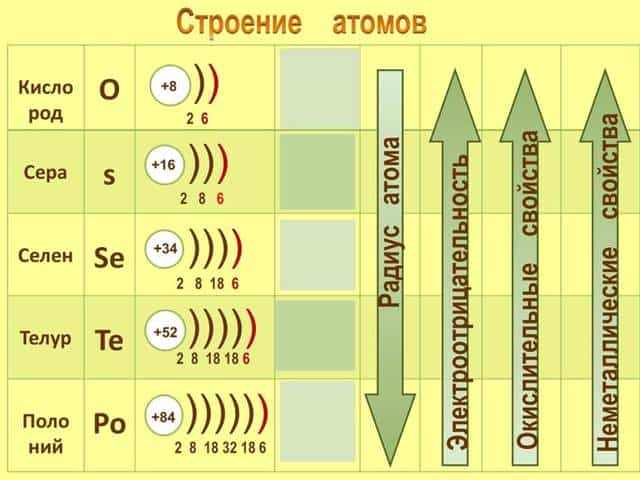
Селен состоит в 4-м периоде VI группы химических элементов. Неметалл имеет порядковый номер 34, его обозначение в таблице — Se. Атомная масса составляет 78,96 а. е. м., электронная формула селена — 1s22s22p63s23p63d104s24p4. Атом химического элемента имеет ядро с положительным зарядом +34. В него входят 34 протона, 45 нейронов и 34 электрона, которые движутся по 3-м орбитам.
Элемент отличается интересной конфигурацией. На внешнем энергетическом уровне располагаются 6 валентных отрицательно заряженных частиц. Поскольку в атоме селена есть два неспаренных электрона, это говорит о его ковалентности.
Вещество может быть представлено в двух модификациях:
- кристаллическая (моноклинный и гексагональный селен);
- аморфная.
Во втором случае неметалл имеет порошкообразную, коллоидную или стекловидную форму. Аморфная модификация неустойчива. Красный порошкообразный или коллоидный селен образуется при восстановлении из раствора селенистой кислоты. Чтобы получить стекловидную форму чёрного цвета, вещество любой модификации нагревают до температуры 220 °C, а потом сразу же охлаждают.
Гексагональный селен тёмно-серого оттенка устойчив в термодинамических условиях. Любую форму вещества нагревают до температуры плавления и затем охлаждают до 180−200°C, выдерживая этот показатель определённый период.
Физические особенности
Селен относится к группе халькогенов. Неметалл представляет собой хрупкое и непрозрачное вещество чёрного цвета. В неустойчивой форме он имеет оттенок киноварь. Обладает металлическим блеском.
Основные характеристики селена в гексагональной модификации:
- твёрдость по шкале Мооса — 2;
- плотность — 4,8 г/см3;
- температура плавления — 217 °C;
- температура кипения — 685−688°C;
- цвет черты — красный.

Гибкий материал относится к диамагнетикам. Он характеризуется высоким оптическим рельефом и анизотропией. Цвет минерала в воздухе — белый. В иммерсии (микроскопическое наблюдение) оттенок становится темнее и может быть серовато-коричневым. Только на просвет химический элемент приобретает красную окраску.
Химические свойства

Так как неметалл характеризуется двумя неспаренными электронами, степень окисления селена равна +2. Но у вещества есть вакантные орбитали на четвёртом уровне 4d-подуровня. Это говорит о том, что элемент может находиться в возбуждённом состоянии, при котором степень окисления меняется на +4.
По химическим свойствам неметалл близок к теллуру и сере, занимая промежуточное место между ними. Однако в соединениях со степенью окисления -2 он служит сильным восстановителем, а с показателем +6 — окислителем.
Простое вещество селен отличается меньшей активностью, чем сера. Элемент способен гореть в воздухе самостоятельно. Окисление неметалла происходит только при нагревании. Вещество горит синим пламенем.
Бурные реакции с селеном наблюдаются при взаимодействии с щелочными металлами.
Химический элемент может образовывать с кислородом несколько оксидов. SeO2 и SeO3 выступают ангидридами селеновой и селенистой кислот, с которыми получают селенат и селенит. Также неметалл может образовывать SeO и SeO5. Диоксид селена (SeO2) представляет собой кристаллическое вещество. Он хорошо растворяется в воде и считается довольно устойчивым соединением.
Меры безопасности

«Лунный» элемент относится к третьему классу опасности, поэтому с токсичным веществом и его соединениями следует работать осторожно. По характеру воздействия на человеческий организм селен напоминает мышьяк. Он может поражать печень, почки и ЦНС. В металлической форме вещество менее токсично. Наиболее опасными соединениями считаются диоксид селена, селеноводород и селениты натрия или лития.
Если вещество в форме металлического порошка попало в организм через рот, тогда у человека возникнут сильные боли в животе и диарея. Пострадавшему не потребуется помощь, если объём токсичного материала не превышал 1 г. Через какое-то время симптомы пройдут самостоятельно.
На кожном покрове могут возникнуть ожоги или аллергическая реакция в виде дерматита при контакте с солями неметалла. Диоксид селена вызывает резкую боль и онемение. Соединения химического элемента могут сильно раздражить слизистые оболочки. Также они вызывают покраснения, а при попадании в органы зрения — режущую боль, слезотечение и конъюнктивит.
Сферы применения
Селен, а также его соединения и сплавы широко используются в качестве полупроводника для выпрямителей переменного тока. В современной технологии применяют селениды висмута, олова, свинца, сурьмы.
Неметалл используется и в других областях:

- Это вещество необходимо при создании фототехники.
- В виде источника излучения для дефектоскопии применяют радиоактивный изотоп селен-75.
- Селен может использоваться как наполнитель в резиновой промышленности.
- В металлургии элемент необходим для придания полученным сплавам мелкозернистой структуры.
- В стекольной промышленности вещество используется для обесцвечивания или окрашивания прозрачного материала в красные или розовые оттенки. Обычно для этого выбирают металлическую форму элемента или селенистокислый натрий. Селеном окрашены рубиновые звёзды Московского Кремля.
- Материал применяется и в производстве керамических изделий, которым он придаёт красноватые оттенки. Также этим веществом окрашивают эмали.
Хотя селен относится к токсичным веществам, он может использоваться и в сфере медицины благодаря своим антиоксидантным свойствам. Неметалл выступает мощным противораковым средством.
Препараты с селеном применяют в профилактике развития различных болезней. В малых концентрациях вещество подавляет гистамин. Селен обладает противоаллергическим и антидистрофическим эффектом.
Соли неметалла избавляют от гипотонии при шоке и коллапсе.
Значение для человека

Селен — жизненно необходимый для живых организмов микроэлемент. Он содержится в активных центрах некоторых белков в виде аминокислот селеноцистеина. Объём вещества в человеческом организме составляет 10−14 мг. Основная часть находится в печени, почках, селезёнке, яичках и семенных канатиках у мужчин. В небольших количествах микроэлемент присутствует в костном мозге, сердце, лёгких, коже, волосах и ногтях.
Вещество взаимодействует с различными витаминами и ферментами. Он обнаружен в составе более 30 биологических соединений. Благодаря учёным удалось узнать о пользе и вреде селена для организма человека:

- Микроэлемент восстанавливает работу нервной и эндокринной системы.
- Препараты с этим веществом усиливают иммунитет.
- Селен улучшает функцию сосудов и препятствует развитию сердечно-сосудистых патологий.
- Сильный антиоксидант тормозит старение организма и выводит из него чужеродные вещества.
- Неметалл снижает возможность развития злокачественных опухолей.
- Он улучшает работу половых желёз и стимулирует репродуктивную функцию.
- Селен нормализует процессы обменов в человеческом организме и защищает его от возможного токсического действия кадмия, ртути, свинца, серебра и таллия.
- Вещество уменьшает боли при воспалениях.
Микроэлемент также участвует в обмене белков, жиров и углеводов. Без него не обходятся окислительно-восстановительные процессы. Из занимательных фактов о селене нужно отметить, что он контролирует весь цикл жизни клетки.
Полезные продукты
Для людей суточная норма селена составляет 70−110 мкг. Объём зависит от возраста и половой принадлежности человека. Для взрослых мужчин максимальное количество вещества в день составляет 140 мкг.
Селеном богаты продукты как животного, так и растительного происхождения:
- злаковые культуры;
- масло оливы;
- орехи;
- томаты;
- маслины;
- чеснок;
- грибы;
- рыба и другие морепродукты;
- говяжьи почки и печень;
- морская соль;
- ржаной хлеб;
- яйца курицы.
Повышенное содержание микроэлемента в человеческом организме может вызвать тошноту, рвоту или понос. В некоторых случаях развивается депрессия.
На избыток вещества указывают такие симптомы, как желтушность и шелушение кожи, разрушение ногтей, выпадающие волосы, отсутствие аппетита, постоянная усталость и расстройства ЦНС.
Если в организме повышается объём ртути, меди или сульфатов, тогда наблюдается недостаток селена. К дефициту элемента может привести применение медикаментозных средств от малярии.
Селен выполняет важную роль не только в различных сферах жизни человека, но и в его организме. С правильным рационом получится поддерживать объём вещества на нужном уровне.
Селен

Черный металлические кристаллы селена, образованный на горящем угольном отвале. Ширина изображения – 1,8 мм. Германия, Северный Рейн-Вестфалия, Аахен, Альсдорф, шахта Анна
Селен — хрупкий блестящий на изломе неметалл чёрного цвета (устойчивая аллотропная форма, неустойчивая форма — киноварно-красная). Относится к халькогенам.
Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина.
В организме человека содержится 10—14 мг селена, большая его часть сконцентрирована в печени, почках, селезенке, сердце, яичках и семенных канатиках у мужчин. Селен входит в состав белков мышечной ткани, белков миокарда.
СТРУКТУРА
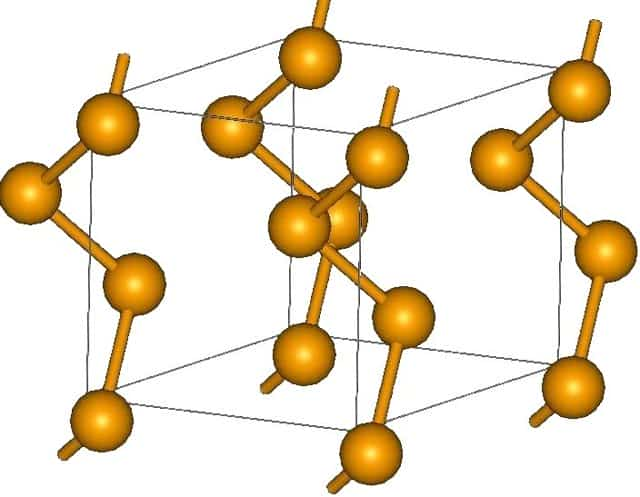
Кристаллическая структура селена
Существует две модификации селена:
1. Кристаллическая (моноклинный селен a- и b-форм, гексагональный селен g-формы).
2. Аморфная (порошкообразная, коллоидная и стекловидная формы селена).
Модификация аморфный красного цвета селен – это одна из неустойчивых модификаций элемента. Порошкообразная и коллоидная формы селена получаются путем восстановления вещества из раствора селенистой кислоты H2SeO3.
Черный стекловидный селен можно получить путём нагревания элемента любой модификации до температуры 220 градусов Цельсия с быстрым охлаждением. Гексагональный селен имеет серый цвет. Эту модификацию, наиболее устойчивую термодинамически, можно получить также путем нагревания до температуры плавления с дальнейшим охлаждением до температуры 180-210 градусов Цельсия. Необходимо некоторое время выдерживать такой температурный режим.
СВОЙСТВА

Черный, стеклообразный аморфный и красный аморфный селен
Температура плавления вещества – 217 (α-Se) и 170–180 градусов Цельсия (β-Se), а закипает он при температуре 6850.
Степени окисления, что селен проявляет в реакциях: (-2), (+2), (+4), (+6), он устойчив к воздуху, кислороду, воде, соляной кислоте и разбавленной серной кислоте.
Поддается растворению в азотной кислоте высокой концентрации, “царской водке”, более длительно растворяется в щелочной среде с окислением. Является диамагнетиком.
Запасы и добыча

Селен
Поскольку селен примешен к сере, элемент извлекают из сульфата железа. Для этого даже делать особо ничего не надо. 34-ый металл накапливается в пылеочистительных камерах сернокислотных заводов. Забирают селен и из установок электролиза меди.
После него остается анодный шлам. Из него-то и выделяют 34-ый элемент. Достаточно обработать шлам растворами гидроксида натрия и диоксида серы. Полученный селен нужно очистить. Для этого используют метод дистилляции. После, металл подсушивают.
ПРОИСХОЖДЕНИЕ

Отличные глянцевые кристаллы из горящих угольных отвалов. Ширина изображения – 1,8 мм. Германия, Северный Рейн-Вестфалия, Аахен, Альсдорф, шахта Анна
Содержание селена в земной коре — около 500 мг/т. Основные черты геохимии селена в земной коре определяются близостью его ионного радиуса к ионному радиусу серы.
Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит FeSe, клаусталит PbSe, тиманнит HgSe, гуанахуатит Bi2(Se, S)3, хастит CoSe2, платинит PbBi2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом. Изредка встречается самородный селен.
Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Концентрация селена в морской воде 4·10-4 мг/л.
ПРИМЕНЕНИЕ

Селен
Одним из важнейших направлений его технологии, добычи и потребления являются полупроводниковые свойства как самого селена, так и его многочисленных соединений (селенидов), их сплавов с другими элементами, в которых селен стал играть ключевую роль.
В современной технологии полупроводников применяются селениды многих элементов, например, селениды олова, свинца, висмута, сурьмы, селениды лантаноидов. Особенно важны свойства фотоэлектрические и термоэлектрические как самого селена, так и селенидов.
Стабильный изотоп селен-74 позволил на своей основе создать плазменный лазер с колоссальным усилением в ультрафиолетовой области (около миллиарда раз). Радиоактивный изотоп селен-75 используется в качестве мощного источника гамма-излучения для дефектоскопии.
Селенид калия совместно с пятиокисью ванадия применяется при термохимическом получении водорода и кислорода из воды (селеновый цикл).
Полупроводниковые свойства селена в чистом виде широко использовались в середине 20-го века для изготовления выпрямителей, особенно в военной технике по следующим причинам: в отличие от германия, кремния, селен малочувствителен к радиации, и, кроме того, селеновый выпрямительный диод обладает уникальным свойством самовосстанавливаться при пробое: место пробоя испаряется и не приводит к короткому замыканию, допустимый ток диода несколько снижается, но изделие остается функциональным. К недостаткам селеновых выпрямителей относятся их значительные габариты.
Селен применяется как мощное противораковое средство, а также для профилактики широкого спектра заболеваний. Согласно исследованиям прием 200 мкг селена в сутки снижает риск заболеваемости раком прямой и толстой кишки — на 58 %, опухолями простаты на 63 %, раком легких — на 46 %, снижает общую смертность от онкологических заболеваний на 39 %.
Малые концентрации селена подавляют гистамин и за счет этого оказывают антидистрофический эффект и противоаллергическое действие. Также селен стимулирует пролиферацию тканей, улучшает функцию половых желез, сердца, щитовидной железы, иммунной системы.
В комплексе с йодом селен используется для лечения иододефицитных заболеваний и патологий щитовидной железы.
Соли селена способствуют восстановлению пониженного артериального давления при шоке и коллапсе
Селен (англ. Selenium) – Se
КЛАССИФИКАЦИЯ
Hey’s CIM Ref1.53
Физические свойства
Оптические свойства
Кристаллографические свойства
Селен | это… Что такое Селен?
| 34 | Селен |
| 3d104s24p4 |
Селе́н — химический элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), 4-го периода в периодической системе, имеет атомный номер 34, обозначается символом Se (лат. Selenium), хрупкий блестящий на изломе неметалл чёрного цвета (устойчивая аллотропная форма, неустойчивая форма — киноварно-красная). CAS-номер: 7782-49-2.
История
Элемент открыт Й. Я. Берцелиусом в 1817.
Сохранился рассказ самого Берцелиуса о том, как произошло это открытие:
Я исследовал в содружестве с Готлибом Ганом метод, который применяют для производства серной кислоты в Грипсхольме. Мы обнаружили в серной кислоте осадок, частью красный, частью светло-коричневый.
Этот осадок, опробованный с помощью паяльной трубки, издавал слабый редечный запах и образовывал свинцовый королёк. Согласно Клапроту, такой запах служит указанием на присутствие теллура.
Ган заметил при этом, что на руднике в Фалуне, где собирается сера, необходимая для производства кислоты, также ощущается подобный запах, указывающий на присутствие теллура. Любопытство, вызванное надеждой обнаружить в этом коричневом осадке новый редкий металл, заставило меня исследовать осадок.
Приняв намерение отделить теллур, я не смог, однако, открыть в осадке никакого теллура. Тогда я собрал всё, что образовалось при получении серной кислоты путём сжигания фалюнской серы за несколько месяцев, и подверг полученный в большом количестве осадок обстоятельному исследованию.
Я нашёл, что масса (то есть осадок) содержит до сих пор неизвестный металл, очень похожий по своим свойствам на теллур. В соответствии с этой аналогией я назвал новое тело селеном (Selenium) от греческого σελήνη (луна), так как теллур назван по имени Tellus — нашей планеты[2].
Происхождение названия
Название происходит от греч. σελήνη — Луна. Элемент назван так в связи с тем, что в природе он является спутником химически сходного с ним теллура (названного в честь Земли).
Нахождение в природе
Натуральный селен
Содержание селена в земной коре около 500 мг/т. Основные черты геохимии селена в земной коре определяются близостью его ионного радиуса к ионному радиусу серы. Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит FeSe, клаусталит PbSe, тиманнит HgSe, гуанахуатит Bi2(Se, S)3, хастит CoSe2, платинит PbBi2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом. Изредка встречается самородный селен. Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Концентрация селена в морской воде 4·10−4 мг/л[3].
Получение
Значительные количества селена получают из шлама медно-электролитных производств, в котором селен присутствует в виде селенида серебра.
Применяют несколько способов получения: окислительный обжиг с возгонкой SeO2; нагревание шлама с концентрированной серной кислотой, окисление соединений селена до SeO2 с его последующей возгонкой; окислительное спекание с содой, конверсия полученной смеси соединений селена до соединений Se(IV) и их восстановление до элементарного селена действием SO2.
Физические свойства
Монокристаллический селен (99,9999 %)
Твёрдый селен имеет несколько аллотропных модификаций. Наиболее устойчивой модификацией является серый селен. Красный селен представляет собой менее устойчивую аморфную модификацию.
При нагревании серого селена[4] он даёт серый же расплав, а при дальнейшем нагревании испаряется с образованием коричневых паров. При резком охлаждении паров селен конденсируется в виде красной аллотропной модификации.
Химические свойства
Селен — аналог серы и проявляет степени окисления −2 (H2Se), +4 (SeO2) и +6 (H2SeO4). Однако, в отличие от серы, соединения селена в степени окисления +6 — сильнейшие окислители, а соединения селена (-2) — гораздо более сильные восстановители, чем соответствующие соединения серы.
Простое вещество — селен гораздо менее активно химически, чем сера. Так, в отличие от серы, селен не способен гореть на воздухе самостоятельно[5]. Окислить селен удаётся только при дополнительном нагревании, при котором он медленно горит синим пламенем, превращаясь в двуокись SeO2. Со щелочными металлами селен реагирует (весьма бурно) только будучи расплавленным[6].
В отличие от SO2, SeO2 — не газ, а кристаллическое вещество, хорошо растворимое в воде. Получить селенистую кислоту (SeO2 + H2O → H2SeO3) ничуть не сложнее, чем сернистую. А действуя на неё сильным окислителем (например, HClO3), получают селеновую кислоту H2SeO4, почти такую же сильную, как серная.
Применение
| В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 7 ноября 2012. |
- Одним из важнейших направлений его технологии, добычи и потребления являются полупроводниковые свойства как самого селена, так и его многочисленных соединений (селенидов), их сплавов с другими элементами, в которых селен стал играть ключевую роль. Эта роль селена постоянно растёт, растёт спрос и цены (отсюда дефицит этого элемента).
В современной технологии полупроводников применяются селениды многих элементов, например селениды олова, свинца, висмута, сурьмы, селениды лантаноидов.
Особенно важны свойства фотоэлектрические и термоэлектрические как самого селена, так и селенидов.
- Стабильный изотоп селен-74 позволил на своей основе создать плазменный лазер с колоссальным усилением в ультрафиолетовой области (около миллиарда раз).
- Радиоактивный изотоп селен-75 используется в качестве мощного источника гамма-излучения для дефектоскопии.
- В медицине, а также в сельском хозяйстве используют микродобавки селена к лекарственным средствам, витаминным препаратам, БАД, и т. п.
Селенид калия совместно с пятиокисью ванадия применяется при термохимическом получении водорода и кислорода из воды (селеновый цикл, Ливерморская национальная лаборатория им. Лоуренса, Ливермор, США).
Биологическая роль
Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина.
Микроэлемент, но большинство соединений достаточно токсично (селеноводород, селеновая и селенистая кислота) даже в средних концентрациях.
Изотопы
В природе существует 6 изотопов селена (74Se, 76Se, 77Se, 78Se, 80Se и 82Se), из них пять, насколько это известно, стабильны, а один (82Se) испытывает двойной бета-распад с периодом полураспада 9,7·1019 лет. Кроме того, искусственно созданы ещё 24 радиоактивных изотопа (а также 9 метастабильных возбуждённых состояний) в диапазоне массовых чисел от 65 до 94.
Периоды полураспада некоторых радиоактивных изотопов селена:
| 73Se | — | 7,1 час. |
| 74Se | 0,87 | — |
| 75Se | — | 120,4 сут. |
| 76Se | 9,02 | — |
| 77Se | 7,58 | — |
| 77mSe | — | 17,5 сек. |
| 78Se | 23,52 | — |
| 79Se | — | 6,5·104 лет |
| 79mSe | — | 3,91 мин. |
| 80Se | 49,82 | — |
| 81Se | — | 18,6 мин. |
| 81mSe | — | 62 мин. |
| 82Se | 9,19 | 9,7·1019 лет |
| 83mSe | — | 69 сек. |
| 83Se | — | 25 мин. |
См. также
- Категория:Соединения селена
- Селеновая кислота
Примечания
Селен
| 34 | Селен |
| 3d104s24p4 |
Селен — химический элемент 6-й группы (по устаревшей классификации — главной подгруппы VI группы), 4-го периода в периодической системе, имеет атомный номер 34, обозначается символом Se (лат. Selenium), хрупкий блестящий на изломе неметалл чёрного цвета (устойчивая аллотропная форма, неустойчивая форма — киноварно-красная). Относится к халькогенам.
Элемент открыт Й. Я. Берцелиусом в 1817.
Сохранился рассказ самого Берцелиуса о том, как произошло это открытие:
Я исследовал в содружестве с Готлибом Ганом метод, который применяют для производства серной кислоты в Грипсхольме. Мы обнаружили в серной кислоте осадок, частью красный, частью светло-коричневый.
Этот осадок, опробованный с помощью паяльной трубки, издавал слабый редечный запах и образовывал свинцовый королёк. Согласно Клапроту, такой запах служит указанием на присутствие теллура.
Ган заметил при этом, что на руднике в Фалуне, где собирается сера, необходимая для производства кислоты, также ощущается подобный запах, указывающий на присутствие теллура. Любопытство, вызванное надеждой обнаружить в этом коричневом осадке новый редкий металл, заставило меня исследовать осадок.
Приняв намерение отделить теллур, я не смог, однако, открыть в осадке никакого теллура. Тогда я собрал всё, что образовалось при получении серной кислоты путём сжигания фалюнской серы за несколько месяцев, и подверг полученный в большом количестве осадок обстоятельному исследованию.
Я нашёл, что масса (то есть осадок) содержит до сих пор неизвестный металл, очень похожий по своим свойствам на теллур. В соответствии с этой аналогией я назвал новое тело селеном (Selenium) от греческого σελήνη (луна), так как теллур назван по имени Tellus — нашей планеты.
В 1873 году Уиллоуби Смит обнаружил, что электрическое сопротивление серого селена зависит от освещённости. Это свойство стало основой для чувствительных к свету ячеек. Первый коммерческий продукт на основе селена был представлен на рынке в середине 1870-х годов Вернером фон Сименсом.
Селеновая ячейка использовалась в фотофоне, созданном Александром Беллом в 1879 году. Электрический ток, проходящий через селен, пропорционален количеству света, падающему на его поверхность, — это свойство использовано в различных измерителях освещённости (экспонометрах).
Полупроводниковые свойства селена нашли применение в других областях электроники В 1930-е годы началось развитие селеновых выпрямителей, которые пришли на смену медно-закисным выпрямителям благодаря высокой эффективности Селеновые выпрямители использовались до 1970-х годов, когда им на смену пришли кремниевые выпрямители.
В более позднее время была обнаружена токсичность селена. Были зарегистрированы случаи отравления людей, работавших на селеновых производствах, а также животных, поедавших богатые селеном растения. В 1954 году были обнаружены первые признаки биологического значения селена для микроорганизмов.
В 1957 году была установлена важная роль селена в биологии млекопитающих. В 1970-е годы было показано наличие селена в двух независимых группах энзимов, а затем обнаружен селеноцистеин в белках. В 1980-е годы было установлено, что селеноцистеин кодируется кодоном UGA.
Механизм кодирования был установлен сначала для бактерий, а затем для млекопитающих (SECIS-элемент).
Происхождение названия
Название происходит от греч. σελήνη — Луна. Элемент назван так в связи с тем, что в природе он является спутником химически сходного с ним теллура (названного в честь Земли).
Нахождение в природе
Содержание селена в земной коре — около 500 мг/т. Основные черты геохимии селена в земной коре определяются близостью его ионного радиуса к ионному радиусу серы. Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит FeSe, клаусталит PbSe, тиманнит HgSe, гуанахуатит Bi2(Se, S)3, хастит CoSe2, платинит PbBi2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом. Изредка встречается самородный селен. Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Концентрация селена в морской воде 0,4 мкг/л. На территории Кавказских Минеральных Вод есть источник с содержанием биогенного Se более 50 мкг/л.
Получение
Значительные количества селена получают из шлама медно-электролитных производств, в котором селен присутствует в виде селенида серебра.
Применяют несколько способов получения: окислительный обжиг с возгонкой SeO2; нагревание шлама с концентрированной серной кислотой, окисление соединений селена до SeO2 с его последующей возгонкой; окислительное спекание с содой, конверсия полученной смеси соединений селена до соединений Se(IV) и их восстановление до элементного селена действием SO2.
Физические свойства
Монокристаллический селен (99,9999 %)
Твёрдый селен имеет несколько аллотропных модификаций:
- Серый селен (γ-Se, «металлический селен») — наиболее устойчивая модификация с гексагональной кристаллической решёткой;
- Красный кристаллический селен — три моноклинные модификации: оранжево-красный α-Se, тёмно-красный β-Se, красный γ-Se;
- Красный аморфный селен;
- Чёрный стекловидный селен.
При нагревании серого селена он даёт серый же расплав, а при дальнейшем нагревании испаряется с образованием коричневых паров. При резком охлаждении паров селен конденсируется в виде красной аллотропной модификации.
Химические свойства
Селен — аналог серы и проявляет степени окисления −2 (H2Se), +4 (SeO2) и +6 (H2SeO4). Однако, в отличие от серы, соединения селена в степени окисления +6 — сильнейшие окислители, а соединения селена (−2) — гораздо более сильные восстановители, чем соответствующие соединения серы.
Простое вещество селен гораздо менее активно химически, чем сера. Так, в отличие от серы, селен не способен гореть на воздухе самостоятельно. Окислить селен удаётся только при дополнительном нагревании, при котором он медленно горит синим пламенем, превращаясь в двуокись SeO2. Со щелочными металлами селен реагирует (весьма бурно), только будучи расплавленным.
В отличие от SO2, SeO2 — не газ, а кристаллическое вещество, хорошо растворимое в воде. Получить селенистую кислоту (SeO2 + H2O → H2SeO3) ничуть не сложнее, чем сернистую. А действуя на неё сильным окислителем (например, HClO3), получают селеновую кислоту H2SeO4, более сильную, чем серная.
Биологическая роль
Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина. Является необходимым для жизни микроэлементом, но большинство соединений достаточно токсичны (селеноводород, селеновая и селенистая кислота) даже в средних концентрациях.
В организме человека содержится 10—14 мг селена, бо́льшая его часть сконцентрирована в печени, почках, селезёнке, сердце, яичках и семенных канатиках у мужчин. Селен присутствует в ядре клетки.
Суточная потребность человека в селене составляет 70-100 мкг. Повышенное содержание селена в организме может приводить к депрессии, тошноте, рвоте, диарее, поражению ЦНС и др.
Согласно данным эпидемиологических исследований 1990-х годов, более чем у 80 % россиян наблюдается дефицит селена.
Селен в организме взаимодействует с витаминами, ферментами и биологическими мембранами, участвует в регуляции обмена веществ, в обмене жиров, белков и углеводов, а также в окислительно-восстановительных процессах. Селен является составным компонентом более 30 жизненно важных биологически активных соединений организма.
Селен входит в активный центр ферментов системы антиоксидантно-антирадикальной защиты организма, метаболизма нуклеиновых кислот, липидов, гормонов (глутатионпероксидазы, йодотиронин-дейододиназы, тиоредоксинредуктазы, фосфоселенфосфатазы, фосфолипид-гидропероксид-глутатионпероксидазы, специфических протеинов Р и W и др.).
Селен входит в состав белков мышечной ткани, белков миокарда. Также селен способствует образованию трийодтиронина (гормонов щитовидной железы).
Селен является синергистом витамина E и иода. При дефиците селена иод плохо усваивается организмом. Согласно исследованиям, селен необходим для нормального функционирования иммунной системы. Он задействован в механизмах противодействия вирусным инфекциям, включая ВИЧ. Было доказано, что у пациентов, уже заразившихся ВИЧ, он замедляет переход заболевания в СПИД.
- Одним из важнейших направлений его технологии, добычи и потребления являются полупроводниковые свойства как самого селена, так и его многочисленных соединений (селенидов), их сплавов с другими элементами, в которых селен стал играть ключевую роль. В современной технологии полупроводников применяются селениды многих элементов, например, селениды олова, свинца, висмута, сурьмы, лантаноидов. Особенно важны свойства фотоэлектрические и термоэлектрические как самого селена, так и селенидов.
- Радиоактивный изотоп селен-75 используется в качестве источника гамма-излучения для дефектоскопии.
- Селенид калия совместно с пятиокисью ванадия применяется при термохимическом получении водорода и кислорода из воды (селеновый цикл).
- Полупроводниковые свойства селена в чистом виде широко использовались в середине 20-го века для изготовления выпрямителей, особенно в военной технике по следующим причинам: в отличие от германия и кремния, селен малочувствителен к радиации, и, кроме того, селеновый выпрямительный диод самовосстанавливается при пробое: место пробоя испаряется и не приводит к короткому замыканию, допустимый ток диода несколько снижается, но изделие остается функциональным. К недостаткам селеновых выпрямителей относятся их значительные габариты.
- Соединения селена применяются для окрашивания стекла в красный и розовый цвет. Обычно используют металлический селен и селенистокислый натрий Na2SeO3. Красные стекла, окрашенные селеном, называют селеновым рубином. Селен применялся при производстве стекла рубиновых звёзд Московского Кремля.
Селен применяется как мощное противораковое средство, а также для профилактики широкого спектра заболеваний.
Из-за его влияния на репарацию ДНК, апоптоз, эндокринную и иммунную системы, а также другие механизмы, включая его антиоксидантные свойства, селен может играть роль в профилактике рака.
Согласно исследованиям, приём 200 мкг селена в сутки снижает риск заболеваемости раком прямой и толстой кишки на 58 %, опухолями простаты — на 63 %, раком легких — на 46 %, снижает общую смертность от онкологических заболеваний на 39 %.
Малые концентрации селена подавляют гистамин и за счёт этого оказывают антидистрофический эффект и противоаллергическое действие. Также селен стимулирует пролиферацию тканей, улучшает функцию половых желез, сердца, щитовидной железы, иммунной системы.
В комплексе с йодом селен используется для лечения иододефицитных заболеваний и патологий щитовидной железы.
Соли селена способствуют восстановлению пониженного артериального давления при шоке и коллапсе..
Токсичность
Общий характер воздействия селена и его соединений
Селен и его соединения ядовиты, по характеру действия несколько напоминает мышьяк; обладает политропным действием с преимущественным поражением печени, почек и ЦНС. Металлический селен менее ядовит.
Из неорганических соединений селена наиболее токсичными являются селеноводород, диоксид селена (ЛД50 = 1,5 мг/кг, крысы, интратрахеально) и селениты натрия (ЛД50 = 2,25 мг/кг, кролик, перорально) и лития (ЛД50 = 8,7 мг/кг, крысы, перорально).
Особенно токсичен селеноводород, однако, ввиду его отвратительного запаха, ощущаемого даже в ничтожных концентрациях (0,005 мг/л), удаётся избежать отравлений.
Органические соединения селена, такие как алкил- или арил-производные (например, диметилселен, метилэтилселен или дифенилселен), являются сильнейшими нервными ядами, с очень отвратительными запахами; так, порог восприятия для диэтилселена составляет 0,0064 мкг/л.
При попадании металлического порошкового селена в количестве 1 грамма перорально вызывает боль в животе в течение двух суток и учащённый стул, со временем симптомы проходят.
Действие на кожу
Соли селена при непосредственном соприкосновении с кожей вызывают ожоги и дерматиты. Диоксид селена при контакте с кожей способен вызывать резкую боль и онемение. При попадании на слизистые оболочки соединения селена могут вызывать раздражение и покраснение, при попадании в глаза резкую боль, слезотечение и конъюктивит.
Изотопы
Основная статья: Изотопы селена
Селен в природе состоит из 6 изотопов: 74Se (0,87 %), 76Se (9,02 %), 77Se (7,58 %), 78Se (23,52 %), 80Se (49,82 %), 82Se (9,19 %). Из них пять, насколько это известно, стабильны, а один (82Se) испытывает двойной бета-распад с периодом полураспада 9,7⋅1019 лет.
Кроме того, искусственно созданы ещё 24 радиоактивных изотопа (а также 9 метастабильных возбуждённых состояний) в диапазоне массовых чисел от 65 до 94.
Из искусственных изотопов применение нашел 75Se как источник гамма-излучения для неразрушающего контроля сварных швов и целостности конструкций.
Периоды полураспада некоторых радиоактивных изотопов селена:
| 73Se | — | 7,1 час. |
| 74Se | 0,87 | — |
| 75Se | — | 120,4 сут. |
| 76Se | 9,02 | — |
| 77Se | 7,58 | — |
| 77mSe | — | 17,5 сек. |
| 78Se | 23,52 | — |
| 79Se | — | 6,5⋅104 лет |
| 79mSe | — | 3,91 мин. |
| 80Se | 49,82 | — |
| 81Se | — | 18,6 мин. |
| 81mSe | — | 62 мин. |
| 82Se | 9,19 | 9,7⋅1019 лет |
| 83mSe | — | 69 сек. |
| 83Se | — | 25 мин. |






