- Коррозия металлов
- Электрохимическая коррозия: причины, типы, скорость протекания
- Какие механизмы отвечают за протекание электрохимической коррозии
- Из-за чего начинает развиваться коррозия
- Главные внутренние факторы протекания электрохимической коррозии
- Текущее состояние поверхности металла
- Степень термодинамической стойкости металла
- Кристаллографическая структура
- Гетерогенность
- Не стоит сбрасывать со счетов и механические факторы
- Основные внешние факторы электрохимической коррозии
- Чем отличаются анодный и катодный процессы
- Анодный процесс
- Катодный процесс
- Поляризация и ее влияние на скорость протекания коррозии
- Обеспечиваем эффективную защиту от коррозии
- Электрохимическая коррозия металлов
- Защита от коррозии.
- Лекция 2. Электрохимическая коррозия
- Химическая коррозия
- Сплавы с магнием и кремнием
- Электрохимическая коррозия: примеры
- Материалы естественного происхождения
- Причины
- Механизм взаимодействия
- Свойства
- Содержание:
- Механизм электрохимической коррозии
- Причины возникновения местных гальванических элементов
- Анодный и катодный электродные процессы
- Электродный потенциал
- Поляризация
Электрохимическая коррозия — самый распространенный вид коррозии. Электрохимическая коррозия возникает при контакте металла с окружающей электролитически проводящей средой. При этом восстановление окислительного компонента коррозионной среды протекает не одновременно с ионизацией атомов металла и от электродного потенциала металла зависят их скорости. Первопричиной электрохимической коррозии является термодинамическая неустойчивость металлов в окружающих их средах. Ржавление трубопровода, обивки днища морского суда, различных металлоконструкций в атмосфере — это, и многое другое, примеры электрохимической коррозии.
К электрохимической коррозии относятся такие виды местных разрушений, как питтинги, межкристаллитная коррозия, щелевая. Кроме того процессы электрохимической коррозии происходят в грунте, атмосфере, море.
- Механизм электрохимической коррозии может протекать по двум вариантам:
- 1) Гомогенный механизм электрохимической коррозии:
- — поверхностный слой мет. рассматривается как гомогенный и однородный;
- — причиной растворения металла является термодинамическая возможность протекания катодного или же анодного актов;
- — К и А участки мигрируют по поверхности во времени;
- — скорость протекания электрохимической коррозии зависит от кинетического фактора (времени);
- — однородную поверхность можно рассматривать как предельный случай, который может быть реализован и в жидких металлах.
- 2) Гетерогенный механизм электрохимической коррозии:
— у твердых металлов поверхность негомогенная, т.к. разные атомы занимают в сплаве различные положения в кристаллической решетке;
— гетерогенность наблюдается при наличии в сплаве инородных включений.
Электрохимическая коррозия имеет некоторые особенности: делится на два одновременно протекающих процесса (катодный и анодный), которые кинетически зависимы друг от друга; на некоторых участках поверхности электрохимическая коррозия может принять локальный характер; растворение основного мет. происходит именно на анодах.
Поверхность любого металла состоит из множества короткозамкнутых через сам металл микроэлектродов. Контактируя с коррозионной средой образующиеся гальванические элементы способствуют электрохимическому его разрушению.
- Причины возникновения местных гальванических элементов могут быть самые разные:
- 1) неоднородность сплава
- — неоднородность мет. фазы, обусловленная неоднородностью сплава и наличием микро- и макровключений;
- — неравномерность окисных пленок на поверхности за счет наличия макро- и микропор, а также неравномерного образования вторичных продуктов коррозии;
- — наличие на поверхности границ зерен кристаллов, выхода дислокации на поверхность, анизотропность кристаллов.
- 2) неоднородность среды
- — область с ограниченным доступом окислителя будет анодом по отношению к области со свободным доступом, что ускоряет электрохимическую коррозию.
- 3) неоднородность физических условий
- — облучение (облученный участок — анод);
- — воздействие внешних токов (место входа блуждающего тока — катод, место выхода — анод);
— температура (по отношению к холодным участкам, нагретые являются анодами) и т. д.
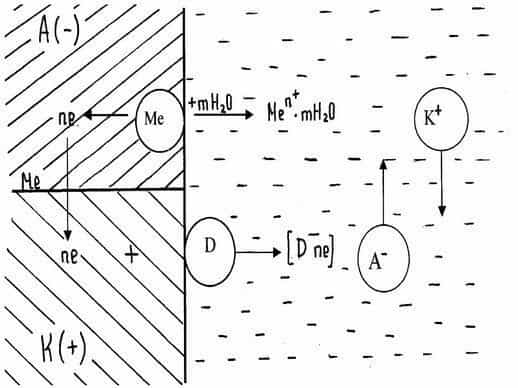
- При работе гальванического элемента одновременно протекает два электродных процесса:
- Анодный — ионы металла переходят в раствор
- Fe → Fe2+ + 2e
- Происходит реакция окисления.
Катодный — избыточные электроны ассимилируются молекулами или атомами электролита, которые при этом восстанавливаются. На катоде проходит реакция восстановления.
- O2 + 2H2O + 4e → 4OH- (кислородная деполяризация в нейтральных, щелочных средах)
- O2 + 4H+ + 4e → 2H2O (кислородная деполяризация в кислых средах)
- 2 H+ + 2e → H2 (при водородной деполяризации).
- Торможение анодного процесса приводит к торможению и катодного.
- Коррозия металла происходит именно на аноде.
При соприкосновении двух электропроводящих фаз (например, мет. — среда), когда одна из них заряжена положительно, а другая отрицательно, между ними возникает разность потенциала. Это явление связано с возникновением двойного электрического слоя (ДЭС). Заряженные частицы располагаются несимметрично на границе раздела фаз.
Скачек потенциалов в процессе электрохимической коррозии может происходить из-за двух причин:
При достаточно большой энергии гидратации ионы металла могут отрываться и переходить в раствор, оставляя на поверхности эквивалентное число электронов, которые определяют ее отрицательный заряд. Отрицательно заряженная поверхность притягивает к себе катионы мет. из раствора. Так на границе раздела фаз возникает двойной электрический слой.
На поверхности металла разряжаются катионы электролита. Это приводит к тому, что поверхность мет. приобретает положительный заряд, который с анионами раствора образует двойной электрический слой.
Иногда возникает ситуация, когда поверхность не заряжена и, соответственно, отсутствует ДЭС. Потенциал, при котором это явление наблюдается называется потенциалом нулевого заряда (φN). У каждого металла потенциал нулевого заряда свой.
Величина электродных потенциалов оказывает очень большое влияние на характер коррозионного процесса.
Скачок потенциала между двух фаз не может быть измерен, но при помощи компенсационного метода можно измерить электродвижущую силу элемента (ЭДС), который состоит из электрода сравнения (его потенциал условно принят за ноль) и исследуемого электрода.
В качестве электрода сравнения берется стандартный водородный электрод. ЭДС гальванического элемента (стандартный водородный электрод и исследуемый элемент) называют электродным потенциалом.
Электродами сравнения могут также выступать хлорсеребряный, каломельный, насыщенный медно-сульфатный.
Международной конвенцией в Стокгольме 1953г. решено при записях электрод сравнения всегда ставить слева. При этом ЭДС рассчитывать, как разность потенциалов правого и левого электродов.
- E = Vп — Vл
- Если положительный заряд внутри системы движется слева направо — ЭДС элемента считается положительной, при этом
- Emax=-(ΔGT)/mnF,
- где F — число Фарадея. Если положительные заряды будут двигаться в противоположном направлении, то уравнение будет иметь вид:
- Emax=+(ΔGT)/mnF.
- При коррозии в электролитах самыми распространенными и значимыми являются адсорбционные (адсорбция катионов или анионов на границе раздела фаз) и электродные потенциалы (переход катионов из металла в электролит или наоборот).
Электродный потенциал, при котором металл находится в состоянии равновесия с собственными ионами называется равновесный (обратимый). Он зависит от природы металлической фазы, растворителя, температуры электролита, активности ионов мет.
Равновесный потенциал подчиняется уравнению Нернста:
E=Eο+ (RT/nF) LnαMen+
где, Eο — стандартный потенциал мет.; R — молярная газовая постоянная; n — степень окисления иона мет.; Т — температура; F — число Фарадея;αMen+ — активность ионов мет.
При установленном равновесном потенциале электрохимическая коррозия не наблюдается.
Если по электроду проходит электрический ток — равновесное состояние его нарушается. Потенциал электрода изменяется в зависимости от направления и силы тока. Изменение разности потенц., приводящее к уменьшению силы тока, принято называть поляризацией. Уменьшение поляризуемости электродов называют деполяризацией.
Скорость электрохимической коррозии тем меньше, чем больше поляризация. Поляризация характеризуется величиной перенапряжения.
- Поляризация бывает трех типов:
- — электрохимическая (при замедлении анодного или катодного процессов);
- — концентрационная (наблюдается, когда скорость подхода деполяризатора к поверхности и отвода продуктов коррозии мала);
- — фазовая (связана с образованием на поверхности новой фазы).
Электрохимическая коррозия наблюдается также при контакте двух разнородных металлов. В электролите они образуют гальванопару. Более электроотрицательный из них будет анодом. Анод в процессе будет постепенно растворяться.
При этом идет замедление или даже полное прекращение электрохимической коррозии на катоде (более электроположительном).
Например, при контакте в морской воде дюралюминия с никелем интенсивно растворятся будет именно дюралюминий.
Коррозия металлов
Коррозия – это самопроизвольный окислительно-восстановительный процесс разрушения металлов и сплавов вследствие взаимодействия с окружающей средой.
Различают два вида коррозии – химическую и электрохимическую. Химическая коррозия обусловлена взаимодействием металлов с веществами, содержащимися в окружающей среде. В производственных условиях такими веществами, помимо О2, являются SO2, CO2, H2S, NH3 и др.
Химическую коррозию, обусловленную взаимодействием металлов с газами, называют газовой. Основной вклад в газовую коррозию металла вносит кислород воздуха. Различные металлы обладают различной устойчивостью по отношению к О2.
Некоторые металлы (Al, Cr, Zn, Pb, Sn) образуют на воздухе плотные пленки оксидов, не разрушающиеся при изгибе или нагревании.
Такие пленки защищают металл от дальнейшего доступа к нему газов и жидкостей, и процесс коррозии резко замедляется. Оксидные пленки других металлов (например, Fe) представляют собой рыхлые, пористые, механически непрочные образования.
Они не предохраняют металл от доступа к нему газов и жидкостей. Поэтому такие металлы корродируют особенно быстро.
- Процесс химической коррозии Fe схематически можно представить следующими уравнениями:
- 2Fe + O2=2FeO
- 4Fe + 3O2 = 2Fe2O3
- 3Fe + 2O2 =FeO · Fe2O3
- 4Fe + 3O2 +6H2O=4Fe(OH)3
- Fe(OH)3=t H2O+FeOOH (ржавчина)
Однако наибольший вред приносит не химическая, а электрохимическая коррозия, связанная с переходом электронов от одних участков металла к другим. Химическая коррозия сопровождает электрохимическую и усиливает ее.
Сущность электрохимической коррозии
Металлы обычно содержат примеси других металлов и неметаллов.
При соприкосновении таких металлов с электролитом (которым может служить Н2О, адсорбированная из воздуха, поскольку в ней как правило имеются ионы растворенных веществ) на поверхности металла возникает множество микрогальванических пар. В этих парах атомы более активного металла (обычно Fe) играют роль анода, а атомы менее активного – роль катода.
На катоде идет процесс восстановления молекул О2 в нейтральной и щелочной средах, или ионов Н+ – в кислой среде.
На аноде происходит окисление атомов металла, из которых состоит анод, с образованием катионов Men+.
Последние переходят в электролит (растворение анода) и соединяются с ионами ОН–, с образованием гидроксида Me(OH)n и других продуктов. Называемых ржавчиной. В результате металл, играющий роль анода, разрушается.
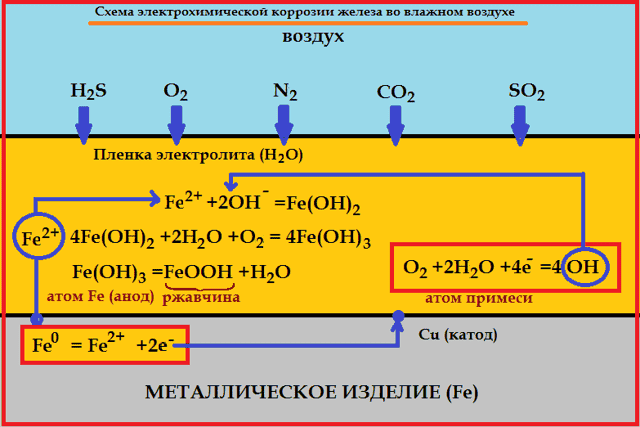
Скорость электрохимической коррозии тем больше, чем дальше друг от друга расположены металлы в ряду напряжений, и чем выше температура окружающей среды.
Чистые металлы устойчивы к коррозии.
Однако, так ка абсолютно чистым металлов нет, а также вследствие того, что гальваническая пара может быть образована отдельными участками одного и того же металла, находящимися в различных условиях (под разными электролитами или под одним и тем же электролитом разной концентрации), то электрохимическая коррозия имеет место всегда при соприкосновении металла с электролитом (атмосферной влагой).
Роль катода при электрохимической коррозии могут выполнять не только менее активные металлы, но и примеси неметаллов, способных принимать электроны.
Коррозия – процесс поверхностный и при отсутствии трещин внутри металла развиваться не может. Поэтому одним из способов защиты от коррозии является нанесение на поверхность металла металлических и неметаллических покрытий.
В качестве металлических покрытий используются пленки Au, Ag, Ni, Cr, Zn и других металлов, которые мало подвергаются коррозии из-за своей индифферентности или по причине образования прочных оксидных пленок. Некоторые из этих металлов (Au, Ag, Ni, Cr), помимо защитной, выполняют и эстетическую – придают изделиям приятный внешний вид.
Различают два вида металлических покрытий – анодное и катодное. Покрытие называется
- анодным, если оно изготовлено из металла более активного, чем защищаемый;
- катодным, если изготовлено из менее активного металла.
Примером анодных покрытий для изделий из железа являются пленки из Cr, Zn, примером катодных – пленки из Ni, Sn, Ag, Au. Катодные покрытия не защищают металлы в случае нарушения их целостности (трещины, царапины), так как при наличии электролита возникает гальваническая пара, роль растворимого анода в которой играет защищаемый металл.
Неметаллические покрытия также делятся на два вида: неорганические и органические. В качестве органических покрытий используются пленки лаков, красок, пластмасс, резины, битума, в качестве неорганических – эмали.
Протекторная защита заключается в соединении защищаемого изделия проводником с протектором – пластиной из более активного металла (Al, Mg, Zn). В процессе коррозии протектор служит анодом и разрушается, предохраняя от коррозии металлическое изделие или конструкцию.
Электрохимическая (катодная) защита заключается в соединении защищаемого изделия с катодом внешнего источника тока, вследствие чего изделие становится катодом. Анодом служит вспомогательный, обычно стальной, электрод (кусок металла), который и разрушается в процессе коррозии.
Метельский А.В. Источник: Метельский А.В., Химия в Экзаменационных вопросах и ответах, Минск, изд. «Беларуская энцыклапедыя», 1999 год Дата в источнике: 1999 год
Электрохимическая коррозия: причины, типы, скорость протекания
Электрохимическая коррозия относится к наиболее часто встречающимся процессам постепенного разрушения металла.
Как мы знаем, наше окружение наполнено электричеством.
В зависимости от среды, меняются показатели проводимости. Не отличается то, что при контакте с такой средой сталь начинает постепенно портиться.
- У процесса есть несколько важных отличий.
- В первую очередь – неодновременное протекание восстановления окислительного процесса и ионизации атомов металла.
- На интенсивность распространения при этом влияет такой параметр, как электродный потенциал металла.
Главная причина электрохимической коррозии в том, что большинство металлов проявляют термодинамическую неустойчивость.
- Примеры распространения коррозии такого типа встречаются в воде, почве, на открытом воздухе.
- Она часто становится причиной потери прочности и постепенного разрушения металла на днище судов, трубопроводов, опор ЛЭП и других объектов.
- Если говорить о типах электрохимической коррозии, то называют 3 разновидности:
- щелевые поражения;
- питтинги;
- межкристаллическое повреждение.
Повреждаться могут разные типы металлов в зависимости от их расположения. Ржавчина появляется при контакте со стоячей и текущей водой, в местах соединения разных металлов, а также на сварных швах.
Какие механизмы отвечают за протекание электрохимической коррозии
Такое повреждение металла проводится двумя механизмами – гомогенным и гетерогенным. Рассмотрим каждый из них подробно.
- Гомогенный. Первоначально затрагивается поверхностный слой металлического изделия. Постепенно металл начинает растворяться под действием актов – катодного или анодного. На протяжении определенного времени происходит миграция катода и анода. Со временем процесс ускоряется. Особенность гомогенного механизма в том, что затрагивает как твердые, так и жидкие металлы. Меняется только скорость течения.
- Гетерогенный. У большинства твердых металлов не наблюдается гомогенной поверхности. Это связано с тем, что в самом материале состав кристаллической решетки может отличаться. Также как и в описанном выше случае, формируется анодный и катодный процессы, металл начинает постепенно разрушаться.
У такого вида процесса есть несколько особенностей.
В первую очередь – четкое деление на катодный и анодный процесс. Один из основных факторов, влияющих на их скорость протекания относительно друг друга – это время.
Схема электрохимической коррозии
В зависимости от типа металла, коррозия может быть локализована на отдельных участках. Также наблюдается растворение поверхностного слоя на анодах, что позволяет поражению затронуть обширные площади.
Здесь появляется еще одна особенность протекания процесса – формирование гальванических элементов. Это происходит из-за специфики структуры поверхности, на которой присутствуют микроэлектроды.
Из-за чего начинает развиваться коррозия
После того, как мы рассмотрели суть электрохимической коррозии, пришло время обратить внимание на причины распространения коррозии.
Среди них три распространенные:
- Сплав имеет неоднородную структуру. В большинстве сплавов поверхность негомогенная, потому что в кристаллической решетке присутствуют посторонние включения. Ухудшает ситуацию и присутствие пор макро и микротипа. Это приводит к тому, что продукты коррозии также начинают образовываться неравномерно.
- Неоднородная среда, в которой находится металл. Чтобы коррозия протекла быстрее, важен фактор доступа окислителя. Электрохимическая реакция может быть ускорена.
- Отличие физических условий. Коррозия усиливается в том случае, если происходит облучение, в среде присутствуют блуждающие тока. Негативно влияет и температура, особенно при перепадах. В таком случае разница между холодными и теплыми местами становится причиной появления анода.
Именно по причине различия в критических факторах, скорость электрохимической коррозии может сильно меняться.
Главные внутренние факторы протекания электрохимической коррозии
На интенсивность распространения коррозийного поражения влияют две группы факторов – внешние и внутренние.
Текущее состояние поверхности металла
Когда поверхность металла неровная, коррозийный процесс протекает намного интенсивнее. Если на поверхности присутствуют небольшие выступы, они начинают накапливать воду.
- Это может негативно повлиять на интенсивность распространения.
- Чтобы не допустить такого фактора, важно использовать отшлифованный или отполированный металл.
- Когда сталь гладкая, вода не так сильно повреждает ее, потому что постепенно происходит формирование равномерной пленки по всей поверхности.
- Также хорошим средством для уменьшения поражения становится применение пассивирования, а также ряд других способов.
Степень термодинамической стойкости металла
Разные виды материалов отличаются разными показателями термодинамической устойчивости.
Наиболее стойкие разновидности материала не разрушаются при помещении в агрессивную среду.
Чтобы понять, есть ли у металла склонность к коррозии под действием термодинамических факторов, измеряют потенциал анодного и катодного процесса, а также изобарно-изотермического.
Именно такой фактор оказывает большое влияние на потенциальное воздействие среды на постепенное развитие коррозии.
К сожалению, у большинства представленных в продаже марок металлов стойкость невысокая. Есть и неустойчивые разновидности, у которых этот риск нивелируется благодаря склонности к образованию пассивных пленок на поверхности.
Кристаллографическая структура
Оказывает прямое воздействие на металл.
Как известно, атомы в кристаллической решетке располагаются по-разному. Лучше защищены те разновидности, у которых атомы упакованы неплотно.
Особенности решетки также учитывают при планировании защиты материала методом создания на нем специальных пленок. И пленка и сам основной материал должны четко соответствовать по составу друг другу или быть максимально приближенными.
В этом случае исключается появление напряжения, которое негативно отражается на текущем состоянии заготовки. Если контакт с агрессивной средой все-таки происходит, материал начинает разрушаться слой за слоем.
Гетерогенность
Этот фактор рассматривается в непосредственной связи с величиной зерна металла.
Если в сплаве есть выраженные анодные включения, они сильно влияют на ускорение протекания коррозии.
Катодные включения не столь опасны, потому что на интенсивности процесса не отражаются. Величина зерна как фактор риска рассматривается не так часто и этим показателем можно пренебречь.
Не стоит сбрасывать со счетов и механические факторы
Важно понимать, что многие конструкции из металла используются под постоянным напряжением.
К этой категории относится повышенное внутреннее напряжение, когда сильно увеличивается риск деформации.
Негативно влияют на качество металла также воздействие истирания, периодические контакты с другими металлическими изделиями.
- Такой фактор оказывает значительное влияние на интенсивность распространения повреждения.
- Даже если само сырье первоначально обладало стойкостью к потенциальным повреждениям, в таком случае она уменьшится – формируемые пленки просто не будут закрепляться на поверхности.
- Потому лучше сразу исключить это условие электрохимической коррозии – постараться не использовать металлоконструкции под пиковыми сильными нагрузками, не допускать возникновения трения и соприкосновения между собой стальных деталей.
Основные внешние факторы электрохимической коррозии
- Кроме внутренних, на металл также влияют и внешние факторы.
- Они могут не только ускорять, но и замедлять процесс, а также влиять на характер его протекания.
- К ним относятся следующие:
- Температура. Температура сильно влияет на то, как себя ведет металл в разных условиях. От нее сильно зависит то, насколько быстро будут растворяться вторичные продукты коррозии. Среди других особенностей – запуск и стимуляция диффузионных процессов в металле, создание перенапряжения на электродах и другие проявления. Когда металлическое изделие помещается в растворы с кислородной деполяризацией, по мере прогрева электролита диффузия окислителя ускоряется. На фоне этого наблюдается сильное снижение перенапряжения ионизации кислорода.
Если деталь помещается в растворы неокисляющихся кислот, наблюдается коррозия с водородной деполяризацией.
Повышение температуры уменьшает скорость распространения повреждений, потому что сильно снижается перенапряжение водорода.
Отдельно стоит отметить ситуацию, когда металл уже покрывается специальной защитной пленкой. В этом случае сам тип пленки будет влиять на то, как именно она поведет себя при контакте с разными видами внешних угроз, в том числе, с повышением температуры.
- Нагрев и охлаждение могут отразиться на состоянии катодов и анодов через их внутренние процессы.
- В некоторых случаях полярность электродов значительно меняется.
- Как мы уже отмечали выше, проблемы могу возникать из-за того, что разные участки детали нагреты до отличающихся друг от друга температур.
- В этом случае стремительно увеличивается количество термогальванических пар, стимулирующих распространение коррозии на новые участки.
- Уровень рН раствора, в который помещен металл. Такой показатель как рН указывает, насколько в растворе будут активными ионы водорода, и как быстро коррозия будет распространяться по материалу. Это опасно, потому что может непредсказуемо менять потенциал катодных процессов, формирование окисных пленок. Также создается значительное перенапряжение реакции на электродах. Рекомендуется не допускать контакта металла со средами, у которых показатель рН высокий.
- Если по каким-то причинам металлическая заготовка оказалась помещена в раствор, большое значение будет иметь скорость, с которой он движется, а также само наличие внутренних колебаний.
- Заранее определить точное воздействие будет сложно по той причине, что всегда непросто предсказать, как поведут себя нейтральные электролиты.
- Cчитается, что при смешении электролита, меняются показатели диффузии кислорода, что значительно отражается на процессе протекания коррозии.
- Можно уделять меньше внимания скорости движения электролита в том случае, если вы имеете дело со средами повышенной кислотности.
- На них подобное поражение оказывает минимум влияния.
Чем отличаются анодный и катодный процессы
Если вы внимательно проследите за тем, как работает гальванический элемент, то увидите, что в нем протекают сразу два связанных друг с другом процесса – анодный и катодный.
Рассмотрим их более подробно.
Анодный процесс
В химии показывается формулой Fe → Fe2+ + 2e. Она показывает, что постепенно запускается окисление, ионы металла начинают переход в раствор.
Катодный процесс
Может протекать по-разному.
В частности, переизбыток электронов решается ассимиляцией атомами электролита и его молекул. На фоне этого происходит восстановительная реакция непосредственно на самом катоде.
- Формула будет зависеть от того, в каких условиях протекает реакция.
- Так при наличии водородной деполяризации можно записать процесс как 2 H+ + 2e → H2.
- Важно понимать, что оба процесса сильно связаны друг с другом под влиянием кинетического фактора.
С течением времени может происходить взаимное замедление или ускорение анодного или катодного процесса. При этом сам анод всегда будет оставаться тем местом, на котором формируется коррозия металла.
Во время анализа протекания процесса коррозии часто обращают внимание на электропроводящие фазы и момент после их соприкосновения.
Обычно одна фаза имеет положительный заряд, в то время как другая – отрицательный. Это приводит к появлению разности потенциалов.
Таким образом возникает ДЭС или как его часто называют ученые – двойной электрический слой с ассиметричным расположением частиц в местах, где фазы разделяются.
Опасным для металла становится скачок потенциалов. Он может стимулироваться двумя центральными причинами:
- Большая накопленная энергия гидратации. В таком случае наблюдается отрыв ионов металла и постепенное перетекание их в раствор. На поверхности в результате остается аналогичное число электронов, заряд становится отрицательным. Далее, в соответствии с законами физики, наблюдается перетекание катионов из раствора, формируется ДЭС на границе, как мы уже описывали выше.
- Разряжение катионов электролита. В результате металл начинает стремительно принимать положительный заряд. ДЭС появляется из-за активности анионов раствора в контакте с катионами электролита.
- Что происходит в том случае, если поверхностный слой металла совсем не имеет определенного заряда?
- В таком случае ДЭС наблюдаться не будет, возникнет явление нулевого заряда.
- Его потенциал будет отличаться в зависимости от того, с каким металлом вам приходится работать.
- Описанный процесс значительно отражается на том, как протекает коррозия и как быстро она захватывает все новые и новые участки металла.
В современной науке нет средств, которые могли бы точно измерить величину скачка потенциала, значит и процесс формирования электродвижущей силы оказывается на таким интенсивным.
Если рассматривать вопросы, связанные с процессом поляризации, можно написать отдельную статью на эту тему.
Потому далее мы рассмотрим другой важный показатель – поляризацию.
Поляризация и ее влияние на скорость протекания коррозии
- Процесс поляризации связан с интенсивностью распространения электрохимической коррозии.
- Этот показатель отражает, насколько сильное перенапряжение наблюдается на определенном участке.
- Принято выделять три вида поляризации:
- Электрохимическая. Чаще всего наблюдается в ситуации, когда катодный и анодный процессы начинают замедляться.
- Фазовая. Возникает в том случае, если на поверхности материала формируется новая фаза.
- Концентрационная. Этот процесс появляется в том случае, если есть очень малые показатели скорости отвода продуктов коррозии, а также подхода деполяризатора.
Особенности поляризации также стоит учитывать в том случае, если вы заинтересованы в дополнительной защите металлов от постепенного разрушения.
Обеспечиваем эффективную защиту от коррозии
- Наша компания предлагает заказчикам защиту металлоконструкций разных типов от коррозии.
- Мы используем методику горячего цинкования.
- В пользу работы с нами говорит сразу несколько факторов:
- Опыт работы с 2007 года, есть постоянные заказчики.
- Большие производственные площади. Три цеха для горячего цинкования, мощность 120 тысяч тонн в год.
- Универсальность. Работаем со множеством видов изделий благодаря установленной на предприятии самой глубокой ванны в ЦФО – 3,43 метра.
Мы используем в процессе проверенное европейское оборудование.
Даем гарантию соответствия качества товаров требованиям ГОСТ 9.307-89.
Чтобы получить дополнительные консультации и ответы на интересующие вас вопросы, звоните нам или оставляйте заявку на сайте.
Вернуться к статьям
Электрохимическая коррозия металлов
Коррозия — это самопроизвольно протекающий процесс разрушения металлов в результате химического или электрохимического взаимодействия их с окружающей средой.
Электрохимическая коррозия — наиболее распространенный вид коррозии металлов, это разрушение металла в среде электролита с возникновением внутри системы электрического тока.
Примером коррозионных процессов электрохимического характера является разрушение деталей машин и различных металлических конструкций в почвенных, грунтовых, речных и морских водах, во влажной атмосфере, в технических растворах, под действием смазочно-охлаждающих жидкостей, применяемых при механической обработке металлов и т.д.
Причиной электрохимической коррозии является образование на поверхности металла большого количества микрогальванических пар, которые возникают по следующим причинам:
1. Наличие примесей металлов или других веществ, отличающихся по активности от основного металла.
2. Структурная неоднородность поверхности металла, что определяет наличие участков с разной активностью.
3. Неравномерность распределения деформаций в металле после термической и механической обработки и др.
- При электрохимической коррозии на поверхности металла одновременно протекают два процесса:
- — анодный — окисление металла: Ме — n? = Men+
- — катодный — восстановление ионов водорода в кислой среде:
- 2H+ + 2e = H2 или молекул кислорода, растворенного в воде, в случае атмосферной коррозии:
2H2O + O2 + 4? = 4OH-.
Ионы или молекулы, которые восстанавливаются на катоде, называются деполяризаторами. При атмосферной коррозии — коррозии во влажном воздухе при комнатной температуре — деполяризатором является кислород.
Пример 20. Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Решение. При таком контакте возникает коррозионный гальванический микроэлемент. Цинк имеет более отрицательный потенциал (-0,763 В), чем кадмий (-0,403) (табл. 12.1), поэтому он является анодом, а кадмий — катодом.
Анодный процесс: Zn — 2? = Zn2+ .
Катодный процесс: в кислой среде: 2H+ + 2? = H2 ;
в нейтральной среде: 2H2O + O2 + 4? = 4OH- .
Так как ионы Zn2+ с гидроксильной группой образуют нерастворимый гидроксид, то продуктом коррозии в нейтральной среде будет Zn(OH)2.
Скорость коррозии тем больше, чем сильнее различаются электродные потенциалы металлов, т.е. чем дальше они расположены друг от друга в ряду напряжений. Кроме того, скорость коррозии повышается при увеличении концентрации электролита и повышении температуры.
Защита от коррозии.
Все методы защиты условно делятся на следующие группы:
1. Легирование металлов. Это эффективный, хотя и дорогой метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты, вызывающие пассивность металла вследствие образования на их поверхностях прочных оксидных пленок. В качестве таких компонентов применяют хром, никель, вольфрам и др.);
2. Защитные покрытия (металлические, неметаллические). Металлические покрытия подразделяются на анодные и катодные.
При анодном покрытии металл покрывается более активным металлом, расположенным в ряду напряжения левее, например железо – цинком, и вэтом случае при коррозии идет окисление цинка.
При катодном покрытии металл покрывается менее активным металлом, например железо — оловом, и в этом случае при коррозии тдет окисление железа;
3. Электрохимическая защита (этот метод основан на торможении анодных или катодных реакций коррозионного процесса. Защита осуществляется присоединением к защищаемой конструкции металла с более отрицательным значением электродного потенциала — протектора, а также катодной или анодной поляризацией за счет тока от внешнего источника);
4. Изменение свойств коррозионной среды. Для снижения агрессивности среды уменьшают концентрацию компонентов, опасных в коррозионном отношении, например снижают концентрацию Н+- ионов – подщелачивание, удаляют кислород и др.
Пример 21. Какие процессы протекают при коррозии оцинкованного и луженого железа?
а) в кислой среде;
б) на воздухе?
Решение. 1. Оцинкованное железо получают, покрывая железо тонким слоем цинка. При таком контакте возникает гальванический элемент. Цинк имеет более отрицательный потенциал (-0,763 В), чем железо (-0,44 В) (табл. 7.1), поэтому он является анодом, а железо — катодом. а) Схема ГЭ записывается в кислой среде:
(-) Zn ½ HCl ½ Fe (+).
Анодный процесс: Zn — 2? = Zn2+ ;
катодный процесс: 2H+ + 2? = H2 .
Следовательно, цинк в этом случае корродирует вместо железа. Подобная защита металла, при которой он играет роль катода в процессе электрохимической коррозии, называется катодной защитой, а цинк в этом случае является анодным покрытием.
б) Для коррозии на воздухе схема ГЭ: (-) Zn ½ H2O, O2 ½ Fe (+).
Анодный процесс: Zn — 2? = Zn2+ ;
катодный процесс: 2H2O + O2 + 4? = 4OH-.
Цинк защищает железо от коррозии даже после нарушения целостности покрытия.
2. Так называемую «белую жесть» получают, покрывая тонким слоем олова листовое железо. Сравнение электродных потенциалов железа (-0,44 В) и олова (-0,13 В) показывает, что железо окисляется легче олова, поэтому железо в этой паре играет анода.
a) В кислой среде: (-) Fe ½ HCl ½ Sn (+).
Анодный процесс: Fe — 2?= Fe2+ ;
катодный процесс: 2H+ + 2? = H2 .
б) Во влажной атмосфере: (-) Fe ½ H2O, O2 ½ Sn (+).
Анодный процесс: Fe — 2?= Fe2+ ;
катодный процесс: 2H2O + O2 + 4? = 4OH-.
- Суммарный процесс: 2Fe + 2H2O + O2 = 2Fe2+ + 4OH-.
- 2Fe + 2H2O + O2 = 2Fe(OH)2 (продукт коррозии).
- 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 .
Олово защищает железо лишь до тех пор, пока защитный слой остается неповрежденным. Стоит только его повредить, как на железо начинают воздействовать воздух и влага.
Олово даже ускоряет коррозию железа, потому что служит катодом в электрохимическом процессе коррозии.
Подобная защита металла, при которой он играет роль анода в процессе электрохимической коррозии, называется анодной защитой, а олово в этом случае является катодным покрытием.
Пример 22. Как будет протекать процесс коррозии в том случае, если железную водосточную трубу прибить к дому алюминиевыми гвоздями?
Решение. Сравнение электродных потенциалов железа (-0,44 В) и алюминия (-1,7 В) показывает, что алюминий этой паре является анодом, а железо — катодом. Схема ГЭ:
(-) Al ½ H2O, O2 ½ Fe (+).
Таким образом, вблизи алюминиевого гвоздя труба будет защищена от коррозии. Однако алюминиевый гвоздь должен в этих условиях быстро корродировать, и в конце концов труба упадет. Продуктом коррозии будет белый порошок гидроксида алюминия.
Анодный процесс: Al — 3? = Al3+ , х4
катодный процесс: 2H2O + O2 + 4? = 4OH-. х3
Суммарный процесс: 4Al + 6H2O + 3O2 = 4Fe2+ + 12OH-.
4Al + 6H2O + 3O2 = 4Al(OH)3 (продукт коррозии).
Лекция 2. Электрохимическая коррозия
Электрохимическая коррозия металлов – одна из насущных проблем человечества с того момента, как в производстве различных, необходимых человеку предметов, стали использоваться изделия из металла.
Проблема защиты металлов от коррозии всегда стояла остро, потому что под действием разрушительных процессов окисления предметы теряли функциональность, деформировались и приходили в негодность, и нужно было искать способы их защиты.
Когда химия выделилась в отдельную науку, а использование металлов стало приобретать широкое промышленное значение, человечество начало исследовать эти процессы и искать способы борьбы с разрушениями от внешних воздействий.
Химическая коррозия
Она возникает обычно при воздействии на металлическую структуру сухих газов, жидкостей или растворов, не проводящих электрический ток. Суть этого типа коррозии – прямое взаимодействие металла с агрессивной средой.
Элементы химически корродируют во время термической обработки или в результате длительной эксплуатации при достаточно высоких температурах. Это касается лопаток газовых турбин, арматуры плавильных печей, деталей двигателей внутреннего сгорания и так далее.
В результате на поверхности образуются определенные соединения: оксиды, нитриды, сульфиды.
Сплавы с магнием и кремнием
Такие материалы чаще всего применяются в машиностроении и в строительстве. Mg2Si делают сплавы этой разновидности очень прочными. Иногда составляющим подобных элементов является и медь. Ее также вводят в сплав для упрочения.
Однако добавляют медь в такие материалы в очень небольших количествах. Иначе антикоррозийные свойства алюминиевого сплава могут сильно понизиться. Межкристаллическое ржавление в них начинается уже при добавлении свыше 0.5% меди.
Также склонность к коррозии у таких материалов может возрастать при неоправданном увеличении количества входящего в их состав кремния. Это вещество добавляют в алюминиевые сплавы обычно в таких пропорциях, чтобы после образования Mg2Si не оставалось ничего лишнего. Кремний в чистом виде содержат лишь некоторые материалы этой разновидности.
Электрохимическая коррозия: примеры
Ее разделяют на:
- Атмосферную, которая возникает при наличии на поверхности металла жидкостной пленки, в которой газы, содержащиеся в атмосфере (например, О2, СО2, SO2), способны растворяться с образованием электролитных систем.
- Жидкостную, которая протекает в токопроводящей жидкой среде.
- Грунтовую, что протекает под воздействием грунтовых вод.
Материалы естественного происхождения
Не действуют на алюминий:
- Каменная соль.
- Продукты нефтеперегонки: бензин, керосин, парафин, масла, смолы.
- Воск.
- Каучук.
- Эфирные масла.
- Каменный уголь, антрацит, бурый уголь.
- Целлюлоза.
- Белки.
- Природный гипс.
- Особо чистые виды нефти.
Действуют на алюминий:
- Нефть, а точнее — содержащиеся в ней загрязнения, в основном, вода с растворенными в ней солями, которые в результате гидролиза образуют кислоты.
- Дубильные вещества.
- Средства для импрегнации древесины.
- Глина.
Причины
Поскольку обычно любой металл, который используется для промышленных нужд, не является идеально чистым и содержит включения различного характера, то электрохимическая коррозия металлов возникает вследствие образования на поверхности железа большого количества короткозамкнутых локальных гальванических элементов.
Появление их может быть связано не только с наличием различных (особенно металлических) примесей (контактная коррозия), но и с неоднородностью поверхности, дефектами кристаллической решетки, механическими повреждениями и тому подобное.
Механизм взаимодействия
Процесс электрохимической коррозии зависит от химического состава материалов и особенностей внешней среды.
Если так называемый технический металл покрыт влажной пленкой, то в каждом из указанных гальванических микроэлементов, которые образуются на поверхности, протекают две независимые реакции.
Более активный компонент коррозионной пары отдает электроны (к примеру, цинк в паре Zn-Fe) и переходит в жидкую среду в качестве гидратированных ионов (то есть корродирует) по следующей реакции (анодный процесс):
- М + nH2O = Mz+* nH2O + ze.
- Эта часть поверхности является отрицательным полюсом локального микроэлемента, где металл электрохимически растворяется.
- На менее активном участке поверхности, которая является положительным полюсом микроэлемента (железо в паре Zn-Fe), электроны связываются за счет протекания реакции восстановления (катодный процесс) по схеме:
- Ox + ze = Red.
Таким образом, наличие окислителей в водяной пленке, которые способны связывать электроны, обеспечивает возможность дальнейшего хода анодного процесса. Соответственно, электрохимическая коррозия может развиваться только при условии одновременного протекания как анодного, так и катодного процессов. Вследствие торможения одного из них скорость окисления уменьшается.
Самодельный электрокультиватор своими руками видео






