- Основные виды классификации металлов
- Химическая классификация металлов
- Классификация металлов по кристаллической решетке
- Техническая классификация металлов
- Классификатор металлов по ГОСТ
- Классификация металлов
- Поиск сплава в классификаторе ГОСТ
- Сферы применения основных металлов
- Коротко по каждому виду, применяемому для изготовления крепежей
- Металлы
- Таблица Менделеева для чайников – HIMI4KA
- Периодический закон
- Группы и периоды Периодической системы
- Свойства таблицы Менделеева
- Лантаниды (редкоземельные элементы) и актиниды
- Галогены и благородные газы
- Переходные металлы
- Металлоиды
- Постпереходными металлами
- Неметаллы
- Виды металла: классификация и сферы применения
- Классификация металлов
- Черные
- Цветные
- Механические свойства металлов
- Прочность металлов
- Пластичность металлов
- Твердость
- Модуль продольной упругости
- Литература по прочности
- Основные виды сплавов
- Цинковые сплавы
- Алюминиевые сплавы
- Медные сплавы
- Свойства сплавов
- Физические свойства
- Химические свойства
- Механические свойства
- Технологические свойства
- Технологические и химические свойства твердых металлов
Металлы – обобщенное название химических элементов, объеденных по ряду признаков. В периодической таблице они занимают большую часть, однако до сих пор не существует документа, позволяющего разделить их на классы.
Отличаются металлы в первую очередь своими качественными характеристиками. Какие-то имеют высокую теплопроводимость, другие выдерживают высокие нагрузки на разрыв и растяжение.
В зависимости от этих качеств определяется и сфера применения, но металлы в природном виде, даже очищенные, не обладают необходимыми показателями в достаточном виде, поэтому применяется технология сплавов, то есть соединения нескольких элементов в одну молекулярную решетку. Это позволяет существенно улучшить характеристики, и придать сплаву необходимые качества.
Простой пример: возьмем распространенный в промышленности сплав бронзу. Это соединение, где основным элементом выступает медь. В качестве легирующего, то есть улучшающего качество, компонента используется олово. В результате соединения получается новый металл, более твердый и упругий по сравнению с чистой медью, который часто используют для изготовления крепежа.
Основные виды классификации металлов
Существует несколько видов классификации металлов. Начнем с основного типа – деления на две большие группы: черные и цветные. Черные металлы отличает высокая температура плавления, плотность и повышенная твердость. Цветные металлы, в большинстве случаев, плавятся при более низких температурах и обладают повышенной электро и теплопроводимостью.
Такое разделение обусловлено распространением элементов в природе. На добычу черных элементов приходится более 90 процентов от всей массы добываемых металлов, в то время как на цветную группу приходится не более 5-10 процентов.
Необходимо отметить, что виды классификации являются условными, и используются в зависимости от назначения конечного продукта, который производят из этих металлов.
Так, для изготовления крепежа используется классификация по техническим характеристикам, а для изготовления сложных сплавов химическая и кристаллическая. Рассмотрим эти виды подробнее.
Химическая классификация металлов

Все элементы в периодической таблице делятся на четыре основных группы, маркируемые латинскими буквами:
- S. Отмечены розовым цветом.
- P. Желтые элементы.
- D. Бирюзовый цвет.
- F. Зеленые элементы в таблице.
Каждая группа содержит в себе металлы. Элементы из первых двух категорий (S и P) называют простым видом, а элементы из групп D и F переходным. Также каждая группа делится еще на несколько категорий. В группу S входят щелочные и щелочеземеленые металлы, а в группы D и F платиновые, урановые и редкоземельные.
При этом в каждой группе существуют исключения, из чего можно сделать вывод, что деление металлов по химическим группам является условностью, и редко применяется в практических сферах. Такое деление интересно только для научных изысканий, и практически не применимо в промышленности и производстве.
Например, изготовление крепежа отталкивается от технических аспектов, и лишь в малой степени от химических.
Классификация металлов по кристаллической решетке
Все элементы имеют, так называемую, кристаллическую решетку. Абстрактная структура, определяющая расположение атомов и электронов, а также их привязку к ядру.
В аморфных материалах, таких как стекло, атомы расположены хаотично, и не имеют строгой конструкции. В отличие от металлов, которые в твердом виде обладают строго структурированной решеткой, с четким построением молекулярных элементов.
Всего разделяют 4 вида кристаллических решеток, которые проще представить в виде таблицы:
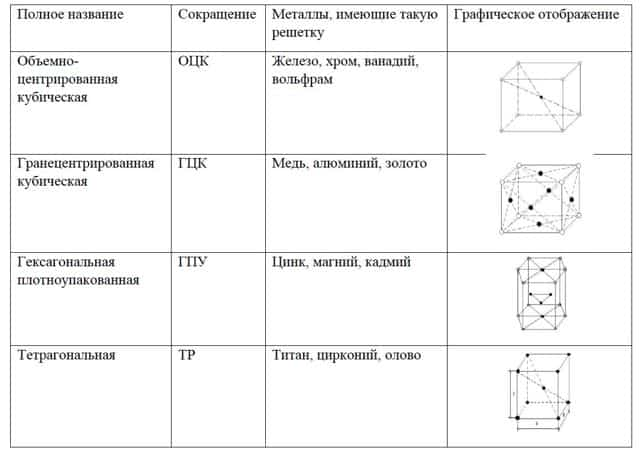
Это наиболее распространенные типы кристаллических решеток, часто встречающиеся у металлов. В общей сложности система классификации насчитывает 14 конфигураций, но у металлов они или встречаются крайне редко, или не встречаются вообще.
Также следует отметить, что правильное построение решетки возможно только при естественном затвердевании металла, без искусственных ускорений. Если процесс остывания был ускорен, форма решетки изменится.
В производстве это называют закаливанием, в результате которого меняется не только молекулярная структура, но и технические свойства.
Также, при нарушении норм производства металлического проката, может наблюдаться замена в кристаллической решетке. Это ведет к полному изменению качеств готового изделия. Чтобы условия производства соблюдались, были разработаны нормы стандартизации, гарантирующие четкое соответствие готового проката техническому описанию его свойств.
Техническая классификация металлов
Наиболее полную систему классификации предложил профессор Гуляев, хотя современные ученые и не согласны с некоторыми ее аспектами, ничего нового пока предложено не было. Итак, черные металлы делят на 5 основных подгрупп:
- Железные металлы. Сюда входят марганец, кобальт, никель, и конечно, железо. Наиболее распространенная в природе группа, используемая в сплавах как основной компонент.
- Тугоплавкие. Элементы, имеющие высокую температуру расплавления. В качестве эталона принята мера в 1539 градусов по Цельсию.
- Редкоземельные. Дорогостоящие в плане добычи и обработки элементы, к которым относят неодим, европий, самарий и другие металлы, используемые в качестве присадок к основному сплаву. Способны даже при небольшом проценте вмешательства существенно повысить или полностью изменить характеристики сплава.
- Щелочные. Особая группа, практически не применяемая в чистом виде. Чаще всего используются в атомной энергетике. Сюда относят: литий, барий, радий и другие.
- Урановые. Торий, уран, плутоний. Применяются исключительно в атомной энергетике.
Цветные металлы также делят на несколько подгрупп. Их три:
- Легкие. Алюминий, магний, бериллий. Обладают низким удельным весом и часто применяются в авиастроении и прочих сферах, где необходим твердый, но в то же время легкий материал.
- Легкоплавкие. Металлы с наиболее низкой температурой плавления: цинк, олово, свинец. Используются как в чистом виде, в качестве припоя и соединительного элемента, и как легирующие добавки, повышающие или изменяющие характеристики сплава.
- Благородные или драгоценные металлы. Наиболее редкие элементы, к которым относят: золото, серебро, палладий, платину. Обладают максимальной устойчивостью к коррозии и окислению, благодаря чему получают широкое распространение в различных промышленных сферах.
Практически все металлы из двух групп поддаются смешению, то есть производству из них сплавов с необходимыми техническими характеристиками.
Классификатор металлов по ГОСТ
Если рассматривать метлы с точки зрения геологии и распространения в природе, их делят на две большие группы: черные и цветные. Об этом мы уже говорили выше. В химии деление происходит по 4 направлениям, но чтобы привести виды металлов к общему знаменателю, необходимо более точное разделение.
Начнем с основного типа классификации: металлы и сплавы. Металлы – это материалы, используемые в чистом, или практически чистом виде. Здесь допускаются примеси, но в незначительной степени, то есть те, которые не способны оказать влияния и изменить технические характеристики.
Сплавами называют соединения, с высоким содержанием двух и более элементов.
Для того чтобы сплав получил маркировку, в его составе должно быть не менее 50 процентов основного компонента.
То есть, если мы берем бронзу, то понимаем, что в ее составе больше половины занимает медь, а остальное делится между другими металлическими компонентами. Чистые металлы, в свою очередь, делятся на стали и чугуны.
Эти металлы имеют в составе углерод. Если его содержание не превышает 2,14 %, его называют сталью. Свыше этого значения уже чугун.
Классификация металлов
Чтобы привести все виды металлов к единому стандарту качества, необходимо разделить их на группы. Таких групп 3:
- Стали,
- Чугуны,
- Сплавы на основе цветных металлов.
Каждая группа имеет деление на подгруппы. У стали это:
- углеродистая,
- легированная,
- специальная.
Углеродистая сталь не имеют легирующих, то есть изменяющих структуру элементов. Допускаются примеси, но в незначительном количестве. Углеродистая сталь в свою очередь делится на инструментальную и конструкционную. Кардинальные различия заключаются в процентах содержания в составе углерода.
Конструкционная сталь содержит не более 0,6%, а инструментальная от 0,7 до 1,5%. Далее конструкционная сталь делится на обычное качество и высокое. В обычном качестве допускаются примеси серы и фосфора, но в количестве, не превышающем 0,3 процента.
Соответственно высококачественная сталь не предусматривает наличия этих элементов в составе, или их количество должно быть меньше установленной нормы.
Далее легированная сталь, то есть материал, имеющий в составе компонент, влияющий на качественные характеристики сплава. Список легирующих элементов довольно большой, и здесь его приводить не имеет смысла.
Содержание легирующего элемента начинается от 2,5%. Такая сталь называется низколегированной.
Если в составе от 2,5 до 10 процентов, это уже среднелегированная марка, а при содержании свыше 10 процентов, получается высоколегированная сталь.
Помимо этого легированные стали делятся по назначению. Здесь три группы:
- инструментальная,
- конструкционная,
- специальная
В стандартизации каждый элемент имеет буквенное обозначение, а для причисления легированной стали к тому или иному классу используется отдельный список. Все легированные стали обозначаются сочетанием букв и цифр. Для примера рассмотрим такое соединение: 10Г2СД.
Первая цифра здесь – это количество углерода в сотых долях процента. Далее буква Г, в классификаторе означающая марганец. Следующая за буквой Г цифра 2 говорит нам о том, что марганец в этом составе присутствует в двухпроцентной доле. И последние две буквы – это дополнительные элементы, процентная доля которых менее 1,5%. В данном случае сюда добавлены медь и кремний.
Последний вид стали – специальный. Он делится на несколько групп:
- строительная,
- подшипниковая,
- арматурная,
- котельная,
- автоматная.
Соответственно для каждой группы имеются свои стандарты.
Далее идут чугуны, делящиеся на три группы:
- белый,
- отбеленный,
- и графитизированный.
У каждой группы также имеется свое разделения, но наибольший интерес представляет графитизированный чугун, который делится на:
- серый,
- вермикулярный,
- ковкий
- и высокопрочный.
- Отношение к какой-либо группе определяется процентным соотношением углерода к металлу в составе, а также наличию примесей, допустимых стандартами, то есть ГОСТами.
- И, наконец, последняя крупная группа – сплавы на основе цветных металлов. Здесь очень много разделений и видов классификации, поэтому остановимся на трех основных категориях, и представим их в виде таблиц:
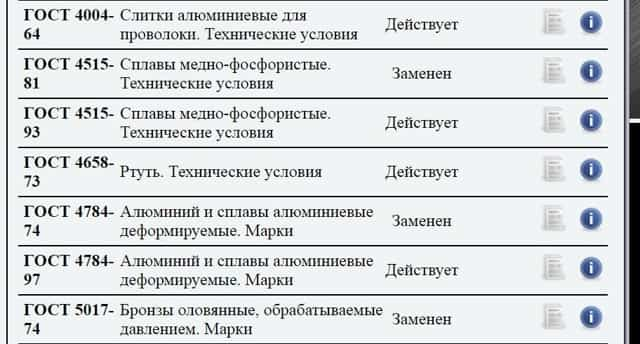
- Алюминиевые сплавы:
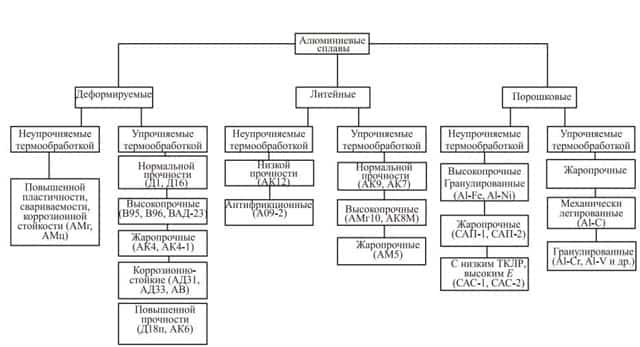
Медные сплавы:
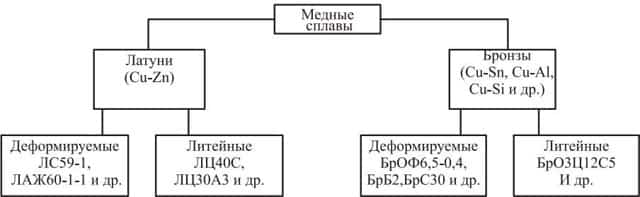
Поиск сплава в классификаторе ГОСТ
Государственные стандарты четко определяют не только виды металлов и сплавов, но и качество производства заготовок для дальнейшей обработки и производства металлоизделий. Реестр очень большой, и первый пункт, который нам нужен – металлы и металлические изделия.
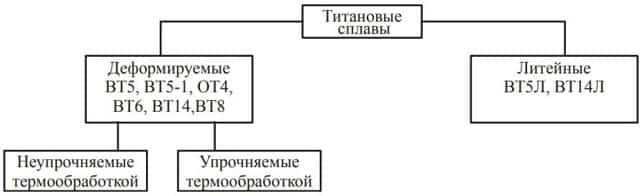
Далее переходим в необходимый раздел. Углеродистая и качественная сталь имеет маркировку В2 и В3 соответственно, а цветные металлы и их сплавы находятся в разделе В5. Также имеет смысл поискать в разделе В8, где перечислены стандарты литейных отливок.

Если мы говорим про изготовление крепежа, наибольший интерес представляет раздел В5, а внутри него подраздел В51.

Перед нами открывается список всех ГОСТов, связанных с этими определениями.

Он довольно большой, и не зная конкретного номера найти необходимую статью довольно сложно. Если же номер известен изначально, то на сайте ГосСтандарта есть готовый поиск, куда необходимо внести свой номер, чтобы сразу получить доступ к необходимому элементу.
Сферы применения основных металлов
Рассматривать радиоактивные и редкоземельные металлы не имеет смысла, так как в производстве крепежа они практически не принимают участия, как и в других сферах, не связанных с атомной энергетикой и некоторыми редкими видами промышленности. Нас интересуют основные металлы и сплавы рассмотренные выше.
Сферы их применения очень разнообразны:
- строительство,
- авиастроение,
- машиностроение,
- производство инструментов,
- металлоконструкции,
- станкостроение.
И так далее. Изготовление крепежа можно отнести нескольким категориям, но по сути, это металлоконструкции, называемые в народе Метизы. Для производства метизов используются десятки различных металлов и сплавов, от конструкционной стали и чугуна, до сложных сплавов на основе титана и меди.
Коротко по каждому виду, применяемому для изготовления крепежей
Перед тем как перейти к описанию конкретных видов металлов и сплавов, необходимо определиться, какие основные технические требования предъявляются к продуктам, попадающим под категорию «крепеж». Их несколько:
- прочность учитывается прочность на разрыв и излом.
- Пружинистость. Возможность металла возвращать изначальную форму после сжатия.
- Устойчивость к коррозии и окислению. Актуально для всех видов крепежа.
И многое друге. Теперь поговорим о конкретных металлах и сплавах. Их список выглядит следующим образом:
- Алюминий и сплавы на его основе,
- Медь,
- Латунь,
- Бронза,
- Инструментальная сталь,
- Легированная сталь,
- Ковкий чугун,
- Сталь нержавеющая.
Начнем по порядку: первый пункт – это алюминий и сплавы на его основе. Он применяется при изготовлении клепок и различных зажимов. Также в клепках может быть использована медь для повышения качества метиза. Помимо этого из меди изготавливают гайки специального назначения. Они используются, в частности, при судостроении, так как медь при контакте с другими металлами не создает искру.
Латунь и бронза отличаются повышенной, по сравнению с медью, прочностью, поэтому из них изготавливают различные шпонки, элементы анкеров, а также болты, шурупы и винты. Еще одна особенность этих сплавов заключается в отсутствии скипания. То есть при электрическом замыкании, сталь сплавляется, а медь остается цельной и не разрушается.

Из легированной и конструкционной стали изготавливаются барашковые гайки, струбцины и прочие удерживающие элементы. Это обусловлено высокой прочностью этих марок. Нержавеющая сталь, в свою очередь применяется там, где необходима максимальная устойчивость к коррозии. Что касается чугуна, то он чаще всего применяется при производстве запорной арматуры, то есть вентилей и запоров.
Металлы


Средняя оценка: 4
Всего получено оценок: 1819.
Средняя оценка: 4
Всего получено оценок: 1819.
К металлам относится большая часть элементов периодической системы – 82 химических элементов. Какими свойствами они обладают, и чем отличаются от неметаллов?
Металлами называют группу элементов, в виде простых веществ, которые обладают металлическими свойствами (пластичность, ковкость, блеск, электронная проводимость и т. д.)
Основное отличие элементов-металлов – они обладают только восстановительными свойствами, а в реакциях могут только окисляться. В соединениях они могут иметь только положительные степени окисления как в элементарных положительно заряженных ионах, так и в сложных ионах, где они образуют положительные центры.
Рис. 1. Список металлов.
Как правило, на внешнем уровне элементов металлов находится небольшое число электронов (1-3), значения электроотрицательности невысокие.
К металлам относятся все s-элементы (кроме водорода и гелия), d- и f-элементы, а также p-элементы под чертой бор-астат. Для типичных металлов характерен большой размер атомов, что способствует легкости отдачи валентных электронов.
Образующиеся положительные ионы устойчивы, так как имеют завершенную внешнюю электронную оболочку.
Все металлы, кроме ртути, при нормальных условиях в виде простых веществ находятся в твердом агрегатном состоянии и образуют металлическую кристаллическую решетку.
 Рис. 2. Металлы в таблице Д.И. Менделеева.
Рис. 2. Металлы в таблице Д.И. Менделеева.
В следующей таблицы представлены группы основных металлов:
| Группа металлов | Металл |
| Щелочные | литий, натрий, калий и т.д. |
| Щелочноземельные | кальций, стронций, барий и т.д. |
| Переходные | уран, титан, железо, платина и т.д. |
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Металлы пластичны и ковки, особенно если на внешнем электронном уровне атомов по одному электрону: слои атомов перемещаются относительно друг друга без разрушения кристаллической решетки (щелочные металлы, медь, серебро, золото). В атомах непластичных хрупких металлов хрома и марганца – большое число валентных электронов.
Плотность, твердость, температура плавления металлов изменяются в широком диапазоне и зависят от атомной массы, строения атома и геометрии кристаллической решетки. Самый легкий металл – литий (плотность 0,53 г/см3), самый тяжелый – осмий (плотность 22,5 г/см3). Металлы с плотностью больше 5 г/см3 относят к тяжелым, меньше 5 г/см3 – к легким металлам.
Самая низкая температура плавления у ртути (-39 градусов по Цельсию), самый тугоплавкий металл – вольфрам (температура плавления 3410 градусов по Цельсию.) Энергия атомизации вольфрама составляет 836 кДж/моль, а температура кипения его 5930 градусов.
Металлы вступают в реакцию как с простыми, так и со сложными веществами. Как типичные восстановители металлы реагируют почти со всеми неметаллами-окислителями (кислород, сера, азот и т. д.):
Также металлы реагируют с такими сложными веществами, как оксиды и гидроксиды, разбавленные растворы кислот, с растворенными в воде щелочами.
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются; в пределах одной и той же группы (в главной подгруппе) металлические свойства усиливаются, а неметаллические ослабевают
 Рис. 3. Металлы главных подгрупп.
Рис. 3. Металлы главных подгрупп.
Самый распространенный на земле элемент-металл – алюминий. За ним следуют железо, кальций, натрий.
Некоторые металлы встречаются в природе в самородном состоянии (золото, ртуть, платина), но в основном они находятся в природе в виде оксидов и солей.
Получение металлов происходит с помощью металлургии (получение из руд), пирометаллургии (получение с помощью реакции восстановления при высокой температуре), гидрометаллургии (извлечение из руд в виде растворимых соединений), электрометаллургии (получение металлов электролизом расплавов и растворов их соединений).
Металлы – вещества, которые обладают высокой электро- и теплопроводностью, ковкостью, пластичностью и металлическим блеском. В данной статье по химии 9 класса рассматриваются их физические и химические свойства, формулы класса металлов, а также способы получения.
Чтобы попасть сюда — пройдите тест.
Средняя оценка: 4
Всего получено оценок: 1819.
А какая ваша оценка?
Гость завершил
Тест на тему «Социализация»с результатом 6/10
Гость завершил
Тест на тему «Ускорение»с результатом 3/5
Гость завершил
Тест «Толстый и тонкий»с результатом 7/8
Гость завершил
Тест «Тихое утро»с результатом 9/10
Гость завершил
Тест «Бирюк»с результатом 10/12
Не подошло? Напиши в х, чего не хватает!
Таблица Менделеева для чайников – HIMI4KA
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории.
Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная.
Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
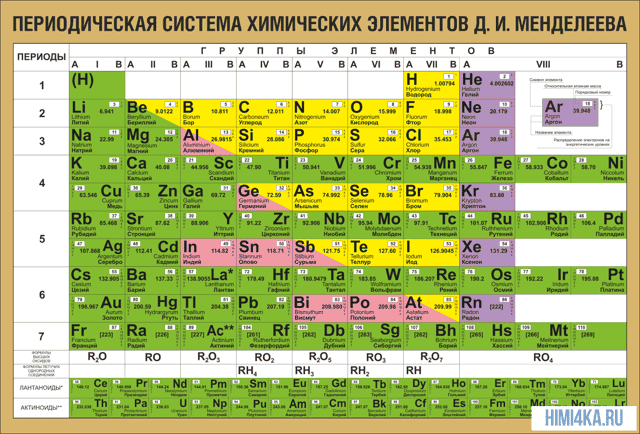 Периодическая система химических элементов Д. И. Менделеева
Периодическая система химических элементов Д. И. Менделеева
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом.
Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу.
Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме.
Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.

Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп.
Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов.
Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.

Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений.
В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы.
Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
- Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
- Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
- В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.

К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию.
Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами.
По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Показать / Скрыть текст
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы.
Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов.
Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
Показать / Скрыть текст
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке.
В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е.
ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
Показать / Скрыть текст
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Показать / Скрыть текст
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Показать / Скрыть текст
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску.
В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке.
Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
Показать / Скрыть текст
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
Показать / Скрыть текст
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Виды металла: классификация и сферы применения
Металлические изделия и детали используются в разных сферах промышленности. Существует множество видов металлов и каждый из них обладает сильными и слабыми сторонами. При изготовлении деталей для машин, самолётов или промышленного оборудования мастера обращают внимание на характеристики материала. Поэтому требуется знать свойства металлов и сплавов.
Свойства металлов и сплавов
Классификация металлов
Металлы разделяются на две большие группы — черные и цветные. Представители обоих видов различаются не только характеристиками, но и внешним видом.
Черные
Представители этой группы считаются самыми распространёнными и недорогими. В большинстве своем имеют серый или тёмный цвет. Плавятся при высокой температуре, обладают высокой твердостью и большой плотностью. Главный представитель этой группы — железо. Эта группа разделяется на подгруппы:
- Железные — к представителям этой подгруппы относится железо, никель и кобальт.
- Тугоплавкие — сюда входят металлы температура плавления которых начинается с 1600 градусов. Их применяют при создании основ для сплавов.
- Редкоземельные — к ним относятся церий, празеодим и неодим. Обладают низкой прочностью.
Существуют урановые и щелочноземельные металлы, однако они менее популярны.
Технические характеристики легированной стали 20Х13
Цветные
Представители этой группы отличаются яркой окраской, меньшей прочностью, твердостью и температурой плавления (не для всех). Разделяется эта группа на следующие подгруппы:
- Лёгкие — подгруппа, включающая в себя металлы с плотностью до 5000 кг/м3. Это такие материалы, как литий, натрий, калий, магний и другие.
- Тяжёлые — сюда относится серебро, медь, свинец и другие. Плотность превышает 5000 кг/м3.
- Благородные — представили этой подгруппы имеют высокую стоимость и устойчивость к коррозийным процессам. К ним относятся золото, палладий, иридий, платина, серебро и другие.
Выделяются тугоплавкие и легкоплавкие металлы. К тугоплавким относится вольфрам, молибден и ниобий, а к легкоплавким все остальные.
Механические свойства металлов
Прочность металлов
Прочность
— свойство твердых тел сопротивляется разрушению, а также необратимыми изменениями формы. Основным показателем прочности является временное сопротивление, определяемое при разрыве цилиндрического образца, предварительно подвергнутого отжигу.
- По прочности металлы можно разделить на следующие группы:
- непрочные металлы
- — (временное сопротивление не превышает 50 МПа) — олово, свинец, висмут, а также мягкие щелочные металлы.
- прочные металлы
- — (от 50 до 500 МПа) — магний, алюминий, медь, железо, титан и другие металлы, составляющие основу важнейших конструкционных сплавов
- высокопрочные металлы
- — (более 500 МПа) — молибден, вольфрам, ниобий и др.
- К ртути понятие прочности неприменимо, поскольку это жидкость.
- Временное сопротивление металлов указано в таблице 10.
- Таблица 10. Прочность металлов
| Металл | Временное сопротивление, МПа | Металл | Временное сопротивление, МПа |
| Титан | 580 | Цинк | 120-140 |
| Железо | 200-300 | Алюминий | 80-120 |
| Медь | 200-250 | Золото | 120 |
| Магний | 120-200 | Олово | 27 |
| Серебро | 150 | Свинец | 18 |
Пластичность металлов
Пластичность
Урок «Свойства и применение металлов»
— свойство твердых тел сохранять часть деформации при снятии нагрузок, которые их вызвали. В качестве показателя пластичности выборочно относительное удлинение, определяемое при тех же испытаниях, что и временное сопротивление.
- По степени пластичности металлы принято подразделять следующим образом:
- высокопластичные металлы
- — (относительное удлинение превосходит 40 %) — металлы, составляющие основу большинства конструкционных сплавов (алюминий, медь, железо, титан, свинец) и «легкие» металлы (натрий, калий, рубидий идр.)
- пластичные металлы
- — (относительное удлинение лежит в диапазоне между 3% и 40%) — магний, цинк, молибден, вольфрам, висмут и др. (наиболее обширная группа)
- хрупкие металлы
- — (относительное удлинение меньше 3%) — хром, марганец, кольбат, сурьма.
Высокая очистка хрупких металлов несколько повышает пластичность. Сплавы, полученные на их основе, почти не поддаются обработке давлением. Промышленные изделия из них часто получают путем литья. Относительное удлинение металлов характеризует таблица 11.
Таблица 11. Пластичность металлов
| Металл | Относительное удлинение, % | Металл | Относительное удлинение, % |
| Золото | 65 | Титан | 50 |
| Серебро | 65 | Олово | 40 |
| Свинец | 65 | Алюминий | 30-40 |
| Медь | 50-60 | Цинк | 30 |
| Железо | 40-50 | Магний | 10-22 |
Твердость
Твердость
— характеристика материала, отражающая его прочность и пластичность, определяемая путем вдавливания шарика (метод Бринелля) или призмы (метод Виккерса). Количественный оценкой твердости является число твердости НВ, равное отношению нагружения (Н) к площади поверхности отпечатка (мм2).
Значения твердости металлов по Бринеллю приведена в таблице 12.
Таблица 12. Твердость металлов
| Металл | НВ | Металл | НВ |
| Титан | 160 | Алюминий | 16-25 |
| Железо | 70-80 | Серебро | 25 |
| Магний | 30-40 | Золото | 18 |
| Медь | 40 | Олово | 5 |
| Цинк | 33 | Свинец | 4 |
Модуль продольной упругости
Модуль продольной упругости, модуль Юнга, Е
Легирующие элементы придающие стали теплостойкость
— определяет жесткость металла, т.е. интенсивность увеличения напряжения по мере увеличения упругости деформации.
Таблица 13. Модуль Юнга металлов при 20 oС
| Металл | Е * 10-5, МПа | Металл | Е * 10-5, МПа |
| Железо | 2,17 | Золото | 0,83 |
| Цинк | 1,30 | Алюминий | 0,72 |
| Медь | 1,25 | Олово | 0,55 |
| Титан | 1,08 | Магний | 0,45 |
| Серебро | 0,83 | Свинец | 0,18 |
Литература по прочности
- Гуль В. Е., Структура и прочность полимеров, 3 изд., М., 1978;
- Разрушение, пер. с англ., т. 1, М., 1973;
- Регель В. Р., Слуцкер А. И., Томашевский Э. Е., Кинетическая природа прочности твердых тел, М., 1974.
к библиотеке к оглавлению FAQ по эфирной физике ТОЭЭ ТЭЦ ТПОИ
Знаете ли Вы,
что в 1965 году два американца Пензиас (эмигрант из Германии) и Вильсон заявили, что они открыли излучение космоса. Через несколько лет им дали Нобелевскую премию, как-будто никто не знал работ Э. Регенера, измерившего температуру космического пространства с помощью запуска болометра в стратосферу в 1933 г.? Подробнее читайте в FAQ по эфирной физике.
Основные виды сплавов
Человечество знакомо с различными металлическими сплавами. Самыми многочисленными из них являются соединения на основе железа. К ним относятся ферриты, стали и чугун. Ферриты имеют магнитные свойства, в чугуне содержится более 2,4% углерода, а сталь — это материал с высокой прочность и твердостью.
Отдельное внимания требуют металлические сплавы из цветных металлов.
Производство стали
Цинковые сплавы
Соединения металлов, которые плавятся при низких температурах. Смеси на основе цинка устойчивы к воздействию коррозийных процессов. Легко обрабатываются.
Алюминиевые сплавы
Популярность алюминий и сплавы на его основе получили во второй половине 20 века. Этот материал обладает такими преимуществами:
- Устойчивость к низким температурам.
- Электропроводность.
- Малый вес заготовок в сравнении с другими металлами.
- Износоустойчивость.
Однако нельзя забывать про то, что алюминий плавится при низких температурах. При температуре около 200 градусов характеристики ухудшаются.
Алюминий применяется при изготовлении комплектующих к машинам, производстве деталей для самолётов, составляющих промышленного оборудования, посуды, инструментов. Не многие знают, что алюминий популярен в сфере производства оружия. Связано это с тем, что детали из алюминия не искрят при сильном трении.
Чтобы увеличить прочность детали, алюминий смешивают с медью. Чтобы заготовка выдерживала давление — с марганцем. Кремний добавляют, чтобы получить обычную отливку.
Медные сплавы
Сплавы на основе меди — марки латуни. Из этого материала изготавливаются детали высокой точности, так как латунь легко обрабатывать. В составе сплава может содержаться до 45% цинка.
Свойства сплавов
Чтобы изготавливать детали и конструкции, нужно знать основные свойства металлов и сплавов. При неправильной обработке готовая деталь может быстро выйти из строя и разрушить оборудование.
Двигатель внутреннего сгорания
Физические свойства
Сюда относятся визуальные параметры и характеристики материала, изменяющиеся при обработке:
- Теплопроводность. От этого зависит насколько поверхность будет передавать тепло при нагревании.
- Плотность. По этому параметру определяется количество материла, которое содержится в единице объёма.
- Электропроводность. Возможность металла проводить электрический ток. Этот параметр называется электрическое сопротивление.
- Цвет. Этот визуальный показатель меняется под воздействием температур.
- Прочность. Возможность материала сохранять структуру при обработке. Сюда же относится твердость. Эти показатели относятся и к механическим свойствам.
- Восприимчивость к действию магнитов. Это возможность материала проводить через себя магнитные лучи.
Физические основы позволяют определить в какой сфере будет использоваться материал.
Химические свойства
Сюда относятся возможности материала противостоять воздействию химических веществ:
- Устойчивость к коррозийным процессам. Этот показатель определяет на сколько материал защищён от воздействия воды.
- Растворимость. Устойчивость металла к воздействию растворителей — кислотам или щелочным составам.
- Окисляемость. Параметр указывает на выделение оксидов металлом при его взаимодействии с кислородом.
Обуславливаются эти характеристики химическим составом материала.
Механические свойства
Механические свойства металлов и сплавов отвечают за целостность структуры материала:
- прочность;
- твердость;
- пластичность;
- вязкость;
- хрупкость;
- устойчивость к механическим нагрузкам.
Технологические свойства
Технологические свойства определяют способность металла или сплава изменяться при обработке:
- Ковкость. Обработка заготовки давлением. Материал не разрушается. Структура изменяется.
- Свариваемость. Восприимчивость детали к работе сварочным оборудованием.
- Усадка. Происходит этот процесс при охлаждении заготовки после её разогрева.
- Обработка режущим инструментом.
- Ликвация (затвердевание жидкого металла при понижении температуры).
Основной способ обработки металлических деталей — нагревание.
Свойства металлов и сплавов отвечают за то, как себя будет вести готовое изделие при эксплуатации. При обработке материалов также важно знать его характеристики.
Технологические и химические свойства твердых металлов
К технологическим свойствам относятся свариваемость, жидкотекучесть, ковкость, обрабатываемость резанием, пр. От этих особенностей зависит возможность осуществления каких-либо операций, так как они влияют на пригодность металла к обработке определенными способами.
Фен строительный — какой выбрать, для чего нужен?
Свариваемость позволяет добиваться надежных сварных соединений без трещин и иных дефектов, в том числе на прилегающих к шву участках.
В некоторых случаях металл может подходить для сварки одним методом, но давать некачественный результат при смене технологии. Так, элементы из дюралюминия удовлетворительно скрепляются при помощи точечной сварки, чего не скажешь о соединении методом газовой сварки.
На чугуне получаются хорошие швы за счет газовой сварки с подогревом и слабые при дуговой.
Жидкотекучесть – это свойство, которое дает возможность заливать горячие металлы и их сплавы в литерную форму.
Ковкость, то есть свойство твердых металлов и сплавов изменять форму под действием давления.
Обрабатываемость резанием позволяет относительно легко работать с металлом острым режущим инструментом: резцом, фрезой, пр. Данное свойство очень важно на таких этапах механической обработки, как резание, фрезерование, пр.
Под химическими свойствами понимают способность металлов вступать в реакцию с другими веществами, в том числе, с кислородом. Если металл быстро реагирует с вредными для него элементами, это приводит к быстрой потере им свойств.
Разрушение металлов под действием окружающей среды – это коррозия. Отрицательно сказываться на состоянии материала могут воздух, влага, растворы солей, кислот, щелочей.
Для защиты изделий от всех перечисленных факторов используют специальные нержавеющие, кислотостойкие и другие виды сталей.






