- Общее описание
- Этапы производства
- Использование H2SO4 в разбавленном виде
- Свойства концентрированной кислоты
- Токсичность и сферы применения
- Серная кислота
- Серная кислота — химические свойства и промышленное производство
- Промышленное производство серной кислоты (контактный способ):
- Химические свойства серной кислоты:
- Особые свойства концентрированной H 2 SO 4 :
- Окислительные свойства серной кислоты | Дистанционные уроки
- Обсуждение: «Окислительные свойства серной кислоты»
- Оксид серы(VI), серная кислота, сульфаты — урок. Химия, 9 класс

Общее описание
Серная кислота является токсичным реагентом, который отличается специфичностью применения и высоким показателем опасности для живого организма. Эта жидкость характеризуется как сильный окислитель. Температура плавления H2SO4 составляет +10 °C. Закипает кислота при +296 °C.
В результате выделяется вода и оксид серы SO3. Так как эта жидкость способна поглощать пары воды, её часто используют для осушения газов.
Добывают серу промышленным путём, используя для этого диоксид серы SO2, который можно получить только в результате горения серы либо серного колчедана.

Под воздействием низких температур H2SO4 пассивирует некоторые металлы, например алюминий, железо, хром, никель, титан. Благодаря этому транспортировать кислоту можно в герметичных железных цистернах.
Добыть H2SO4 можно двумя способами:
- Нитрозным (концентрация 75%). Происходит окисление диоксида серы с помощью диоксида азота при взаимодействии воды. Формула выглядит так: SO2 + NO2 + H2O → H2SO4 + NO.
- Контактным (концентрация находится в пределах 94%). В промышленных условиях происходит окисление диоксида серы до трехокиси серы с последующим гидролизом. Пример формулы: 2SO2 + O2 → 2SO3; SO3 + H2O → H2SO4.
Присутствующий в кислоте раствор SO3 называется олеумом, который также используют для получения H2SO4. Реакция на металлы и неметаллы всегда отличается. При использовании двухосновной маслянистой жидкости образуется 2 вида солей: средние — сульфаты (барий, кальций), кислые — гидросульфаты (натрий, калий).
Этапы производства

Изготовление кислоты является довольно интересным и познавательным процессом. Изначально серный колчедан (измельчённый влажный пирит) засыпают в специальную печь для обжига. В нижней части оборудования пускают воздух, который специально обогащают кислородом. Постепенно из печи начинает выходить газ, в состав которого входят: SO2, O2, микроскопические частицы огарка (оксида железа) и пары воды (использовался влажный пирит). С помощью электрофильтра и циклона газ очищают от примесей твёрдых частиц. Сушильная башня удаляет все пары воды.
Окисление полученного серного газа происходит благодаря катализатору V2O5 в контактном аппарате. Такой подход позволяет ускорить химическую реакцию.
Процесс окисления одного оксида в другой на практике является обратным. Специалисты стараются создать оптимальные условия, чтобы добиться протекания прямой реакции — повышенное давление и температура от +500 °C.
Всё это позволяет получить необходимую экзотермическую реакцию.
В специальной башне поглощается оксид серы концентрированной кислоты. Приём с водой не используют, так как оксид серы легко растворяется с выделением большого количества теплоты, из-за чего жидкость закипает и превращается в пар. Избежать сернокислотного тумана помогает H2SO4 в концентрации 98%. Оксид серы хорошо растворяется и образует олеум: H2SO4*nSO3.
Использование H2SO4 в разбавленном виде
Серная кислота имеет одну особенность — она может отнимать воду, из-за чего её часто используют как надёжное гигроскопическое средство во многих химических реакциях.
С помощью этой жидкости можно получать органические вещества, провести осушку, а также снизить вероятность поглощения воды конкретными элементами.
Для решения всех этих задач в лабораторных условиях используются специальные герметические ёмкости, которые называются эксикаторами.
Востребованность H2SO4 никогда не уменьшается, так как она имеет широкую сферу применения. Концентрированная жидкость может обугливать органические вещества (например, древесину), а также вызывать сильные ожоги кожного покрова.
Если для проведения химических экспериментов нужно использовать кислоту, тогда должны быть соблюдены все правила безопасности.
Если капля разбавленной жидкости H2SO4 попала на кожу либо одежду, то по мере испарения воды она постепенно будет увеличивать свою концентрацию.

Разбавленная кислота может вступать в реакцию замещения, что спровоцировано окислением катионов. По этой причине на все активные металлы, которые находятся до водорода в ряду напряжений, H2SO4 реагирует как обычная кислота. Постепенно происходит вытеснение водорода.
Этот эффект подробно объясняют на уроках химии в 8 классе. С разбавленной серной кислотой не взаимодействуют благородные металлы (например, золото, платина) и те элементы, которые стоят после водорода в ряду напряжения.
Другими окислительными свойствами разбавленная маслянистая жидкость H2SO4 не обладает.
Лабораторные исследования подтвердили, что кислота реагирует на основные оксиды и основания, из-за чего образуется сразу 2 ряда солей: кислые — гидросульфаты, средние — сульфаты.
К качественным реакциям на H2SO4 можно отнести взаимодействие с солями бария, в результате чего образуется белый осадок, который не растворяется в воде и кислой среде.
Эту химическую реакцию можно изобразить с помощью формулы: H2SO4 + BaCl 2 = BaSO 4↓ + 2HCl.
Свойства концентрированной кислоты
В концентрированном виде жидкость H2SO4 способна максимально проявить свои окислительные свойства. Это вызвано тем, что в молекулах кислоты находятся атомы серы в высшей степени окисления (+6).
В концентрированном виде H2SO4 взаимодействует с металлами, которые находятся в электрохимическом ряду напряжения (правее водорода). Речь касается серебра, ртути и меди. В результате химической реакции образуется вода, сульфаты и продукты восстановления серы.
Степень восстановления кислоты зависит от металлов. Например:
- До свободной серы возможно восстановление в том случае, если речь касается металлов, которые расположены в ряду напряжений от алюминия до железа.
- Калий, натрий, литий. Активные металлы восстанавливают H2SO4 до сероводорода.
- Металлы с меньшей активностью позволяют образовать сернистый газ.

В концентрированном виде H2SO4 не вступает в реакцию с платиной и золотом, так как эти металлы обладают небольшой активностью. Если речь касается хрома, алюминия и железа, тогда понадобится нагревание. В противном случае реакция не произойдёт, что связано с пассивированием этих металлов (на поверхности образуется тонкая защитная плёнка).
Продукт восстановления кислоты всецело зависит от концентрации H2SO4 и активности используемого металла. Каждая химическая реакция должна быть рассмотрена индивидуально.
Алюминий, хром и железо могут растворяться в концентрированной кислоте, но при условии сильного нагревания. В результате образуется соль металла и продукты восстановления серной кислоты.
Формулы выглядят следующим образом:
- 2Cr + 6H2SO4 = Cr2 (SO4)3 + 3SO2↑ + 6H2O.
- 8Al + 15H2SO4 = 4AL2 (SO4)3 + 3H2S↑ + 12H2O.
- 2Fe + 6H2SO4 = FE (SO4)3 + 3SO2↑ + 6H2O.
Совершенно другую реакцию можно наблюдать в том случае, если нужно проверить взаимодействие кислоты с металлами. Происходит выделение SO2 и окисление неметаллов до высшей степени. Например:
- S + 2H2SO4 = 3SO2↑ + 2H2O.
- C + 2H2SO4 = CO2↑ + 2SO2↑ + 2H2O.
- H2SO4 + H2S = SO2↑ + S↓ + 2H2O.
- 2P + 5H2SO4 = 2H3PO4 + 5SO2↑ + 2H2O.
В разбавленном виде кислота ничем не отличается от других похожих жидкостей. В категорию исключений входит только то, что H2SO4 не вступает в реакцию со свинцом, так как образовавшийся сульфат свинца невозможно растворить.
Токсичность и сферы применения
Серная кислота и олеум относятся к категории наиболее едких веществ. Они могут обжечь кожу, слизистые оболочки и дыхательные пути. Из-за неаккуратного обращения с агрессивной жидкостью не исключено возникновение химического ожога.
Вдыхание паров этих веществ может спровоцировать кашель, затруднённое дыхание, бронхит. В атмосфере может образовываться аэрозоль из-за ядовитого дыма металлургических и химических производств. В такой ситуации могут выпадать кислотные дожди.

- При правильном применении H2SO4 может пригодиться в следующих случаях:

- Серийное производство минеральных удобрений.
- Изготовление электролита для свинцовых аккумуляторов.
- Производство химических волокон, взрывчатых и дымообразующих веществ, а также красителей.
- Получение солей и минеральных кислот.
- Изготовление пищевой добавки (эмульгатора) Е513.
- Использование в металлообрабатывающей, нефтяной, кожевенной, текстильной промышленности.
- Гидратация (например, этанол из этилена).
- Дегидратация (получение сложных и диэтиловых эфиров).
- Алкилирование. H2SO4 позволяет получить полиэтилен гликоль, изооктан, капролактам.
- Восстановление смол в очистительных фильтрах на участке производства дистиллированной воды.
Во всём мире в год используется до 160 тонн кислоты. Больше всего эту жидкость применяют в производстве минеральных удобрений. По этой причине сернокислотные заводы стараются возводить вместе с предприятиями, которые будут заниматься изготовлением удобрений.
Не менее востребованными являются соли серной кислоты. Мирабилит (Nа2SO4•10Н2O) был получен немецким химиком И. Глаубером, который экспериментировал с тем, как действует H2SO4 на хлорид натрия. В медицинской практике это средство используется в качестве слабительного.
Спрос также получил железный купорос (FeSO4*7H2O), который ранее применяли для лечения диагностированной чесотки.
Но в настоящее время этот химический компонент используется только для борьбы с сельскохозяйственными вредителями. Применение большой концентрации железного купороса чревато гибелью обработанной культуры.
Медный купорос (CuSO4*5H2O) получил большой спрос в сельском хозяйстве для борьбы с вредителями растений.
Серная кислота
Серная кислота — сильная двухосновная кислота, при н.у. маслянистая жидкость без цвета и запаха.
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Замечу, что существует олеум — раствор SO3 в безводной серной кислоте, дымящее жидкое или твердое вещество. Олеум применяется при изготовлении красителей, органическом синтезе и в производстве серной кислот.
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
- FeS2 + O2 → (t) Fe2O3 + SO2↑
- SO2 + O2 ⇄ (кат. — V2O5) SO3
- Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
- Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
- 2. NO + NO2 + 2H2SO4 = 2NO(HSO4) + H2O
- 3. NO(HSO4) + H2O = H2SO4 + HNO2
- NO2 + SO2 + H2O = H2SO4 + NO
- Кислотные свойства
- В водном растворе диссоциирует ступенчато.
- H2SO4 ⇄ H+ + HSO4-
- HSO4- ⇄ H+ + SO42-
- MgO + H2SO4 → MgSO4 + H2O
- KOH + H2SO4 = KHSO4 + H2O (гидросульфат калия, соотношение 1:1 — кислая соль)
- 2KOH + H2SO4 = K2SO4 + 2H2O (сульфат калия, соотношение 2:1 — средняя соль)
- Реакции с солями
- BaBr2 + H2SO4 → BaSO4↓ + 2HBr
- MgCO3 + H2SO4 → MgSO4 + CO2↑ + H2O
- Na2CO3 + H2SO4 → Na2SO4 + CO2↑ + H2O
- Реакция с неметаллами
- Серная кислота окисляет неметаллы — серу и углерод — соответственно до угольной кислоты (нестойкой) и сернистого газа.
- S + H2SO4 → SO2 + H2O
- C + H2SO4 → CO2 + SO2 + H2O
- Реакции с металлами
- Fe + H2SO4(разб.) → FeSO4 + H2↑
- Zn + H2SO4(разб.) → ZnSO4 + H2↑
- Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
- Na + H2SO4(конц.) → Na2SO4 + H2S + H2O
- Zn + H2SO4(конц.) → ZnSO4 + S + H2O
- Cu + H2SO4(конц.) → CuSO4 + SO2 + H2O
Сильная кислота. Реагирует с основными оксидами, основаниями, образуя соли — сульфаты.

С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.

Реакции разбавленной серной кислоты с металлами не составляют никаких трудностей: она реагирует как самая обычная кислота, например HCl. Все металлы, стоящие до водорода, вытесняют из серной кислоты водород, а стоящие после — не реагируют с ней.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.

Концентрированная серная кислота ведет себя совершенно по-иному. Водород никогда не выделяется, вместо него с активными металлами выделяется H2S, с металлами средней активности — S, с малоактивными металлами — SO2.
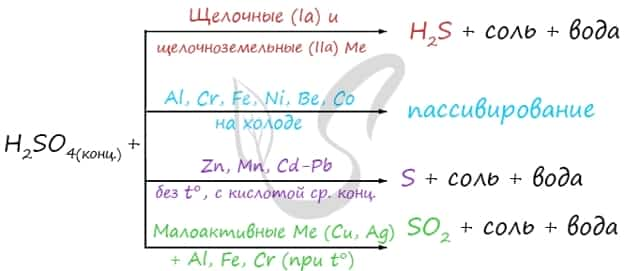

Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
Fe + H2SO4(конц.) → (t) Fe2(SO4)3 + SO2 + H2O
Cr + H2SO4(конц.) → (t) Cr2(SO4)3 + SO2 + H2O

Иногда в тексте задания даны подсказки. Например, если написано, что выделился газ с неприятным запахом тухлых яиц — речь идет об H2S, если же написано, что выделилось простое вещество — речь о сере (S).
Серная кислота — химические свойства и промышленное производство
Физические свойства серной кислоты: Тяжелая маслянистая жидкость («купоросное масло»); плотность 1,84 г/см3; нелетучая, хорошо растворима в воде – с сильным нагревом; t°пл. = 10,3°C, t°кип. = 296°С, очень гигроскопична, обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара).
Теплота гидратации настолько велика, что смесь может вскипать, разбрызгиваться и вызывать ожоги. Поэтому необходимо добавлять кислоту к воде, а не наоборот, поскольку при добавлении воды к кислоте более легкая вода окажется на поверхности кислоты, где и сосредоточится вся выделяющаяся теплота.
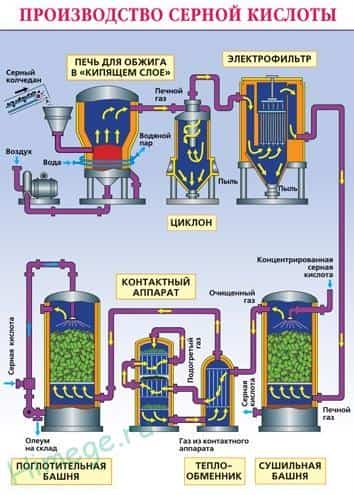
Промышленное производство серной кислоты (контактный способ):
-
 1) 4FeS 2 + 11O 2 → 2Fe 2 O 3 + 8SO 2
1) 4FeS 2 + 11O 2 → 2Fe 2 O 3 + 8SO 2 - 2) 2SO 2 + O 2 V 2 O 5 → 2SO 3
- 3) nSO 3 + H 2 SO 4 → H 2 SO 4 ·nSO 3 (олеум)
Измельчённый очищенный влажный пирит (серный колчедан) сверху засыпают в печь для обжига в « кипящем слое «. Снизу (принцип противотока) пропускают воздух, обогащённый кислородом. Из печи выходит печной газ, состав которого: SO 2 , O 2 , пары воды (пирит был влажный) и мельчайшие частицы огарка (оксида железа). Газ очищают от примесей твёрдых частиц (в циклоне и электрофильтре) и паров воды (в сушильной башне). В контактном аппарате происходит окисление сернистого газа с использованием катализатора V 2 O 5 ( пятиокись ванадия) для увеличения скорости реакции. Процесс окисления одного оксида в другой является обратимым. Поэтому подбирают оптимальные условия протекания прямой реакции — повышенное давление (т.к прямая реакция идет с уменьшением общего объема) и температура не выше 500 С ( т.к реакция экзотермическая).
В поглотительной башне происходит поглощение оксида серы (VI) концентрированной серной кислотой. Поглощение водой не используют, т.
к оксид серы растворяется в воде с выделением большого количества теплоты, поэтому образующаяся серная кислота закипает и превращается в пар.
Для того, чтобы не образовывалось сернокислотного тумана, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H 2 SO 4 ·nSO 3
Химические свойства серной кислоты:
- H 2 SO 4 — сильная двухосновная кислота, одна из самых сильных минеральных кислот, из-за высокой полярности связь Н – О легко разрывается.
- 1) В водном растворе серная кислота диссоциирует , образуя ион водорода и кислотный остаток: H 2 SO 4 = H + + HSO 4 — ; HSO 4 — = H + + SO 4 2- . Суммарное уравнение:
- H 2 SO 4 = 2H + + SO 4 2- .
- 2) Взаимодействие серной кислоты с металлами : Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
- Zn 0 + H 2 +1 SO 4 (разб) → Zn +2 SO 4 + H 2
- 3) Взаимодействие серной кислоты с основными оксидами: CuO + H 2 SO 4 → CuSO 4 + H 2 O
- 4) Взаимодействие серной кислоты с гидроксидами: H 2 SO 4 + 2NaOH → Na 2 SO 4 + 2H 2 O H 2 SO 4 + Cu(OH) 2 → CuSO 4 + 2H 2 O
- 5) Обменные реакции с солями: BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl Образование белого осадка BaSO 4 (нерастворимого в кислотах) используется для обнаружения серной кислоты и растворимых сульфатов (качественная реакция на сульфат ион).
Особые свойства концентрированной H 2 SO 4 :
1) Концентрированная серная кислота является сильным окислителем ; при взаимодействии с металлами (кроме Au, Pt) восстанавливаться до S +4 O 2 , S 0 или H 2 S -2 в зависимости от активности металла. Без нагревания не реагирует с Fe, Al, Cr – пассивация.
При взаимодействии с металлами, обладающими переменной валентностью, последние окисляются до более высоких степеней окисления , чем в случае с разбавленным раствором кислоты: Fe 0 → Fe 3+ , Cr 0 → Cr 3+ , Mn 0 → Mn 4+ , Sn 0 → Sn 4+
-
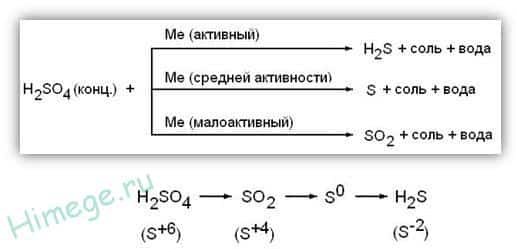
- Активный металл
- 8 Al + 15 H 2 SO 4(конц.) →4Al 2 (SO 4 ) 3 + 12H 2 O + 3 H 2 S 4│2Al 0 – 6 e — → 2Al 3+ — окисление 3│ S 6+ + 8e → S 2– восстановление
- 4Mg+ 5H 2 SO 4 → 4MgSO 4 + H 2 S + 4H 2 O
- Металл средней активности
- 2Cr + 4 H 2 SO 4(конц.) → Cr 2 (SO 4 ) 3 + 4 H 2 O + S 1│ 2Cr 0 – 6e →2Cr 3+ — окисление 1│ S 6+ + 6e → S 0 – восстановление
- Металл малоактивный
- 2Bi + 6H 2 SO 4( конц .) → Bi 2 (SO 4 ) 3 + 6H 2 O + 3 SO 2 1│ 2Bi 0 – 6e → 2Bi 3+ – окисление 3│ S 6+ + 2e →S 4+ — восстановление
- 2Ag + 2H 2 SO 4 →Ag 2 SO 4 + SO 2 + 2H 2 O
- 2) Концентрированная серная кислота окисляет некоторые неметаллы как правило до максимальной степени окисления, сама восстанавливается до S +4 O 2 :
- С + 2H 2 SO 4 (конц) → CO 2 + 2SO 2 + 2H 2 O
- S+ 2H 2 SO 4 (конц) → 3SO 2 + 2H 2 O
- 2P+ 5H 2 SO 4 (конц)→5SO 2 + 2H 3 PO 4 + 2H 2 O
- 3) Окисление сложных веществ: Серная кислота окисляет HI и НВг до свободных галогенов:
- 2 КВr + 2Н 2 SO 4 = К 2 SО 4 + SO 2 + Вr 2 + 2Н 2 О
2 КI + 2Н 2 SО 4 = К 2 SO 4 + SO 2 + I 2 + 2Н 2 О Концентрированная серная кислота не может окислить хлорид-ионы до свободного хлора, что дает возможность получать НСl по реакции обмена:
NаСl + Н 2 SO 4 (конц.) = NаНSO 4 + НСl
Серная кислота отнимает химически связанную воду от органических соединений, содержащих гидроксильные группы. Дегидратация этилового спирта в присутствии концентрированной серной кислоты приводит к получению этилена: С 2 Н 5 ОН = С 2 Н 4 + Н 2 О.
Обугливание сахара, целлюлозы, крахмала и др. углеводов при контакте с серной кислотой объясняется также их обезвоживанием: C 6 H 12 O 6 + 12H 2 SO 4 = 18H 2 O + 12SO 2 ↑ + 6CO 2 ↑.

Окислительные свойства серной кислоты | Дистанционные уроки
ОВР в статье специально выделены цветом. Обратите на них особое внимание. Эти уравнения могут попасться в ЕГЭ.
- Разбавленная серная ведет себя, как и остальные кислоты, окислительные свои возможности прячет:
- Zn + H2SO4 → ZnSO4 + H2↑
- Автор статьи — Саид Лутфуллин
И еще, что надо помнить про разбавленную серную кислоту: она не реагирует со свинцом. Кусок свинца, брошенный в разбавленную H2SO4 покрывается слоем нерастворимого (см. таблицу растворимости) сульфата свинца и реакция моментально прекращается.
Pb + H2SO4 ≠
Концентрированная серная кислота – тяжелая маслянистая жидкость, не летучая, не имеет вкуса и запаха
За счет серы в степени окисления +6(высшей) серная кислота приобретает сильные окислительные свойства.
Правило для задания 24 (по-старому А24) при приготовлении растворов серной кислоты никогда нельзя в нее лить воду. Концентрированую серную кислоту нужно тонкой струйкой вливать в воду, постоянно помешивая.
Взаимодействие концентрированной серной кислоты с металлами
Эти реакции строго стандартизированны и идут по схеме:
H2SO4(конц.) + металл → сульфат металла + H2O + продукт восстановленной серы.
Есть два нюанса:
1) Алюминий, железо и хром с H2SO4 (конц) в нормальных условиях не реагируют, из-за пассивации. Нужно нагреть.
2) С платиной и золотом H2SO4 (конц) не реагирует вообще.
Сера в концентрированной серной кислоте – окислитель
- значит, сама будет восстанавливаться;
- то, до какой степени окисления будет восстанавливаться сера, зависит от металла.
Рассмотрим диаграмму степеней окисления серы:
- До -2 серу могут восстановить только очень активные металлы — в ряду напряжений до алюминия включительно.
- Реакции будут идти вот так:
- 8Li + 5H2SO4(конц.) → 4Li2SO4 + 4H2O + H2S↑
- 4Mg + 5H2SO4(конц.) → 4MgSO4 + 4H2O + H2S↑
- 8Al + 15H2SO4(конц.) (t)→ 4Al2(SO4)3 + 12H2O + 3H2S↑
- при взаимодействии H2SO4 (конц) с металлами в ряду напряжений после алюминия, но до железа, то есть с металлами со средней активностью сера восстанавливается до :
- 3Mn + 4H2SO4(конц.) → 3MnSO4 + 4H2O + S↓
- 2Cr + 4H2SO4(конц.) (t)→ Cr2(SO4)3 + 4H2O + S↓
- 3Zn + 4H2SO4(конц.) → 3ZnSO4 + 4H2O + S↓
- все остальные металлы, начиная с железа в ряду напряжений (включая те, что после водорода, кроме золота и платины, конечно), могут восстановить серу только до +4. Так как это малоактивные металлы:
- 2Fe + 6H2SO4(конц.) (t)→ Fe2(SO4)3 + 6H2O + 3SO2↑
- (обратите внимание, что железо окисляется до +3, до максимально возможной, высшей степени окисления, так как оно имеет дело с сильным окислителем)
- Cu + 2H2SO4(конц.) → CuSO4 + 2H2O + SO2↑
- 2Ag + 2H2SO4(конц.) → Ag2SO4 + 2H2O + SO2↑

Конечно, все относительно. Глубина восстановления будет зависеть от многих факторов: концентрации кислоты (90%, 80%, 60%), температуры и т.д. Поэтому совсем уж точно предсказать продукты нельзя.
Приведенная выше таблица тоже имеет свой процент приблизительности, но пользоваться ей можно.
Еще необходимо помнить, что в ЕГЭ, когда продукт восстановленной серы не указан, и металл не отличается особой активностью, то, скорее всего, составители имеют в виду SO2. Нужно смотреть по ситуации и искать зацепки в условиях.
SO2 – это вообще частый продукт ОВР с участием конц. серной кислоты.
- H2SO4 (конц) окисляет некоторые неметаллы (которые проявляют восстановительные свойства), как правило, до максимальной — высшей степени окисления (образуется оксид этого неметалла). Сера при этом тоже восстанавливается до SO2:
- C + 2H2SO4(конц.) → CO2↑ + 2H2O + 2SO2↑
- 2P + 5H2SO4(конц.) → P2O5 + 5H2O + 5SO2↑
- Свежеобразованный оксид фосфора (V) реагирует с водой, получается ортофосфорная кислота. Поэтому реакцию записывают сразу:
- 2P + 5H2SO4(конц) → 2H3PO4 + 2H2O + 5SO2↑
- То же самое с бором, он превращается в ортоборную кислоту:
- 2B + 3H2SO4(конц) → 2H3BO3 + 3SO2↑
Очень интересны взаимодействие серы со степенью окисления +6 (в серной кислоте) с «другой» серой (находящейся в другом соединении). В рамках ЕГЭ рассматривается взаимодействиеH2SO4 (конц) с серой (простым веществом) и сероводородом.
Начнем с взаимодействия серы (простого вещества) с концентрированной серной кислотой. В простом веществе степень окисления 0, в кислоте +6. В этой ОВР сера +6 будет окислять серу 0. Посмотрим на диаграмму степеней окисления серы:
- Сера 0 будет окисляться, а сера +6 будет восстанавливаться, то есть понижать степень окисления. Будет выделяться сернистый газ:
- 2H2SO4(конц.) + S → 3SO2↑ + 2H2O
- Но в случае с сероводородом:
- Образуется и сера (простое вещество), и сернистый газ:
- H2SO4(конц.) + H2S → S↓ + SO2↑ + 2H2O
Этот принцип часто может помочь в определении продукта ОВР, где окислитель и восстановитель – один и тот же элемент, в разных степенях окисления. Окислитель и восстановитель «идут навстречу друг другу» по диаграмме степеней окисления.
- H2SO4 (конц) , так или иначе, взаимодействует с галогенидами. Только вот тут надо понимать, что фтор и хлор – «сами с усами» и с фторидами и хлоридами ОВР не протекает, проходит обычный ионно-обменный процесс, в ходе которого образуется газообразный галогеноводород:
- CaCl2 + H2SO4(конц.) → CaSO4 + 2HCl↑
- CaF2 + H2SO4(конц.) → CaSO4 + 2HF↑
А вот галогены в составе бромидов и иодидов (как и в составе соответствующих галогеноводородов) окисляются ей до свободных галогенов. Только вот сера восстанавливается по-разному: иодид является более cильным восстановителем, чем бромид. Поэтому иодид восстанавливает серу до сероводорода, а бромид до сернистого газа:
- 2H2SO4(конц.) + 2NaBr → Na2SO4 + 2H2O + SO2↑ + Br2
- H2SO4(конц.) + 2HBr → 2H2O + SO2↑ + Br2
- 5H2SO4(конц.) + 8NaI → 4Na2SO4 + 4H2O + H2S↑ + 4I2↓
- H2SO4(конц.) + 8HI → 4H2O + H2S↑ + 4I2↓
- Хлороводород и фтороводород (как и их соли) устойчивы к окисляющему действию H2SO4 (конц).
И наконец, последнее: для концентрированной серной кислоты это уникально, больше никто так не может. Она обладает водоотнимающим свойством.
Это позволяет использовать концентрированную серную кислоту самым разным образом:
Во-первых, осушение веществ. Концентрированная серная кислота забирает воду от вещества и оно «становится сухим».
- Во-вторых, катализатор в реакциях, в которых отщепляется вода (например, дегидратация и этерификация):
- H3C–COOH + HO–CH3 (H2SO4(конц.))→ H3C–C(O)–O–CH3 + H2O
- H3C–CH2–OH (H2SO4(конц.))→ H2C=CH2 + H2O
Обсуждение: «Окислительные свойства серной кислоты»
(Правила комментирования)
Оксид серы(VI), серная кислота, сульфаты — урок. Химия, 9 класс
- Оксид серы(VI)
- Oксид серы((VI)) образуется при каталитическом окислении сернистого газа:
- 2SO2+O2⇄t,k2SO3.
- При обычных условиях это жидкость, которая реагирует с водой с образованием серной кислоты:
- SO3+H2O=H2SO4.
Эта реакция протекает даже с парами воды. Поэтому оксид серы((VI)) дымит на воздухе.
- Особенностью оксида серы((VI)) является его способность растворяться в концентрированной серной кислоте с образованием олеума.
- Оксид серы((VI)) — типичный кислотный оксид. Он реагирует с основаниями и основными оксидами c образованием солей:
- SO3+2NaOH=Na2SO4+H2O,
- SO3+CaO=CaSO4.
Степень окисления серы в этом оксиде — (+6). Это максимальное значение для серы, поэтому в окислительно-восстановительных реакциях он может быть только окислителем.
Серная кислота H2SO4 — важнейшее соединение серы. Чистая серная кислота представляет собой бесцветную вязкую маслянистую жидкость, котoрая почти в два раза тяжелее воды.
Серная кислота неограниченно смешивается с водой. Растворение серной кислоты сопровождается сильным разогреванием раствора, и может происходить его разбрызгивание. Поэтому серную кислоту растворяют осторожно: тонкой струйкой кислоту вливают в воду при постоянном перемешивании.
Рис. (1). Смешивание серной кислоты с водой
- Серная кислота очень гигроскопична и используется для осушки разных веществ.
- Химические свойства серной кислоты зависят от её концентрации.
- Серная кислота любой концентрации реагирует:
- с основными и амфотерными оксидами и гидроксидами с образованием соли и воды:
H2SO4+CuO=CuSO4+H2O,
H2SO4+Zn(OH)2=ZnSO4+2H2O;
- с солями, если образуется газ или нерастворимое вещество:
H2SO4+CaCO3=CaSO4+H2O+CO2↑,
H2SO4+BaCl2=BaSO4↓+2HCl.
Разбавленная кислота реагирует только с металлами, расположенными в ряду активности до водорода. В реакции образуются сульфаты и выделяется водород. Окислительные свойства в этом случае проявляют атомы водорода:
H2+1SO4+Zn0=Zn+2SO4+H2↑0.
Концентрированная кислота реагирует:
- со всеми металлами, кроме золота и платины, за счёт сильных окислительных свойств атома серы:
2H2S+6O4+Cu0=Cu+2SO4+S+4O2+2H2O.
В реакциях с активными металлами продуктами реакции могут быть сернистый газ, сероводород или сера.
Обрати внимание!
При низкой температуре пассивирует железо и алюминий и с ними не реагирует.
- С твёрдыми солями других кислот:
H2SO4(к)+2NaNO3(тв)=Na2SO4+2HNO3.
- Со многими органическими веществами (происходит обугливание сахара, бумаги, древесины и т. д., так как отнимается вода):
Рис. (2). Обугливание сахара концентрированной серной кислотой
Серная кислота образует два ряда солей. Средние соли называются сульфатами (Na2SO4,CaSO4), а кислые — гидросульфатами (NaHSO4,Ca(HSO4)2).
- Качественной реакцией на серную кислоту и её соли является реакция с растворимыми солями бария — выпадает белый осадок сульфата бария:
- Na2SO4+BaCl2=BaSO4↓+2NaCl,SO42−+Ba2+=BaSO4↓.
- Серная кислота — одно из важнейших химических веществ. Она используется:
- для получения других кислот;
- для производства минеральных удобрений;
- для очистки нефтепродуктов;
- в свинцовых аккумуляторах;
- в производстве моющих средств, красителей, лекарств.
Соли серной кислоты также находят применение. Медный купорос CuSO4⋅5H2O используется для борьбы с заболеваниями растений, гипс CaSO4⋅2H2O применяется в строительстве, сульфат бария BaSO4 — в медицине.
Источники:
Рис. 1. Смешивание серной кислоты с водой © ЯКласс
Рис. 2. Обугливание сахара концентрированной серной кислотой © ЯКласс






