- Атом и молекула калия. Формула калия. Строение калия:
- Изотопы и модификации калия:
- Свойства калия (таблица): температура, плотность, давление и пр.:
- Физические свойства калия:
- Химические свойства калия. Взаимодействие калия. Реакции с калием:
- Получение калия:
- Применение калия:
- Калий – полезные свойства и особенности металла
- Что представляет собой калий
- История
- Калий в природе
- Технология получения
- Физико-химические характеристики
- Где используется калий
- Жизненные процессы
- Суточная потребность
- Питание
- Симптомы недостатка/избытка
- Цены
- Калий | это… Что такое Калий?
- История и происхождение названия
- Нахождение в природе
- Месторождения
- Получение
- Физические свойства
- Химические свойства
- Взаимодействие с простыми веществами
- Взаимодействие со сложными веществами
- Соединения с кислородом
- Гидроксид
- Применение
- Важные соединения
- Биологическая роль
- Калий в организме человека
- Изотопы
- См. также
- Примечания
K 19 Калий
39,0983(1) 1s2 2s2 2p6 3s2 3p6 4s1
Калий — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 19. Расположен в 1-й группе (по старой классификации — главной подгруппе первой группы), четвертом периоде периодической системы.
Атом и молекула калия. Формула калия. Строение калия
- Изотопы и модификации калия
- Свойства калия (таблица): температура, плотность, давление и пр.
- Физические свойства калия
Химические свойства калия. Взаимодействие калия. Реакции с калием
Получение калия
Применение калия
Таблица химических элементов Д.И. Менделеева
Атом и молекула калия. Формула калия. Строение калия:
Калий (лат. Kalium, от араб. аль-кали – «поташ») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением K и атомным номером 19. Расположен в 1-й группе (по старой классификации – главной подгруппе первой группы), четвертом периоде периодической системы.
Калий – металл. Относится к группе щелочных металлов.
- Калий обозначается символом K.
- Как простое вещество калий при нормальных условиях представляет собой мягкий металл серебристо-белого цвета.
- Молекула калия одноатомна.
- Химическая формула калия K.
Электронная конфигурация атома калия 1s2 2s2 2p6 3s2 3p6 4s1. Потенциал ионизации (первый электрон) атома калия равен 418,81 кДж/моль (4,34066369(9) эВ).
Строение атома калия. Атом калия состоит из положительно заряженного ядра (+19), вокруг которого по четырем оболочкам движутся 19 электронов. При этом 18 электронов находятся на внутреннем уровне, а 1 электрон – на внешнем. Поскольку калий расположен в четвертом периоде, оболочек всего четыре.
Первая – внутренняя оболочка представлена s-орбиталью. Вторая и третья – внутренние оболочки представлена s- и р-орбиталями. Четвертая – внешняя оболочка представлена s-орбиталью. На внешнем энергетическом уровне атома калия – на 4s-орбитали находится один неспаренный электрон. В свою очередь ядро атома калия состоит из 19 протонов и 20 нейтронов.
Калий относится к элементам s-семейства.
Радиус атома калия (вычисленный) составляет 243 пм.
Атомная масса атома калия составляет 39,0983(1) а. е. м.
Калий – седьмой по распространённости элемент в земной коре. Содержание его в земной коре составляет 1,5 %, в океанах и морях – 0,042 %.
Калий очень легко вступает в химические реакции.
Калий, свойства атома, химические и физические свойства
Изотопы и модификации калия:
Свойства калия (таблица): температура, плотность, давление и пр.:
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Калий |
| 102 | Прежнее название | |
| 103 | Латинское название | Kalium |
| 104 | Английское название | Potassium |
| 105 | Символ | K |
| 106 | Атомный номер (номер в таблице) | 19 |
| 107 | Тип | Металл |
| 108 | Группа | Щелочной металл |
| 109 | Открыт | Хемфри Дэви, Великобритания, 1807 г. |
| 110 | Год открытия | 1807 г. |
| 111 | Внешний вид и пр. | Мягкий, серебристо-белый металл |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | 39K, 41K |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 1,5 % |
| 120 | Содержание в морях и океанах (по массе) | 0,042 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,0003 % |
| 122 | Содержание в Солнце (по массе) | 0,0004 % |
| 123 | Содержание в метеоритах (по массе) | 0,07 % |
| 124 | Содержание в организме человека (по массе) | 0,2 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 39,0983(1) а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 4s1 |
| 203 | Электронная оболочка | K2 L8 M8 N1 O0 P0 Q0 R0 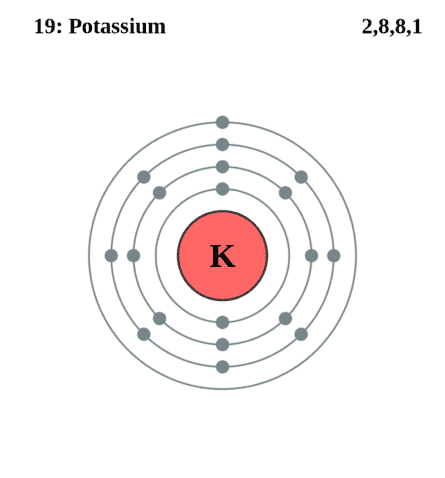 |
| 204 | Радиус атома (вычисленный) | 243 пм |
| 205 | Эмпирический радиус атома* | 220 пм |
| 206 | Ковалентный радиус* | 203 пм |
| 207 | Радиус иона (кристаллический) | K+
|
| 208 | Радиус Ван-дер-Ваальса | 275 пм |
| 209 | Электроны, Протоны, Нейтроны | 19 электронов, 19 протонов, 20 нейтронов |
| 210 | Семейство (блок) | элемент s-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 1-ая группа (по старой классификации – главная подгруппа 1-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | 0, +1 |
| 302 | Валентность | I |
| 303 | Электроотрицательность | 0,82 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 418,81 кДж/моль (4,34066369(9) эВ) |
| 305 | Электродный потенциал | K+ + e– → K, Eo = -2,924 В |
| 306 | Энергия сродства атома к электрону | 48,383(2) кДж/моль (0,501459(13) эВ) |
| 400 | Физические свойства | |
| 401 | Плотность* | 0,862 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 0,828 г/см3 (при температуре плавления 63,5 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | 63,5 °C (336,7 K, 146,3 °F) |
| 403 | Температура кипения* | 759 °C (1032 K, 1398 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 2,33 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 76,9 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость | 29,6 Дж/(K·моль) |
| 411 | Молярный объём | 45,675584 см³/моль |
| 412 | Теплопроводность | 102,5 Вт/(м·К) (при стандартных условиях), 79,0 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Кубическая объёмно-центрированная 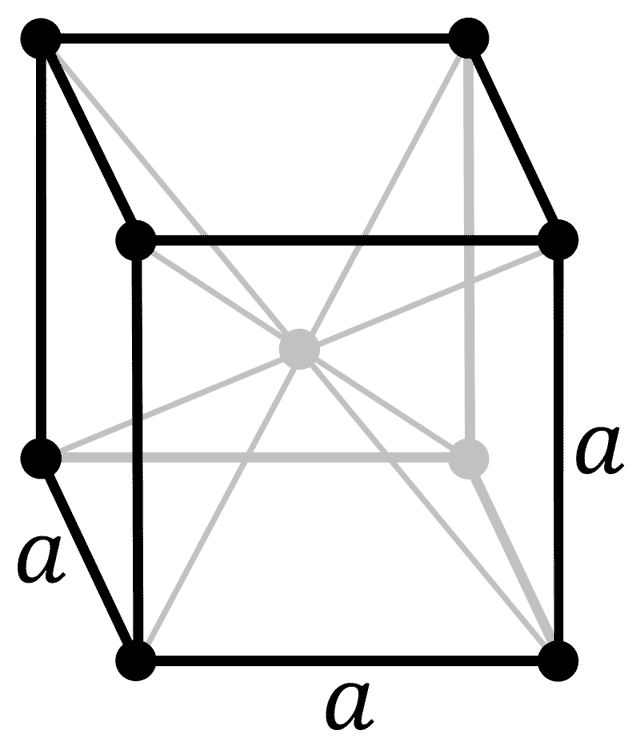 |
| 513 | Параметры решётки | 5,332 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 100 К |
| 516 | Название пространственной группы симметрии | Im_ 3m |
| 517 | Номер пространственной группы симметрии | 229 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-09-7 |
- Примечание:
- 205* Эмпирический радиус атома калия согласно [1] и [3] составляет 227 пм и 235 пм соответственно.
- 206* Ковалентный радиус калия согласно [1] составляет 203±12 пм.
- 401* Плотность калия согласно [3] составляет 0,856 г/см3 (при 0 °C и иных стандартных условиях, состояние вещества – твердое тело), согласно [4] 0,826 г/см3 (при 64 °C и иных стандартных условиях, состояние вещества – жидкость).
- 402* Температура плавления калия согласно [3] и [4] составляет 63,65 °C (336,8 K, 146,57 °F) и 63,55 °C (336,7 K, 146,39 °F) соответственно.
- 403* Температура кипения калия согласно [3] и [4] составляет 773,85 °C (1047 K, 1424,93 °F) и 776 °C (1049,15 K, 1428,8 °F) соответственно.
- 407* Удельная теплота плавления (энтальпия плавления ΔHпл) калия согласно [4] составляет 2,38 кДж/моль.
- 408* Удельная теплота испарения (энтальпия кипения ΔHкип) калия согласно [4] составляет 79,2 кДж/моль.
Физические свойства калия:
Химические свойства калия. Взаимодействие калия. Реакции с калием:
Получение калия:
Применение калия:
Таблица химических элементов Д.И. Менделеева
Таблица химических элементов Д.И. Менделеева
Источники:
Примечание: © Фото https://www.pexels.com, https://pixabay.com
карта сайта
калий атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка
атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома
электронные формулы сколько атомов в молекуле калия
сколько электронов в атоме свойства металлические неметаллические термодинамические
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
- Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
- Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
- Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
- Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Калий – полезные свойства и особенности металла
Это вещество известно всем, особенно фанатам гигиены и чувствительным людям. Достоинства калия сделали его обязательным компонентом в науке, промышленном производстве, сельском хозяйстве.
Что представляет собой калий
Калий – это химический элемент, номер 19 таблицы Менделеева:
- Это мягкое вещество серебристо-белого цвета.
- Относится к щелочным металлам.
- Структура решетки кубическая.
- Международное обозначение – K (Kalium).
Химические свойства схожи с натрием, отличия выявлены на биологическом уровне.
Калий включает в себя три изотопа. Изотоп K40 – источник энергии, извлекаемой из геотермальных источников планеты.
Естественные либо синтезированные заменители металла не выявлены.
История
Калий упоминается, начиная со времени первых цивилизаций. Соединения вещества использовали еще древние египтяне. Речь о поташе, которым стирали одежду, мыли посуду.
Процесс был простым. Сжигали ветви, солому, оставшуюся золу заливали водой. Полученную щелочную массу отфильтровывали, выпаривали.
История получения металла европейскими учеными начинается с 19 века:
- В 1807 году английский химик Гемфри Дэви выбрал исходником едкий кали. Применив электролиз, получил калий.
- Через два года его французские коллеги прокалили едкий кали с углем и также получили металл.
С названием металла определились не сразу:
- Первооткрыватель окрестил вещество «потассием» (лат. Potassium).
- Немец Людвиг Гильберт предложил термин «калий».
Латинское kalium восходит к арабскому аль-кали. Так арабы именовали поташ.
Термин «калий» понравился немцам. Его переняли ученые Европы (в том числе российские).
Калий в природе
В природе свободный калий не обнаружен (этому препятствует высокая химическая активность), только как компонент соединений с другими химическими элементами в составе. Такая форма существует в почве, растительной золе, минералах, морской воде.
 Калий под слоем ТГФ
Калий под слоем ТГФ
Самые известные минералы – каинит, сильвин, сильвинит, карналлит.
Калий – элемент клеток живых организмов.
Тонна земной коры содержит 24 кг калия, литр морской воды – 380 мг.
По распространенности калий – пятый среди металлов, седьмой среди всех элементов.
Сырье извлекают из шахт либо подземных соленых вод.
Крупнейшими залежами располагают Канада, Россия, Белоруссия.
Технология получения
Подобно другим щелочным металлам, калий извлекают электролизом расплава хлоридов либо щелочей.
При таком способе получения используют – как менее тугоплавкие – щелочи плюс сода либо поташ:
- На катоде и аноде появляются, соответственно, расплавленный калий и кислород.
- Вода из расплава испаряется.
- Чтобы исключить взаимодействие с кислородом, используют медный катод.
- Над катодом укрепляют медный цилиндр. В нем оседает расплавленный калий.
Анод изготовляют из никеля (для щелочей) либо графита (хлоридов).
Физико-химические характеристики
Калий как металл проявляет типично «щелочные» характеристики:
- Химически суперактивен: без проблем взаимодействует с неметаллами, сложными веществами. В результате образуются галогениды, фосфиды, оксиды, амальгамы, соли.
- Взаимодействие с металлами возможно только при нагревании. Образуются сплавы-интерметаллиды.
- Почти мгновенно окисляется на воздухе.
- С кислородом реагирует так бурно, что получается супероксид – K2O4.
- Легкий (кубик с ребром в 1 см весит меньше грамма), легкоплавок.
- Это мягкий металл – легко режется ножом, раскатывается до фольги.
- Не тонет в воде.
Взаимодействие металла с водой взрывоопасно, на воздухе он разрушается. Для нейтрализации этих недостатков калий хранят в бензине, керосине либо плотно закрываемых сосудах.
 Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH.
Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH.
| Калий / Kalium (K), 19 |
| 39,0983(1) а. е. м. (г/моль) |
| [Ar] 4s1 |
| 235 пм |
| 203 пм |
| 133 пм |
| 0,82 (шкала Полинга) |
| −2,92 В |
| 0; +1 |
| 418,5 (4,34) кДж/моль (эВ) |
| 0,856 г/см³ |
| 336,8 К; +63,65 °C |
| 1047 К; 773,85 °C |
| 2,33 кДж/моль |
| 76,9 кДж/моль |
| 29,6 Дж/(K·моль) |
| 45,3 см³/моль |
| кубическая объёмно-центрированная |
| 5,332 Å |
| 100 K |
| (300 K) 79,0 Вт/(м·К) |
| 7440-09-7 |
Калий, его соединения придают пламени горелки розовато-фиолетовый оттенок. По этому признаку его легко отличить от других щелочных металлов.
Где используется калий
Калиево-натриевый сплав используется как теплоноситель в атомных реакторах.
Минералы, содержащие калий, аккумулируют изотопы аргона. Благодаря этому возможно определение возраста геологических формаций.
Калийные соединения используются в промышленности:
- Флюс для пайки цветных металлов, сталей.
- Монокристаллы в лазерах, пьезоэлектрики.
- Серебрение, золочение, другие гальванические операции. Используется цианид калия – один из сильнейших ядов.
- Очистка ацетилена от примесей.
- Регенерация воздуха на субмаринах и в противогазах.
 Советский изолирующий противогаз ИП-5
Советский изолирующий противогаз ИП-5 - Щелочные аккумуляторы, сушка газов. Здесь нашлось применение свойству гидроксида калия (едкого кали) усиленно поглощать влагу из окружающей среды.
- Производство стекла.
- Компонент пороха, взрывчатки, спичек (калийная селитра).
- Начинка пиротехники.
- Дубление кожи, отбеливание текстиля.
Перманганат калия задействуют для получения кислорода. Это оказалось жизненно важным в период пандемии коронавируса.
Без перманганата – марганцовки – и бромида (успокоительного) не обходится домашняя аптечка.
 Кристаллы перманганата калия
Кристаллы перманганата калия
Химическое вещество с формулой KMnO4 – это обычная марганцовка.
Достоинства металла оценили аграрии. 90% продукции – это калийные удобрения: поташ, селитра, сильвин («калийная соль»).
Растения, высаженные в бедную калием почву, чахнут, плохо плодоносят. Не меньшее значение имеет микроэлемент для человека.
Жизненные процессы
В организме человека действует связка калий-натрий.
Она контролирует следующие процессы:
- Нормализация кислотно-щелочного, водного баланса, сердечного ритма.
- Содействие появлению мембранного потенциала, работе мышц.
- Поддержание кондиций крови.
Плюс активация ферментов.
Суточная потребность
Суточная норма микроэлемента (г):
- Дети – 0,61 – 1,72.
- Взрослые – 1,82 – 5,1.
Потребность в калии увеличивается при обезвоживании организма (расстройство ЖКТ, рвота, прием мочегонных препаратов, потение).
Питание
Калий поступает в организм с пищей.
Основные поставщики микроэлемента:
- Печень, рыба.
- Бобовые.
- Картофель.
- Молоко.
- Брокколи.
- Цитрусовые, виноград, курага, финики, дыня.
Калием насыщены экзотичные фрукты – помело, киви, авокадо, бананы. Он есть в ореховом масле.
Усвоению калия содействует витамин В6, тормозит алкоголь.
Симптомы недостатка/избытка
Недостаток металла влечет сбои в работе сердечной и скелетной мышц. В тяжелых случаях – невралгию.
Переизбыток опознается по язве тонкого кишечника. Случается остановка сердца.
Цены
На рынке представлена промышленная, аптечная продукция, удобрения с калием.
Цены доступны (руб. / кг):
- Калийные соединения – 50 – 350 (вольфрамат – 2,9 тыс.).
- Минеральные удобрения – 50 – 75.
Стоимость аптечных препаратов определяется брендом либо страной-производителем.
Проверить совместимость мужчины и женщины по Знаку Зодиака
Калий | это… Что такое Калий?
| 19 | Калий |
| [Ar]4s1 |
Ка́лий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета.
В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах.
Очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь.
Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они всё же отличаются.
История и происхождение названия
Калий (точнее, его соединения) использовался с давних времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
В 1807 году английский химик Дэви электролизом расплава едкого кали (KOH) выделил калий и назвал его «потассий» (лат. potassium; это название до сих пор употребительно в английском, французском, испанском, португальском и польском языках).
В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ).
Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Нахождение в природе
В свободном состоянии не встречается. Породообразующий элемент, входит в состав слюд, полевых шпатов и т.д.
Также калий входит в состав сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел Биологическая роль).
Кларк калия в земной коре составляет 2,4 % (5-й по распространённости металл, 7-й по содержанию в коре элемент). Концентрация в морской воде 380 мг/л[3].
Месторождения
Крупнейшие месторождения калия находятся на территории Канады (производитель PotashCorp), России (ОАО «Уралкалий», г. Березники, ОАО «Сильвинит», г. Соликамск, Пермский край, Верхнекамское месторождение калийных руд[4]), Белоруссии (ПО «Беларуськалий», г. Солигорск, Старобинское месторождение калийных руд[5]).
Получение
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расплавленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Важное промышленное значение имеют и методы термохимического восстановления:
и восстановление из расплава хлорида калия карбидом кальция, алюминием или кремнием.[6][7]
Физические свойства
Калий под слоем ТГФ
Калий — серебристое вещество с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки, калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет[8].
Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH.
Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,5247 нм, Z = 2.
Химические свойства
Элементарный калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. На воздухе свежий срез быстро тускнеет из-за образования плёнок соединений (оксиды и карбонат).
При длительном контакте с атмосферой способен полностью разрушиться. С водой реагирует со взрывом. Хранить его необходимо под слоем бензина, керосина или силикона, дабы исключить контакт воздуха и воды с его поверхностью.
С Na, Tl, Sn, Pb, Bi калий образует интерметаллиды.
Взаимодействие с простыми веществами
Калий при комнатной температуре реагирует с кислородом воздуха, галогенами; практически не реагирует с азотом (в отличие от лития и натрия). При умеренном нагревании реагирует с водородом с образованием гидрида (200—350 °C):
с халькогенами (100—200 °C, E = S, Se, Te):
При сгорании калия на воздухе образуется надпероксид калия KO2 (с примесью K2O2):
В реакции с фосфором в инертной атмосфере образуется фосфид зелёного цвета (200 °C):
Взаимодействие со сложными веществами
- Калий при комнатной температуре активно реагирует с водой, кислотами, растворяется в жидком аммиаке (−50 °C) с образованием тёмно-синего раствора.
- Калий глубоко восстанавливает разбавленные серную и азотную кислоты:
- При сплавлении металлического калия со щелочами он восстанавливает водород гидроксогруппы:
- При умеренном нагревании реагирует с газообразным аммиаком с образованием амида (65—105 °C):
- Металлический калий реагирует со спиртами с образованием алкоголятов:
- Алкоголяты щелочных металлов (в данном случае, этаноат калия) являются очень сильными основаниями и широко используются в органическом синтезе.
Соединения с кислородом
- При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
- Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
Советский изолирующий противогаз ИП-5
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия.
Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
- В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
- Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
- Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
- Также известен озонид калия KO3, оранжево-красного цвета. Получить его можно взаимодействием гидроксида калия с озоном при температуре не выше 20 °C:
- Озонид калия является очень сильным окислителем, например, окисляет элементарную серу до сульфата и дисульфата уже при 50 °C:
Гидроксид
Основная статья: Гидроксид калия
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого кали при 20 °C в 100 г воды составляет 112 г.
Применение
- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава: натрий 12 %, калий 47 %, цезий 41 % — обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений.
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединения
Кристаллы перманганата калия
Биологическая роль
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в организме человека
| В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 12 мая 2011. |
Калий содержится большей частью в клетках, до 40 раз больше чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса.
Калий и натрий между собой функционально связаны и выполняют следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых от 1800 до 5000 миллиграммов. Потребность в калии зависит от общего веса тела, физической активности, физиологического состояния, и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются сушёные абрикосы, дыня, бобы, киви, картофель, батат, авокадо, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Практически все сорта рыбы содержат более 200 мг калия в 100 г. Количество калия в разных видах рыбы различается. Овощи, грибы и травы также содержат много калия, однако в консервированных продуктах его уровень может быть гораздо меньше. Много калия содержится в шоколаде.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин B6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При переизбытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
Изотопы
Основная статья: Изотопы калия
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным с периодом полураспада 1,251·109 лет.
В каждом грамме природного калия в секунду распадается в среднем 32 ядра 40K, благодаря чему, например, в организме человека массой 70 кг ежесекундно происходит около 4000 радиоактивных распадов. Поэтому легкодоступные в быту соединения калия (поташ, хлорид калия, калийная селитра и т. д.
) можно использовать как пробные радиоактивные источники для проверки бытовых дозиметров. 40K наряду с ураном и торием считается одним из основных источников геотермальной энергии, выделяемой в недрах Земли (полная скорость энерговыделения оценивается в 40—44 ТВт).
В минералах, содержащих калий, постепенно накапливается калий-аргоновый метод является одним из основных методов ядерной геохронологии.
См. также
- Натрий
- Щелочные металлы
- Банановый эквивалент
Примечания
- ↑ Atomic Weights and Isotopic Compositions for All Elements. NIST Physical Measurement Laboratory. Архивировано из первоисточника 22 августа 2011. Проверено 16 ноября 2010.
- ↑ Химическая энциклопедия: в 5 т / Редкол.: Кнунянц И. Л. (гл. ред.). — М.: Советская энциклопедия, 1990. — Т. 2. — С. 284. — 671 с. — 100 000 экз.
- ↑ J. P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- ↑ КАЛИЙНОЕ МЕСТОРОЖДЕНИЕ
- ↑ Химическое и агрохимическое сырье.
- ↑ А. Ф. Алабышев, К. Д Грачев, С. А. Зарецкий, М. Ф. Лантратов, Натрий и калий (получение, свойства, применение), Л: Гос. н-т. изд-во хим. лит., 1959, С. 321.
- ↑ Хим.энциклопедия, т.2, М.: Сов. энциклопедия, 1990, С.562.
- ↑ Элементы: проба на окрашивание пламени (рус.). Архивировано из первоисточника 22 августа 2011. Проверено 26 января 2010.
- Пилипенко А. Т. Натрий и калий // Справочник по элементарной химии. — 2-е изд. — Киев: Наукова думка, 1978. — С. 316—319.
- Дроздов А. Яростные металлы // Энциклопедия для детей. Химия. — М.: Аванта +, 2002. — С. 184—187. — ISBN 5-8483-0027-5
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Некрасов Б. В. Основы общей химии. — М.: Химия, 1974.
- Спицын В. И., Мартыненко Л. И. Неорганическая химия. — М.: МГУ, 1991, 1994.
- Лидин Р. А. и др.






