- Содержание:
- Кристаллизация металлов









- Кристаллизация металла Энергетические условия кристаллизации любое вещество может находиться в трех агрегатных состояниях: твердом, жидком и газообразном. Переход из одного состояния в другое происходит при определенной температуре, называемой температурой плавления, кристаллизации, кипения или сублимации. 40 этот переход осуществляется при определенных условиях (температура и давление). При атмосферном давлении, которое характерно для большинства производственных процессов, основным параметром перехода является температура.
В газах нет никакой регулярности в расположении частиц, частицы движутся хаотично, и газы стремятся занять как можно больший объем. Твердые кристаллические тела имеют правильную структуру, в которой атомы и ионы находятся в узлах кристаллической решетки (так называемый ближний порядок), а отдельные ячейки и блоки находятся определенным образом относительно друг друга. В жидкости определенная ориентация приходится не на весь объем, а на относительно устойчивую группу или небольшое число атомов, образующих флуктуации. При понижении температуры стабильность колебаний возрастает,
что свидетельствует о способности расти. Таким образом, жидкость характеризуется только близким порядком атомов. Людмила Фирмаль
По мере повышения температуры твердого тела подвижность атомов в узле решетки увеличивается, амплитуда колебаний увеличивается, и при достижении определенной температуры, называемой температурой плавления, температура плавления атома из узла является важной константой, и информация о ней содержится во всех справочниках: ртуть-38,9, температура плавления до температуры плавления нержавеющей стали 3410°C При охлаждении жидкости с последующим затвердеванием наблюдается обратная картина. При охлаждении жидкости, наоборот, подвижность атома уменьшается, и атом образуется ближе к точке плавления атома, заполняя его подобно кристаллу.
Эти группы являются центрами кристаллизации или зародышем, который впоследствии увеличивает слой кристаллов. При достижении температуры плавления-затвердевания кристаллическая решетка вновь формируется, и металл доводится до твердого состояния.
Переход металлов из жидкого состояния в твердое при определенной температуре называется кристаллизацией. Рассмотрены термодинамические условия кристаллизации.
Энергетическое состояние любой системы складывается из энергии движения молекул, атомов, электронов, ядерной энергии, энергии упругого изгиба кристаллической решетки и других видов энергии. Харрис 1.
21 неравновесные (1), метастабильные (2)и стабильные (3)Положения шариков Свободная энергия — это такая составляющая внутренней энергии, которая может быть преобразована в работу в изотермических условиях.
- Свободная энергия изменяет свое значение за счет изменения температуры, плавления, полиморфных превращений и др.:F=U-TS, где F-свободная энергия, U-полная внутренняя энергия системы, T-температура, S-энтропия. Согласно второму закону термодинамики, каждая система стремится к минимуму свободной энергии. Самопроизвольно текущий процесс идет только в том случае, если новое состояние более стабильно, то есть запас свободной энергии меньше. Например, шар стремится скатиться вниз по наклонной плоскости, уменьшая при этом свою свободную энергию. Естественно, самопроизвольный возврат шара с наклонной плоскостью вверх невозможен, так как он увеличивает свободную энергию(рис. 1.21). Процесс кристаллизации подчиняется тем же законам.
Металл затвердевает, когда твердое тело имеет меньше свободной энергии и когда жидкое состояние имеет меньше свободной энергии. Изменение свободной энергии жидкости и твердого тела с изменением температуры показано на рисунке. 1.
22 при повышении температуры величина свободной энергии обоих состояний уменьшается, но закон изменения свободной энергии изменяется в зависимости от жидкого состояния вещества и состояния твердого тела. Существуют теоретические и практические температуры кристаллизации. Ts-это теория RJ=Fn или равновесной температуры кристаллизации.
При такой температуре Рав- ТПЛ ТКР Присутствие металлов как в жидком, так и в твердом состоянии маловероятно.
Фактическая кристаллизация начинается только в том случае, если этот процесс термодинамически благоприятен для системы DR=RZh-RTV, что требует переохлаждения. Людмила Фирмаль
Температура, при которой фактически происходит кристаллизация, называется Рис 1.22 влияние температуры на изменение энергии Гельмгольца F (свободная энергия) жидких и твердых металлов Ирис 1.
23 кривая температуры кристаллизации металла с различными скоростями охлаждения Фактическая температура кристаллизации T. разность между теоретической и фактической температурами кристаллизации называется степенью переохлаждения: at=Ts-TKR.
Чем больше степень переохлаждения, тем больше разница в свободной энергии AR, тем сильнее происходит кристаллизация. На диаграмме показаны тепловые кривые, характеризующие процесс охлаждения при различных скоростях.
Степень переохлаждения мала и происходит при температуре, близкой к равновесию кристаллизации, с постепенным охлаждением, соответствующим кривой 1.23..
Горизонтальная область на тепловой кривой объясняется выделением скрытой теплоты кристаллизации, которая компенсирует тепловыделение. По мере увеличения скорости охлаждения (кривые v2, v3) степень переохлаждения возрастает, и процесс кристаллизации протекает при постоянно понижающейся температуре.
Помимо скорости охлаждения, степень переохлаждения зависит от чистоты металла. Чем чище металл, тем выше степень переохлаждения.
Поскольку переохлаждение до фактической температуры кристаллизации необходимо во время затвердевания, перегрев происходит во время плавления до тех пор, пока не будет достигнута фактическая температура плавления. Д. К.
Даже в Черновцах процесс кристаллизации состоит из 1)зарождения центров кристаллизации;2) роста кристаллов из этих центров. При температуре, близкой к температуре затвердевания, в жидком металле образуется небольшая группа атомов, называемых колебаниями, и атомы заполняются таким же образом, как и твердые кристаллы.
Из некоторых таких колебаний образуются зародыши, или центры кристаллизации. По мере увеличения степени переохлаждения увеличивается число центров кристаллизации, образующихся за единицу времени. Кристаллы начинают расти вокруг образовавшихся центров кристаллизации. В то же время в жидкой фазе образуется новый центр кристаллизации.
Увеличение общей массы затвердевшего металла происходит за счет появления новых центров кристаллизации и роста существующих.
Схема последовательных стадий процесса коагуляции показана на рисунке. 1.24, а-Г. 43A5 рисунок. 1.24 схема кристаллизации металла — *Х0 Четыре.- Х: 8г Взаимный рост кристаллов объясняет неправильную форму частиц.
Настоящие твердые кристаллы неправильной формы называются кристаллитами. Скорость полной кристаллизации зависит от хода обоих элементарных процессов. Она определяется скоростью зарождения центров кристаллизации (NW) и скоростью роста (CP) кристаллов из этих центров(рис. 1.25).
Величины СЗ и СР зависят от степени переохлаждения. При равновесной температуре=0 и Sz=O, CP=0. С увеличением Ат разница в свободной энергии AR=RZh-RTV увеличивается, растет с хорошей степенью подвижности атомов Sz и CP и достигает максимума.
Последующее уменьшение Sz и CP объясняется уменьшением подвижности атома с уменьшением температуры.
При низких значениях коэффициента диффузии перегруппировка атомов жидкости в твердую кристаллическую решетку затруднена. При очень сильном переохлаждении NW и CP равны нулю, жидкость не кристаллизуется, а превращается в аморфное тело.
В реальных металлах, как правило, реализуются только восходящие ветви кривых NW и SR, а с ростом at скорость обоих процессов возрастает.
Ранее, если аморфное состояние достигалось только для солей, силикатов, органических веществ, то с помощью специальной технологии можно добиться высокой скорости охлаждения (более 106°С/С) и высокой температуры стекла металла.
Металл в стеклянном состоянии характеризуется особыми физико-механическими свойствами. Ядрами кристаллизации могут быть основные металлы, примеси, колебания в атомах различных твердых тел. Первый- Т. » Степень переохлаждения — это температура В одних случаях образуется однородный эмбрион, в других-гетерогенный.
Возникновение однородного центра кристаллизации требует значительных энергозатрат. Для того чтобы эмбрион обладал достаточной термодинамической и физической силой, необходимо соответствовать- Рис 1.25 влияние степени переохлаждения на нуклеацию и скорость роста кристаллов Ирис 1.
26, энергия Гельмгольца изменяется в зависимости от размера эмбриона В случае критического размера ГК.
Изменение свободной энергии при равномерном зарождении центров кристаллизации описывается формулой AF=-4/Zpg3&.ФГ++4lg2st, гдеФГ является изменение свободной энергии объема, и является свободной поверхностной энергии.
Энергия, определяемая приведенной зависимостью, включает в себя затраты на появление зародыша и формирование интерфейса. Изменение энергии отрицательно, если процесс кристаллизации происходит при уменьшении свободной энергии, и положительно, если энергия системы увеличивается.
Графически эта связь имеет вид, показанный на рисунке. Если зародыш 1,26 G0, если g=GK, так как AF положительна и ее значение увеличивается.
Размер зародыша g>ha, когда его роль в процессе кристаллизации становится определяющей, в это время DG
Pereosnastka.ru
- Кристаллизация металлов
- Категория:
- Металлы
Кристаллизация металлов
При рассмотрении жидких расплавленных металлов можно подумать, что они представляют собой аморфные изотропные тела с хаотическим тепловым движением атомов.
Рентгеноструктурное исследование жидкого металла вблизи точки плавления обнаруживает некоторую упорядоченность в расположении атомов, сходную с упорядоченностью кристаллической решетки твердого металла.
Предположение о том, что эта упорядоченность то возникает, то исчезает, кажется вероятным. Представляется несомненным, что в огромном количестве движущихся атомов могут возникать мгновенные пространственные комбинации, напоминающие мельчайшие кристаллические образования и являющиеся потенциальными зародышами будущих кристаллов.
Устойчивость таких случайных сочетаний должна повышаться с уменьшением энергии движения атомов, т. е. с понижением^ температуры жидкого металла. Тем не менее истинно устойчивых зародышей не образуется и затвердевание не начинается, даже при теоретической температуре кристаллизации (плавления).
Образование устойчивых зародышей и начало их роста обычно требует возникновения поверхности раздела между жидким твердым металлами (между жидкой и твердой фазой). Однако возникновение поверхности раздела требует определенных
условий, которых при температуре плавления еще не может создаться. С точки зрения термодинамики дело здесь связано с запасом свободной энергии твердой и жидкой фазы.
Под свободной энергией понимается часть энергии системы, уменьшающаяся при протекании в последней самопроизвольных процессов (в условиях постоянной температуры).
Как общее правило, устойчивой в каких-то определенных условиях оказывается та из фаз, у которой свободная энергия меньше. Образование поверхности раздела обязательно связано с увеличением свободной энергии, почему при температуре плавления устойчивой является уже существующая жидкая фаза и кристаллизация оказывается теоретически невозможной.
Образование и начало роста устойчивых зародышей, как правило, происходит при некотором переохлаждении ниже теоретической температуры кристаллизации и может быть облегчено рядом дополнительных факторов.
Сюда относятся: неоднородность распределения энергии между атомами и неоднородность распределения плотности жидкого металла, а также наличие готовых поверхностей раздела между жидкой и твердой фазами.
В последнем случае в качестве готовых поверхностей раздела могут служить поверхности частиц твердых кристаллических примесей, действующих особенно эффективно, если они обладают пространственной решеткой, сходной с решеткой кристаллизующегося металла.
Итак, кристаллизация чистых металлов из расплавленного состояния есть скачкообразный процесс изменения интенсивности движения атомов жидкого металла и размещения их в узлах кристаллической решетки. Процесс этот растянут во времени.
Он начинается, когда в результате переохлаждения ниже температуры плавления и воздействия других ранее названных факторов энергия движения некоторых атомов настолько уменьшается, что образовавшиеся кристаллические зародыши, развивающиеся в дальнейшем как отдельные металлические кристаллы, становятся устойчивыми и способными к росту. Энергия атомов при этом освобождается в форме скрытой теплоты кристаллизации, в результате чего температура металла поднимается до точки плавления или, несколько не достигая ее, поддерживается на этом постоянном уровне до завершения кристаллизации.
Одним из распространенных способов изучения процесса затвердевания, позволяющим определить температуру, а также начало и конец кристаллизации во времени является метод термического анализа. Кривые, полученные при термическом анализе процесса кристаллизации, представлены на рис. 1, а в схематизированном виде и на рис. 6,в в том виде, как это иногда наблюдается в действительности.
Для ряда металлов переохлаждение колеблется от десятых полей до нескольких градусов, вследствие чего без применения точной методики исследования его бывает трудно обнаружить. Некоторые металлы, обладающие сложной решеткой, способны переохлаждаться на несколько десятков градусов. Так, например, сурьма переохлаждается примерно на 40, а олово на 53°.
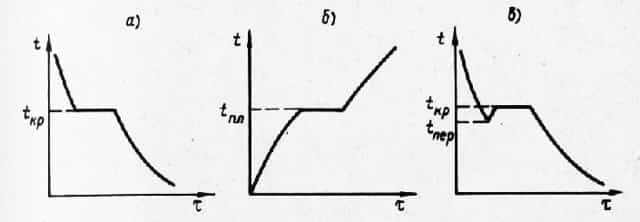
Рис. 1. Термические кривые с точками затвердевания и плавления: а — при охлаждении (схематическая); б — при нагреве; в — при охлаждении (действительная)
При наличии готовых центров кристаллизации, например тугоплавких металлических включений, явление переохлаждения проявляется в меньшей степени.
После образования зародышей и по мере их развития температура, как правило, повышается и дальнейшая кристаллизация может идти без переохлаждения. Однако в ряде случаев после начала кристаллизации температура не поднимается до точки плавления и процесс до конца протекает при некотором переохлаждении.
Особенно часто гистерезис наблюдается при кристаллизации и в процессе превращения металлов и сплавов в твердом состоянии, например, при переходе одной аллотропической модификации в другую.
Процесс образования кристалла может состоять в послойной укладке групп атомов в порядке, диктуемом расположением атомов в зародыше. В этом случае при определенных благоприятных условиях образуется правильный полногранный кристалл.
В обычных условиях, когда рост идет одновременно из нескольких центров и увеличивающиеся полногранные кристаллы, сталкиваясь, мешают росту друг друга, получаются кристаллические образования с искаженными внешними очертаниями, обычно называемые не кристаллами, а кристаллитами или зернами.
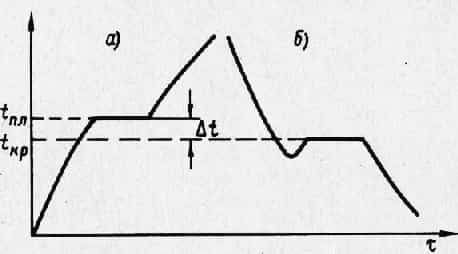
Рис. 2. Температурный гистерезис при плавлении и затвердевании чистого металла: а — кривая нагрева; б — кривая охлаждения
Развитие полногранных кристаллов не является единственным путем образования кристаллитов в металле.
Часто кристаллы, зародившиеся как полногранные, в дальнейшем приобретают характер не послойного, а так называемого дендритного развития, в результате которого кристаллические образования получают скелетную или древовидную форму. Обычно эти кристаллы называют дендритными. Дендритные кристаллы с искаженной внешней формой также носят название кристаллитов, или зерен.
Дендритная кристаллизация была подмечена еще Д. К. Черновым. Кристалл его имени представляет образец дендрита, выросшего в условиях кристаллизации стального слитка до огромных размеров и веса (высота 39 см, вес 3,45 кг).
Схема образования дендритов по Чернову представлена на рис. 3,а.
Пример дендритного строения металла представлен на рис. 3, б, где изображено кристаллическое образование из большого количества ярко выраженных дендритных кристаллов железа).
Разновидностью дендритной кристаллизации является образование в слитках столбчатых (шестоватых) кристаллов. Явление образования столбчатых дендритов, пронизывающих слиток от периферии до сердцевины, носит название транс-кристаллизации.

Рис. 3. Иллюстрации дендритной кристаллизации: а — схема образования дендритов по Чернову; б — дендриты железа
Следует подчеркнуть, что независимо от сложности строения и разделения на огромное количество ветвей дендрит представляет собой монокристалл, растущий из одного центра кристаллизации.
Схема образования дендритного кристалла по А. А. Бочвару представлена на рис. 6. Она показывает, что зародыш полно-гранного кристалла под влиянием условий кристаллизации постепенно приобретает преимущественное развитие у ребер и вершин кристалла.
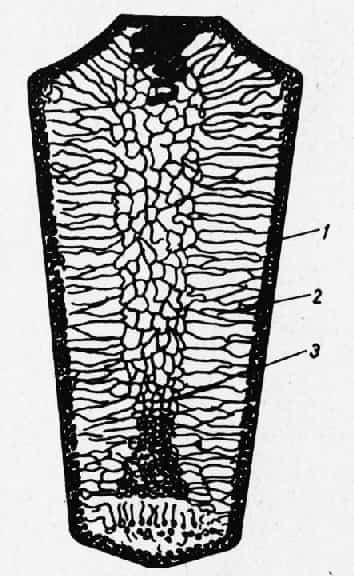
Рис. 4. Схема структуры стального слитка (по Н, А. Минкевичу)
Рис. 5. Макроструктура слитка с транскристаллизацией
Предполагается, что основной причиной неоднородного развития кристалла является торможение роста инородными примесями, всегда имеющимися в достаточном количестве в любом, даже самом чистом реальном металле.
Эти примеси скопляются на гранях кристалла и в наибольшей степени мешают кристаллизации в их центре, в то время как на ребрах, и особенно на вершинах, они смываются конвекционными токами жидкого металла, почему эти места получают возможность преимущественного роста.
Строение литого металла, например в слитке, получающееся в результате первичной кристаллизации из жидкого состояния, зависит от условий охлаждения, определяемых температурой расплавленного металла, температурой формы (или изложницы), характером отвода тепла и т. д.
Схема структуры слитка металла представлена на рис. 3.
- Различают три зоны слитка:
1) зону мелких кристаллитов, образовавшихся в первый момент кристаллизации;
2) зону столбчатых (шестоватых) кристаллитов, образовавшихся в условиях более медленного отвода тепла, направленного перпендикулярно стенкам формы; - 3) зону равноосных крупных кристаллитов, выросших в условиях очень медленного отвода тепла без видимой его направленности.
Д. К.
Чернов установил, что процесс кристаллизации состоит в возникновении из жидкого сплава кристаллических образований весьма малого размера, названных им зачатками, и в последующем росте этих зачатков.
Позже в лекциях по сталелитейному делу (1898 г.) Чернов говорил уже о «центрах кристаллизации», т. е. применял термин, широко используемый и в современной физической химии и металловедении.
Образование новых центров кристаллизации протекает одновременно с ростом центров кристаллизации, уже возникших ранее.
Схемы кристаллизации на базе представлений Д. К. Чернова успешно разрабатывал И. Л. Миркин. Одна из таких схем представлена на рис. 7.
Используя теорию вероятности, Миркин показывает, что в первые секунды кристаллизации ежесекундно возникает примерно одинаковое число центров (на схеме 5 центров в секунду), а участие в процессе роста принимает все большее количество кристаллов (в первую секунду 5, во вторую 10).
Поэтому процесс кристаллизации в первые секунды идет, все ускоряясь.
Однако в дальнейшем наблюдается его замедление: в третью и четвертую секунды в уменьшившемся по объему жидком сплаве возникает только по 4 центра, в пятую — 3, в шестую — 2, в седьмую процесс кристаллизации заканчивается образованием 23 кристаллов вместо 30, как можно было предположить в начале кристаллизации. На четвертой секунде наблюдается начало столкновения растущих кристаллов друг с другом, взаимная помеха их росту, а следовательно, опять-таки замедление процесса кристаллизации.
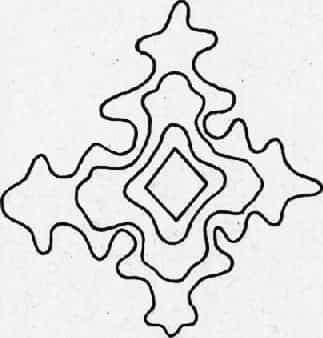
Рис. 6. Схема образования дендритного кристалла по А. А. Бочвару
Немецкий металловед Г. Тамман исследовал важнейшие факторы, определяющие процесс кристаллизации, с целью найти количественные зависимости процесса от этих факторов.
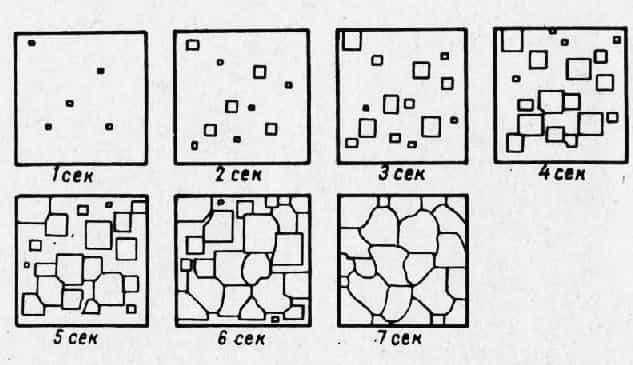
Рис. 7. Схема процесса кристаллизации
линейное перемещение граней кристалла в единицу времени. Так, например, если в одном кубическом сантиметре кристаллизующегося металла в течение одной секунды возникает 5 центров, то vc = 5, и если за одну минуту грань растущего кристалла переместилась на 0,2 мм, то vK — 0,2 мм/мин.
Тамман установил качественную связь vt и vK со скоростью охлаждения (переохлаждением). Для металлов эта связь имеет вид кривых, представленных на рис. 8.
Для металлов существует оптимальная скорость охлаждения, при которой получается наиболее мелкозернистая структура. Это некоторая средняя скорость. Медленное охлаждение дает крупнозернистую структуру, очень быстрое — тоже.
- Отсюда возникает практический вывод: получению мелкозернистой структуры способствует литье в слегка подогретую форму, но не в горячую (очень медленное охлаждение) и не в холодную (очень быстрое).
- Зависимости, установленные Тамманом, относятся к чистым металлам, застывающим в спокойном состоянии.
- В реальных условиях кроме скорости охлаждения на величину зерна оказывают влияние и другие факторы.
- Важнейшими из них являются: 1) наличие или отсутствие субмикроскопических примесей, взвешенных в расплавленном металле;
- 2) состояние металла в момент кристаллизации — спокоен он или встряхивается.
Присутствие в расплавленном металле субмикроскопических твердых частиц, могущих выполнять роль центров кристаллизации, значительно ускоряет процесс зарождения кристаллов.
При большом количестве таких готовых центров структура получается мелкозернистой.
Роль готовых центров кристаллизации, как было указано, могут выполнять различные тугоплавкие неметаллические включения, например окислы металлов и в частности окись алюминия.
Состояние металла в момент кристаллизации также оказывает существенное влияние на его зернистость. Еще Д. К. Чернов отметил влияние вибраций на структуру и сам применил встряхивание при кристаллизации с целью получения более мелкозернистого строения металла.
Реклама:
Процесс кристаллизации металлов
Кристаллизацией называется переход из жидкого в твердое состояние с образованием кристаллических решеток или кристаллов. В реальных металлических телах кристаллизация расплавов заканчивается образованием структуры сложно переплетенных кристаллов — дендритов. Их морфология определяет свойства материалов. При образовании кристаллов их развитие идет в основном в направлении, перпендикулярном плоскостям с максимальной плотностью упаковки атомов. Это приводит к тому, что первоначально образуются длинные ветви, так называемые оси первого порядка. Одновременно с удлинением осей первого порядка на их ребрах зарождаются и растут перпендикулярные к ним такие же ветви второго порядка. в свою очередь на них растут оси третьего порядка и т.д. Образуются кристаллы древовидной — дендритной формы. Преимущественный рост кристалла происходит в направлении отвода тепла. Ветви дендритов разделены очень тонкими прослойками нерастворимых в жидком и особенно в твердом состоянии примесей и мельчайшими полостями и порами, возникшими в результате уменьшения объема при переходе металла из жидкого состояния в твердое. При tпл, определенной для каждого металла, твердый металл переходит в жидкий. Многие свойства при этом меняются незначительно. Например, плотность падает на 5-7% , электропроводность и теплопроводность возрастают. Характер внутренних сил не изменяется. Металлическая жидкость по своему строению близка к твердому телу. Кристаллическая решетка сохраняется до температуры плавления. После расплавления решетка разрушается, но сохраняется динамический ближний порядок. Затвердевание происходит при температуре tзатв, она меньше tпл. Существует переохлаждение и перенагрев.
При температуре Тп величины свободных энергий жидкого и твердого состояния равны. Процесс кристаллизации протекает при температуре, меньшей Тп. Для начала затвердевания необходимо переохлаждение (разность энергий). Переохлаждение тем больше, чем больше скорость изменения.
Процесс кристаллизации происходит в два этапа: образование зародышей кристаллов; рост образовавшихся кристаллов.
В реальных металлах центрами кристаллизации являются тугоплавкие частицы и стенки литейной формы.
В чистых металлах центрами кристаллизации служат области с дальним порядком расположения атомов (кластеры), т.е. их строение близко к строению кристаллической решетки.
Чем больше скорость охлаждения (степень переохлаждения), тем более мелкозернистая структура образуется. Если скорость охлаждения порядка 105-106 градусов в секунду, получается аморфная структура.
5.Строение металлического слитка. Особенности строения литого и деформированного металла.
Кристаллизация стального слитка идет в три стадии. Сначала на поверхности слитка образуется зона мелких кристаллов за счет влияния холодных стенок формы, которые обеспечивают в начальный момент времени высокую скорость охлаждения. Затем растут большие кристаллы, вытянутые по направлению отвода теплоты (столбчатые кристаллы).
В середине слитка, где наблюдается наименьшая степень переохлаждения, образуются большие равновесные кристаллы. При некоторых условиях (перегретый жидкий металл, малое содержание примесей) зона крупных равновесных кристаллов почти исчезает. Структура слитка состоит практически из одних столбчатых кристаллов — транскристаллическая.
Зона столбчатых кристаллов обладает наибольшей плотностью, но в местах стыка столбчатых кристаллов собираются нерастворимые примеси, и такие слитки часто расьтрескиваются при обработке давлением.
В верхней части слитка, затвердевающей в последнюю очередь, концентрируется усадочная раковина. Там содержится много количества усадочных пор. Слиток имеет неоднородный состав.
По направлению от поверхности к центру и снизу вверх увеличивается концентрация углерода и вредных примесей: серы и фосфора. Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией.
Она отрицательно влияет на механические свойства.
Пластическая деформация металлов и сплавов как тел поликристаллических, имеет некоторые особенности по сравнению с пластической деформацией монокристалла. Деформация поликристаллического тела складывается из деформации отдельных зерен и деформации в приграничных объемах.
Плоскости скольжения зерен произвольно ориентированны в пространстве, поэтому под влиянием внешних сил напряжения в плоскостях скольжения отдельных зерен будут различны.
Деформация начинается в отдельных зернах, в плоскостях скольжения которых возникают максимальные касательные напряжения. Соседние зерна будут разворачиваться и постепенно вовлекаться в процесс деформации.
Деформация приводит к изменению формы зерен: зерна получают форму, вытянутую в направлении наиболее интенсивного течения металла (поворачиваются осями наибольшей прочности вдоль направления деформации.
Металл приобретает волокнистое строение. Волокна с вытянутыми вдоль них неметаллическими включениями являются причиной неодинаковости свойств вдоль и поперек волокон. Одновременно с изменением формы зерен в процессе пластической деформации происходит изменение ориентировки в пространстве их кристаллической решетки.
Деформированный металл находится в неравновесном состоянии. Переход к равновесному состоянию связан с уменьшением искажений в кристаллической решетке, снятием напряжений, что определяется возможностью перемещения атомов.
- При повышении температуры металла в процессе нагрева после пластической деформации диффузия атомов увеличивается и начинают действовать процессы разупрочнения, приводящие металл в более равновесное состояние – возврат и рекристаллизация.
- Возврат. Небольшой нагрев вызывает ускорение движения атомов, снижение плотности дислокаций, устранение внутренних напряжений и восстановление кристаллической решетки
- Рекристаллизация – процесс зарождения и роста новых недеформированных зерен при нагреве наклепанного металла до определенной температуры.
Нагрев металла до температур рекристаллизации сопровождается резким изменением микроструктуры и свойств. Нагрев приводит к резкому снижению прочности при одновременном возрастании пластичности. Также снижается электросопротивление и повышается теплопроводность.
1 стадия – первичная рекристаллизация (обработки) заключается в образовании центров кристаллизации и росте новых равновесных зерен с неискаженной кристаллической решеткой. Новые зерна возникают у границ старых зерен и блоков, где решетка была наиболее искажена. Количество новых зерен постепенно увеличивается и в структуре не остается старых деформированных зерен.
Движущей силой первичной рекристаллизации является энергия, аккумулированная в наклепанном металле. Система стремится перейти в устойчивое состояние с неискаженной кристаллической решеткой.
2 стадия – собирательная рекристаллизация заключается в росте образовавшихся новых зерен.
Движущей силой является поверхностная энергия зерен. При мелких зернах поверхность раздела большая, поэтому имеется большой запас поверхностной энергии. При укрупнении зерен общая протяженность границ уменьшается, и система переходит в более равновесное состояние.
Основными факторами, определяющими величину зерен металла при рекристаллизации, являются температура, продолжительность выдержки при нагреве и степень предварительной деформации
С повышением температуры происходит укрупнение зерен, с увеличением времени выдержки зерна также укрупняются. Наиболее крупные зерна образуются после незначительной предварительной деформации 3…10 %. Такую деформацию называют критической. И такая деформация нежелательна перед проведением рекристаллизационного отжига.
Практически рекристаллизационный отжиг проводят дпя малоуглеродистых сталей при температуре 600…700oС, для латуней и бронз – 560…700oС, для алюминевых сплавов – 350…450oС, для титановых сплавов – 550…750oС.
Процесс кристаллизации расплавов металлов
Кристаллизация — переход металла (сплава) из жидкого состояния в твердое — происходит в условиях, когда расплав переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией (свободная энергия кристалла меньше свободной энергии жидкой фазы).
Влияние температуры на свободную энергию жидкой (Gж) и твердой фазы (Gт) показано на рис. 1а.
При температуре плавления Тпл жидкая и твердая фазы существуют одновременно. Реальный процесс кристаллизации протекает при переохлаждении металла ниже теоретической температуры кристаллизации Тпл. Величина ?Т= Тпл — Ткр называется степенью переохлаждения.
Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, приведены на рис. 1 б (v— скорость охлаждения, v1 < v2 < v3).
Вначале, когда металл находится в жидком состоянии, температура системы уменьшается плавно. При достижении температуры Тпл на кривой охлаждения появляется горизонтальная площадка, так как отвод теплоты в окружающую среду компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации.
По окончании кристаллизации температура вновь уменьшается плавно. При медленном охлаждении (v1) степень переохлаждения мала, и кристаллизация протекает при температуре, близкой к теоретической температуре кристаллизации Тпл. С увеличением скорости охлаждения степень переохлаждения возрастает, и кристаллизация происходит при более низких температурах.
Рисунок 1. Охлаждение расплава и начало кристаллизации
а — изменение свободной энергии (G) в жидком (G Ж) и твердом (G т) состоянии в зависимости от температуры: Ткр — температура начала кристаллизации; Тпл — температура, при которой жидкая и твердая фазы существуют одновременно; ?T — степень переохлаждения; б — кривые охлаждения металлов при кристаллизации: ?T1, ?T2, ?T3 — степень переохлаждения при скорости охлаждения v1, v2, v3 соответственно.
Чем «чище» жидкий металл, тем выше температура переохлаждения.
Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров.
С повышением степени переохлаждения увеличиваются число зародышей и скорость кристаллизации. Но при дальнейшем повышении степени переохлаждения скорость роста зародышей и скорость кристаллизации уменьшаются.
Рост кристаллов заключается в присоединении к зародышам все новых атомов из жидкой фазы (рис. 2 а). Центры кристаллизации — зародыши (черные квадраты) — самопроизвольно возникают при переохлаждении металла.
Очень маленькие зародыши неустойчивы, возникнув, они растворяются. Чем больше степень переохлаждения, тем устойчивее зародыши, тем меньше их критический размер.
Далее зародыши увеличиваются в размере, одновременно появляются новые зародыши.
Пока число зародышей невелико, кристаллы растут свободно и сохраняют правильную геометрическую форму. В местах соприкосновения отдельных кристаллов рост их отдельных граней прекращается, развиваются грани в тех местах, где есть свободная жидкость. В результате кристаллы не имеют правильной геометрической формы.
Такие кристаллы называются кристаллитами. Чем больше центров кристаллизации, тем больше образуется кристаллов в данном объеме, тем мельче окончательный размер кристаллов.
Однако уменьшение скорости зарождения числа зародышей при критических температурах ограничивает возможность регулирования их размера повышением скорости охлаждения.
С целью регулирования размеров зерен часто применяют искусственное введение в расплав веществ, создающих центры кристаллизации (модифицирование). В технических металлах в качестве центров кристаллизации часто выступают инородные включения (например, шлаковые включения, частички футеровки печи, оксиды металлов).
Рис. 2. Схема кристаллизации металла
а — схема роста кристаллов; б — структура дендрита; в — схема образования дендрита; ¦ — зародыши; 1, 2, 3 — оси кристаллизации.
В большинстве случаев кристаллизация металлов происходит с большой скоростью (кристаллизация при заливке металла в изложницу, кристаллизация расплава при литье в металлические формы).
При ускоренном охлаждении металла кристаллы растут неравномерно.
Рост зародышей по одной из осей (в направлении наибольшего градиента температур) значительно опережает рост по другим осям, происходит так называемая дендритная кристаллизация.
Д.К.Чернов, описывая рост дендрита (рис. 2 б), ввел понятие «порядок осей кристаллизации». После образования зародыша его развитие (рис. 2 в) идет в направлении наибольшего градиента температур (ось первого порядка).
Увеличение размеров осей первого порядка происходит не только в длину, одновременно увеличивается и ее ширина.
В дальнейшем от осей первою порядка под определенными углами начинают расти новые оси, называемые осями второго и третьего порядка.
По мере роста осей более высокого порядка (четвертого, пятого и т.д.) постепенно заполняются все промежутки, ранее занятые жидким металлом, — дендритная кристаллизация замедляется.
Дендритная кристаллизация отчетливо выражена в условиях недостатка жидкого металла для заполнения пространства (поверхностные слои, усадочная раковина) и при наличии примесей и посторонних атомов в расплаве (кристаллизация реальных сплавов).
Процесс кристаллизации расплавов
- Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией.
- Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров.
- Процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры кристаллизации Т„, при которой жидкая и твердая фазы могут сосуществовать одновременно и притом бесконечно долго. Разность между температурами Т„ и Гк, при которых может протекать процесс кристаллизации, носит название степени переохлаждения:
png»>
При переохлаждении сплава ниже температуры ТЛЧ во многих участках жидкого сплава образуются устойчивые, способные к росту кристаллические зародыши, называемые критическими.
Пока образовавшиеся кристаллы растут свободно, они имеют более или менее правильную геометрическую форму. Однако при столкновении растущих кристаллов их правильная форма нарушается, так как в этих участках рост граней прекращается.
Рост продолжается только в тех направлениях, где есть свободный доступ жидкости.
В результате растущие кристаллы, имевшие сначала геометрически правильную форму, после затвердевания получают неправильную внешнюю форму и поэтому называются кристаллитами или зернами.
Процесс кристаллизации протекает тем быстрее, чем больше образуется зародышей (центров кристаллизации) в единицу времени и в единице объема и чем больше скорость их роста.
Чем больше скорость образования зародышей и меньше скорость их роста, тем меньше размер кристалла, выросшего из одного зародыша (зерно) и, следовательно, более мелкозернистой будет структура металла.
При небольшой степени переохлаждения АТ (малой скорости охлаждения) число зародышей мало. В этих условиях будет получено крупное зерно. С увеличением степени переохлаждения скорость образования зародышей возрастает и размер зерна в затвердевшем металле уменьшается.
Размер зерна металла сильно влияет на его механические свойства. Эти свойства, особенно вязкость и пластичность, выше, если металл имеет мелкое зерно.
На размер зерна оказывают влияние:
- — температура нагрева и разливки жидкого металла;
- — химический состав и особенно присутствие в металле посторонних примесей.
В технических металлах всегда присутствует большое количество различных примесей (окислов, неметаллических включений и т.д.), которые облегчают образование зародышей, когда:
- — примесь имеет более высокую температуру плавления, чем основной металл;
- — кристаллические решетки примеси и основного металла одинаковы и примерно одинаковы параметры решеток.
Чем больше примесей, тем больше центров кристаллизации, тем мельче получается зерно. Такое образование зародышей называют гетерогенным.
Для получения мелкого зерна создают искусственные центры кристаллизации. Для этого в жидкий металл вводят специальные примеси, называемые модификаторами. Эти примеси, практически не изменяя химического состава сплава, вызывают при кристаллизации измельчение зерна и в итоге улучшение механических свойств.
Кристаллизация металлов и сплавов
-
Процесс
перехода из жидкого или газообразного
состояния в твердое, в результате чего
образуется кристаллическая решетка и
возникают кристаллы, называется
кристаллизацией.
-
Чем
объясняется существование при одних
температурах жидкого, а при других
температурах твердого состояния и
почему превращение происходит при
строго определенных температурах? -
В
природе все самопроизвольно протекающие
превращения, а следовательно, кристаллизация
и плавление обусловлены тем, что новое
состояние в новых условиях является
энергетически более устойчивым, обладает
меньшим запасом энергии. -
Энергетическое
состояние системы, имеющей огромное
число охваченных тепловым движением
частиц (атомов, молекул), характеризуется
особой термодинамической функцией (F
), называемой свободной
энергией,
которая определяется: -
F=
U
– TS, -
где U
– внутренняя энергия системы; -
Т
— абсолютная температура; -
S
— энтропия -
Можно
сказать, что чем больше свободная энергия
системы, тем система менее устойчива,
и если имеется возможность, то система
переходит в состояние, где свободная
энергия меньше.
С
изменением внешних условий, например
температуры, свободная энергия системы
изменяется по сложному закону, но
различно для жидкого и твердого состояний
(рис. 3.1).
Рис.
3.1. Изменение свободной энергии жидкого
и кристаллического состояний в зависимости
от температуры
Выше
температуры Тs
меньшей
свободной энергией обладает вещество
в жидком состоянии, ниже
Ts
– вещество
в твердом состоянии. Следовательно,
выше Ts
вещество должно находиться в жидком
состоянии, а ниже Ts
– в твердом, кристаллическом.
Очевидно,
что при температуре, равной Ts
свободные энергии жидкого и твердого
состояний равны, металл в обоих состояниях
находится в равновесии.
Эта температура
Ts
и есть равновесная
или теоретическая
температура
кристаллизации.
Однако, при Ts
Fж
= Fкр,
и процесс кристаллизации (плавления)
не может идти, так как при равенстве
свободных энергий обеих фаз плавление
(кристаллизация) не будут сопровождаться
уменьшением свободной энергии.
Для
начала кристаллизации необходимо, чтобы
процесс был термодинамически выгоден
системе и сопровождался уменьшением
свободной энергии системы. Их кривых
(рис. 3.1) видно, что это возможно только
тогда, когда жидкость будет охлаждена
ниже точки Ts.
-
Температура,
при которой практически начинается
кристаллизация, может быть названа
фактической
температурой кристаллизации. -
Охлаждение
жидкости ниже температуры кристаллизации
называется переохлаждением. -
Обратное
превращение из кристаллического
состояния в жидкое может произойти
только выше температуры Ts,
это явление называется перенагреванием. -
Величиной
или степенью переохлаждения называют
разность между теоретической и фактической
температурами кристаллизации T
= Ts
— Tф.
Процесс
перехода металла из жидкого состояния
в кристаллическое можно изобразить
кривыми в координатах время – температура
(рис. 3.2).
Рис.
3.2. Кривые охлаждения, полученные при
кристаллизации металла
Охлаждение
металла в жидком состоянии сопровождается
плавным понижением температуры и может
быть названо простым охлаждением, так
как при этом нет качественного изменения
состояния.
При достижении температур
кристаллизации на кривой температура
– время появляются горизонтальные
площадки (рис.3.
2), так как отвод тепла
компенсируется выделяющейся при
кристаллизации скрытой
теплотой кристаллизации.
3.2.
Механизм процесса кристаллизации
Процесс
кристаллизации состоит из двух
элементарных процессов. Первый процесс
заключается в зарождении мельчайших
частиц кристаллов, которые называются
зародышами
или центрами кристаллизации.
Второй процесс состоит в росте кристаллов
из этих центров.
Модель
кристаллизации металла в первые 7 секунд
охлаждения представлена схемой процесса
кристаллизации (рис.3.3) и кинетической
кривой кристаллизации (рис.3.4).
Рис.
3.3. Схема процесса кристаллизации
Рис.
3.4. Кинетическая кривая кристаллизации
По
мере развития кристаллизации в нем
участвуют все большее и большее число
кристаллов. Поэтому процесс вначале
ускоряется, пока в какой-то момент
взаимное столкновение растущих кристаллов
начинает заметно препятствовать их
росту.
Рост кристаллов замедляется еще
и потому, что количество жидкости, в
которой образуются новые кристаллы,
становится все меньше. В процессе
кристаллизации, пока кристалл окружен
жидкостью, он часто имеет правильную
форму, но при столкновении и срастании
кристаллов их правильная форма нарушается.
Внешняя форма кристалла оказывается
зависимой от условий соприкосновения
растущих кристаллов. Вот почему кристаллы
металла — зерна (кристаллиты) не имеют
правильной формы.
Скорость
всего процесса кристаллизации
количественно определяется двумя
величинами: скоростью зарождения центров
кристаллизации и скоростью роста
кристаллов (рис.3.5).
Рис.
3.5. Зависимость скорости кристаллизации
(СК) и скорости зарождения центров
кристаллизации (ЧЦ) от степени
переохлаждения
Величины
оптимального переохлаждения до достижения
максимальной скорости кристаллизации
(СК) и до образования максимального
числа центров кристаллизации (ЧЦ) не
совпадают.
Размер
образовавшихся кристаллов зависит от
соотношения СК и ЧЦ. При большом значении
СК и малом значении ЧЦ образуется мало
крупных кристаллов. При малых значениях
СК и больших ЧЦ образуется большое число
мелких кристаллов.
Минимальный
размер способного к росту зародыша
называется критическим
размером
зародыша.
Кристаллизация металлов и сплавов
Процесс кристаллизации.
При переходе металла из жидкого состояния в твердое образуются кристаллы. Такой процесс называют кристаллизацией.
Процесс кристаллизации металла можно рассматривать по кривым охлаждения, которые обычно получают опытным путем. Например, для чистого металла, охлаждаемого очень медленно, кривая охлаждения показывает, что, если металл находится в жидком состоянии, температура понижается почти равномерно.
Если металл охладить до температуры плавления Тпл (точка а на кривой), то начинается кристаллизация ипадение температуры прекращается, несмотря на непрерывную отдачу тепла окружающей атмосфере.
Получаемый горизонтальный участок на кривой охлаждения показывает, что в металле происходит процесс образования кристаллов с выделением тепла, называемый теплотой кристаллизации. Кристаллизация протекает от точки а до точки б, где она заканчивается и металл затвердевает.
Дальнейшее падение температуры на кривой указывает на охлаждение затвердевшего слитка (рис. А).
В металлических сплавах кривая охлаждения имеет несколько иной вид. Охладившись до температуры плавления ТПл, сплав еще некоторое время остается жидким. Кристаллизация сплава начинается при температуре переохлаждения Тп, лежащей ниже теоретической температуры плавления.
Разность между теоретической и фактической температурами кристаллизации называют степенью переохлаждения. Она зависит от природы сплава, его чистоты и скорости охлаждения. Чем больше скорость охлаждения сплава, тем больше степень переохлаждения.
Петля на кривой охлаждения показывает, что кристаллизация сопровождается выделением тепла, которое повышает температуру сплава до температуры плавления, поддерживая ее до полного затвердевания металла. (рис.Б)
Аморфные тела затвердевают постепенно. В этом случае кривая охлаждения будет плавной, без горизонтальных площадок. (рис.В)
Процесс образования кристаллов состоит из двух одновременно протекающих стадий: появления зародышей — устойчивых центров кристаллизации и роста кристалликов вокруг этих центров.
Сначала каждый кристаллик в жидкости растет свободно, сохраняя правильную геометрическую форму.
Так как одновременно образуется много кристаллических центров и рост кристалликов идет по всем направлениям, то смежные кристаллы, увеличиваясь, начинают непосредственно соприкасаться друг с другом и правильная форма их нарушается.
В результате кристалл приобретает округленную форму, напоминающую зерно. Такие кристаллы принято называть кристаллитами, или зернами.
В зависимости от условий затвердевания зерна могут быть крупными, хорошо различимыми невооруженным глазом, и мелкими, которые можно рассмотреть только при помощи металлографического микроскопа.
Процесс кристаллизации может быть описан количественно, если известны зарождение центров кристаллизации и скорость роста кристалликов.
Число центров кристаллизации и скорость роста кристалликов зависят от степени переохлаждения металла.
С увеличением степени переохлаждения ∆T число центров и скорость роста также возрастают, достигая максимального значения. Однако характер роста величин числа центров и скорости роста различен.
Если степень переохлаждения невелика, то скорость роста преобладает над числом центров, в результате чего образуется крупнозернистая структура.С увеличением степени переохлаждения скорость роста не изменяется, число центров продолжает расти, что приводит к образованию мелкозернистой структуры.






