- Атомная кристаллическая решетка
- Молекулярная кристаллическая решетка
- Ионная кристаллическая решетка
- Металлическая кристаллическая решетка
- Кристаллические решетки
- Молекулярная кристаллическая решетка
- Ионная кристаллическая решетка
- Металлическая кристаллическая решетка
- Атомная кристаллическая решетка
- Виды кристаллических решёток: атомная, молекулярная, металлическая и ионная
- Виды кристаллических решёток
- Атомная кристаллическая решётка
- Ионная кристаллическая решётка
- Молекулярная кристаллическая решётка
- Металлическая кристаллическая решётка
- Видео
- Типы кристаллических решёток
- 1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения
- В узлах молекулярной кристаллической решетки
- В узлах атомной кристаллической решетки
- У веществ с ионной кристаллической решеткой
- Металлическая кристаллическая решетка
- Урок 4. строение кристаллов. кристаллические решётки. причины многообразия веществ — Химия — 11 класс — Российская электронная школа
- Абросимова Елена Владимировна учитель химии и биологии — Кристаллические решетки
Как известно, все вещества состоят из частиц — атомов, которые могут располагаться хаотично или в определенном порядке.
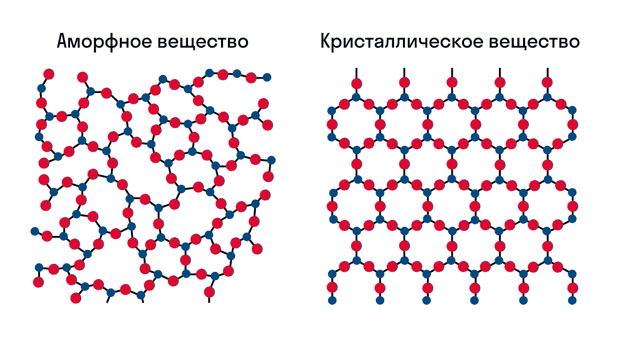
У аморфных веществ частицы расположены беспорядочно, а у кристаллических они образуют определенную структуру. Эта структура называется кристаллической решеткой.
Она определяет такие характеристики вещества, как твердость, хрупкость, температура кипения и/или плавления, пластичность, растворимость, электропроводность и т. д.
Кристаллическая решетка — это внутренняя структура кристалла, порядок взаимного расположения атомов, ионов или молекул. Точки, в которых находятся эти частицы, называются узлами решетки.
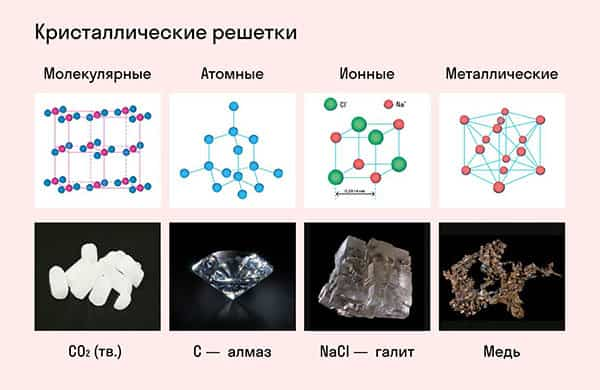
Частицы удерживаются на своих местах благодаря химическим связям между ними. В зависимости от того, какой вид связи удерживает атомы или ионы данного вещества, в химии выделяют основные типы кристаллических решеток:
- атомная (ковалентные связи),
- молекулярная (ковалентные связи и притяжение между молекулами),
- металлическая (металлические связи),
- ионная (ионные связи).
Не путайте эти два понятия — кристаллическая решетка и химическая связь. Тип решетки говорит о том, как расположены атомы/ионы в молекуле вещества, а тип связи — по какому принципу они между собой взаимодействуют.
Атомная кристаллическая решетка
Согласно своему названию, атомная кристаллическая решетка — это структура, в узлах которой расположены атомы. Они взаимодействуют с помощью ковалентных связей, то есть один атом отдает другому свободный электрон или же электроны из разных атомов образуют общую пару. В кристаллах с атомной решеткой частицы прочно связаны, что обуславливает ряд физических характеристик.
Свойства веществ с атомной решеткой:
- прочность,
- твердость,
- неспособность к растворению в воде,
- высокая температура кипения и плавления.
К примеру, атомную кристаллическую решетку имеет алмаз — самый твердый минерал в мире.
Другие примеры: германий Ge, кремний Si, нитрид бора BN, карборунд SiC.
Если нужно рассказать о свойствах веществ с атомной кристаллической решеткой, достаточно вспомнить песок и перечислить его характеристики. 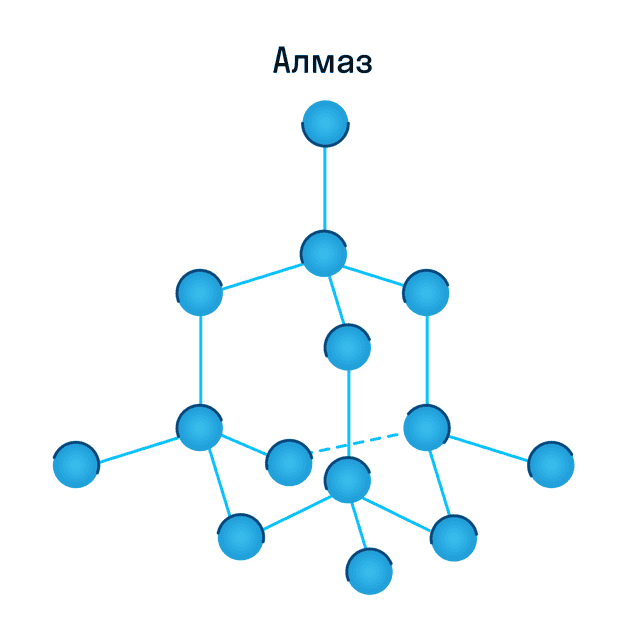
Молекулярная кристаллическая решетка
Как и в предыдущей группе, в этой находятся вещества с ковалентными связями между атомами. Но физические характеристики этих веществ совершенно иные — они легко плавятся, превращаются в жидкость, растворяются в воде. Почему так происходит? Все дело в том, что здесь кристаллы строятся не из атомов, а из молекул.
Молекулярная кристаллическая решетка — это структура, в узлах которой находятся не атомы, а молекулы.
Внутри молекул атомы имеют прочные ковалентные связи, но сами молекулы связаны между собой слабо. Поэтому кристаллы таких веществ непрочные и легко распадаются.
Молекулярная кристаллическая решетка характерна для воды. При комнатной температуре это жидкость, но стоит нагреть ее до температуры кипения (которая сравнительно низка), как она тут же начинает превращаться в пар, т. е. переходит в газообразное состояние.
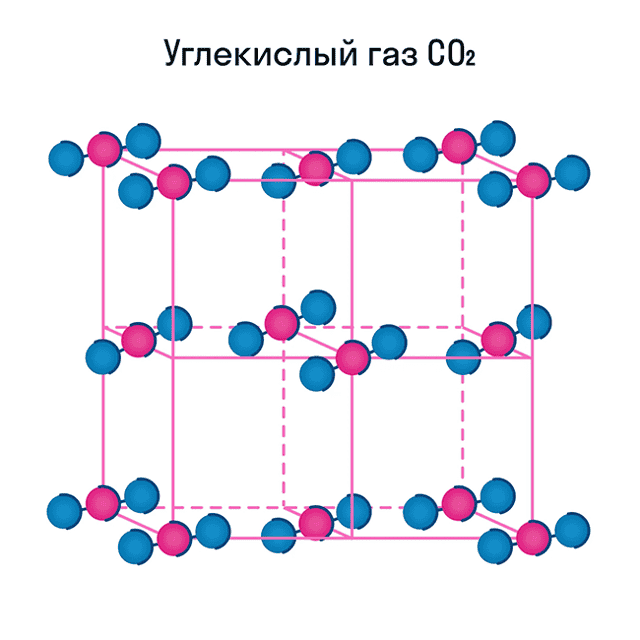
Некоторые молекулярные вещества — например, сухой лед CO2, способны преобразоваться в газ сразу из твердого состояния, минуя жидкое (данный процесс называется возгонкой).
Свойства молекулярных веществ:
- небольшая твердость;
- низкая прочность;
- легкоплавкость;
- летучесть;
- у некоторых — наличие запаха.
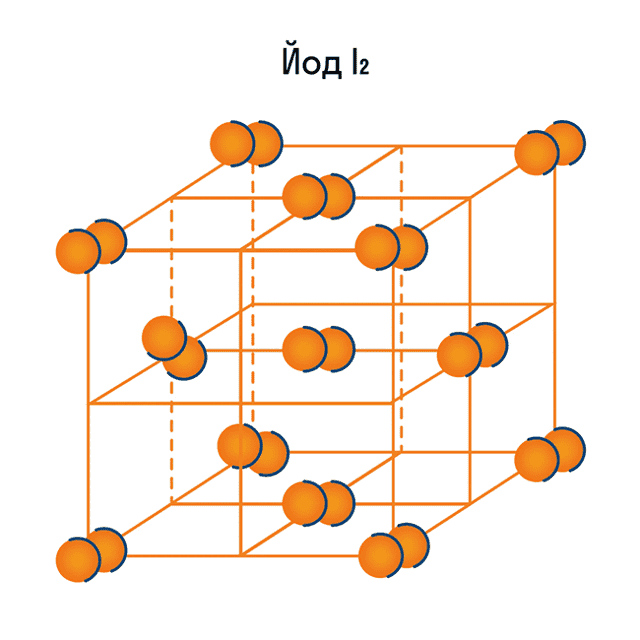
Помимо воды к веществам с молекулярной кристаллической решеткой относятся аммиак NH3, гелий He, радон Rn, йод I, азот N2 и другие. Все благородные газы — молекулярные вещества. Также к этой группе принадлежит и большинство органических соединений (например, сахар).
Ионная кристаллическая решетка
Как известно, при ионной химической связи один атом отдает другому ионы и приобретает положительный заряд, в то время как принимающий атом заряжается отрицательно. В итоге появляются разноименно заряженные ионы, из которых и состоит структура кристалла.
Ионная решетка — это кристаллическая структура, в узловых точках которой находятся ионы, связанные взаимным притяжением.
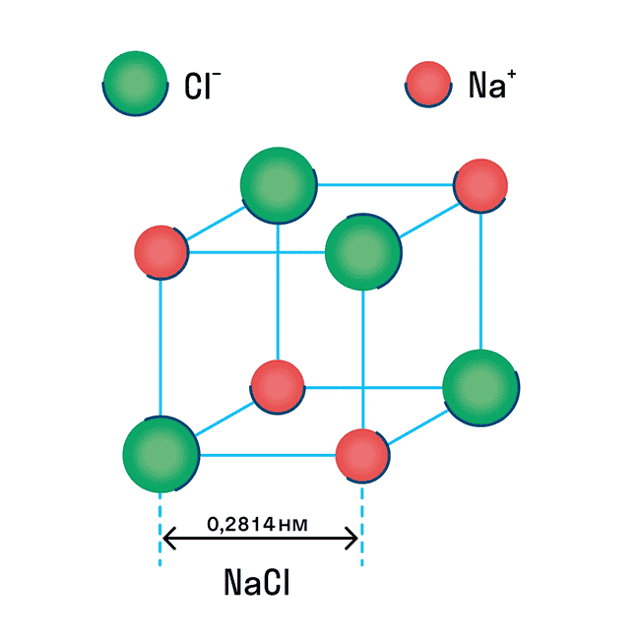
Ионную кристаллическую решетку имеют практически все соли, типичным представителем можно считать поваренную соль NaCl. О ней стоит вспомнить, если нужно перечислить физические характеристики этой группы. Также ионную решетку имеют щелочи и оксиды активных металлов.
Свойства веществ с ионной структурой:
- твердость;
- хрупкость;
- тугоплавкость;
- нелетучесть;
- электропроводность;
- способность растворяться в воде.
Примеры веществ с ионной кристаллической решеткой: оксид кальция CaO, оксид магния MgO, хлорид аммония NH4Cl, хлорид магния MgCl2, оксид лития Li2O и другие.
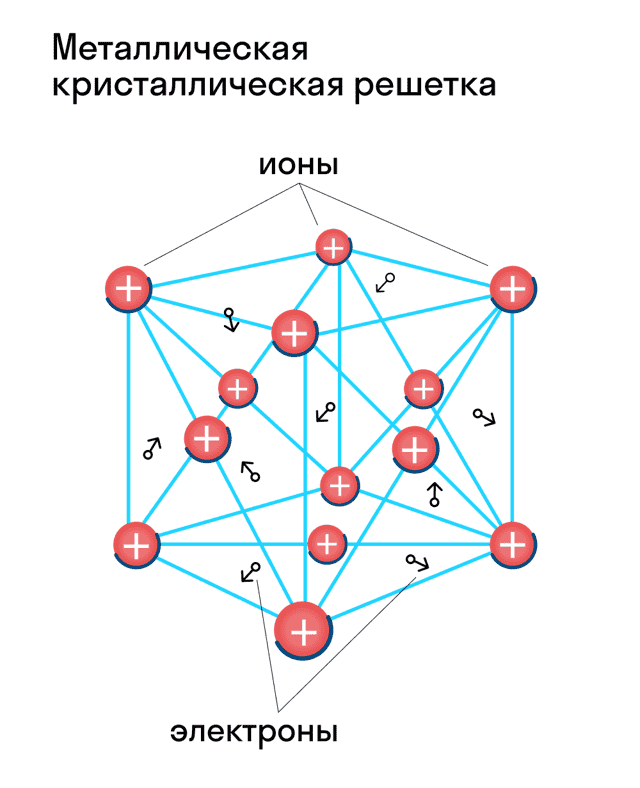
Металлическая кристаллическая решетка
Для начала вспомним, как проходит металлическая химическая связь. В молекуле металла свободные отрицательно заряженные электроны перемещаются от одного иона к другому и соединяются с некоторыми из них, а после отрываются и мигрируют дальше. В результате получается кристалл, в котором ионы превращаются в атомы и наоборот.
Металлическая кристаллическая решетка — это структура, которая состоит из ионов и атомов металла, а между ними свободно передвигаются электроны. Как несложно догадаться, она характерна лишь для металлов и сплавов.
Свободные электроны, мигрирующие между узлами решетки, образуют электронное облако, которое под воздействием электротока приходит в направленное движение. Это объясняет такое свойство металлов, как электрическая проводимость.
В химии типичным примером вещества, которое имеет металлическую кристаллическую решетку, считается медь. Она очень ковкая, пластичная, имеет высокую тепло- и электропроводность. Впрочем, все металлы ярко демонстрируют эти характеристики, поэтому назвать физические свойства данной группы несложно.
Свойства веществ с металлической кристаллической решеткой:
- характерный блеск;
- хорошая ковкость;
- высокая теплопроводность;
- электропроводность.
При этом температура плавления веществ может существенно различаться. Например, у ртути это −38,9°С, а у бериллия целых +1287°С.
Подведем итог: о характеристиках разных типов кристаллических решеток расскажет таблица.
Кристаллические решетки
Кристаллической решеткой называют пространственное расположение атомов или ионов в кристалле. Точки кристаллической решетки, в которых расположены атомы или ионы, называют узлами кристаллической решетки.
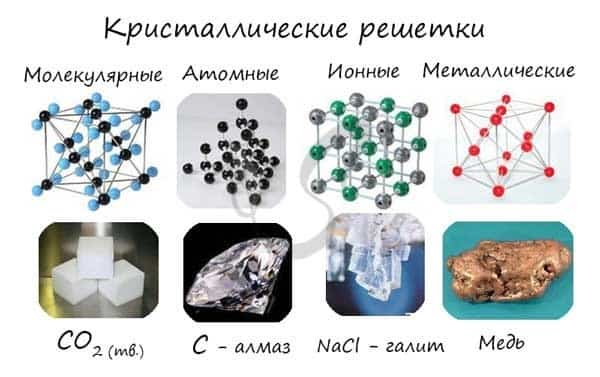
Кристаллические решетки подразделяют на молекулярные, атомные, ионные и металлические.
Очень важно не перепутать вид химической связи и кристаллической решетки. Помните, что кристаллические решетки отражают пространственное расположение атомов.
Молекулярная кристаллическая решетка
В узлах молекулярной решетки расположены молекулы. При обычных условиях молекулярную решетку имеют большинство газов и жидкостей. Связи чаще всего ковалентные полярные или неполярные.
Классическим примером вещества с молекулярной решеткой является вода, так что ассоциируйте свойства этих веществ с водой. Вещества с молекулярной решеткой непрочные, имеют небольшую твердость, летучие, легкоплавкие, способны к возгонке, для них характерны небольшие температуры кипения.
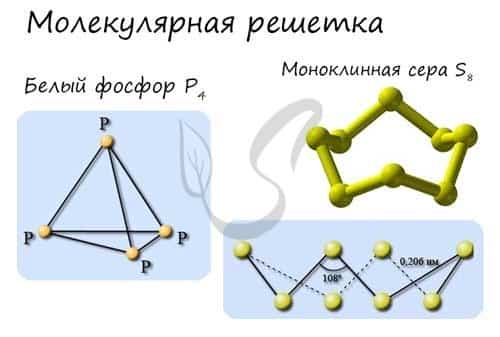
Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2. Особо хочется отметить белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы подробно изучили в статье, посвященной классификации веществ.
Ионная кристаллическая решетка
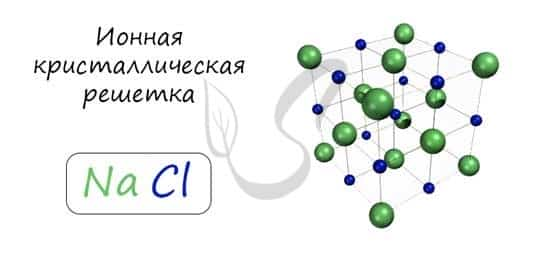
В узлах ионной решетки находятся атомы, связанные ионной связью. Этот тип решетки характерен для веществ, обладающих ионной связь: соли, оксиды и гидроксиды металлов.
Ассоциируйте этот ряд веществ с поваренной солью — NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.
Примеры: NaCl, MgCl2, NH4Br, KNO3, Li2O, Na3PO4.
Металлическая кристаллическая решетка
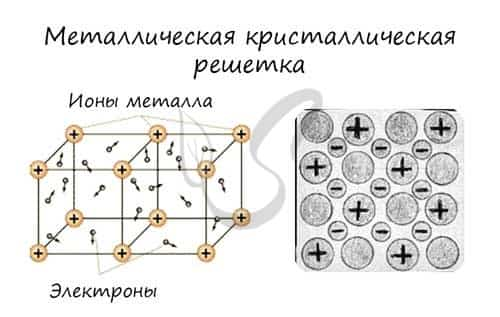
В узлах металлической решетки находятся атомы металла. Этот тип решетки характерен для веществ, образованных металлической связью.
Ассоциируйте свойства этих веществ с медью. Они обладают характерным металлическим блеском, ковкие и пластичные, хорошо проводят электрический ток и тепло, имеют высокие температуры плавления и кипения.
Примеры: Cu, Fe, Zn, Al, Cr, Mn.
Атомная кристаллическая решетка
В узлах атомной решетки находятся атомы, связанные ковалентной полярной или неполярной связью.
Ассоциируйте эти вещества с песком. Они очень твердые, очень тугоплавкие (высокая температура плавления), нелетучие, прочные, нерастворимы в воде.
Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), красный и черный фосфор (P).

Виды кристаллических решёток: атомная, молекулярная, металлическая и ионная
Согласно атомно-молекулярной теории Бойля, все вещества состоят из молекул, которые находятся в постоянном движении. Но существует ли какая-то определённая структура в веществах? Или они просто состоят из хаотично движущихся молекул?
Виды кристаллических решёток
В действительности чёткую структуру имеют все вещества, пребывающие в твёрдом состоянии.
Атомы и молекулы движутся, но силы притяжения и отталкивания между частицами сбалансированы, поэтому атомы и молекулы располагаются в определённой точке пространства (но продолжают совершать небольшие колебания, зависящие от температуры). Такие структуры называются кристаллическими решётками.
Места, в которых находятся сами молекулы, ионы или атомы, называют узлами. А расстояния между узлами получили название – периоды идентичности. В зависимости от положения частиц в пространстве, различают несколько типов:
- атомная;
- ионная;
- молекулярная;
- металлическая.
В жидком и газообразном состоянии вещества не имеют чёткой решётки, их молекулы движутся хаотично, именно поэтому они не имеют формы.
Например, кислород, находясь в газообразном состоянии, представляет собой бесцветный газ без запаха, в жидком (при -194 градусов) – раствор голубоватого цвета.
Когда температура опускается до -219 градусов, кислород переходит в твёрдое состояние и приобретает кр. решётку, при этом он превращается в снегообразную массу синего цвета.
Интересно, что у аморфных веществ нет чёткой структуры, поэтому у них и нет строгой температуры плавления и кипения. Смола и пластилин при нагревании постепенно размягчаются и становятся жидкими, у них нет чёткой фазы перехода.
Атомная кристаллическая решётка
В узлах находятся атомы, о чём и говорит название. Эти вещества очень крепкие и прочные, так как между частицами образуется ковалентная связь.
Соседние атомы образуют между собой общую пару электронов (а, точнее, их электронные облака наслаиваются друг на друга), и поэтому они очень хорошо связаны друг с другом. Самый наглядные пример – алмаз, который по шкале Мооса обладит наибольшей твёрдостью.
Интересно, что алмаз, как и графит, состоит из углевода. Графит является очень хрупким веществом (твёрдость по шкале Мооса – 1), что является наглядным примером того, как много зависит от вида.
Атомная кр. решётка плохо распространена в природе, к ней относятся: кварц, бор, песок, кремний, оксид кремния (IV), германий, горный хрусталь.
Для этих веществ характерна высокая температура плавления, прочность, а также эти соединения очень твёрдые и нерастворимые в воде.
Из-за очень сильной связи между атомами, эти химические соединения почти не взаимодействуют с другими и очень плохо проводят ток.
Ионная кристаллическая решётка
В этом типе ионы располагаются в каждом узле. Соответственно, этот вид характерен для веществ с ионной связью, например: хлорид калия, сульфат кальция, хлорид меди, фосфат серебра, гидроксид меди и так далее. К веществам с такой схемой соединения частиц относятся;
- соли;
- гидроксиды металлов;
- оксиды металлов.
Хлорид натрия имеет чередование положительных (Na +) и отрицательных (Cl -) ионов. Один ион хлора, находящийся в узле, притягивает к себе два иона натрия (благодаря электромагнитному полю), которые находятся в соседних узлах. Таким образом, образуется куб, в котором частицы связаны между собой.
Для ионной решётки характерна прочность, тугоплавкость, устойчивость, твёрдость и нелетучесть. Некоторые вещества могут проводить электрический ток.
Молекулярная кристаллическая решётка
В узлах этой структуры находятся молекулы, которые плотно упакованы между собой. Для таких веществ характерна ковалентная полярная и неполярная связь. Интересно, что независимо от ковалентной связи, между частицами образуете очень слабое притяжение (из-за слабых ван-дер-вальсовых сил).
Именно поэтому такие вещества очень хрупкие, обладают низкой температурой кипения и плавления, а также они летучие.
К таким веществам относятся: вода, органические вещества (сахар, нафталин), оксид углерода (IV), сероводород, благородные газы, двух– (водород, кислород, хлор, азот, йод), трёх- (озон), четырёх- (фосфор), восьмиатомные (сера) вещества и так далее.
Одна из отличительных черт — это то, что структурная и пространственная модель сохраняется во всех фазах (как в твёрдых, так в жидких и газообразных).
Металлическая кристаллическая решётка
Из-за наличия в узлах ионов, может показаться, что металлическая решетка похожа на ионную. На самом деле, это две совершенно разные модели, с разными свойствами.
Металлическая гораздо гибче и пластичнее ионной, для неё характерна прочность, высокая электро- и теплопроводность, эти вещества хорошо плавятся и отлично проводят электрический ток.
Это объясняется тем, что в узлах находятся положительно заряженные ионы металлов (катионы), которые могут перемещаться по всей структуре, тем самым обеспечивают течение электронов.
Частицы хаотично движутся около своего узла (они не имеют достаточной энергии, чтобы выйти за пределы), но как только появляется электрическое поле, электроны образуют поток и устремляются из положительной в отрицательную область.
Металлическая кристаллическая решётка характерна для металлов, например: свинец, натрий, калий, кальций, серебро, железо, цинк, платина и так далее.
Помимо прочего, она подразделяется ещё на несколько типов упаковок: гексагональная, объёмно центрированная (наименее плотная) и гранецентрированная.
Первая упаковка характерна для цинка, кобальта, магния, вторая для бария, железа, натрия, третья для меди, алюминия и кальция.
Таким образом, от типа решётки зависят многие свойства, а также строение вещества. Зная тип, можно предсказать, к примеру, какой будет тугоплавкость или прочность объекта.
Видео
Дополнительную информацию о кристаллических решетках вы найдете в нашем видео.
Типы кристаллических решёток
Кристаллические решетки
Большинство веществ, в зависимости от условий (темература, давление) могут находится в трех агрегатных состояниях. Все твердые вещества можно разделить на аморфные и кристаллические.
КРИСТАЛЛИЧЕСКОЕ ВЕЩЕСТВО: твердое вещество, у которого атомы или молекулы образуют правильную упорядоченную решетку.
Большинство твердых веществ существует в кристаллическом состоянии, которое отличается повышенной стабильностью, но это не означает, что они имеют кристаллы в прямом смысле этого слова; например, чистая медь является кристаллической только потому, что ее атомы расположены в регулярном порядке.
АМОРФНОЕ ВЕЩЕСТВО: твердое вещество, не имеющее кристаллической структуры. Его атомы и молекулы расположены без соблюдения регулярности. Переохлажденные жидкости, такие как стекло, резина и некоторые пластмассы, являются аморфными.
Сейчас мы будем рассматривать только кристаллические вещества.
В зависимости от того, из каких частицы построена кристаллическая решетка и каков характер химической связи между ними, выделяют различные типы кристаллов. Выделяют 4 типа кристаллических решеток (КР): Молекулярная, ионная, металлическая и атомная.
| Тип кристаллической решетки | Частицы в узлах решетки | Характеристики | Вещества | тип связи |
| Молекулярная | Молекулы | Не прочный, Низкая Тпл, Летучие |
|
Ковалентная (полярная и неполярная) |
| Ионная | Ионы |
|
Соли, оксиды и гидроксиды металлов | Ионная |
| Металлическая | Атомы и ионы | Пластичные Электро- и теплопроводные | Металлы и сплавы | Металлическая |
| Атомная | Атомы | Очень прочная, Очень высокие Тпл |
|
Ковалентная |
Ионные кристаллы образованы катионами и анионами (например, соли и гидроксиды большинства металлов). В них между частицами имеется ионная связь.
Ионные кристаллы могут состоять из одноатомных ионов. Так построены кристаллы хлорида натрия, иодида калия, фторида кальция.
В ионном кристалле невозможно выделить одиночные молекулы. Каждый катион притягивается к каждому аниону и отталкивается от других катионов.
Атомные кристаллы состоят из отдельных атомов, объединенных ковалентными связями. Из простых веществ только бор и элементы IVA-группы имеют такие кристаллические решетки. Нередко соединения неметаллов друг с другом (например, диоксид кремния) также образуют атомные кристаллы. Они очень прочные и твердые, плохо проводят теплоту и электричество.
Молекулярные кристаллы построены из отдельных молекул, внутри которых атомы соединены ковалентными связями. Между молекулами действуют более слабые межмолекулярные силы. Они легко разрушаются, поэтому молекулярные кристаллы имеют низкие температуры плавления, малую твердость, высокую летучесть.
Для металлов характерна металлическая кристаллическая решетка. В ней имеется металлическая связь между атомами. В металлических кристаллах ядра атомов расположены таким образом, чтобы их упаковка была как можно более плотной. Связь в таких кристаллах является делокализованной и распространяется на весь кристалл..
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения
- Для большинства веществ характерна способность в зависимости от условий находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном.
- Например, вода при нормальном давлении в интервале температур 0-100oC является жидкостью, при температуре выше 100оС способна существовать только в газообразном состоянии, а при температуре менее 0оС представляет собой твердое вещество.
- Вещества в твердом состоянии различают аморфные и кристаллические.
Характерными признаками аморфных веществ является отсутствие четкой температуры плавления: их текучесть плавно увеличивается с ростом температуры. К аморфным веществам относятся такие соединения, как воск, парафин, большинство пластмасс, стекло и т.д.
Все же кристаллические вещества обладают конкретной температурой плавления, т.е. вещество с кристаллическим строением переходит из твердого состоянии в жидкое не постепенно, а резко, при достижении конкретной температуры. В качестве примера кристаллических веществ можно привести поваренную соль, сахар, лед.
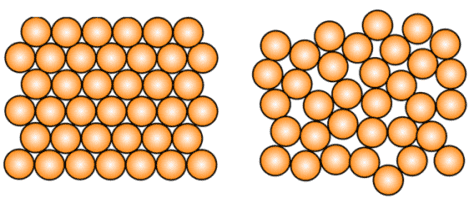
Разница в физических свойствах аморфных и кристаллических твердых веществ обусловлена прежде всего особенностями строения таких веществ. В чем заключается разница между веществом в аморфном и кристаллическом состоянии, проще всего понять из следующей иллюстрации:
Как можно заметить, в аморфном веществе, в отличие от кристаллического, отсутствует какой-либо порядок в расположении частиц. Если же в кристаллическом веществе мысленно соединить прямой два близкорасположенных друг к другу атома, то можно обнаружить, что на этой линии на строго определенных промежутках будут лежать одни и те же частицы:
- Таким образом, в случае кристаллических веществах можно говорить о таком понятии, как кристаллическая решетка.
- Кристаллической решеткой называют пространственный каркас, соединяющий точки пространства, в которых находятся частицы, образующие кристалл.
- Точки пространства, в которых находятся образующие кристалл частицы, называют узлами кристаллической решетки.
- В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают: молекулярную, атомную, ионную и металлическую кристаллические решетки.
В узлах молекулярной кристаллической решетки
Кристаллическая решетка льда как пример молекулярной решетки
находятся молекулы, внутри которых атомы связаны прочными ковалентными связями, однако сами молекулы удерживаются друг возле друга слабыми межмолекулярными силами. Вследствие таких слабых межмолекулярных взаимодействий кристаллы с молекулярной решеткой являются непрочными. Такие вещества от веществ с иными типами строения отличаются существенно более низкими температурами плавления и кипения, не проводят электрический ток, могут как растворяться, так и не растворяться в различных растворителях. Растворы таких соединений могут как проводить, так и не проводить электрический ток в зависимости от класса соединения. К соединениям с молекулярной кристаллической решеткой относятся многие простые вещества — неметаллы (отвержденные H2, O2, Cl2, ромбическая сера S8, белый фосфор P4), а также многие сложные вещества – водородные соединения неметаллов, кислоты, оксиды неметаллов, большинство органических веществ. Следует отметить, что, если вещество находится в газообразном или жидком состоянии, говорить о молекулярной кристаллической решетке неуместно: корректнее использовать термин — молекулярный тип строения.
Кристаллическая решетка алмаза как пример атомной решетки
В узлах атомной кристаллической решетки
находятся атомы. При этом все узлы такой кристаллической решетки «сшиты» между собой посредством прочных ковалентных связей в единый кристалл. Фактически, такой кристалл является одной гигантской молекулой.
Вследствие особенностей строения все вещества с атомной кристаллической решеткой являются твердыми, обладают высокими температурами плавления, химически мало активны, не растворимы ни в воде, ни в органических растворителях, а их расплавы не проводят электрический ток.
Следует запомнить, что к веществам с атомным типом строения из простых веществ относятся бор B, углерод C (алмаз и графит), кремний Si, из сложных веществ — диоксид кремния SiO2 (кварц), карбид кремния SiC, нитрид бора BN.
У веществ с ионной кристаллической решеткой
в узлах решетки находятся ионы, связанные друг с другом посредством ионных связей.
Поскольку ионные связи достаточно прочны, вещества с ионной решеткой обладают сравнительно высокой твердостью и тугоплавкостью. Чаще всего они растворимы в воде, а их растворы, как и расплавы проводят электрический ток.
К веществам с ионным типом кристаллической решетки относятся соли металлов и аммония (NH4+), основания, оксиды металлов. Верным признаком ионного строения вещества является наличие в его составе одновременно атомов типичного металла и неметалла.
Кристаллическая решетка хлорида натрия как пример ионной решетки
Однако следует отметить, что в веществах с ионным типом строения нередко можно обнаружить, помимо ионных, также ковалентные полярные связи. Это наблюдается в случае сложных ионов, т.е. состоящих из двух или более химических элементов (SO42-, NH4+, PO43- и т.д.). Внутри таких сложных ионов атомы связаны друг с другом ковалентными связями.
Металлическая кристаллическая решетка
наблюдается в кристаллах свободных металлов, например, натрия Na, железа Fe, магния Mg и т.д. В случае металлической кристаллической решетки, в ее узлах находятся катионы и атомы металлов, между которыми движутся электроны.
При этом движущиеся электроны периодически присоединяются к катионам, таким образом нейтрализуя их заряд, а отдельные нейтральные атомы металлов взамен «отпускают» часть своих электронов, превращаясь, в свою очередь, в катионы.
Фактически, «свободные» электроны принадлежат не отдельным атомам, а всему кристаллу.
Металлическая кристаллическая решетка
Такие особенности строения приводят к тому, что металлы хорошо проводят тепло и электрический ток, часто обладают высокой пластичностью (ковкостью). Разброс значений температур плавления металлов очень велик.
Так, например, температура плавления ртути составляет примерно минус 39 оС (жидкая в обычных условиях), а вольфрама — 3422 °C.
Следует отметить, что в обычных условиях все металлы, кроме ртути, являются твердыми веществами.
Урок 4. строение кристаллов. кристаллические решётки. причины многообразия веществ — Химия — 11 класс — Российская электронная школа
Химия, 11 класс
Урок № 4. Строение кристаллов. Кристаллические решётки. Причина многообразия веществ
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению кристаллического состояния вещества, зависимости свойств веществ от типов кристаллических решеток. Объясняются причины многообразия веществ, такие как изотопия элементов, аллотропия, изомерия, гомология. Дается понятие химического синтеза.
- Глоссарий
- Аллотропия – существование нескольких простых веществ, образованных одним и тем же химическим элементом.
- Атомная кристаллическая решётка – регулярная структура твёрдого вещества, в узловых точках которой находятся атомы химического элемента.
- Гомология – явление наличия в природе органических соединений, имеющих одинаковое строение и химические свойства, но отличающихся на некоторое целое число групп СН2- состав.
- Изомерия – явления наличия нескольких веществ, имеющих один и тот же состав, но отличающихся по порядку соединения атомов.
- Ионная кристаллическая решетка – регулярная структура твёрдого вещества, в узлах которой расположены положительно и отрицательно заряженные ионы.
- Кристаллическая решетка – особая структура твёрдого вещества, в которой частицы вещества расположены в строго определенном порядке.
- Кристаллы – твёрдые вещества, имеющие форму правильных многогранников, образованных в результате многократного регулярного повторения расположения составляющих вещество частиц.
- Металлическая кристаллическая решетка – регулярная структура твёрдого вещества, в узлах которой расположены ионы металла.
- Молекулярная кристаллическая решетка – регулярная структура твёрдого вещества, в узлах которой находятся молекулы вещества.
- Полиморфизм – способность твёрдого вещества образовывать различные кристаллические структуры, состоящие из одних и тех же частиц.
- Полиморфные модификации – разные кристаллические структуры, которые образованы частицами одного и того же вещества.
- Химический синтез – процесс искусственного создания новых веществ физическими и химическими методами.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Строение кристаллов и типы кристаллических решеток
Кристаллами называются твёрдые вещества, частицы которых образуют трёхмерную периодическую пространственную структуру, называемую кристаллической решёткой. Грани кристаллов представляют собой правильные многоугольники. Свойства кристаллических тел различны.
Например, алмаз обладает максимальной твёрдостью, а графит можно сломать руками, хотя эти вещества состоят атомов углерода. Свойства веществ зависят от типа кристаллической решетки.
Различают четыре типа кристаллических решёток: атомную, ионную, молекулярную и металлическую.
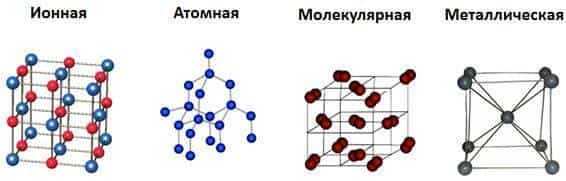
Зависимость свойств веществ от типа кристаллической решетки
В узлах атомной кристаллической решётки расположены атомы, соединённые ковалентной связью. Примерами веществ, имеющих атомную кристаллическую решетку, являются алмаз, кремний, германий, бор. Вещества, имеющие атомную кристаллическую решетку, характеризуются высокой температурой плавления, большой твёрдостью.
В узлах ионной кристаллической решётки находятся положительные и отрицательные ионы, связь между ними ионная. Ионную кристаллическую решетку имеют соли, щёлочи и оксиды типичных металлов. Для веществ с ионной кристаллической решеткой характерны высокие температуры плавления, твёрдость, плотность, хорошая электропроводность.
В узлах молекулярной кристаллической решетки находятся молекулы, которые удерживаются за счет межмолекулярных вандервальсовых сил. Примером веществ с молекулярной кристаллической решеткой являются лёд, йод, нафталин, углекислый газ.
Межмолекулярные связи значительно слабее ковалентных и ионных, поэтому для веществ с молекулярной кристаллической решёткой характерны низкие температуры плавления, невысокая твёрдость, возможность возгонки (переход из твёрдого состояния в газообразное, минуя жидкое).
Для металлов характерна металлическая кристаллическая решётка, в узлах которой расположены положительно заряженные ионы металлов, а между ними свободно перемещаются валентные электроны (так называемый электронный газ). Для веществ с металлической кристаллической решеткой характерны механическая прочность, плавкость, ковкость, хорошая тепло- и электропроводность, металлический блеск.
Свойства кристаллических тел определяются не только характером связи между частицами, но и их взаимным расположением относительно друг друга.
В кристаллах алмаза все атомы углерода связаны ковалентными неполярными связями и находятся на одинаковом расстоянии друг от друга, образуя тетраэдры.
В кристаллах графита каждые шесть атомов углерода связаны ковалентными неполярными связями, а между собой такие плоские шестиугольники связаны слабыми межмолекулярными связями.
Причины многообразия веществ
Не только углерод может образовывать разные вещества в зависимости от типа кристаллической решётки. Известно несколько веществ, образованных фосфором (белый, красный, чёрный и металлический фосфор).
Сера может существовать в виде трёх модификаций (ромбическая, моноклинная и пластическая).
Явление существования нескольких простых веществ, образованных одним и тем же элементом, называется аллотропией (полиморфизмом), а сами простые вещества – аллотропными (полиморфными) модификациями.
Существование изотопов – атомов одного и того же химического элемента, имеющих разные массовые числа — ещё одна причина огромного многообразия веществ.
Изучая органическую химию, вы узнали о существовании изомеров – молекул, имеющих одинаковый состав, но разную последовательность атомов и их расположение в пространстве. Изомеры встречаются не только среди органических соединений, например, изомером карбамида является цианат аммония.
Причиной разнообразия органических соединений является и гомология – существование ряда соединений, имеющих одинаковое строение и химические свойства, но отличающихся друг от друга на целое число групп СН2-.
118 известных на сегодняшний день химических элементов образуют миллионы различных веществ, но человек искусственным путём создает новые вещества с нужными ему свойствами. Создание человеком новых веществ получило название химического синтеза.
- Таким образом, явления аллотропии (полиморфизма), изомерии, изотопии, гомологии, химический синтез новых соединений являются причинами многообразия веществ.
- ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
- 1. Расчет количества молекул в кристалле
Условие задачи: Молекула белого фосфора состоит из четырех атомов этого элемента. Сколько молекул белого фосфора содержится в кристалле фосфора массой 2,48 г? Ответ запишите в виде числа, приведенного к стандартному виду.
Шаг первый: найдём молярную массу молекулы белого фосфора Р4. Относительная атомная масса фосфора равна 31 а.е.м., молярная масса Р4 равна 4·31 = 124 (г/моль).
- Шаг второй: найдём количество молей белого фосфора в кристалле массой 2,48 г. Для этого разделим массу кристалла на молярную массу Р4:
- 2,48 : 124 = 0,02 (моль).
- Шаг третий: найдём количество молекул, содержащееся в 0,02 моль белого фосфора. Для этого число моль умножим на число Авогадро:
- 0,02·6,02·1023 = 1,2·1022 (молекул).
- Ответ: 1,2·1022.
- 2. Расчёт числа атомов в молекуле фуллерена
Условие задачи: Одной из аллотропных модификаций углерода, применяемых в электронике, является фуллерен. 0,5 моль фуллерена имеют массу 360 г. Сколько атомов углерода входит в состав одной молекулы фуллерена?
- Шаг первый: найдём молярную массу фуллерена.
- Для этого массу имеющегося образца разделим на количество молей:
- 360 : 0,5 = 720 (г/моль).
Шаг второй: найдём количество атомов углерода в 1 моль фуллерена. Для этого молярную массу фуллерена разделим на массу 1 моль атомов углерода. 1 моль атомов углерода имеет массу 12 г.
720 : 12 = 60 (атомов).
Ответ: 60.
Абросимова Елена Владимировна учитель химии и биологии — Кристаллические решетки
- Взаимосвязь типа химической связи с видом кристаллической решетки
- Вещества и кристаллические решетки
- Твердые вещества бывают аморфные или кристаллические (чаще всего имеют кристаллическое строение).
Кристаллическое строение характеризуется правильным расположением частиц в определенных точках пространства. При соединении этих точек воображаемыми прямыми линиями образуется так называемая кристаллическая решетка.
Точки, в которых размещены частицы, называются узлами кристаллической решетки.
- В узлах кристаллической решетки могут находиться ионы, атомы или молекулы.
- В зависимости от вида частиц, расположенных в узлах кристаллической решетки, и характера связи между ними различают четыре типа кристаллических решеток:
- · ионные,
- · атомные,
- · молекулярные и
- · металлические.
- Ионная решетка
Эту решетку образуют все вещества с ионным типом связи — соли, щелочи, бинарные соединения активных металлов с активными неметаллами (оксиды, галогениды, сульфиды), алкоголяты, феноляты, соли аммония и аминов. В узлах решетки — ионы, между которыми существует электростатическое притяжение. Ионная связь очень прочная.
- Примеры: КОН, СаСО3, СН3СООК, NH4NO3, [CH3NH3]Cl, С2Н5ОК.
- Свойства ионных кристаллов:
- · твердые, но хрупкие;
- · отличаются высокими температурами плавления;
- · нелетучи, не имеют запаха;
- · расплавы ионных кристаллов обладают электропроводностью;
- · многие растворимы в воде; при растворении в воде диссоциируют на катионы и анионы, и образующиеся растворы проводят электрический ток.
- Металлическая решетка
Характерна для веществ с металлической связью. Реализуется в простых веществах — металлах и их сплавах.
В узлах решетки — атомы и катионы металла, при этом электроны металла обобществляются и образуют так называемый электронный газ, который движется между узлами решетки, обеспечивая ее устойчивость.
Именно свободно перемещающимися электронами и обусловлены свойства веществ с металлической решеткой:
- · тепло- и электропроводность;
- · обладают металлическим блеском;
- · высокие температуры плавления.
- Атомная решетка
В узлах решетки — атомы, связанные ковалентными связями. Химическая связь — ковалентная полярная или неполярная. Атомная кристаллическая решетка характерна для углерода (алмаз, графит), бора, кремния, германия, оксида кремния SiO2(кремнезем, кварц, речной песок), карбида кремния SiC (карборунд), нитрида бора BN.
- Свойства веществ с атомной решеткой:
- · высокая твердость;
- · высокие температуры плавления;
- · нерастворимость;
- · нелетучесть;
- · отсутствие запаха.
- Молекулярная решетка
- В узлах — молекулы веществ, которые удерживаются в решетке с помощью слабых межмолекулярных сил.
- Молекулярное строение имеют:
- o все органические вещества (кроме солей);
- o вещества — газы и жидкости;
- o легкоплавкие и летучие твердые вещества, в молекулах которых ковалентные связи (полярные и неполярные).
- Подобные вещества часто имеют запах.
- Обобщающая таблица
- Кристаллические решетки, вид связи и свойства веществ






