- Физические свойства металлов: твердость, плотность и др
- Твёрдость:
- Таблица твёрдости металлов по шкале Мооса:
- Температура плавления:
- Таблица температуры плавления легкоплавких металлов и сплавов:
- Таблица температуры плавления среднеплавких металлов и сплавов:
- Таблица температуры плавления тугоплавких металлов и сплавов:
- Плотность:
- Пластичность:
- Электропроводность:
- Теплопроводность:
- Цвет:
- Физические свойства металлов
- Физические свойства металлов
- Общие химические свойства металлов
- 1. РЕАКЦИИ МЕТАЛЛОВ С НЕМЕТАЛЛАМИ
- 2. РЕАКЦИИ МЕТАЛЛОВ С КИСЛОТАМИ
- Физические и химические свойства металлов
- Физические свойства металлов
- Химические свойства металлов
- Получение металлов
- Примеры решения задач
- Физические свойства металлов
- Металл: что это такое, его физические свойства, из чего состоит
- Что это такое – металл
- Физические свойства
- Основные химические свойства металлов
- Признаки
- Классификация и виды металлов
- Черные
- Что относится к цветным металлам
- Медь и ее сплавы являются популярными металлами
- К металлам относятся алюминий и сплавы
- Все о металлах магний, титан и их сплавах
- Антифрикционные сплавы
- Мягкие
- Что значит твердый металл
- Металлические материалы в энергетике
- Особенности черных вторичных металлов
- Щелочноземельные сплавы
- Понятие щелочной металл
- Общая характеристика материалов из d- и f-семейств
- Из чего состоят побочные подгруппы металлов системы Менделеева
- Сплавы
- Сравнение свойств
Содержание:
§ 1 Свойства металлов 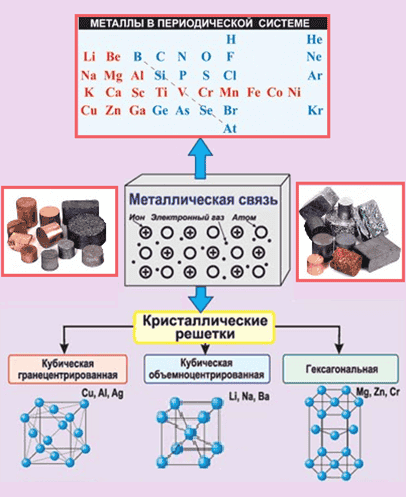
Физические свойства металлов объясняются особенностями строения их кристаллических решеток. В узлах решеток располагаются или положительно заряженные ионы металлов, или их атомы, а между ними перемещаются свободные электроны. Связь, между свободными электронами и ионами металла в кристаллической решетке, называется металлической.
Для металлов характерны как общие физические свойства, так и индивидуальные свойства. Металлический блеск, пластичность и ковкость, теплопроводность и электропроводность – это свойства, характерные для всех металлов, по ним отличают их от неметаллов. Температура плавления, плотность, твердость для каждого металла свои, в этом они отличаются друг от друга.
§ 2 Общие физические свойства металлов
Пластичность– способность металла изменять форму под действием внешних сил без разрушения и сохранять ее после прекращения воздействия. При воздействии на металлическую кристаллическую решетку происходит смещение слоев атом-ионов металла относительно друг друга без разрыва связей, поэтому для них характерна высокая пластичность.
Наиболее пластичные металлы: золото, серебро, медь, олово, свинец. Например из 1 г золота можно получить тончайшую проволоку длиной около 3 км или же лист, способный покрыть потолок трехкомнатной квартиры площадью около 50 м2.
Тончайшие листы золота, толщиной от 1 мкм до 3 мкм, называют сусальным золотом. Его применяют для декоративной отделки изделий, изготовленных в основном из дерева.
Листочками сусального золота оклеивают резные деревянные рельефы, предназначенные для украшения интерьеров дворцов, храмов, дорогой мебели.
- Электропроводность – свойство вещества проводить электрический ток.
- В металлической кристаллической решетке присутствуют свободные электроны, которые при обычных условиях двигаются в беспорядке, а при попадании в электрическое поле начинают двигаться направлено, в результате чего возникает электрический ток.
- Наибольшей электропроводностью обладают серебро, медь, золото, алюминий, железо;
а наименьшей – свинец, марганец, вольфрам и ртуть.
При повышении температуры электропроводность металлов уменьшается, это объясняется усилением колебательного движения атомов-ионов металлов, что затрудняет направленное движение электронов.
При понижении температуры электропроводность увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Медь и алюминий наиболее доступные металлы, поэтому их используют в виде проводников электрического тока.
Теплопроводность – способность металла передавать теплоту от более нагретых его частей менее нагретым. Это свойство металлов также объясняется подвижностью свободных электронов, они при движении сталкиваются с колеблющимися в узлах решетки ионами и обмениваются с ними энергией.
При повышении температуры колебания одних ионов передаются другим ионам с помощью электронов, и температура всего металлического предмета быстро выравнивается. Теплопроводность металлов изменяется в той же последовательности, что и электропроводность.
Наибольшей теплопроводностью обладают серебро, медь, золото, алюминий, железо; а наименьшей – свинец, марганец, вольфрам и ртуть.
Если одновременно в горячую воду опустить например чайные ложки, изготовленные из серебра, меди, золота, алюминия, железа, то быстрее нагреется ложка из серебра, так как ее теплопроводность выше теплопроводности других металлов, затем медная, золотая, алюминиевая и затем железная ложки.
§ 3 Отличительные особенности металлов
Твердость – способность твердого тела сопротивляться проникновению в него другого более твердого тела. Все металлы, за исключением ртути, при обычных условиях являются твердыми веществами.
По твердости металлы сравнивают с алмазом, твердость которого принята за 10.
Самыми мягкими являются щелочные металлы (цезий, рубидий, калий, натрий) их можно резать ножом, а самым твердым является хром, он царапают стекло.
Плотность – величина, определяемая отношением массы тела к его объему.
По плотности металлы делятся на легкие (с плотностью менее 5 г/см3) и тяжелые (с плотностью более 5 г/см3). К легким металлам относятся щелочные (литий, натрий), щелочноземельные (кальций, магний) и алюминий. К тяжелым – цинк, железо, никель, медь, серебро, свинец, ртуть, золото, платина. Самый легкий металл – литий (0,53 г/см3), а самый тяжелый – осмий (22,6 г/см3).
Плавкость металлов – это процесс перехода вещества из твердого в жидкое состояние. По температуре плавления металлы можно разделить на легкоплавкие и тугоплавкие.
К легкоплавким относятся металлы, температура плавления которых ниже 10000 С. Это ртуть, галлий, цезий, калий, олово, свинец, цинк, магний, алюминий.
Если температура плавления выше температуры плавления железа 15390 С, то металл является тугоплавким. К ним относятся: титан, хром, ванадий, цирконий, гафний, ниобий, молибден, вольфрам.
Самая низкая температура плавления у ртути – 390 С, поэтому это единственный металл, который при комнатной температуре находится в расплавленном состоянии. Самая высокая температура плавления у вольфрама 34200 С, из этого металла изготавливают нити накаливания электрических ламп.
§ 4 Краткие итоги по теме урока
К физическим свойствам металлов относятся: металлический блеск, пластичность и ковкость, теплопроводность и электропроводность, твердость, плотность, плавкость. Свойства металлов зависят от особенностей строения их кристаллических решеток.
Все металлы обладают металлическим блеском, электропроводностью, теплопроводностью, пластичностью.
Твердость, плотность и температура плавления и кипения металлов отличаются, на эти показатели влияют расположение атомов и ионов в узлах кристаллической решетки и их атомные радиусы.
Список использованной литературы:
- Габриелян О.С. Химия. 9 класс: учебник для общеобразовательных учреждений / М.: Дрофа, 2010.
- Химия. 9 класс: Настольная книга учителя / О.С. Габриелян, И.Г. Остроумов. – М.: Дрофа, 2003
- Рудзитис Г.Е., Фельдман Ф.Г. Химия: Неорган. химия. Орган. химия: Учеб. для 9 кл. общеобразоват. учреждений. – М.: Просвещение, 1999
Использованные изображения:
Физические свойства металлов: твердость, плотность и др
Металлы имею такие физические свойства, как твердость, температуру плавления, плотность, пластичность, электропроводность, теплопроводность и цвет.
Твёрдость:
Все металлы, кроме ртути и, условно, франция, при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью.
Таблица твёрдости металлов по шкале Мооса:
| Твёрдость | Металл |
| 0.2 | Цезий |
| 0.3 | Рубидий |
| 0.4 | Калий |
| 0.5 | Натрий |
| 0.6 | Литий |
| 1.2 | Индий |
| 1.2 | Таллий |
| 1.25 | Барий |
| 1.5 | Стронций |
| 1.5 | Галлий |
| 1.5 | Олово |
| 1.5 | Свинец |
| 1.5 | Ртуть |
| 1.75 | Кальций |
| 2.0 | Кадмий |
| 2.25 | Висмут |
| 2.5 | Магний |
| 2.5 | Цинк |
| 2.5 | Лантан |
| 2.5 | Серебро |
| 2.5 | Золото |
| 2.59 | Иттрий |
| 2.75 | Алюминий |
| 3.0 | Медь |
| 3.0 | Сурьма |
| 3.0 | Торий |
| 3.17 | Скандий |
| 3.5 | Платина |
| 3.75 | Кобальт |
| 3.75 | Палладий |
| 3.75 | Цирконий |
| 4.0 | Железо |
| 4.0 | Никель |
| 4.0 | Гафний |
| 4.0 | Марганец |
| 4.5 | Ванадий |
| 4.5 | Молибден |
| 4.5 | Родий |
| 4.5 | Титан |
| 4.75 | Ниобий |
| 5.0 | Иридий |
| 5.0 | Рутений |
| 5.0 | Тантал |
| 5.0 | Технеций |
| 5.0 | Хром |
| 5.5 | Бериллий |
| 5.5 | Осмий |
| 5.5 | Рений |
| 6.0 | Вольфрам |
| 6.0 | β-Уран |
Температура плавления:
- Температуры плавления чистых металлов лежат в диапазоне от −38,83 °C (ртуть) до 3422 °C (вольфрам).
- Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые металлы, например, олово и свинец, могут расплавиться на обычной электрической или газовой плите.
- В зависимости от температуры плавления металлы делятся на: легкоплавкие (до 600 °C); среднеплавкие (от 600 до 1600 °C); тугоплавкие (выше 1600 °C).
Таблица температуры плавления легкоплавких металлов и сплавов:
| Название металла | Температура плавления, оС |
| Ртуть | -38,83 |
| Франций | 25 |
| Цезий | 28,44 |
| Галлий | 29,7646 |
| Рубидий | 39,3 |
| Калий | 63,5 |
| Натрий | 97,81 |
| Индий | 156,5985 |
| Литий | 180,54 |
| Олово | 231,93 |
| Полоний | 254 |
| Висмут | 271,3 |
| Таллий | 304 |
| Кадмий | 321,07 |
| Свинец | 327,46 |
| Цинк | 419,53 |
Таблица температуры плавления среднеплавких металлов и сплавов:
| Название металла | Температура плавления, оС |
| Сурьма | 630,63 |
| Нептуний | 639 |
| Плутоний | 639,4 |
| Магний | 650 |
| Алюминий | 660,32 |
| Радий | 700 |
| Барий | 727 |
| Стронций | 777 |
| Церий | 795 |
| Иттербий | 824 |
| Европий | 826 |
| Кальций | 841,85 |
| Лантан | 920 |
| Празеодим | 935 |
| Германий | 938,25 |
| Серебро | 961,78 |
| Неодим | 1024 |
| Прометий | 1042 |
| Актиний | 1050 |
| Золото | 1064,18 |
| Самарий | 1072 |
| Медь | 1084,62 |
| Уран | 1132,2 |
| Марганец | 1246 |
| Бериллий | 1287 |
| Гадолиний | 1312 |
| Тербий | 1356 |
| Диспрозий | 1407 |
| Никель | 1455 |
| Гольмий | 1461 |
| Кобальт | 1495 |
| Иттрий | 1526 |
| Эрбий | 1529 |
| Железо | 1538 |
| Скандий | 1541 |
| Тулий | 1545 |
| Палладий | 1554,9 |
| Протактиний | 1568 |
Таблица температуры плавления тугоплавких металлов и сплавов:
| Название металла | Температура плавления, оС |
| Лютеций | 1652 |
| Титан | 1668 |
| Торий | 1750 |
| Платина | 1768,3 |
| Цирконий | 1855 |
| Хром | 1907 |
| Ванадий | 1910 |
| Родий | 1964 |
| Технеций | 2157 |
| Гафний | 2233 |
| Рутений | 2334 |
| Иридий | 2466 |
| Ниобий | 2477 |
| Молибден | 2623 |
| Тантал | 3017 |
| Осмий | 3033 |
| Рений | 3186 |
| Вольфрам | 3422 |
Плотность:
В зависимости от плотности металлы делят на лёгкие (плотность от 0,53 до 5 г/см³) и тяжёлые (от 5 до 22,6 г/см³).
Самым лёгким металлом является литий (плотность 0,53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22,6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Пластичность:
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними.
Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются.
Пластичность зависит и от чистоты металла. Так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы, такие, как золото, серебро, свинец, алюминий, осмий, могут срастаться между собой, но на это могут уйти десятки лет.
Электропроводность:
Все металлы хорошо проводят электрический ток, обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля.
Серебро, медь и алюминий имеют наибольшую электропроводность. По этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также и натрий.
В экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием.
Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Теплопроводность:
Теплопроводность металлов зависит от подвижности свободных электронов.
Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла. Широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Наименьшая теплопроводность — у висмута и ртути.
Цвет:
Цвет у большинства металлов примерно одинаковый — светло-серый, иногда с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Металлы подразделяются на цветные и черные.
Чёрные металлы – железо и сплавы на его основе (стали, ферросплавы, чугуны). К чёрным металлам также зачастую относят марганец и, иногда, – хром и ванадий.
Цветные металлы — это особый класс нержавеющих металлов и сплавов, в составе которых нет железа. Металлы называются цветными, потому что каждый из них имеет определенный окрас. К цветным металлам относятся медь, молибден, свинец, цинк, олово, никель, кадмий, кобальт, алюминий, титан, магний, висмут, вольфрам, ртуть, золото, платину, серебро, палладий, родий, рутений, осмий, иридий.
Примечание: © Фото https://www.pexels.com, https://pixabay.com
карта сайта
Физические свойства металлов


Средняя оценка: 4.2
Всего получено оценок: 283.
Средняя оценка: 4.2
Всего получено оценок: 283.
Физические свойства металлов отличают их от неметаллов. Все металлы, кроме ртути, – твёрдые кристаллические вещества, являющиеся восстановителями в окислительно-восстановительных реакциях.
Металлы занимают I-II группы и побочные подгруппы III-VIII групп. Металлические свойства, т.е.
способность отдавать валентные электроны или окисляться, увеличиваются сверху вниз по мере увеличения количества энергетических уровней.
Слева направо металлические свойства ослабевают, поэтому наиболее активные металлы находятся в I-II группах, главных подгруппах. Это щелочные и щелочноземельные металлы.
Определить степень активности металлов можно по электрохимическому ряду напряжений. Металлы, стоящие до водорода, наиболее активны. После водорода стоят слабоактивные металлы, не вступающие в реакцию с большинством веществ.
Рис. 1. Электрохимический ряд напряжений металлов.
Вне зависимости от активности все металлы имеют общее строение. Атомы в простом металле расположены не хаотично, как в аморфных веществах, а упорядоченно – в виде кристаллической решётки. Удерживает атомы в одном положении металлическая связь.
Такой вид связи осуществляется за счёт положительно заряженных ионов, находящихся в узлах кристаллической ячейки (единицы решётки), и отрицательно заряженных свободных электронов, которые образуют так называемый электронный газ. Электроны отделились от атомов, превратив их в ионы, и стали перемещаться в решётке хаотично, скрепляя ионы вместе. Без электронов решётка бы распалась за счёт отторжения одинаково заряженных ионов.
Различают три типа кристаллической решётки. Кубическая объемно-центрированная состоит из 9 ионов и характерна хрому, железу, вольфраму. Кубическая гранецентрированная включает 14 ионов и свойственная свинцу, алюминию, серебру. Из 17 ионов состоит гексагональная плотноупакованная решётка цинка, титана, магния.
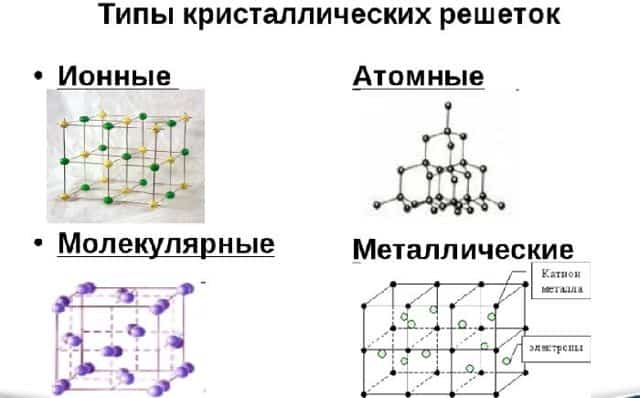 Рис. 2. Виды кристаллических решёток.
Рис. 2. Виды кристаллических решёток.
Строение кристаллической решётки определяет основные физические и химические свойства металлов. Металлы блестят, плавятся, проводят тепло и электричество.
Промышленность и металлургия нашли применение физическим свойствам металлов в изготовлении деталей, фольги, корпусов машин, зеркал, бытовой и промышленной химии.
Особенности металлов и их использование представлены в таблице физических свойств металлов.
| Свойства | Особенности | Примеры | Применение |
| Металлический блеск | Способность отражать солнечный свет | Наиболее блестящими металлами являются Hg, Ag, Pd | Изготовление зеркал |
| Плотность | Лёгкие – имеют плотность меньше 5 г/см3 | Na, K, Ba, Mg, Al. Самый лёгкий металл – литий с плотностью 0,533 г/см3 | Изготовление облицовки, деталей самолётов |
| Тяжёлые – имеют плотность больше 5 г/см3 | Sn, Fe, Zn, Au, Pb, Hg. Самый тяжёлый – осмий с плотностью 22,5 г/см3 | Использование в сплавах | |
| Пластичность | Способность изменять форму без разрушений (можно раскатать в тонкую фольгу) | Наиболее пластичные – Au, Cu, Ag. Хрупкие – Zn, Sn, Bi, Mn | Формовка, сгибание труб, изготовление проволоки |
| Твёрдость | Мягкие – режутся ножом | Na, K, In | Изготовление мыла, стекла, удобрений |
| Твёрдые – сравнимы по твёрдости с алмазом | Самый твёрдый – хром, режет стекло | Изготовление несущих конструкций | |
| Температура плавления | Легкоплавкие – температура плавления ниже 1000°С | Hg (38,9°С), Ga (29,78°С), Cs (28,5°С), Zn (419,5°C) | Производство радиотехники, жести |
| Тугоплавкие – температура плавления выше 1000°С | Cr (1890°С), Mo (2620°С), V (1900°С). Наиболее тугоплавкий – вольфрам (3420°С) | Изготовление ламп накаливания | |
| Теплопроводность | Способность передавать тепло другим телам | Лучше всего проводят ток и тепло Ag, Cu, Au, Al | Приготовление пищи в металлической посуде |
| Электропроводность | Способность проводить электрический ток за счёт свободных электронов | Передача электричества по проводам |
 Рис. 3. Примеры применения металлов.
Рис. 3. Примеры применения металлов.
Из урока 9 класса узнали о физических свойствах металлов. Кратко рассмотрели положение металлов в периодической таблице и особенности строения кристаллической решётки.
Благодаря строению металлы обладают пластичностью, твёрдостью, способностью плавиться, проводить электрический ток и тепло. Свойства металлов неоднородны. Различают лёгкие и тяжёлые металлы, лёгкоплавкие и тугоплавкие, мягкие и твёрдые.
Физические свойства используются для изготовления сплавов, электрических проводов, посуды, мыла, стекла, конструкций различной формы.
Чтобы попасть сюда — пройдите тест.
Средняя оценка: 4.2
Всего получено оценок: 283.
А какая ваша оценка?
Гость завершил
Тест «Отрочество»с результатом 9/14
Гость завершил
Тест «Судьба человека»с результатом 12/12
Гость завершил
Тест «Детство»с результатом 11/14
Гость завершил
Тест Мышцыс результатом 8/10
Гость завершил
Тест «Герой нашего времени»с результатом 7/16
Гость завершил
Тест «Гранатовый браслет»с результатом 8/14
Гость завершил
Тест на тему «Виды крестьян»с результатом 4/5
Гость завершил
Тест «Биография Бунина»с результатом 6/11
Гость завершил
Тест «После бала»с результатом 5/10
Не подошло? Напиши в х, чего не хватает!
Физические свойства металлов
- Общие физические свойства металлов
- Благодаря наличию свободных электронов (“электронного газа”) в кристаллической решетке все металлы проявляют следующие характерные общие свойства:
- 1) Пластичность – способность легко менять форму, вытягиваться в проволоку, прокатываться в тонкие листы.
2) Металлический блеск и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл светом.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т.к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение “электронного газа”.
4) Теплопроводность. Обусловлена высокой подвижностью свободных электронов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность – у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и больше радиус атома. Самый легкий – литий (ρ=0,53 г/см3); самый тяжелый – осмий (ρ=22,6 г/см3). Металлы, имеющие плотность менее 5 г/см3 считаются “легкими металлами”.
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т.пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C). Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
Общие химические свойства металлов
Сильные восстановители: Me0 – nē → Men+
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
1. РЕАКЦИИ МЕТАЛЛОВ С НЕМЕТАЛЛАМИ
- 1) С кислородом:2Mg + O2 → 2MgO
- 2) С серой:Hg + S → HgS
- 3) С галогенами:Ni + Cl2 –t°→ NiCl2
- 4) С азотом:3Ca + N2 –t°→ Ca3N2
- 5) С фосфором:3Ca + 2P –t°→ Ca3P2
- 6) С водородом (реагируют только щелочные и щелочноземельные металлы):2Li + H2 → 2LiH
- Ca + H2 → CaH2
2. РЕАКЦИИ МЕТАЛЛОВ С КИСЛОТАМИ
- 1) Металлы, стоящие в электрохимическом ряду напряжений до H восстанавливают кислоты-неокислители до водорода:
- Mg + 2HCl → MgCl2 + H2
- 2Al+ 6HCl → 2AlCl3 + 3H2
- 6Na + 2H3PO4 → 2Na3PO4 + 3H2
- 2) С кислотами-окислителями:
- При взаимодействии азотной кислоты любой концентрации и концентрированной серной с металлами водород никогда не выделяется!
Физические и химические свойства металлов
Металлы широко распространены в природе и могут встречаться в различном виде: в самородном состоянии (Ag, Au, Rt, Cu), в виде оксидов (Fe3O4, Fe2O3, (NaK)2O×AlO3), солей (KCl, BaSO4, Ca3(PO4)2), а также сопутствуют различным минералам (Cd – цинковые руды, Nb, Tl – оловянные и т.д.).
Физические свойства металлов
Всем металлам присущи металлический блеск (однако In и Ag отражают свет лучше других металлов), твердость (самый твердый металл – Cr, самые мягкие металлы – щелочные), пластичность (в ряду Au, Ag, Cu, Sn, Pb, Zn, Fe наблюдается уменьшение пластичности), ковкость, плотность (самый легкий металл – Li, самый тяжелый – Os), тепло – и электропроводность, которые уменьшаются в ряду Ag, Cu, Au, Al, W, Fe.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип > 1000С) и легкоплавкие (Tкип < 1000С). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Среди металлов присутствуют s-, p-, d- и f-элементы. Так, s- элементы – это металлы I и II групп Периодической системы (ns1, ns2), р- элементы – металлы, расположенные в группах III – VI (ns2np1-4). Металлы d-элементы имеют большее число валентных электронов по сравнению с металлами s- и p-элементами.
Общая электронная конфигурация валентных электронов металлов d-элементов – (n-1)d1-10ns2. Начиная с 6 периода появляются металлы f-элементы, которые объединены в семейства по 14 элементов (за счет сходных химических свойств) и носят особые названия лантаноидов и актиноидов.
Общая электронная конфигурация валентных электронов металлов f-элементов – (n-2)f1-14(n-1)d0-1ns2.
Химические свойства металлов
- Металлы способны реагировать с простыми веществами, такими как кислород (реакция горения), галогены, азот, сера, водород, фосфором и углеродом:
- 2Al + 3/2 O2 = Al2O3 (оксид алюминия)
- 2Na + Cl2 = 2NaCl (хлорид натрия)
- 6Li + N2 = 2Li3N (азид лития)
- 2Li+2C = Li2C2 (карбид лития)
- 2K +S = K2S (сульфид калия)
- 2Na + H2 = NaH (гидрид натрия)
- 3Ca + 2P = Ca3P2 (фосфид кальция)
- Металлы взаимодействуют друг с другом, образуя интерметаллические соединения:
- 3Cu + Au = Cu3Au
- Щелочные и некоторые щелочноземельные металлы (Ca, Sr, Ba) взаимодействуют с водой с образованием гидроксидов:
- Ba + 2H2O = Ba(OH)2 + H2↑
- 2Na + 2H2O = 2NaOH + H2↑
В ОВР металлы являются восстановителями – отдают валентные электроны и превращаются в катионы. Восстановительная способность металла — его положение в электрохимическом ряду напряжений металлов. Так, чем левее в ряду напряжений стоит металл, тем более сильные восстановительные свойства он проявляет.
- Металлы, стоящие в ряду активности до водорода способны реагировать с кислотами:
- 2Al + 6HCl = 2AlCl3 + 3 H2↑
- Zn + 2HCl = ZnCl2 + 2H2↑
- Fe + H2SO4 = FeSO4 + H2↑
Получение металлов
- Щелочные, щелочноземельные металлы и алюминий получают электролизом расплавов солей или оксидов этих элементов:
- 2NaCl = 2Na + Cl2↑
- CaCl2 = Ca + Cl2↑
- 2Al2O3 = 4Al + 3O2↑
- Тяжелые металлы получают восстановлением из руд при высоких температурах и в присутствии катализатора (пирометаллургия) (1) или восстановлением из солей в растворе (гидрометаллургия) (2):
- Cu2O + C = 2Cu + CO (1)
- CuSO4 + Fe = Cu + FeSO4 (2)
- Некоторые металлы получают термическим разложением их неустойчивых соединений:
- Ni(CO)4 = Ni + 4CO
Примеры решения задач
Физические свойства металлов
9. Физические свойства металлов
Металлическая связь и особенности кристаллического строения обуславливают особые физические свойства металлов.
Металлическая связь основана на обобществлении электронов, входящих в состав атомов металла. Все электроны на внешних энергетических уровнях атомов металлов обобществленные, т.е. принадлежат всем атомам вещества.
И эти электроны легко отрываются и попадают на энергетические уровни таких же атомов металлов.
Постоянно перемещаясь по кристаллической решетке, электроны компенсируют силы электростатического отталкивания между положительно заряженными ионами и тем самым связывают их в устойчивую металлическую решетку.
Металлическая связь – это связь в металлах и сплавах между атом-ионами посредством обобществленных электронов.
Разобраться в том, какой электрон принадлежал какому атому, просто невозможно, так как все оторвавшиеся электроны становятся общими, соединяясь с ионами. Эти электроны временно образуют атомы, потом снова отрываются и соединяются с другим ионом. Этот процесс продолжается бесконечно. Таким образом, в металлических соединениях атомы непрерывно превращаются в ионы и наоборот.
Именно строением металлической связи обусловлены физические свойства металлов.
К физическим свойствам металлов относятся:
-
Металлический блеск.
-
Электропроводность и теплопроводность.
-
Пластичность.
-
Твердость.
-
Высокая плотность и температура плавления.
Рассмотрим каждое из свойств более подробно.
Металлический блеск.
Металлический блеск обусловлен металлической связью между атомами, для которой свойственны обобществленные электроны. Они как раз и испускают под воздействием света свои, вторичные волны излучения, которые мы воспринимаем как металлический блеск.
- В порошкообразном состоянии большинство металлов теряют металлический блеск и приобретают серую или черную окраску.
- Металлический блеск в порошкообразном состоянии сохраняют алюминий и магний.
- Прекрасно отражают свет палладий Pd, ртутьHg, сереброAg, медьCu.
- Из алюминия, серебра и палладия, основываясь на их отражательной способности, изготавливают зеркала, в том числе и применяемые в прожекторах.
- Электропроводность и теплопроводность.
Все металлы хорошо проводят электрический ток и имеют высокую теплопроводность, также благодаря наличию металлической связи. При нагревании металла, увеличивается скорость движения электронов. Быстро движущиеся по кристаллической решетке электроны выравнивают температуру по всей поверхности металла, проводя тепло. Высокая теплопроводность металлов используется для изготовления из нихпосуды.
Высокая электропроводность металлов обусловлена направленным движением электронов в кристаллической решетке при воздействии электрического тока. СереброAg, медьCu, золотоAu и алюминий Al обладают наибольшей электропроводностью, поэтому медьCu и алюминийAl используют в качестве материала для изготовления электрических проводов.
- Наименьшей электропроводностью обладают марганец Mn, свинец Pb, ртуть Hgи вольфрам W.
- Пластичность.
- Пластичность – это физической свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
- Большинство металлов пластично, так как слои атом-ионов металлов легко смещаются относительно друг друга и между ними не происходит разрыва связи.
Наиболее пластичные металлы – золотоAu, сереброAg, медьCu. Из золотаAu можно изготовить тонкую фольгу толщиной 0,003 мм, которую используют для золочения изделий.
Именно на пластичности металлов основано кузнечное дело и возможность изготавливать различные предметы с помощью механического воздействия на металл.
Твердость.
Все металлы (кроме ртути) при нормальных условиях представляют собой твердые вещества. Твердость металлов различна. Наиболее твердыми являются металлы побочной подгруппы шестой группы Периодической системы Д.И. Менделеева. Наименее твердыми являются щелочные металлы.
Плотность.
По плотности металлы классифицируют на легкие (их плотность от 0,53 до 5 г/см3) и тяжелые (плотность этих металлов от 5 до 22,6 г/см3). Самым легким металлом является литий Li, плотность которого 0,53 г/см3. Самыми тяжелыми металлами в настоящее время считают осмий Os и иридий Ir (плотность около 22,6 г/см3).
Температура плавления.
Температура плавления металлов находится в диапазоне от 39 (ртутьHg) до 3410оС (вольфрам W). Температура плавления большинства металлов высока, однако некоторые металлы, например, олово Sn и свинец Pl, можно расплавить на электрической плите.
- Физические свойства металлов и в настоящее время широко используются в промышленности и электронике.
- В технике все металлы делятся на черные, к ним относятся железо и его сплавы, и цветные.
- Изделия из различных видов металлов используются повсеместно благодаря их пластичности, но чаще всего в сплавах.
- К драгоценным металлам относят золото, серебро, платину и некоторые другие редко встречающиеся металлы.
Металл: что это такое, его физические свойства, из чего состоит
05Дек
Содержание статьи
Обнаружение общих физических и химических свойств металлов и сплавов привело к повсеместному использованию материала. Со временем ученые начали подробно изучать его характеристики, а также создавать различные методы металлообработки, которые увеличивают прочность, улучшают кристаллическую решетку.
На настоящий момент есть такие составы, которые используются при кораблестроении. Все больше сфер жизни не может обойтись без металлических элементов – от бытовой ложки или авторучки до сложных механических узлов и микросхем. Но обыватели часто не понимают, что за вещество мы используем, и какие особенности дают ему такую распространенность.
В статье мы подробно поговорим про это.
Что это такое – металл
Древнегреческое слово metallion как раз обозначает «выкапывать из земли» – добытое из горной руды. На настоящий момент известно 96 значений в чистом виде и неограниченное количество сплавов.
Все они отличаются от неметаллов повышенными прочностными качествами и проводимостью, поэтому из них делают провода.
На первый взгляд отличить металлический образец от каменного или иного можно по специфическому блеску.
Физические свойства
В условиях комнатной температуры и без применения давления все вещества обладают твердым состоянием. Но есть галлий, он уже при 30 градусах тепла начинает деформироваться, тает в руках. Можно отметить характеристики:
- Высокая пластичность. Хрупкие только марганец, олово и цинк.
- Могут быть легкие и тяжелые. Сравни алюминий с осмием.
- Температура плавления очень большая. Есть и исключения, например, ртуть, именно по этой причине ее используют в классических термометрах.
- Цвет – серый, серебристый, голубоватый. Редкими являются цветные изделия, например, желтые или красные.
- Увеличенная проводимость тепла и электричества, особенно у меди, поэтому имеют популярность медные провода.
Основные химические свойства металлов
В данной категории нет общих правил, так как все они разделяются на множество подгрупп по уровню активности – щелочные, актиноиды, полуметаллы и другие.
Многие взаимодействуют с водой, почти все – с кислородом (кроме золота и платины),происходит окисление. Процесс проходит в нормальных условиях, если в составе много щелчки, только при нагреве – если нет.
Также почти все элементы вступают в реакцию с серой и хлором.
Признаки
Перечислим черты, по которым обыватель может отличить вещества этой категории от неметаллов:
- Блеск.
- Хорошая проводимость тепла и электричества.
- Прочность.
- Подвергаются ковке и свариванию.
- Кристаллическое строение тела.
- Высокая температура плавления и кристаллизации.
Классификация и виды металлов
Есть чистые, однокомпонентные структуры и сплавы. Самым классическим примером можно назвать различные виды стали. Они различаются по ГОСТу в соответствии с добавлением легирующих добавок. Чем больше содержание углерода, тем крепче материал. Также есть общепринятое разграничение, ниже представим подтипы.
Черные
Их добывают из металлической руды. В производстве они занимают 90% от всего сырья. Обычно это чугуны и стали.
Для изменения характеристик добавляют большее или меньшее количество углерода и легирующие добавки: медь, кремний, хром, никель.
Одним из очень популярных подвидов является нержавейка, которая отличается своим блеском поверхности и уникальными свойствами – легкостью, высокой прочностью и устойчивостью к влажности, температурным перепадам.
Что относится к цветным металлам
Второе название – нежелезные, то есть сплавы не содержат в себе железа, а состоят из более дорогостоящих материалов. Вещества имеют различный цвет, отличаются уникальными качествами:
- долговечность;
- длительное сохранение свойств;
- образование оксидной пленки, которая препятствует коррозии.
Благодаря этому, определенные разновидности можно использовать в медицине, ювелирном деле, химической промышленности, при изготовлении электрических проводов. К цветмету относится алюминий, цинк, олово, свинец, никель, хром, серебро, золото и другие.
Медь и ее сплавы являются популярными металлами
Медная руда была обработана человеком одна из первой, потому что она подвергается холодному методу ковки и штамповки. Податливость привела к востребованности повсеместно. Кислород в составе приводит к красному отливу.
Но уменьшение валентности в различных соединениях приведет к желтому, зеленому, синему цвету. Привлекательным качеством считается отличная теплопроводность – на втором месте после серебра, поэтому она применяется для проводов.
Соединения могут быть:
- твердыми – в сочетании с железом, мышьяком, цинком, фосфором;
- с плохой растворимостью с висмутом, свинцом;
- хрупкими – с серой или кислородом.
К металлам относятся алюминий и сплавы
Al открыт в 1825 году и отличается легкостью и простотой в металлообработке. Производится из бокситов, при этом запасы этой горной породы практически неиссякаемы. Далее элемент соединяют в различных пропорциях с медью, марганцем, магнием, цинком, кремнием. Реже с титаном, литием, бериллием. Особенности в зависимости от добавок:
- хорошая свариваемость;
- устойчивость к коррозии;
- высокая усталостная прочность;
- пластичность.
Его применяют для изготовления ювелирных изделий, столовых приборов, а также для стекловарения, в пищевой и военной промышленности, для создания ракет и для производства водорода и тепла в алюмоэнергетике.
Все о металлах магний, титан и их сплавах
Mg – самое легкое вещество из этой группы. Не обладает прочностью, но есть достоинства, например, пластичность, химическая активность. Благодаря высокой конструкционной способности его добавляют в составы, чтобы увеличивать свариваемость, простоту металлообработки режущим ножом. Необходимо учитывать, что магний очень восприимчив к ржавлению.
Титан имеет похожие качества – легкость, пластичность, серебристый цвет. Но антикоррозийная пленка появляется при первом соприкосновении с кислородом. Отличительные особенности – низкая теплопроводность, электропроводность, отсутствие магнитизма.
Металл, содержащий титан, – это вещество, используемое для авиационной, химической, судостроительной промышленности.
Антифрикционные сплавы
Характерная особенность этой группы – удобство применения при механических воздействиях. Они практически не создают трения, а также снижают его у других композитов. Очень часто они выступают в качестве твердой смазки для узлов, например, для подшипников. В составе обычно бывает фторопласт, латунь, бронза, железографит и баббит.
Мягкие
Это те, у которых ослаблены металлические связи. По этой причине они имеют более низкую температуру плавления и кипения, просто деформируются.
Иногда можно одним нажатием пальца сделать вмятину, ногтем оставить царапину К ним относятся: медь, серебро, золото, бронза, свинец, алюминий, цезий, натрий, калий, рубидий и другие.
Одним из наиболее мягких является ртуть, она находится в природе в жидком состоянии.
Что значит твердый металл
В природе такая руда встречается крайне редко. Порода находится у упавших метеоритов. Один из наиболее популярных – хром. Он тугоплавкий и легко поддается металлообработке. Еще один элемент – вольфрам. Он очень плохо плавится, но при правильной обработке используется в осветительных приборах благодаря устойчивости к теплу и гибкости.
Металлические материалы в энергетике
Мы бы не имели такую развитую электросеть и массу приборов, потребляющих электричество, если бы ряд веществ не отличались наличием свободных электронов, положительных ионов и высокой проводимостью. Провода делают из свинца, меди и алюминия. Отлично бы подошло серебро, но его редкость влияет на стоимость, поэтому редко используется.
Особенности черных вторичных металлов
Это отходы, которые образуются в результате одного из этапа металлообработки – ковки, резки. Это могут быть обрезки или стружки. Они отправляются в сталеплавильные печи, но перед этим должны пройти проверки по ГОСТу. Лом называют чермет, его различают на стальной и чугунный по цене. Его использование очень востребовано вместо обработки руды.
Щелочноземельные сплавы
Это твердые вещества, которые имеют высокую химическую активность. В чистом виде встречаются очень редко, зато применяются в соединениях. Их значение нельзя переоценить с точки зрения анатомии человека и животного. Магний и кальций – необходимые микроэлементы.
Понятие щелочной металл
Они способны растворяться в воде, образуя щелочь. Из-за своей повышенной химической активности (вступление в реакцию происходит с бурным действием, воспламенением, выделением газа, дыма) в природе почти не встречается. Ведь на внешнем уровне всего один электрон, который легко отдается любому веществу. Гидроксиды очень важны в промышленности.
Общая характеристика материалов из d- и f-семейств
Это переходные элементы, которые могут являться как окислителями, так и восстановителями. Свойства зависят от среды, в которой они находятся. Но есть и общие:
- на внешнем уровне много электронов;
- несколько степеней окисления;
- увеличенная валентность;
- прочность;
- тягучесть;
- ковкость.
Из чего состоят побочные подгруппы металлов системы Менделеева
По сути это разновидности предыдущей категории – переходные элементы. Это линейка от скандия до цинка. Они часто выплавляются и обладают фактически такими же характеристиками, как и вышеперечисленные материалы из d- и f-семейств.
Сплавы
Чистые слитки, добываемые из руды, используются максимально редко. Это обусловлено как дороговизной, так и недостаточно хорошими качествами (чтобы исправить, добавляют углерод, легирующие добавки). Иногда в природе встречаются соединения, и нужно только подкорректировать состав. Самые известные:
- латунь;
- бронза;
- сталь;
- чугун.
Сравнение свойств
Вторая часть элементов в периодической системой отличается многообразием характеристик, поэтому почти невозможно привести полную сводную таблицу. Мы предлагаем таблицу, на которой представлено 4 отличительные черты:
| Признаки | Металлы | Неметаллы |
| Положение в П. С. | Под диагональю бор-астат | Над ней |
| Строение атома | Большой атомный радиус, чисто электронов на последнем слое — от 1 до 3 | Маленький, от 4 до 7 — соответственно |
| Физические св-ва | Электропроводность, теплопроводность, блеск, ковкость, пластичность, по агрегатному состоянию, в основном, твёрдые | Диэлектрики, неблестящие, хрупкие, газы, жидкости и летучие твёрдые вещества |
| Кристаллические решетки | Металлическая | Молекулярная, атомная |
| Химические св-ва | Восстановители | Окислительные (иногда восстанов-ли) |
Мы рассказали про металл, что это за материал, как он используется. Если вам нужны станки по металлообработке, закажите их в компании «Роста».
У нас в наличии и на заказ имеются ручные и полуавтоматические ленточнопильные станки, а также маятниковые, вертикальные и двухстоечные агрегаты. Цена на товары снижена в 1.5 — 2 раза по сравнению с зарубежными аналогами.
Чтобы уточнить интересующую вас информацию, свяжитесь с менеджерами, мы с радостью поможем в выборе оборудования.






