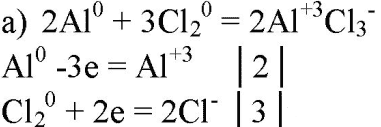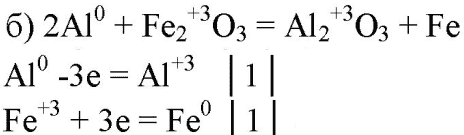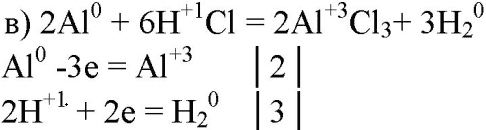- 2. Почему алюминий в природе встречается только в соединениях?
- 3. Охарактеризуйте важнейшие природные соединения алюминия
- 4. Для получения алюминия из АlСl3 в качестве восстановителя можно использовать кальций. Охарактеризуйте этот процесс и составьте уравнение реакции, покажите переход электронов. Почему эту реакцию нельзя проводить в водном растворе?
- 5. Составьте уравнения реакций, в которых алюминий восстанавливает: а) галогены; б) железо; в) ионы водорода; г) серу; д) кислород. Покажите переход электронов
- 6. Могут ли быть окислителями: а) атомы алюминия; б) ионы алюминия? Ответ подтвердите уравнениями реакций
- 7. Сколько потребуется алюминия, чтобы при реакции с соляной кислотой получить столько водорода, сколько его выделяется при взаимодействии 1 моль натрия с водой?
- 8. На сплав алюминия и меди подействовали избытком концентрированного раствора гидроксида натрия при нагревании. Выделилось 2,24 л некоторого газа (н. у.). Вычислите процентный состав сплава, если его общая масса была 10 г
- Тестовые задания
- 1. Схема строения иона Аl — это:
- 2. Один из способов получения металлов, например, по уравнению реакции
- Fe2O3 + 2Аl = Аl2O3 + 2Fe называют:
- 3. Химическую реакцию, уравнение которой 2Аl + 6НСl→2АlСl3 + ЗН2↑, относят к реакциям:
- 1) соединения
- 2) разложения
- 3) обмена
- 4) замещения
- 4. Установите соответствие между названием минерала и его формулой
- 1) боксит
- 2) корунд
- 3) каолинит
- 4) полевой шпат
- А. Аl2O3
- Б. К2O • Аl2O3 • 6SiO2
- В. Аl2O3 • 2SiO2 • 2Н2O
- Г. Аl2O3 • nН2O
- Алюминий, его соединения
- Варианты ответов
- Варианты ответов
- Варианты ответов
- Варианты ответов
- Варианты ответов
- Варианты ответов
- Варианты ответов
- Решу егэ
- Задания ЕГЭ по химии: Электролиз расплавов и растворов

Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
Издательство: Просвещение
Тип: Учебник
От Na через Mg до Al относительные массы возрастают и постепенно ослабляются металлические (восстановительные) и усиливаются неметаллические (окислительные) свойства. Это происходит из-за увеличения количества электронов на внешнем энергетическом уровне и уменьшения радиуса. Чем количество электронов меньше и больше радиус (Na), тем сильнее проявляются восстановительные свойства.
2. Почему алюминий в природе встречается только в соединениях?
В электрохимическом ряду напряжений алюминий находится за самыми активными металлами. Он легко вступает в реакции с другими веществами и в природе встречается в составе разнообразных соединений.
3. Охарактеризуйте важнейшие природные соединения алюминия
- Каолинит
- Боксит
- Корунд
- Ортоклаз или полевой шпат
- Нефелин
4. Для получения алюминия из АlСl3 в качестве восстановителя можно использовать кальций. Охарактеризуйте этот процесс и составьте уравнение реакции, покажите переход электронов. Почему эту реакцию нельзя проводить в водном растворе?
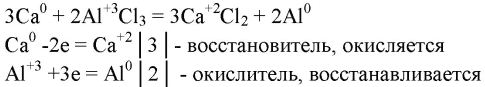
- Реакцию проводят в расплаве, а не в водном растворе, потому что кальций вступит в реакцию с водой:
5. Составьте уравнения реакций, в которых алюминий восстанавливает: а) галогены; б) железо; в) ионы водорода; г) серу; д) кислород. Покажите переход электронов
6. Могут ли быть окислителями: а) атомы алюминия; б) ионы алюминия? Ответ подтвердите уравнениями реакций
- а) Атомы алюминия не могут быть окислителями, потому что металлы не имеют способности принимать электроны.
- б) Ионы алюминия могут быть окислителями
7. Сколько потребуется алюминия, чтобы при реакции с соляной кислотой получить столько водорода, сколько его выделяется при взаимодействии 1 моль натрия с водой?
8. На сплав алюминия и меди подействовали избытком концентрированного раствора гидроксида натрия при нагревании. Выделилось 2,24 л некоторого газа (н. у.). Вычислите процентный состав сплава, если его общая масса была 10 г
Тестовые задания
1. Схема строения иона Аl — это:
2. Один из способов получения металлов, например, по уравнению реакции
Fe2O3 + 2Аl = Аl2O3 + 2Fe называют:
Алюмотермией
3. Химическую реакцию, уравнение которой 2Аl + 6НСl→2АlСl3 + ЗН2↑, относят к реакциям:
1) соединения
2) разложения
3) обмена
4) замещения
4) замещения
4. Установите соответствие между названием минерала и его формулой
1) боксит
2) корунд
3) каолинит
4) полевой шпат
А. Аl2O3
Б. К2O • Аl2O3 • 6SiO2
В. Аl2O3 • 2SiO2 • 2Н2O
Г. Аl2O3 • nН2O
Вам также может понравиться
Алюминий, его соединения
Будьте внимательны! У Вас есть 10 минут на прохождение теста. Система оценивания — 5 балльная. Разбалловка теста — 3,4,5 баллов, в зависимости от сложности вопроса. Порядок заданий и вариантов ответов в тесте случайный. С допущенными ошибками и верными ответами можно будет ознакомиться после прохождения теста. Удачи!
Варианты ответов
- оксид и гидроксид алюминия имеют амфотерные свойства
- гидроксид алюминия может быть получен при взаимодействии оксида алюминия с водой
- в окислительно-восстановительных реакциях алюминий ведёт себя как окислитель
- поверхность алюминия покрыта прочной оксидной плёнкой, предохраняющей металл от окисления
Варианты ответов
- 2Al + 6H2O = 2Al(OH)3↓ + 3H2↑
- Cr2O3 + 2Al = 2Cr + Al2O3
- 4Al + 3O2 = 2Al2O3
- 2Al + 6HCl = 2AlCl3 + 3H2↑
Гидроксид алюминия реагирует с:
Варианты ответов
- гидроксидом натрия
- хлоридом натрия
- железом
- азотной кислотой
Для осуществления превращения по схеме Al → AlCl3 → Al(OH)3 → Na[Al(OH)4] необходимо последовательно использовать вещества:
Варианты ответов
- Cl2, KOH, NaOH
- HCl, NaOH, KOH
- Cl2, Ca(OH)2, KOH
- BaCl2, Cu(OH)2, NaOH
Варианты ответов
Варианты ответов
- общее число электронов
- число энергетических уровней
- степень окисления
- заряд ядра
- число нейтронов
Установите соответствие между реакцией и суммой всех коэффициентов:
Варианты ответов
- Al + O2 →
- Al + Cl2 →
- Al + P →
- Al + C →
Чему равна масса (г) оксида алюминия, который образуется при взаимодействии алюминия с 134,4 л кислорода (н.у.)?
Запишите название минерала состава Al2O3, разновидностью которого является наждак, применяемый как шлифовальный материал.
Сохранить этот тест в личном кабинете и раздать его своим ученикам
Чтобы добавить комментарий зарегистрируйтесь или войдите на сайт
Лицензия на осуществление образовательной деятельности №5251 от 25.08.2017 г.
Решу егэ
Тип 25 № 9782
Установите соответствие между простым веществом и основным способом его промышленного получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- ПРОСТОЕ ВЕЩЕСТВО
- А) алюминий
- Б) железо
- В) натрий
- Г) кремний
- СПОСОБ ПОЛУЧЕНИЯ
- 1) восстановление оксида углеродом
- 2) восстановление оксида водородом
- 3) реакция замещения в водном растворе
- 4) электролиз раствора
- 5) электролиз расплава
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Спрятать решениеРешение.
Установим соответствие.
А) Алюминий образует прочную химическую связь с кислородом. По сравнению с другими металлами, восстановление алюминия из руды более сложно в связи с его высокой реакционной способностью и с высокой температурой плавления большинства его руд (таких, как бокситы).
Прямое восстановление углеродом применяться не может, потому что восстановительная способность алюминия выше, чем у углерода. Современный метод получения заключается в растворении оксида алюминия в расплаве криолита с последующим электролизом с использованием расходуемых коксовых или графитовых анодных электродов.
Б) В промышленности железо получают из железной руды, в основном из гематита () и магнетита ().
Существуют различные способы извлечения железа из руд. Наиболее распространённым является доменный процесс.
Первый этап производства — восстановление железа углеродом в доменной печи при температуре 2000 °C. В доменной печи углерод в виде кокса, железная руда в виде агломерата подаются сверху, а снизу их встречает поток нагнетаемого горячего воздуха.
В печи углерод в виде кокса окисляется до монооксида углерода. Данный оксид образуется при горении в недостатке кислорода. В свою очередь, монооксид углерода восстанавливает железо из руды.
Чтобы данная реакция шла быстрее, нагретый угарный газ пропускают через оксид железа (III).
В) Первым промышленным способом получения натрия была реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000 °C (способ Девилля). С появлением электроэнергетики более практичным стал другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия. В настоящее время электролиз — основной способ получения натрия.
Ответ: 5151.
Ответ: 5151
Раздел кодификатора ФИПИ: 4.2.2 Общие научные принципы химического производства. Химическое загрязнение окружающей среды и его последствия
Задания ЕГЭ по химии: Электролиз расплавов и растворов
Электролиз расплавов и растворов (солей, щелочей, кислот) 1. Установите соответствие между формулой соли и продуктом, образующемся на инертном аноде при электролизе ее водного раствора.
| ФОРМУЛА СОЛИ А) Na 3 PO 4 Б) NaNO 3 В) Al 2 (SO 4 ) 3 Г) AlBr 3 | ПРОДУКТ ЭЛЕКТРОЛИЗА НА АНОДЕ |
| 1) O 2 2) H 2 S 3) Br 2 4) HBr | 5) NO 2 6) SO 2 |
2. Установите соответствие между формулой соли и уравнением процесса, протекающего на аноде при электролизе ее водного раствора
| ФОРМУЛА СОЛИ А) Al(NO 3 ) 3 Б) CuCl 2 В) SbCl 3 Г) Cu(NO 3 ) 2 | СХЕМА АНОДНОГО ПРОЦЕССА |
| 1) 2H 2 O — 4е → O 2 + 4H + 2) 2H 2 O + 2е → H 2 + 2OH – 3) 2Cl – — 2е → Cl 2 | 4) Sb 3 + + 3е → Sb 0 5) Cl – + 4H 2 O — 8е → ClO 4 – + 8H + 6) 4NO 3 – — 4 е → 2N 2 O + 5O 2 |
3. Установите соответствие между формулой соли и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
| ФОРМУЛА СОЛИ А) CaI 2 Б) Na 2 CO 3 В) AgF Г) AuF 3 | ПРОДУКТ ЭЛЕКТРОЛИЗА НА КАТОДЕ |
| 1) Кальций 2) натрий 3) серебро 4) золото | 5) водород 6) фтор |
4. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на катоде.
| ФОРМУЛА ВЕЩЕСТВА А) AlCl 3 Б) RbOH В) Hg(NO 3 ) 2 Г) AuCl 3 | ПРОДУКТЫ НА КАТОДЕ |
| 1) золото 2) алюминий 3) кислород 4) рубидий | 5) водород 6) ртуть |
5. Установите соответствие между формулой соли и продуктом, образующимся на катоде при электролизе ее водного раствора.
| ФОРМУЛА СОЛИ А) CuCl 2 Б) AgNO 3 В) K 2 S Г) NaBr | ПРОДУКТ НА КАТОДЕ |
| 1) водород 2) кислород 3) металл 4) галоген | 5) сера 6) азот |
6. Установите соответствие между формулой вещества и продуктом, образующемся на инертном аноде при электролизе его водного раствора.
| ФОРМУЛА ВЕЩЕСТВА А) NiSO 4 Б) NiCl 2 В) NiF 2 Г) K 2 S | ПРОДУКТ НА АНОДЕ |
| 1) Cl 2 2) O 2 3) H 2 4) S | 5) SO 2 6) HF |
7. Установите соответствие между формулой соли и продуктом, образующемся на инертном аноде при электролизе ее водного раствора.
| ФОРМУЛА СОЛИ А) Cu(NO 3 ) 2 Б) Na 2 S В) AlCl 3 Г) ZnSO 4 | ПРОДУКТ ЭЛЕКТРОЛИЗА НА АНОДЕ |
| 1) водород 2) кислород 3) металл 4) хлор | 5) сера 6) азот |
8. Установите соответствие между металлом и способом его электролитического получения.
| МЕТАЛЛ А) литий Б) натрий В) медь Г) свинец | ЭЛЕКТРОЛИЗ 1) Расплавленного нитрата 2) Водного раствора гидроксида 3) Расплава хлорида 4) Расплавленного оксида 5) Раствора оксида в расплавленном криолите 6) Водного раствора солей |
9. Установите соответствие между формулой соли и продуктом, образующемся на инертном аноде при электролизе ее водного раствора.
| ФОРМУЛА СОЛИ А) Hg(NO 3 ) 2 Б) MgCl 2 В) Na 2 S Г) CuSO 4 | ПРОДУКТ ЭЛЕКТРОЛИЗА НА АНОДЕ |
| 1) азот 2) сера 3) водород 4) кислород | 5) металл 6) галоген |
10. Установите соответствие между формулой вещества и уравнением процесса, протекающего на аноде при электролизе его водного раствора
| ФОРМУЛА СОЛИ А) Сu(NO 3 ) 2 Б) NaI В) NaOH Г) H 2 SO 4 | СХЕМА АНОДНОГО ПРОЦЕССА |
| 1) 2H 2 O — 4 е → O 2 + 4H + 2) 4OH – — 4е → O 2 + 2H 2 O 3) 2SO 4 2- -4 е → 2SO 3 + O 2 | 4) 2I — — 2е → I 2 5) 2NO 3 – — 2е → 2NO 2 + O 2 6) 2H + + 2е → H 2 |
11. Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) K 2 CO 3 Б) AgNO 3 В) ZnCl 2 Г) NaHC 2 O 4 | КАТОДНЫЙ ПРОДУКТ |
| 1) Кислород 2) Только металл 3) Только водород 4) Металл и водород | 5) Азот 6) Хлор |
12. Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) NaNO 3 Б) Cu(NO 3 ) 2 В) PbHCO 3 Г) SnCl 2 | КАТОДНЫЙ ПРОДУКТ |
| 1) Кислород 2) Только металл 3) Только водород 4) Металл и водород | 5) Азот 6) Хлор |
13. Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) K 2 CO 3 Б) AgNO 3 В) ZnCl 2 Г) NaHC 2 O 4 | АНОДНЫЙ ПРОДУКТ |
| 1) Кислород 2) Металл 3) Водород 4) Азот | 5) Углекислый газ 6) Хлор |
14. Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) NaF Б) Hg(NO 3 ) 2 В) FeCl 2 Г) KHSO 4 | АНОДНЫЙ ПРОДУКТ |
| 1) Кислород 2) Металл 3) Водород 4) Сера | 5) Фтор 6) Хлор |
15. Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) KF Б) K 2 CO 3 В) CuCl 2 Г) KHSO 4 | АНОДНЫЙ ПРОДУКТ 1) Кислород 2) Галоген 3) Водород 4) Сера |
16. Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) Na 2 HPO 4 Б) SnCl 2 В) BeF 2 Г) SnBr 4 | АНОДНЫЙ ПРОДУКТ 1) Кислород 2) Галоген 3) Водород 4) Фосфор |
17. Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) Na 2 HPO 4 Б) BaCl 2 В) Al 2 (SO 4 ) 3 Г) Cu(ClO 3 ) 2 | КАТОДНЫЙ ПРОДУКТ |
| 1) натрий 2) барий 3) алюминий 4) медь | 5) Водород 6) кислород |
18. Установите соответствие между названием металла и электролитическим способом его получения.
| МЕТАЛЛ А) калий Б) медь В) хром Г) кальций | СПОСОБ ПОЛУЧЕНИЯ 1) электролиз водного раствора сульфата 2) электролиз расплавленного хлорида 3) электролиз расплавленного нитрата 4) электролиз водного раствора гидроксида |
19. Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
| ФОРМУЛА ВЕЩЕСТВА А) KI Б) AgF В) FeCl 2 Г) KHCO 3 | АНОДНЫЙ ПРОДУКТ |
| 1) Кислород 2) Металл 3) Йод 4) Фтор | 5) Углекислый газ 6) Хлор |
20. Установите соответствие между названием металла и промышленным электролитическим спосом его получения.
| МЕТАЛЛ А) кальций Б) серебро В) натрий Г) свинец | СПОСОБ ПОЛУЧЕНИЯ 1) электролиз водного раствора хлорида 2) электролиз водного раствора нитрата 3) электролиз расплавленного нитрата 4) электролиз расплавленного хлорида |
21. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора
| ФОРМУЛА ВЕЩЕСТВА А) AgNO 3 Б) NaNO 3 В) Ni(NO 3 ) 2 Г) KF | ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА |
| 1) Ag, N 2 2) Ag, O 2 3) H 2 , O 2 4) Ni, H 2 , O 2 HNO 3 | 5) H 2 , NO 2 , O 2 6) NaOH, H 2 , F 2 |
22. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора, выделяющимися на аноде
| ФОРМУЛА ВЕЩЕСТВА А) KF Б) CaBr 2 В) Na 3 PO 4 Г) AgNO 3 | ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА |
| 1) Ag 2) O 2 3) H 2 4) Br 2 | 5) NO 2 6) F 2 |
23. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора, выделяющимся на катоде
| ФОРМУЛА ВЕЩЕСТВА А) Cu(NO 3 ) 2 Б) Na 2 SO 4 В) AlCl 3 Г) AuCl 3 | ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА |
| 1) Cu 2) Na 3) H 2 4) O 2 | 5) Au 6) Al |
24. Установите соответствие между формулой вещества и схемой катодного процесса, протекающего при электролизе его водного раствора
| НАЗВАНИЕ ВЕЩЕСТВА А) сульфат натрия Б) бромид золота(III) В) бромид бария Г) серная кислота | СХЕМА КАТОДНОГО ПРОЦЕССА |
| 1) Na + + 1е → Na 0 2) 2H 2 O — 4е → O 2 + 4H + 3) 2H 2 O + 2е→ H 2 + 2OH – 4) 2Br – — 2е → Вr 2 | 5) 2H + + 2е → H 2 6) Au 3+ + 3е → Au 0 7) Ba 2+ + 2е→ Ba 0 |
25. Установите соответствие между формулой вещества и схемой анодного процесса, протекающего при электролизе его водного раствора
| НАЗВАНИЕ ВЕЩЕСТВА А) карбонат калия Б) хлорид калия В) гидроксид калия Г) хлорид меди (II) | СХЕМА АНОДНОГО ПРОЦЕССА |
| 1) K + + 1e → K 0 2) 2H 2 O — 4e → O 2 + 4H + 3) 2H 2 O + 2e → H 2 + 2OH – 4) 2Cl – — 2e→ Cl 2 | 5) 2H + + 2e → H 2 6) 4OH – — 4e → O 2 + 2H 2 O 7) Cu 2+ + 2e→ Cu 0 |
26. Установите соответствие между формулой вещества и газообразными продуктами электролиза его водного раствора
| ФОРМУЛА ВЕЩЕСТВА А) СuF 2 Б) CuCl 2 В) NaClO 4 Г) CuSO 4 | ГАЗООБРАЗНЫЕ ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО Р-РА |
| 1) водород 2) кислород 3) водород и кислород 4) фтор | 5) фтор и водород 6) хлор 7) хлор и водород |
27. Установите соответствие между названием вещества и газообразными продуктами электролиза его водного раствора
| НАЗВАНИЕ ВЕЩЕСТВА А) хлорат калия Б) фторид калия В) нитрат меди (II) Г) сульфат калия | ГАЗООБРАЗНЫЕ ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО Р-РА |
| 1) Хлор и водород 2) Хлор 3) Фтор и водород 4) Фтор | 5) Водород 6) Кислород 7) Водород и кислород |
28. Установите соответствие между формулой вещества и газообразными продуктами электролиза его водного раствора, выделяющимися на аноде
| ФОРМУЛА ВЕЩЕСТВА А) HgCl 2 Б) CaCl 2 В) NaNO 3 Г) CuSO 4 | ГАЗООБРАЗНЫЕ ПРОДУКТЫ НА АНОДЕ |
| 1) Хлор и водород 2) Хлор 3) Азот и водород 4) Оксид серы (IV) | 5) Водород 6) Кислород 7) Водород и кислород |
29. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора, образующимся на катоде
| ФОРМУЛА ВЕЩЕСТВА А) LiNO 3 Б) Ba(OH) 2 В) AlCl 3 Г) HgCl 2 | КАТОДНЫЙ ПРОДУКТ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА |
| 1) H 2 2) O 2 3) Cl 2 4) Li | 5) Ba 6) Al 7) Hg |
Продукт, выделяющийся на катоде , зависит от положения катиона в ЭХРН: 1) До алюминия включительно — выделяется водород, т.к катионы активных металлов не восстанавливаются.
|