- Свойства цезия
- Цезий и лечение рака
- Сравнение цезия и франция
- Сравнения цезия и лития
- Активные металлы — список в химии, таблица, реакции и ряд — Природа Мира
- Подведение итогов
- Электрохимический ряд активности металлов | это… Что такое Электрохимический ряд активности металлов?
- История
- Теоретические основы
- Практическое использование ряда напряжений
- Таблица электрохимических потенциалов металлов
- Ссылки
- Литература
- Примечания
- Активные металлы – список в химии, таблица ряда
- Положение в таблице Менделеева
- Литий
- Свойства
- История открытия
- Что мы узнали?
- Каким способом был открыт цезий?
- Сравнение самых активных металлов
- Тест по теме
- Получение в России
- Применение
- Металл франций
- Использование цезия

Наиболее активными металлами являются элементы I и II групп, находящиеся с левой стороны периодической таблицы Менделеева. Металл считается активным, когда он сильно и быстро реагирует с другими элементами.Реакционная способность металла возрастает по мере того, как мы переходим от верхней к нижней части периодической таблицы.
Исключением является водород, который не считается металлом и размещен в верхнем левом углу периодической системы химических элементов Менделеева.
Самые активные металлы в мире 
По реакционной способности металлических элементов, перечисленных в периодической таблице химических элементов, они подразделяются на три группы:
- Активные металлы.
- Средней активности металлы.
- Малоактивные металлы.
Наиболее активные металлы на Земле — литий, цезий и франций.
Цезий — самым активный из нерадиоактивных элементов. Это редкий серебристо-желтый блестящий металл с атомным числом (число протонов в ядре) 55. Это очень мягкий элемент, который будет таять в ваших руках — если не взорвется раньше, так как он сильно реагирует на влагу.
 Caesium (Cs), номер – 55, атомная масса – 132,905
Caesium (Cs), номер – 55, атомная масса – 132,905
Существует также очень радиоактивный элемент, франций, который может быть более активным, чем цезий. Или не может, мы, вероятно, никогда этого не узнаем, потому что франций не только крайне радиоактивный, но и крайне редкий металл.
Последний из тройки наиболее активных металлов — литий — обладает интересным свойством. Он придает малиновый цвет языкам пламени.
- Вот видео-демонстрация активности лития, натрия, калия, рубидия и цезия.
- Что такое цезий
Цезий относится к щелочным металлам. Они очень реакционноспособны, и не встречаются свободно в природе. Эти металлы также очень пластичные, они хорошие тепловые и электрические проводники.
Цезий был первым элементом, который можно было обнаружить со спектроскопом. В 1860 году его открыли немецкие химики Роберт Бунзен и Густав Кирхгоф, когда анализировали спектр минеральной воды из Бад-Дюркхаймского источника.
Цезий встречается естественным образом в минералах поллуцита и лепидолита. Также он содержится во многих алюмосиликатах, таких как берилл, петалит и карналлит.
Самое богатое из известных месторождений цезия находится в Канаде, на берегу озера Берник-Лейк. Там сосредоточено около 70% всех земных запасов.
Любопытно, что это озеро является местом проведения ежегодного фестиваля цезия (24 февраля), когда в снегу сжигаются тонны этого вещества, и преобладает другое цезиевое безумие.
А еще цезий является побочным продуктом ядерного деления в реакторах.
Свойства цезия
Пусть цезий и не самый тяжелый металл в мире, зато он самый активный и обладает рядом уникальных свойств:
- Он спонтанно горит на воздухе и моментально взрывается при контакте с водой или влагой в любой форме, даже со льдом до -116 С.
- Он горит блестящим голубым пламенем. Непосвященным пламя кажется пурпурным, а не синим, однако после достаточной медитации, изучения трудов по химии и блаженных часов, проведенных в благоговении перед тем, как горит цезий, раскрывается истинная синяя природа его пламени
- Название «цезий» происходит от двух ярко-синих линий в его эмиссионном спектре. В переводе с латинского «caesius» означает «небесно-синий».
- Его гидроксид (жидкое расплавленное состояние) способен проесть плоть, стекло и многие другие вещества. Лишь металл родий и ряд его сплавов способны противостоять расплаву гидроксида цезия.
- Иодид и бромид цезия используются в качестве центральных компонентов при производстве высокоточной оптики, в том числе прицелов, очков и биноклей ночного видения. Цезий также экспериментально использовался в ионных силовых установках для космических аппаратов, из-за его низкого потенциала ионизации.
- Цезий используется при создании самых точных атомных часов. Даже лучшие наручные часы в мире могут отставать на несколько секунд или даже минуту. А вот атомные часы на основе цезия теряют всего одну секунду в пять миллиардов лет.
- Природный цезий состоит из одного стабильного изотопа, Cs 133. Известно 30 других радиоактивных изотопов, заполняющих диапазон от Cs 114 до Cs 145. Цезий-137 (он же радиоцезий) является одним из наиболее биологически опасных компонентов радиоактивных отходов и ядерных осадков. Он накапливается в живых организмах и даже в грибах, а самое высокое его содержание обнаружено в у северных оленей и водоплавающих птиц в Северной Америке.
Люди и животные постоянно подвергаются воздействию минимального количеств цезия при еде, дыхании и питье. Хотя маловероятно, что мы будем болеть только из-за цезия, его длительное воздействие может привести к неблагоприятным последствиям для здоровья, включая тошноту, рвоту, кровотечение и повреждение клеток.
Цезий и лечение рака
Еще Парацельс утверждал, что все есть яд, и все есть лекарство. Дело лишь в дозировке. И когда речь заходит о цезии, то слова Парацельса абсолютно верны.
В настоящее время исследуется эффективность цезия для лечения нескольких форм рака, включая опухоли головного мозга. Цезий-131, радиоактивный изотоп цезия, вместе с другим радиоактивным изотопом (йодом-125) помещают в брахитерапевтическую капсулу («семя»).
По данным Американского общества брахитерапии, брахитерапевтическая капсула является радиоактивным «стручком», который помещается непосредственно в раковую ткань. Такие семена эффективны при нескольких формах рака, включая рак простаты, шейки матки и эндометрия.
В одном из исследований группе из 24 пациентов с опухолями головного мозга были имплантированы в опухоль брахиотерапевтические семена с цезием-131. Были отмечены минимальные побочные эффекты, но в целом пациенты хорошо перенесли эту форму лечения.
Идея использования семян брахитерапии с цезием-131 в качестве лечения рака возникла еще в 1960-х годах и была описана в исследовании, опубликованном в журнале « Радиология». В исследовании, опубликованном в журнале Medical Physics, в 2009 году обсуждалось использование семян цезия-131 для лечения рака предстательной железы с положительными результатами.
Необходимо больше исследований, прежде чем лечение цезием прочно займет свое место в медицине. Однако пока что исследования доказывают, что использование цезия-131 для лечения раковых опухолей при помощи брахиотерапии является обнадеживающим.
Сравнение цезия и франция
 Francium (Fr), номер – 87, атомная масса – 223
Francium (Fr), номер – 87, атомная масса – 223
Как и цезий, франций (Fr) относится к щелочным металлам (только радиоактивным) и обладает крайне высокой химической активностью.
- Плотность франция составляет 1,87 грамма на кубический сантиметр, что сопоставимо с плотностью цезия — 1,879 грамма на кубический сантиметр.
- Цезий и франций — два из четырех металлов, которые становятся жидкими при комнатной температуре. Таким же свойством обладают ртуть и галлий.
- Взаимодействие цезия с водой происходит весьма эффектно — со взрывом, образованием гидроксида CsOH и водорода H2. Франций и вода тоже не особо «любят» друг друга, и при их взаимодействии образуется самая сильная щелочь — гидроксид франция.
- Как и цезий, франций накапливается в живых организмах. Поэтому изотопы данного металла нашли свое применение в медицине, для диагностики рака и различных биологических исследований.
- А вот по распространенности цезий далеко опережает франций. Ежегодно в мире добывается около 20 тонн обогащённой руды цезия. По данным PeriodicTable, цезий является 50-м наиболее распространенным элементом земной коры. Франция же во всей земной коре насчитывается около 340 грамм.
То есть по своим свойствам два самых активных металла на планете очень схожи.
Сравнения цезия и лития
 Lithium (Li), номер – 3, атомная масса – 6,94
Lithium (Li), номер – 3, атомная масса – 6,94
Литий входит в топ-3 самых активных металлов на планете. Это ключевой компонент в батареях, которые питают смартфоны, ноутбуки и электромобили. Более половины поставок лития в мире идет из «литиевого треугольника» — Боливии, Чили и Аргентины. Крупнейший источник по получению лития из соли — это чилийская пустыня Атакама.
- Подобно цезию, литий относится к щелочным металлам. И, как и цезий, встречается в природе только в виде соединений. При этом следы лития находятся почти во всех изверженных породах и во многих минеральных источниках. Это был один из трех элементов, созданных Большим взрывом, наряду с водородом и гелием.
- Лития и цезия в земной коре мало — 21 г / т и 3,7 г/т соответственно.
- Если цезий воспламеняется на воздухе, взаимодействуя с кислородом, то литий даже может некоторое время храниться на открытом воздухе. Благодаря подобной «терпимости» литий является единственным представителем щелочных металлов, не требующим хранения в керосине. Он тоже может передать «пламенный привет» при взаимодействии с кислородом, но лишь при высокой температуре.
- Литий -наименее плотный металл (0,533 г/см3). У цезия плотность намного больше — 1,879 грамма на кубический сантиметр. Легкость лития означает, что он может хранить энергию не добавляя тяжести различным устройствам.
- А вот по низкоплавкости литий дает фору цезию. Его температура плавления составляет 180,5 градуса Цельсия. А цезий плавится уже при 28,4 градуса Цельсия.
- Зато литий быстро закипает — при 134 градусах, а вот довести до кипения цезий непросто, необходима температура в 678 градусов.
- И литий и цезий легко режутся обычным ножом.
Илья Захаров. https://basetop.ru
Активные металлы — список в химии, таблица, реакции и ряд — Природа Мира
Среди всех металлов некоторые отличаются тем, что они очень легко вступают в восстановительные реакции. Такие металлы имеют много схожих свойств и объединяются в класс активных металлов.
К активным металлам относятся три группы элементов:
- щелочные металлы;
- щелочноземельные металлы;
- алюминий.
Щелочные металлы находятся в первой группе таблицы Менделеева, то есть занимают в ней крайнее левое положение. В частности щелочными металлами являются:
- литий (Li);
- натрий (Na);
- калий (K);
- рубидий (Rb);
- цезий (Cs);
- франций (Fr).
Щелочноземельные металлы находятся во второй группе, то есть правее щелочных металлов. К ним относятся:
- бериллий (Be);
- магний (Mg);
- кальций (Ca);
- стронций (Sr);
- барий (Ba);
- радий (Ra).
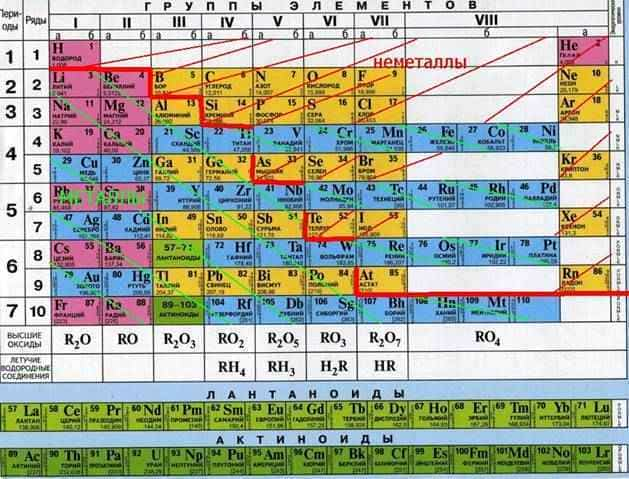 Активные металлы в таблице Менделеева
Активные металлы в таблице Менделеева
В целом активные металлы отличаются тем, что имеют один или два валентных электрона, поэтому они легко отдают эти электроны в ходе химических реакций, выступая в качестве восстановителей.
Степень активности металла можно оценить по его расположению в электрохимическом ряде активности металлов. Чем левее там находится металл, тем сильнее выражены его восстановительные свойства. Крайнее левое положение в ряде занимает литий.
В вот крайне правое положение в ряду занимает золото, именно поэтому оно почти не окисляется кислотами.
 Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов
Алюминий – это так называемый постпереходный металл, по своим свойствам он находится где-то между активными и среднеактивными металлами. Разные ученые придерживаются различного мнения о том, стоит ли считать алюминий активным металлом.
Активные металлы не встречаются в природе в чистом виде, так как они быстро вступают в химические реакции с другими элементами. Чаще всего в природе они присутствуют в виде оксидов. Например, даже если алюминий получен в чистом виде, то на воздухе он быстро покрывается оксидной пленкой.
Цвет всех щелочных металлов – белый, с серебристым оттенком. Исключением является цезий, имеющий серебристо-желтый цвет. Щелочные металлы можно резать простым скальпелем, так как у них низкая твердость. Также они имеют малую плотность – от 534 кг/м3 у лития до 1900 кг/м3 у цезия.
Литий, калий и натрий настолько легкие, что они плавают в воде, но построить корабль из них не получится, так как вода быстро окисляет и разрушает эти металлы.
Франций и цезий плавятся уже при комнатной температуре, а самый тугоплавкий щелочной металл – это литий, плавящийся при 180,6°С.
Для защиты щелочных металлов от воздуха и волы их хранят в керосине. При реагировании лития с водой выделяется водород, а натрий и особенно калий просто взрываются в воде. При взаимодействии с кислородом образуются оксиды.
Щелочноземельные металлы значительно тверже щелочных, их нельзя просто взять и разрежать ножом. Также они тяжелее – их плотность колеблется от 1550 кг/м3 у кальция до 5500 кг/м3 у радия. Цвет щелочноземельных металлов – серый. Температуры плавления этих элементов находятся в диапазоне 650-840°С. Исключение – бериллий, плавящийся лишь при 1278°С.
Чем больше порядковый номер щелочноземельного металла в таблице Менделеева, тем выше его химическая активность. Например, бериллий вообще не взаимодействует с кислородом и по своим свойствам напоминает алюминий. Наиболее активные стронций, барий и радий приходится хранить в керосине, также как и щелочные металлы.
Подведение итогов
Активные металлы отличаются тем, что имеют лишь один-два валентных электрона, которые они легко отдают. Поэтому эти элементы очень быстро вступают в химические реакции, а в природе в чистом виде не встречаются.
Не все нашли? Используйте поиск по сайту
Электрохимический ряд активности металлов | это… Что такое Электрохимический ряд активности металлов?
Электрохимический ряд активности (ряд напряжений, ряд стандартных электродных потенциалов) металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла Men+: Men+ + nē → Me
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительные реакциях в водных растворах.
История
Последовательность расположения металлов в порядке изменения их химической активности в общих чертах была известна уже алхимикам[1]. Процессы взаимного вытеснения металлов из растворов и их поверхностное осаждение (например, вытеснение серебра и меди из растворов их солей железом) рассматривались как проявление трансмутации элементов.
Поздние алхимики вплотную подошли к пониманию химической стороны взаимного осаждения металлов из их растворов.
Так, Ангелус Сала в работе «Anatomia Vitrioli» (1613) пришёл к выводу, что продукты химических реакций состоят из тех же «компонентов», которые содержались в исходных веществах.
Впоследствии Роберт Бойль предложил гипотезу о причинах, по которым один металл вытесняет другой из раствора на основе корпускулярных представлений[2].
В 1793 году Алессандро Вольта, конструируя гальванический элемент («Вольтов столб»), установил относительную активность известных тогда металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. «Сила» гальванического элемента оказывалась тем больше, чем дальше стояли друг от друга металлы в этом ряду («ряд напряжений»). Однако Вольта не связал этот ряд с химическими свойствами металлов.
В 1798 году Иоганн Вильгельм Риттер указал, что ряд Вольта эквивалентен ряду окисления металлов (т. е. последовательности уменьшения их сродства с кислородом). Таким образом, Риттер высказал гипотезу о возникновении электрического тока вследствие протекания химической реакции[3].
В эпоху становления классической химии способность элементов вытеснять друг друга из соединений стала важным аспектом понимания реакционной способности. Й. Берцелиус на основе электрохимической теории сродства построил классификацию элементов, разделив их на «металлоиды» (сейчас применяется термин «неметаллы») и «металлы» и поставив между ними водород.
Последовательность металлов по их способности вытеснять друг друга, давно известная химикам, была в 1860-е и последующие годы особенно основательно и всесторонне изучена и дополнена Н. Н. Бекетовым. Уже в 1859 году он сделал в Париже сообщение на тему «Исследование над явлениями вытеснения одних элементов другими».
В эту работу Бекетов включил целый ряд обобщений о зависимости между взаимным вытеснением элементов и их атомным весом, связывая эти процессы с «первоначальными химическими свойствами элементов – тем, что называется химическим сродством»[4].
Открытие Бекетовом вытеснения металлов из растворов их солей водородом под давлением и изучение восстановительной активности алюминия, магния и цинка при высоких температурах (металлотермия) позволило ему выдвинуть гипотезу о связи способности одних элементов вытеснять из соединений с их плотностью: более лёгкие простые вещества способны вытеснять более тяжёлые («вытеснительный ряд Бекетова»).
Не отрицая значительных заслуг Бекетова в становлении современных представлений об ряде активности металлов, следует считать ошибочным бытующее в отечественной популярной и учебной литературе представление о нём как единственном создателе этого ряда.[5][6].
Многочисленные экспериментальные данные, полученные в конце XIX века, опровергали гипотезу Бекетова. Так, Уильям Одлинг описал множество случаев «обращения активности».
Например, медь вытесняет олово из концентрированного подкисленного раствора SnCl2 и свинец — из кислого раствора PbCl2; она же способна к растворению в концентрированной соляной кислоте с выделением водорода.
Медь, олово и свинец находятся в ряду правее кадмия, однако могут вытеснять его из кипящего слабо подкисленного раствора CdCl2.
Бурное развитие теоретической и экспериментальной физической химии указывало на иную причину различий химической активности металлов. С развитием современных представлений электрохимии (главным образом в работах Вальтера Нернста) стало ясно, что эта последовательность соответствует «ряду напряжений» – расположению металлов по значению стандартных электродных потенциалов.
Таким образом, вместо качественной характеристики — «склонности» металла и его иона к тем или иным реакциям — Нерст ввёл точную количественную величину, характеризующую способность каждого металла переходить в раствор в виде ионов, а также восстанавливаться из ионов до металла на электроде, а соответствующий ряд получил название ряда стандартных электродных потенциалов.
Теоретические основы
Значения электрохимических потенциалов являются функцией многих переменных и поэтому обнаруживают сложную зависимость от положения металлов в периодической системе. Так, окислительный потенциал катионов растёт с увеличением энергии атомизации металла, с увеличением суммарного потенциала ионизации его атомов и с уменьшением энергии гидратации его катионов.
В самом общем виде ясно, что металлы, находящиеся в начале периодов характеризуются низкими значениями электрохимических потенциалов и занимают места в левой части ряда напряжений. При этом чередование (щелочных и щёлочноземельных металлов отражает явление диагонального сходства.
Металлы, расположенные ближе к серединам периодов, характеризуются большими значениями потенциалов и занимают места в правой половине ряда.
Последовательное увеличение электрохимического потенциала (от −3,395 В у пары Eu2+/Eu[источник не указан 228 дней] до +1,691 В у пары Au+/Au) отражает уменьшение восстановительной активности металлов (свойство отдавать электроны) и усиление окислительной способности их катионов (свойство присоединять электроны). Таким образом, самым сильным восстановителем является металлический европий, а самым сильным окислителем — катионы золота Au+.
В ряд напряжений традиционно включается водород, поскольку практическое измерение электрохимических потенциалов металлов производится с использованием стандартного водородного электрода.
Практическое использование ряда напряжений
Ряд напряжений используется на практике для сравнительной оценки химической активности металлов в реакциях с водными растворами солей и кислот и для оценки катодных и анодных процессов при электролизе:
- Металлы, стоящие левее, являются более сильными восстановителями, чем металлы, расположенные правее: они вытесняют последние из растворов солей. Например, взаимодействие Zn + Cu2+ → Zn2+ + Cu возможно только в прямом направлении.
- Металлы, стоящие в ряду левее водорода, вытесняют водород при взаимодействии с водными растворами кислот-неокислителей; наиболее активные металлы (до алюминия включительно) — и при взаимодействии с водой.
- Металлы, стоящие в ряду правее водорода, с водными растворами кислот-неокислителей при обычных условиях не взаимодействуют.
- При электролизе металлы, стоящие правее водорода, выделяются на катоде; восстановление металлов умеренной активности сопровождается выделением водорода; наиболее активные металлы (до алюминия) невозможно при обычных условиях выделить из водных растворов солей.
Таблица электрохимических потенциалов металлов
| Li | Li+ | -3,0401 | реагирует с водой | выделяется водород |
| Cs | Cs+ | -3,026 | ||
| Rb | Rb+ | -2,98 | ||
| K | K+ | -2,931 | ||
| Ra | Ra2+ | -2,912 | ||
| Ba | Ba2+ | -2,905 | ||
| Fr | Fr+ | -2,92 | ||
| Sr | Sr2+ | -2,899 | ||
| Ca | Ca2+ | -2,868 | ||
| Eu | Eu2+ | -2,812 | ||
| Na | Na+ | -2,71 | ||
| Sm | Sm2+ | -2,68 | ||
| Md | Md2+ | -2,40 | реагирует с кислотами | |
| La | La3+ | -2,379 | ||
| Y | Y3+ | -2,372 | ||
| Mg | Mg2+ | -2,372 | ||
| Ce | Ce3+ | -2,336 | ||
| Pr | Pr3+ | -2,353 | ||
| Er | Er3+ | -2,331 | ||
| Ho | Ho3+ | -2,33 | ||
| Nd | Nd3+ | -2,323 | ||
| Tm | Tm3+ | -2,319 | ||
| Sm | Sm3+ | -2,304 | ||
| Pm | Pm3+ | -2,30 | ||
| Fm | Fm2+ | -2,30 | ||
| Dy | Dy3+ | -2,295 | ||
| Tb | Tb3+ | -2,28 | ||
| Lu | Lu3+ | -2,28 | ||
| Gd | Gd3+ | -2,279 | ||
| Es | Es2+ | -2,23 | ||
| Ac | Ac3+ | -2,20 | ||
| Dy | Dy2+ | -2,2 | ||
| Pm | Pm2+ | -2,2 | ||
| Cf | Cf2+ | -2,12 | ||
| Sc | Sc3+ | -2,077 | ||
| Am | Am3+ | -2,048 | ||
| Cm | Cm3+ | -2,04 | ||
| Pu | Pu3+ | -2,031 | ||
| Er | Er2+ | -2,0 | ||
| Pr | Pr2+ | -2,0 | ||
| Eu | Eu3+ | -1,991 | ||
| Lr | Lr3+ | -1,96 | ||
| Cf | Cf3+ | -1,94 | ||
| Es | Es3+ | -1,91 | ||
| Th | Th4+ | -1,899 | ||
| Fm | Fm3+ | -1,89 | ||
| Np | Np3+ | -1,856 | ||
| Be | Be2+ | -1,847 | ||
| U | U3+ | -1,798 | ||
| Al | Al3+ | -1,700 | ||
| Md | Md3+ | -1,65 | ||
| Ti | Ti2+ | -1,63 | конкурирующие реакции: и выделение водорода, и выделение металла в чистом виде | |
| Hf | Hf4+ | -1,55 | ||
| Zr | Zr4+ | -1,53 | ||
| Pa | Pa3+ | -1,34 | ||
| Ti | Ti3+ | -1,208 | ||
| Yb | Yb3+ | -1,205 | ||
| No | No3+ | -1,20 | ||
| Ti | Ti4+ | -1,19 | ||
| Mn | Mn2+ | -1,185 | ||
| V | V2+ | -1,175 | ||
| Nb | Nb3+ | -1,1 | ||
| Nb | Nb5+ | -0,96 | ||
| V | V3+ | -0,87 | ||
| Cr | Cr2+ | -0,852 | ||
| Zn | Zn2+ | -0,763 | ||
| Cr | Cr3+ | -0,74 | ||
| Ga | Ga3+ | -0,560 | ||
| Ga | Ga2+ | -0,45 | ||
| Fe | Fe2+ | -0,441 | ||
| Cd | Cd2+ | -0,404 | ||
| In | In3+ | -0,3382 | ||
| Tl | Tl+ | -0,338 | ||
| Co | Co2+ | -0,28 | ||
| In | In+ | -0,25 | ||
| Ni | Ni2+ | -0,234 | ||
| Mo | Mo3+ | -0,2 | ||
| Sn | Sn2+ | -0,141 | ||
| Pb | Pb2+ | -0,126 | ||
| H2 | H+ | |||
| W | W3+ | +0,11 | низкая реакционная способность | выделение металла в чистом виде |
| Ge | Ge4+ | +0,124 | ||
| Sb | Sb3+ | +0,240 | ||
| Ge | Ge2+ | +0,24 | ||
| Re | Re3+ | +0,300 | ||
| Bi | Bi3+ | +0,317 | ||
| Cu | Cu2+ | +0,338 | ||
| Po | Po2+ | +0,37 | ||
| Тс | Тс2+ | +0,400 | ||
| Ru | Ru2+ | +0,455 | ||
| Cu | Cu+ | +0,522 | ||
| Te | Te4+ | +0,568 | ||
| Rh | Rh+ | +0,600 | ||
| W | W6+ | +0,68 | ||
| Tl | Tl3+ | +0,718 | ||
| Rh | Rh3+ | +0,758 | ||
| Po | Po4+ | +0,76 | ||
| Hg | Hg22+ | +0,7973 | ||
| Ag | Ag+ | +0,799 | ||
| Pb | Pb4+ | +0,80 | ||
| Os | Os2+ | +0,850 | ||
| Hg | Hg2+ | +0,851 | ||
| Pt | Pt2+ | +0,963 | ||
| Pd | Pd2+ | +0,98 | ||
| Ir | Ir3+ | +1,156 | ||
| Au | Au3+ | +1,498 | ||
| Au | Au+ | +1,691 |
Ссылки
Литература
- Корольков Д.В. Основы неорганической химии. — М.:Просвещение, 1982. — 271 с.
Примечания
- ↑ Рабинович В. Л. Алхимия как феномен средневековой культуры. — М.: Наука, 1979
- ↑ Пути познания / Головнер В.Н. Взгляд на мир глазами химика
- ↑ Штрубе В. Пути развития химии: в 2-х томах. Том 2. От начала промышленной революции до первой четверти XX века
- ↑ Беляев А.И. Николай Николаевич Бекетов – выдающийся русский физико-химик и металлург. М., 1953
- ↑ Леенсон И. А. Ряд активности металлов Бекетова: миф или реальность? // Химия в школе. — 2002. — № 9. — С. 90-96.
- ↑ Мчедлов-Петросян Н. О.Труды Н. Н. Бекетова и ряд активности металлов // Вестник Харьковского национального университета. — 2003. — № 596. — Химия. Вып. 10 (33). — С. 221-225.
Активные металлы – список в химии, таблица ряда
- 4.4
- Средняя оценка: 4.4
- Всего получено оценок: 882.
- 4.4
Кузнечный горн своими руками, как сделать горн для ковки
Средняя оценка: 4.4
Всего получено оценок: 882.
Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Положение в таблице Менделеева
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
Рис. 1. Активные металлы в таблице Менделеева.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.
Рис. 2. Электрохимический ряд напряжений металлов.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Литий
При внесении уточнений и рассмотрения наиболее электрохимически активного элемента становится очевидно, что лидирующее положение в плане активности займет литий. Название данного элемента переводится как «камень» – связано это с тем, что он был обнаружен в петалите (минерал).
Металл, обладающий серебристым цветом, тонет в воде, но уверенно держится на поверхности керосина. По электрохимической активности данный элемент превосходит все остальные щелочные элементы, вытесняя другие металлы при химических реакциях.
Это главное свойство лития является определяющим для остальных его характеристик.
Литий является очень важным элементом для нормального функционирования всего организма человека, но необходим он в маленьких дозах. При повышенной концентрации лития в организме человека может произойти отравление, пониженное же его содержание может привести к психической нестабильности человека.
В некоторых напитках литий даже позиционировался, как превосходное средство от похмельного синдрома.
Возможно, это не лишено смысла, и литий действительно помогает справиться с недомоганием после принятия спиртных напитков, однако употреблять его в повышенных дозах не рекомендуется в силу вышеуказанных причин.
Свойства
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
| Реакция | Уравнение | Исключение |
| Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом | K + O2 → KO2 | Литий реагирует с кислородом только при высокой температуре |
| Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются | 2Ca + O2 → 2CaO | |
| Реагируют с простыми веществами, образуя соли | – Ca + Br2 → CaBr2; – 2Al + 3S → Al2S3 | Алюминий не вступает в реакцию с водородом |
| Бурно реагируют с водой, образуя щёлочи и водород | – 2Na + 2H2O → 2NaOH + H2; – Ca + 2H2O → Ca(OH)2 + H2 | Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки |
| Реагируют с кислотами, образуя соли | – Ca + 2HCl → CaCl2 + H2;– 2K + 2HMnO4 → 2KMnO4 + H2 | |
| Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью | 2Na + CuCl2 + 2H2O:– 2Na + 2H2O → 2NaOH + H2; – 2NaOH + CuCl2 → Cu(OH)2↓ + 2NaCl |
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.
Рис. 3. Минералы и чистые металлы.
История открытия
Его открытие принадлежит немецким исследователям Р. Бунзену и Г. Кирхгофу. Уже тогда ученые интересовались, какие металлы активные, а какие – нет. В 1860 году исследователи изучали состав воды из Дюркгеймского водохранилища. Делали они это при помощи спектрального анализа. В образце воды ученые обнаружили такие элементы, как стронций, магний, литий, кальций.
Затем они решили проанализировать каплю воды при помощи спектроскопа. Тогда они и увидели две ярко-голубые линии, находящиеся недалеко друг от друга. Одна из них по своему положению практически совпадала с линией металла стронция. Ученые решили, что выявленное ими вещество является неизвестным и отнесли его к группе щелочных металлов.
В том же году Бунзен написал письмо своему коллеге-фотохимику Г. Роско, в котором рассказывал об этом открытии. А официально о цезии было сообщено 10 мая 1860 года на заседании ученых Берлинской академии.
Через шесть месяцев Бунзен смог выделить около 50 граммов хлороплатинита цезия. Ученые переработали 300 тонн минеральной воды и выделили порядка 1 кг хлорида лития в качестве побочного продукта, чтобы в конечном счете получить самый активный металл.
Это говорит о том, что цезия в минеральных водах содержится очень мало.
Сложность получения цезия постоянно толкает ученых на поиск содержащих его минералов, одним из которых является поллуцит. Но извлечение цезия из руд всегда оказывается неполным, в процессе эксплуатации цезий очень быстро рассеивается.
Это делает его одним из самых труднодоступных веществ в металлургии. В земной коре, к примеру, содержится 3,7 граммов цезия на одну тонну. А в одном литре морской воды лишь 0,5 мкг вещества представляют собой самый активный металл.
Это приводит к тому, что извлечение цезия является одним из самых трудоемких процессов.
Что мы узнали?
К активным металлам относятся элементы I и II групп – щелочные и щелочноземельные металлы, а также алюминий. Их активность обусловлена строением атома – немногочисленные электроны легко отделяются от внешнего энергетического уровня.
Это мягкие лёгкие металлы, быстро вступающие в реакцию с простыми и сложными веществами, образуя оксиды, гидроксиды, соли.
Алюминий находится ближе к водороду и для его реакции с веществами требуются дополнительные условия – высокие температуры, разрушение оксидной плёнки.
Каким способом был открыт цезий?
Самый активный металл был первым химическим элементом, наличие которого в поверхности земной коры было обнаружено при помощи метода спектрального анализа. Когда ученые получили спектр металла, то в нем они увидели две линии небесно-голубого цвета. Таким образом и получил свое название этот элемент. Слово caesius в переводе с латинского языка значит «небесно-голубой».
Сравнение самых активных металлов
Унуненний – это пока еще не открытый металл. Он будет занимать первое место в восьмой строке периодической системы.
Разработка и исследования этого элемента проводятся в России в Объединенном институте ядерных исследований. Этот металл должен будет обладать также очень высокой активностью.
Если же сравнивать уже известные франций и цезий, то самым высоким потенциалом ионизации – 380 кДж/моль – будет обладать франций.
Воронение Силумина. Оптимальное решение.
У цезия этот показатель составляет 375 кДж/моль. Но реагирует франций все же не так быстро, как цезий.
Таким образом, цезий – самый активный металл.
Это – ответ (химия чаще всего является тем предметом, в программе которого можно встретить подобный вопрос), который может быть полезным как на уроке в школе, так и в профессионально-техническом училище.
Тест по теме
- /10 Вопрос 1 из 10
Начать тест
Доска почёта
Чтобы попасть сюда — пройдите тест.
- Александр Котков10/10
- Лидия Маслова10/10
- Анна Богданова10/10
- Сергей Ефремов7/10
Получение в России
Как было указано, главным минералом, из которого получают цезий, является поллуцит. А также этот наиболее активный металл можно получить из редкого авогадрита. В промышленности используется именно поллуцит. Добыча его после распада Советского Союза в России не велась, несмотря на то что еще в те времена были обнаружены гигантские запасы цезия в Вороньей тундре под Мурманском.
К тому моменту, когда отечественная промышленность смогла позволить себе добычу цезия, лицензия на разработку этого месторождения была приобретена компанией из Канады. Сейчас извлечение цезия производит новосибирская .
Применение
Общие химические свойства металлов используются для создания сплавов, моющих средств, применяются в каталитических реакциях. Металлы присутствуют в аккумуляторах, электронике, в несущих конструкциях.
Основные отрасли применения указаны в таблице.
| Отрасль | Производство | Металлы |
| Химическая промышленность | Катализаторы, соли, щёлочи | Pt, Fe, Ni, K |
| Пищевая промышленность | Поваренная соль (NaCl), сода (Na2CO3, NaHCO3) | Na, Ca, Ag |
| Металлургия | Сплавы, покрытия, детали разной формы, проволока, облицовка, строительные материалы и инструменты | Fe, Cr, Ni, W, Mo |
| Приборостроение | Микросхемы, фотоэлементы, датчики | Cs, Co, Ni, Cu |
| Ювелирная промышленность | Украшения | Au, Pt, Ag |
| Медицина | Протезы | Ti, Ni, Au |
Рис. 3. Висмут.
Металл франций
Еще одним из металлов с самыми интенсивными свойствами является франций. Он получил свое название в честь родины первооткрывательницы металла. М. Пере, родившаяся во Франции, открыла новый химический элемент в 1939 году. Он принадлежит к числу таких элементов, о которых даже сами исследователи-химики затрудняются делать какие-либо выводы.
Франций является самым тяжелым металлом. При этом и самый активный металл – это франций, наряду с цезием. Этим редким сочетанием – высокой химической активностью и низкой ядерной устойчивостью и обладает франций.
У его самого долгоживущего изотопа период полураспада составляет всего лишь 22 минуты. Франций используется для обнаружения другого элемента – актиния. А также соли франция раньше предлагалось применять для обнаружения раковых опухолей.
Однако из-за высокой стоимости эту соль невыгодно производить.
Использование цезия
Этот металл используется для изготовления различных фотоэлементов. А также соединения цезия применяются в специальных отраслях оптики – в изготовлении инфракрасных приборов, биноклей ночного видения. Цезий используют в изготовлении прицелов, которые позволяют заметить технику и живую силу врага. Также его применяют для изготовления особых металлогалогенных ламп.
Но этим не исчерпывается круг его применения. На основе цезия был создан также ряд медицинских препаратов. Это лекарства для лечения дифтерии, язвенных болезней, шоков и шизофрении. Как и соли лития, соли цезия обладают нормотимическими свойствами – или, попросту, способны стабилизировать эмоциональный фон.
( 2 оценки, среднее 4 из 5 )






