- Электронная конфигурация атома
- Правила заполнения электронных орбиталей и примеры
- Внешний уровень и валентные электроны
- Тренировка
- Провал электрона
- Основное и возбужденное состояние атома
- Положение металлов в ПС, особенности строения их атомов, физические свойства
- Строение металлов
- Строение электронных оболочек атомов
- Строение металлов и их особенности, схема и примеры
- Электронное строение металлов и их особенности
- Примеры решения задач
- Металлы
Мы приступаем к изучению химии — мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными формулами элементов.
Атом (греч. а — отриц. частица + tomos — отдел, греч. atomos — неделимый) — электронейтральная частица вещества микроскопических размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом
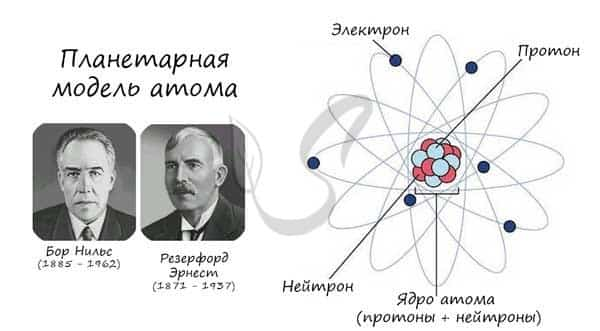
Протон (греч. protos — первый) — положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов элементов. Нейтрон (лат. neuter — ни тот, ни другой) — нейтральная (0) элементарная частица, присутствующая в ядрах всех химических элементов, кроме водорода.
Электрон (греч. elektron — янтарь) — стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома — порядковый номер в таблице Менделеева — равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Энергетические уровни подразделяются на несколько подуровней:
- Первый уровень
- Второй уровень
- Третий уровень
- Четвертый уровень
Состоит из s-подуровня: одной «1s» ячейки, в которой помещаются 2 электрона (заполненный электронами — 1s2)
Состоит из s-подуровня: одной «s» ячейки (2s2) и p-подуровня: трех «p» ячеек (2p6), на которых помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s2), p-подуровня: трех «p» ячеек (3p6) и d-подуровня: пяти «d» ячеек (3d10), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s2), p-подуровня: трех «p» ячеек (4p6), d-подуровня: пяти «d» ячеек (4d10) и f-подуровня: семи «f» ячеек (4f14), на которых помещается 14 электронов
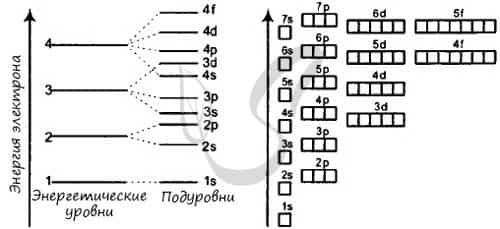
Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
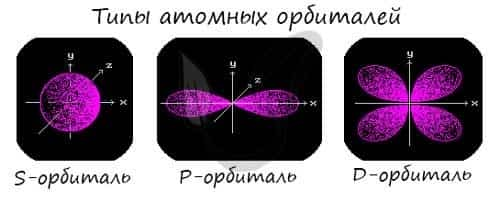
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный «рисунок».
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь — клеверный лист.
Правила заполнения электронных орбиталей и примеры
Существует ряд правил, которые применяют при составлении электронных конфигураций атомов:
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной «ячейке») не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются еще одним электроном с противоположным направлением
- Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе. Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода — 6, у серы — 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
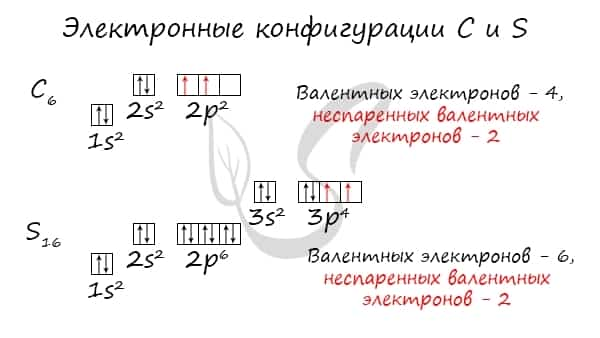
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
Таким образом, электронные конфигурации наших элементов:
- Углерод — 1s22s22p2
- Серы — 1s22s22p63s23p4
Внешний уровень и валентные электроны
Количество электронов на внешнем (валентном) уровне — это число электронов на наивысшем энергетическом уровне, которого достигает элемент. Такие электроны называются валентными: они могут быть спаренными или неспаренными. Иногда для наглядного представления конфигурацию внешнего уровня записывают отдельно:
- Углерод — 2s22p2 (4 валентных электрона)
- Сера -3s23p4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью — способностью атомов образовывать определенное число химических связей.
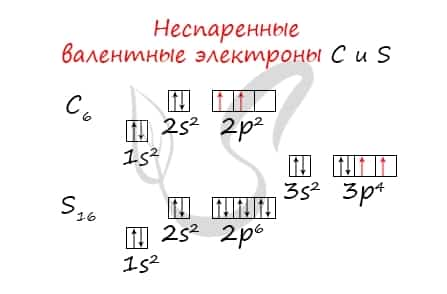
- Углерод — 2s22p2 (2 неспаренных валентных электрона)
- Сера -3s23p4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
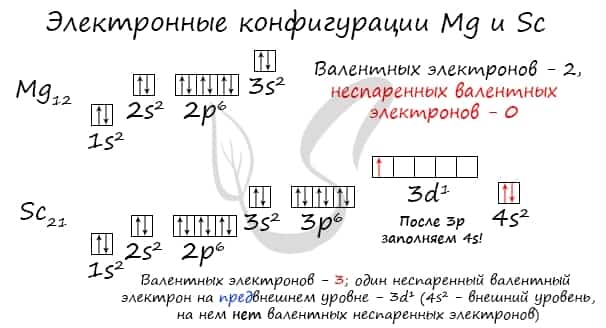
Запишем получившиеся электронные конфигурации магния и фтора:
- Магний — 1s22s22p63s2
- Скандий — 1s22s22p63s23p64s23d1
В целом несложная и интересная тема электронных конфигураций отягощена небольшим исключением — провалом электрона, которое только подтверждает общее правило: любая система стремится занять наименее энергозатратное состояние.
Провал электрона
Провалом электрона называют переход электрона с внешнего, более высокого энергетического уровня, на предвнешний, энергетически более низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций.
Подобное явление характерно лишь для некоторых элементов: медь, хром, серебро, золото, молибден. Для примера выберем хром, и рассмотрим две электронных конфигурации: первую «неправильную» (сделаем вид, будто мы не знаем про провал электрона) и вторую правильную, написанную с учетом провала электрона.
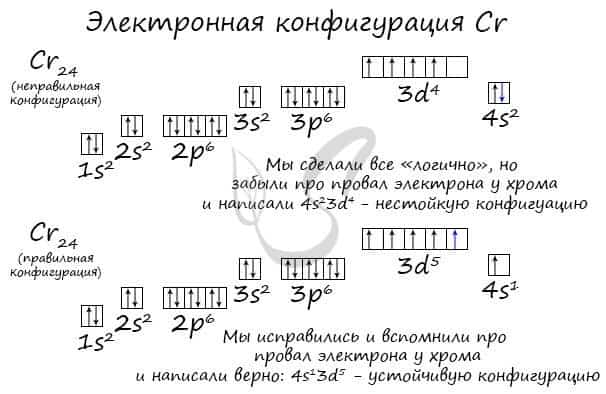
Теперь вы понимаете, что кроется под явлением провала электрона. Запишите электронные конфигурации хрома и меди самостоятельно еще раз и сверьте с представленными ниже.

Основное и возбужденное состояние атома
Основное и возбужденное состояние атома отражаются на электронных конфигурациях. Возбужденное состояние связано с движением электронов относительно атомных ядер. Говоря проще: при возбуждении пары электронов распариваются и занимают новые ячейки.
Возбужденное состояние является для атома нестабильным, поэтому долгое время в нем он пребывать не может. У некоторых атомов: азота, кислорода , фтора — возбужденное состояние невозможно, так как отсутствуют свободные орбитали («ячейки») — электронам некуда перескакивать, к тому же d-орбиталь у них отсутствует (они во втором периоде).
У серы возможно возбужденное состояние, так как она имеет свободную d-орбиталь, куда могут перескочить электроны. Четвертый энергетический уровень отсутствует, поэтому, минуя 4s-подуровень, заполняем распаренными электронами 3d-подуровень.
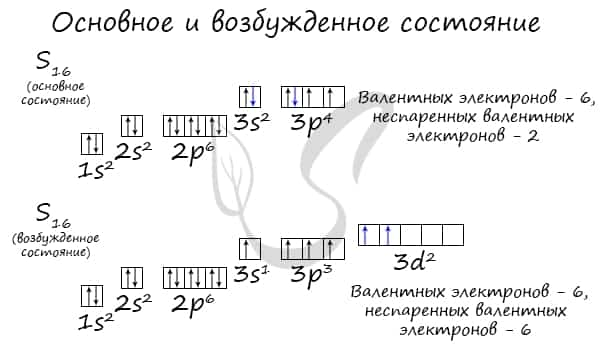
По мере изучения основ общей химии мы еще не раз вернемся к этой теме, однако хорошо, если вы уже сейчас запомните, что возбужденное состояние связано с распаривание электронных пар.
Положение металлов в ПС, особенности строения их атомов, физические свойства
Положение металлов в Периодической системе, особенности строения их атомов, физические свойства.
Большинство химических элементов в Периодической системе относится к металлам, они располагаются по диагонали от бора к астату. К металлам относятся девяноста два химических элемента.
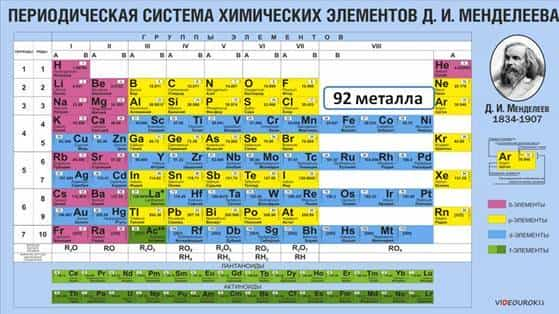
Каждый период (кроме первого) начинается металлом. Так, металлы IA группы называются щелочными металлами. К ним относятся: Li, Na, K, Rb, Cs, Fr.
Своё название они получили благодаря соответствующим гидроксидам, которые называются щелочами, т.е. растворимыми в воде основаниями.
Щелочные металлы имеют на внешнем энергетическом уровне только один электрон, который они легко отдают, при этом проявляют восстановительные свойства.
Ме0 – ē → Ме+
Причём восстановительные свойства в этой группе увеличиваются от лития к францию, как и радиусы атомов, поэтому растёт и способность к отдаче внешнего электрона. Химическая активность щелочных металлов по группе сверху вниз тоже увеличивается.
- Металлы IIA группы также являются типичными металлами и сильными восстановителями, так как в реакциях они отдают два своих электрона.
- Ме0 – 2ē → Ме2+
- Кальций, стронций и барий называют щелочноземельными элементами, потому что их оксиды, которые раньше называли «землями» при растворении в воде образуют щёлочи.
К металлам относятся и элементы IIIA группы кроме бора. У этих металлов на внешнем энергетическом уровне находится три электрона, которые они отдают и превращаются в ионы.
Ме0 – 3ē → Ме3+
В IVA группе к металлам относятся германий, олово, свинец, в VA группе металлами являются сурьма и висмут, в VIA группе – полоний, а в VIIA и VIIIA группе все элементы являются неметаллами.
Элементы побочных подгрупп все являются металлами. Их отличительной особенностью является то, что на внешнем уровне у них обычно содержится один или два электрона, остальные валентные электроны располагаются на предвнешнем слое. К металлам относятся и лантаниды, и актиниды, которые обычно располагаются ниже основной таблицы.
- Запомните:
- · у металлов сравнительно большие радиусы атомов
- · их внешние электроны значительно удалены от ядра и слабо с ним связаны
- · Атомы металлов содержат на внешнем уровне от одного до трех электронов
- · легко отдают электроны, превращаясь при этом в положительные ионы
- · являются восстановителями
- · Металлы не могут присоединять электроны.
- Однако деление элементов на металлы и неметаллы условно.
- Например, аллотропные модификации олова: так серое, или α-олово – неметалл, а белое, или β-олово – металл.
Такая модификация углерода, как алмаз – это неметалл, а графит имеет некоторые характерные свойства металлов.
Такие металлы, как цинк, хром, алюминий и другие – типичные металлы, но образуют оксиды и гидроксиды амфотерного характера. А теллур и йод – типичные неметаллы, но обладают некоторыми свойствами, характерными для металлов.
Физические свойства металлов.
Для металлов характерна металлическая химическая связь. В узлах кристаллической решётки располагаются атомы и положительные ионы металлов, которые связаны благодаря обобществлению внешних электронов, которые принадлежат всему кристаллу.
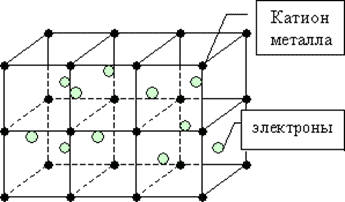
Для всех металлов характерно твёрдое агрегатное состояние, исключение составляет ртуть – она жидкая.
- Для большинства металлов характерен белый или серый цвет, только золото окрашено в желтый цвет, а медь в желто-красный.
- AuCu
Во-первых, для металлов характерна пластичность, которая проявляется в их ковкости, то есть они способны изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Из-за этого, металлы способны расплющиваться от удара или вытягиваться в проволоку. Эти свойства используют кузнецы. При этом слои смещаются относительно друг друга, но связь сохраняется благодаря «свободным» электронам.
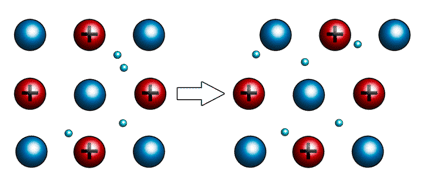
Наиболее пластичными являются золото, серебро, медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий.
Второе свойство металлов – это электропроводность. Оно обусловлено присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются по действием электрического поля.
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости.
А вот при охлаждении, электропроводность металлов усиливается, и близи абсолютного нуля переходят в сверхпроводимость.
Наибольшую электропроводность имеют серебро и медь, а наименьшую – марганец, свинец, ртуть и вольфрам.
Наличие свободных электронов в металлах объясняет и такое их свойство, как электро- и теплопроводность. Лучшими проводниками электрического тока являются: серебро, медь, золото, алюминий.
Третье физическое свойство металлов – это теплопроводность, это свойство тоже связано с высокой подвижностью свободных электронов.
Четвёртое свойство – металлический блеск связано с отражение световых лучей. Металлы обладают металлическим блеском. Свет поглощается поверхностью металла, и электроны начинают испускать свое излучение, которое мы воспринимаем как металлический блеск. Палладий, ртуть, серебро и медь лучше других отражают свет.
В порошкообразном состоянии большинство металлов теряет блеск, приобретая серую или чёрную окраску, но только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия изготавливают зеркала, в том числе и те, которые используются в прожекторах.
Самые твёрдые металлы – это металлы побочной подгруппы VIA группы. Например, хром по твёрдости напоминает алмаз. Наиболее твёрдыми ещё являются титан и молибден. Самые мягкие – щелочные металлы, например, натрий и калий легко режутся ножом.
По плотности различают легкие металлы, у которых плотность меньше 5 г/см3. К таким относятся щелочные и щелочноземельные металлы и алюминий. Из переходных металлов к ним относятся скандий, иттрий и титан. Они имеют большое значение в технике благодаря своей лёгкости и тугоплавкости.
Тяжелыми считаются металлы, у которых плотность больше 5 г/см3. Самым тяжелым является осмий, а самым лёгким – литий.
По температуре плавления металлы делятся на легкоплавкие, у которых эта температура меньше 1000 0С, и тугоплавкие, у которых она больше 1000 0С. Самым легкоплавким металлом является ртуть, а самым тугоплавким – вольфрам, из которого изготавливают нити накаливания для ламп. Кроме того, в конструкцию лампы входит ещё восемь металлов.
Лёгкие металлы, как правило, являются легкоплавкими, например, галлий может плавиться уже на ладони руки, а тяжёлые металлы, напротив, являются тугоплавкими.
Ряд государств, приняло решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например, галогенные, люминесцентные и светодиодные. Галогенная лампа – это тоже лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или йода).
- Люминесцентные лампы – это лампы дневного света, но они содержат ртуть, поэтому нуждаются в особом способе утилизации.
Светодиодные лампы – самые экономичные и долговечные (срок работы до 100 тыс. ч), но и самые дорогие из ламп.
- В технике металлы делятся на чёрные – это железо и его сплавы и цветные – это все остальные.
- Золото, серебро и платину, и некоторые другие металлы относят к драгоценным металлам.
Таким образом, следует запомнить, что большинство элементов в Периодической системе относятся к металлам, для металлов характерна металлическая кристаллическая решётка и металлическая химическая связь, которая обуславливает такие физические свойства металлов, как твёрдость, металлический блеск, ковкость и пластичность, тепло и – электропроводность. У металлов на внешнем энергетическом уровне от 1 до 3 электронов, поэтому они отдают свои электроны и проявляют восстановительные свойства.
Строение металлов


Средняя оценка: 4.7
Всего получено оценок: 83.
Средняя оценка: 4.7
Всего получено оценок: 83.
Металлы – твёрдые элементы, сплавы которых широко применяются в промышленности, строительстве и повседневной жизни. Пластичность, твёрдость, тепло- и электропроводность, а также способность к плавке и ковке обусловлены строением металлов.
Электронное строение атома металла включает:
- положительно заряженное ядро;
- отрицательно заряженные электроны.
Ядро состоит из протонов и нейтронов. Количество протонов, заряд ядра и число электронов соответствуют порядковому номеру металла в периодической таблице.
Электроны в металлических атомах расположены намного дальше от ядра, чем электроны неметаллов. Этим объясняется лёгкость отделения валентных электронов, поэтому металлы всегда являются восстановителями в химических реакциях.
Атомы всех металлов, за исключением ртути, образуют кристаллические решётки. Кристаллическая решётка состоит из повторяющихся комплексов атомов – элементарных кристаллических ячеек, которые бывают трёх видов. Их отличия описаны в таблице строения металлов.
| Вид решётки | Характеристика | Примеры |
| Кубическая объёмно-центрированная (ОЦК) | Восемь ионов находятся по углам условного куба, один – в середине | Fe, Cr, Mo, W, V |
| Кубическая гранецентрированная | Ионы располагаются в углах куба и в центре каждой грани. Центр куба свободен | Cu, Ag, Ni, Pb, Al |
| Гексагональная плотноупакованная | Шестигранная призма. В углах и в центре между ними находятся ионы. Посередине призмы лежат ионы, образующие треугольник | Zn, Ti, Mg, Co, Zr |
Рис. 1. Виды решёток металлов.
Металлы отличаются от неметаллов характерными физическими свойствами:
- имеют металлический блеск;
- проводят электрический ток и тепло;
- не имеют запаха;
- обладают серебристо-серым цветом (исключение – медь и золото).
Благодаря пластичности и плавке металлы могут образовывать сплавы – смеси химических элементов. Большую часть сплавов составляют металлы, остальное – случайные примеси и специально вводимые вещества. Сплавы отличаются высокой прочностью, упругостью, хрупкостью. Широко применяются сплавы на основе железа (чёрные металлы) и алюминия (цветные металлы).
Высокую электропроводность обуславливают свободные электроны, перемещающиеся по кристаллической решётке под действием электрических полей. При нагревании электропроводность уменьшается.
Классификация металлов приведена в таблице.
| Признак | Вид | Пример |
| Температура кипения | Легкоплавкие (Т1000°С) | Au, Cu, Ni |
| Плотность | Лёгкие (ρ5 г/см3) | Os |
| Твёрдость | Мягкие – режутся ножом | Na, Rb, Cs |
| Твёрдые – используются для резки | Cr |
В химии по структуре орбиталей атома металла различают s-, p-, d-, f-металлы.
Металлы являются восстановителями и вступают в реакцию с неметаллами, образуя оксиды, гидроксиды, соли. Самыми активными являются щелочные и щелочноземельные металлы, расположенные в I и II группах таблицы Менделеева. Благородные металлы (Au, Ag, Pt) малоактивны и не взаимодействуют с кислородом и водой.
 Рис. 2. Шкала активности металлов.
Рис. 2. Шкала активности металлов.
Особенности химического взаимодействия металлов с другими элементами описаны в таблице.
| Взаимодействие | Продукты | Уравнение |
| С кислородом | Оксиды | 2Mg + O2 → 2MgO |
| С серой | Сульфиды | Zn + S → ZnS |
| С азотом | Нитриды | 6Li + N2 → 2Li3N |
| С фосфором | Фосфиды | 3Ca + 2P → Ca3P2 |
| С галогенами | Галогениды | 2Na + Cl2 → 2NaCl |
| С водой | Гидроксиды | 2Na + 2H2O → 2NaOH + H2 |
| С кислотами | Соли | 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 |
| С солями (замещают менее активные металлы) | Соль | 2Fe + Cu2SO4 → Fe2SO4 + 2Cu |
Золото растворяется в царской водке (смеси соляной и азотной кислот), серебро – в концентрированной азотной и горячей серной кислотах.
 Рис. 3. Золото.
Рис. 3. Золото.
Рассмотрели особенности строения атомов металлов, физические и химические свойства. Металлы состоят из элементарных кристаллических ячеек, отличающихся конфигурацией.
Элементы обладают металлическим блеском, электропроводностью, пластичностью, твёрдостью. Металлы – восстановители. Наиболее активные находятся в I и II группах таблицы Менделеева.
Металлы реагируют с кислородом, водой, кислотами, галогенами и неметаллами.
Чтобы попасть сюда — пройдите тест.
Средняя оценка: 4.7
Всего получено оценок: 83.
А какая ваша оценка?
Гость завершил
Тест «Чистый понедельник»с результатом 10/12
Гость завершил
Тест «Недоросль»с результатом 16/18
Гость завершил
Тест «Горе от ума»с результатом 14/15
Гость завершил
Тест «Недоросль»с результатом 16/18
Гость завершил
Тест на тему «Алгоритм»с результатом 2/5
Гость завершил
Тест «Биография Набокова»с результатом 8/10
Гость завершил
Тест Капалуха (3 класс)с результатом 10/10
Не подошло? Напиши в х, чего не хватает!
Строение электронных оболочек атомов
На этом уроке вы узнаете, как устроена электронная оболочка атома, и сможете объяснить явление периодичности. Познакомитесь с моделями строения электронных оболочек атомов, с помощью которых можно предсказать и объяснить свойства химических элементов и их соединений.
I. Состояние электронов в атоме
Выдающийся датский физик Нильс Бор (Рис. 1) предположил, что электроны в атоме могут двигаться не по любым, а по строго определенным орбитам.
При этом электроны в атоме различаются своей энергией. Как показывают опыты, одни из них притягиваются к ядру сильнее, другие – слабее.
Главная причина этого заключается в разном удалении электронов от ядра атома. Чем ближе электроны к ядру, тем они прочнее связаны с ним и их труднее вырвать из электронной оболочки.
Таким образом, по мере удаления от ядра атома запас энергии электрона увеличивается.
Электроны, движущиеся вблизи ядра, как бы загораживают (экранируют) ядро от других электронов, которые притягиваются к ядру слабее и движутся на большем удалении от него. Так образуются электронные слои.
Каждый электронный слой состоит из электронов.
Электрон вращается вокруг ядра атома с невообразимой скоростью.
Так, за 1 секунду он делает столько оборотов вокруг ядра атома, сколько оборотов делает пропеллер самолета вокруг оси за 5–5,5 лет непрерывной работы двигателя.
Пропеллер самолета образует «облако», находящееся в одной плоскости, а электрон образует объемное облако –электронное облако, форма и размер которого зависят от энергии электрона.
- Если обозначить точками все вероятные места нахождения электрона в атомном пространстве за некоторое время, то совокупность этих точек будет представлять собойэлектронное облако.
- II. Электронное облако
- Электронное облако– это модель, которая описывает состояние (движение) электрона в атоме.
- Электронное облако не имеет строго очерченных границ и плотность его неравномерна.
- Часть атомного пространства, в котором вероятность нахождения электрона наибольшая (~90%), называетсяорбиталью.
| Виды электронных орбиталей | Форма орбитали в пространстве | Количество орбиталей в атоме. Условное обозначение орбитали – клетка: |
| s – орбиталь (электронное облако s – электрона) | сфера (шар) | Электронное облако такой формы может занимать в атоме одно положение (условное обозначение) |
| p – орбиталь (электронное облако p – электрона) | гантель (восьмёрка) | Электронное облако такой формы может занимать в атоме три положения вдоль осей координат пространства x, y и z. (условное обозначение) |
| d – орбиталь (электронное облако d – электрона) | четырёхлепестковая форма | Все d-орбитали (а их может быть уже пять) одинаковы по энергии, но по-разному расположены в пространстве. Да и по форме, напоминающей перевязанную лентами подушечку, одинаковы только четыре. А пятая — вроде гантели, продетой в бублик (условное обозначение) |
| f – орбиталь (электронное облако f – электрона) | сложная форма | Электронное облако такой формы может занимать в атоме семь положений. (условное обозначение) |
- Условное обозначение электрона – стрелка, направленная вверх↑ (электрон вращается вокруг собственной оси по часовой стрелке) или стрелка, направленная вниз↓ (электрон вращается вокруг собственной оси против часовой стрелки).
- Число электронов в атоме определяют по порядковому номеру
- О – 8 электронов, S – 16 электронов.
- На одной орбитали могут находиться только ДВА электрона, которые вращаются вокруг своей оси в противоположных направлениях (по часовой стрелке и против часовой стрелке) – электроны с противоположными спинами:
- Cледовательно, на s – орбитали максимально может разместиться два электрона (s2); на p – орбитали максимально может разместиться шесть электронов (p6) на d – орбитали максимально может разместиться десять электронов (d10); f – четырнадцать электронов (f14).
- Располагаясь на различных расстояниях от ядра, электроны образуют электронные слои (энергетические уровни) – каждому слою соответствует определённый уровень энергии.
- Условное обозначение уровня — скобка:)
- Число энергетических уровней определяют по номеру периода, в котором находится химический элемент
- О – 2 уровня, S – три уровня.

- Для элементов главных подгрупп (А) число электронов на внешнем уровне = номеру группы.
- +15P – V группа (А) – на внешнем уровне 5 электронов
- Для элементов побочных подгрупп (В) число электронов на внешнем уровне = двум.
- Исключения (один электрон) – хром, медь, серебро, золото и некоторые другие.
- III. Формулы отражающие строение атомов первого и второго периодов
- H +1 )1e
- – схема строения атома, отображает распределение электронов по энергоуровням.
- +1 Н 1s1
- – электронная формула, отображает число электронов по орбиталям.
- +1 Н
- — электронно-графическая формула – показывает распределение электронов по орбиталям и отображает спин электрона.

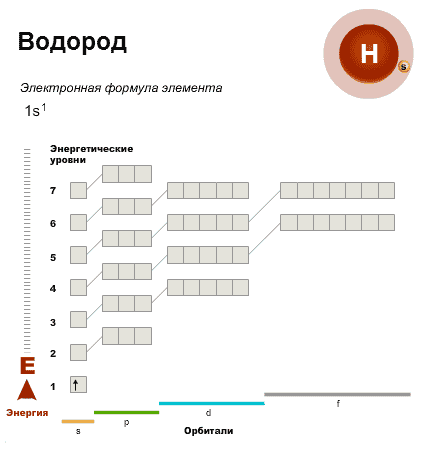
У элементов второго периода начинается заполнение второго энергетического уровня — он включает восемь электронов (n = 2, N = 8). Второй период содержит восемь элементов. У неона, элемента, завершающего второй период, первый и второй энергетические уровни оказываются целиком заполненными.
Американский химик Гилберт Льюис дал объяснение этому и выдвинул правило октета, в соответствии с которым устойчивым является восьмиэлектронный слой (за исключением 1 слоя: т. к. на нем может находиться не более 2 электронов, устойчивым для него будет двухэлектронное состояние).
IV. Распределение электронов по энергетическим уровням элементов третьего и четвертого периодов ПСХЭ
1. Порядок заполнения уровней и подуровней электронами
Электронные формулы атомов химических элементов составляют в следующем порядке:
- Сначала по номеру элемента в таблице Д. И. Менделеева определяют общее число электронов в атоме;
- Затем по номеру периода, в котором расположен элемент, определяют число энергетических уровней;
- Уровни разбивают на подуровни и орбитали, и заполняют их электронами в соответствии Принципом наименьшей энергии
- Для удобства электроны можно распределить по энергетическим уровням, воспользовавшись формулой N=2n2 и с учётом того, что:
- У элементов главных подгрупп (s-;p-элементы) число электронов на внешнем уровне равно номеру группы.
- У элементов побочных подгрупп на внешнем уровне обычно дваэлектрона (исключение составляют атомы Cu, Ag, Au, Cr, Nb, Mo, Ru, Rh, у которых на внешнем уровне один электрон, у Pd на внешнем уровне нольэлектронов);
- Число электронов на предпоследнем уровне равно общему числу электронов в атоме минус число электронов на всех остальных уровнях.
- Порядок заполнения электронами атомных орбиталей определяется:
- Принципом наименьшей энергии
- Шкала энергий:
- 1s
Строение металлов и их особенности, схема и примеры
Металлы можно охарактеризовать при помощи нескольких свойств, которые будут общими для всех элементов. К таким характеристикам следует отнести высокую электрическую проводимость и теплопроводность, пластичность, благодаря которой металлы можно подвергать ковке, прокатке, штамповке или вытягиванию в проволоку, металлический блеск и непрозрачность.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип> 1000oС) и легкоплавкие (Tкип< 1000oС). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Электронное строение металлов и их особенности
Атомы металлов, также как, и неметаллов состоят из положительно заряженного ядра внутри которого находятся протоны и нейтроны, а по орбитам вокруг него движутся электроны. Однако, по сравнению с неметаллами, атомные радиусы металлов намного больше.
Это связано с тем, что валентные электроны атомов металлов (электроны внешнего энергетического уровня) расположены на значительном удалении от ядра и, как следствие, связаны с ним слабее.
По этой причине металлы характеризуются низкими потенциалами ионизации и легко отдают электроны (являются восстановителями в ОВР) при образовании химической связи.
Все металлы за исключением ртути представляют собой твердые вещества с атомной кристаллической решеткой. Рассмотрим строение металлов в кристаллическом состоянии. В атомах металлов имеются «свободные» электроны (электронный газ), которые могут перемещаться по кристаллу даже под действием слабых электрических полей, что обусловливает высокую электропроводимость металлов.
Среди металлов присутствуют s-, p-, d- и f-элементы. Так, s- элементы – это металлы I и II групп Периодической системы (ns1, ns2), р- элементы – металлы, расположенные в группах III – VI (ns2np1-4). Металлы d-элементы имеют большее число валентных электронов по сравнению с металлами s- и p-элементами.
Общая электронная конфигурация валентных электронов металлов d-элементов – (n-1)d1-10ns2. Начиная с 6 периода появляются металлы f-элементы, которые объединены в семейства по 14 элементов (за счет сходных химических свойств) и носят особые названия лантаноидов и актиноидов.
Общая электронная конфигурация валентных электронов металлов f-элементов – (n-2)f1-14(n-1)d0-1ns2.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! |
Металлы
В периодах и группах периодической системы Д. И. Менделеева существуют закономерности в изменении металлических и неметаллических свойств элементов, можно достаточно определённо указать положение элементов-металлов и элементов-неметаллов в периодической системе.
Если провести диагональ от элемента бора B (порядковый номер 5) до элемента астата At (порядковый номер 85), то слева от этой диагонали в периодической системе все элементы являются металлами, а справа от неё элементы побочных подгрупп являются металлами, а элементы главных подгрупп – неметаллами.
Элементы расположенные вблизи диагонали (например, Al, Ti, Ge, Sb, Te, As, Nb), обладают двойственными свойствами: в некоторых своих соединениях ведут себя как металлы; в некоторых – проявляют свойства неметаллов.
Все s-элементы (кроме H и He), d-элементы (все элементы побочных подгрупп) и f-элементы (лантаноиды и актиноиды) являются металлами. Среди p-элементов есть и металлы, и неметаллы, число элементов-металлов увеличивается с увеличением номера периода.
Деление на металлы и неметаллы объясняется различием в строении атомов. Рассмотрим, например, строение атомов третьего периода:
Элементы третьего периода: Na, Mg, Al, Si, P, S, Cl, Ar (аргон).
Радиус атома: 0.19; 0.16; 0.143; 0.134; 0.130; 0.104; 0.099.
Число электронов на внешнем слое: 1, 2, 3, 4, 5, 6, 7.
Электроотрицательность: 0.9; 1.2; 1.5; 1.8; 2.1; 2.5; 3.0.
- Любой гидроксид содержит гидроксидные группы – OH.
- Слева направо:
- а. Радиус атомов уменьшается;
- б. Заряд ядра увеличивается;
- в. Электроотрицательность увеличивается;
- г. Число электронов на внешнем слое увеличивается;
- д. Прочность связи внешних электронов с ядром увеличивается;
е. Способность атомов отдавать электроны уменьшается.
Поэтому:
Na, Mg, Al – металлы, а Si, P, S, Cl – неметаллы.
Атомы большинства металлов на внешнем электронном слое имеют от 1 до 3 электронов. Исключение: атомы германия Ge, олова Sn, свинца Pb на внешнем электронном слое имеют четыре электрона, атомы сурьмы Sb, висмута Bi – пять, атомы полония Po – шесть.
Атомы металла имеют меньший заряд ядра и больший радиус (размер) по сравнению с атомами неметаллов данного периода. Потому прочность связи внешних электронов с ядром в атомах металлов небольшая.
Атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы.
Простые вещества, которые образуют элементы-металлы, при обычных условиях являются твёрдыми веществами (кроме ртути). Кристаллическая решётка металлов образуется за счёт металлической связи.
Имеющиеся между узлами кристаллической решётки свободные электроны могут переносить теплоту и электрический ток, что является причиной главных физических свойств металлов – высокой электро- и теплопроводности.
Металлическая связь образуется во всех металлах. Это связь, которую осуществляют относительно свободные электроны с положительными ионами металлов в кристаллической решётке.
Атомы металла легко отдают валентные электроны и превращаются в положительные ионы.
Относительно свободные электроны перемещаются между положительными ионами металла и между ними возникает металлическая связь, то есть электроны как бы цементируют положительные ионы металла в кристаллической решётке.
Атомы металлов более или менее легко отдают электроны, то есть окисляются.
Энергия, которая необходима для отрыва электрона от атома и превращение его в положительно заряженный ион, называется энергией ионизации. Металлы характеризуются небольшими величинами энергий ионизации.
Атомы металлов не могут присоединять электроны. Поэтому металлы во всех химических реакциях являются восстановителями и в соединениях имеют только положительные степени окисления. Восстановительная активность различных металлов не одинакова.
В периодах слева направо восстановительная активность уменьшается; в главных подгруппах сверху вниз – увеличивается.
Восстановительная активность металлов в химических реакциях, которые протекают в водных растворах различных веществ, характеризуется положением металлов в электрохимическом ряду напряжений металлов.
- Металлы являются восстановителями и вступают в химические реакции с различными окислителями.
- 2. Альдегиды
- Альдегиды – органические вещества, содержащую функциональную группу (альдегидную группу).






