- Химическая активность металлов
- Реакции металлов с кислородом и водой
- Взаимодействие металлов с кислотами. ряд активности металлов
- Взаимодействие металлов с растворами солей
- Активные металлы
- Большая Рнциклопедия Нефти Рё Газа
- Электрохимический ряд активности металлов | это… Что такое Электрохимический ряд активности металлов?
- История
- Теоретические основы
- Практическое использование ряда напряжений
- Таблица электрохимических потенциалов металлов
- Ссылки
- Литература
- Примечания
- ПОИСК
- Содержание:
- Электрохимический ряд активности металлов (ряд напряжений, ряд стандартных электродных потенциалов) — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла Men+: Men+ + nē → Me
- Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
- На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Химическая активность металлов
Электрохимический ряд активности металлов показывает, какие из металлов более активные, какие менее. Расположение элементов в горизонтальном ряду слева направо показывает направление снижения восстановительной способности и возрастание окислительной.
Реакции металлов с кислородом и водой
Что вы знаете о ржавлении железа? Расскажите о разрушении металлов? Как вы думаете, как можно защитить металлы от разрушения? Где применяются металлы? Приведите примеры из жизни.
Металлы мы часто применяем в повседневной жизни. Это алюминий, медь, железо, золото, серебро и т. д. Алюминий и медь применяются для изготовления проводов. Алюминиевой фольгой упаковывают лекарства.
В домашнем обиходе вы часто встречаете алюминиевую посуду и упаковки для напитков. Но больше всего применяется железо для изготовления различных металлоконструкций, трубопроводов, деталей машин и т. д.
Этот металл от воды и кислорода воздуха приходит в негодность, изменяет цвет и тускнеет.
Железо покрывается ржавчиной красно-бурого цвета. Железо + вода + воздух → ржавчина. Такой химический процесс называется коррозией (от лат. corrodere – разъедать).
- Самопроизвольное разрушение металлов в результате их взаимодействия с веществами окружающей среды называется коррозией.
- Поверхность алюминия покрывается оксидной пленкой, которая препятствует коррозии:
Химические активные металлы легко окисляются кислородом воздуха (Na, Mg, Ca). Железо и медь окисляются только при нагревании:
А золото и некоторые благородные металлы вообще не окисляются кислородом.
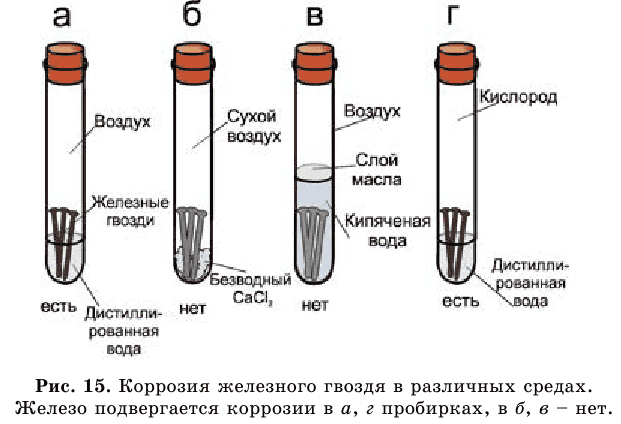
Рассмотрите рисунок 15 и сами сделайте выводы.
Ежегодно четвертая часть всего производимого металла из-за коррозии приходит в негодность (рис. 16).
Знаменитую Эйфелеву башню в Париже красили уже 18 раз, в результате чего ее масса увеличилась на 70 т.
Коррозия вызывает серьезные экологические катастрофы. Из разрушенных трубопроводов может быть утечка газа, нефти, опасных химических продуктов. Это приводит к загрязнению окружающей среды, что отрицательно влияет на здоровье и жизнь людей.
Металлы защищают от коррозии нанесением покрытий на поверхность изделия: окраска металла лаками, красками, эмалями. Но это покрытие недолговечно. Предохраняют металл покрытием другого металла, менее подверженного коррозии.
Это – золото, серебро, хром, никель, олово, цинк и др. В повседневной жизни часто применяют оцинкованные ведра, никелированные кровати. Для консервных банок применяют железо, покрытое оловом. Такое железо называют белой жестью. Белую жесть получают в г.
Темиртау Карагандинской области на металлургическом заводе. Можно уменьшить коррозию железа, добавляя другие металлы: никель, хром, молибден. Таким образом, получают сплав, который называется нержавеющей сталью.
Из этой стали изготавливают столовые приборы, трубы и другие изделия.
Олово — достаточно редкий, но очень полезный металл. Известно, что его начали добывать раньше, чем железо. Олово — это мягкий белый металл, который можно сплавлять с медью, чтобы получить бронзу.
Олово — один из первых освоенных человеком металлов. Оно не подвержено коррозии, поэтому из него делают тару для упаковки. Слой олова, нанесенный на другие металлы, делает их поверхность гладкой и блестящей.
Банки для хранения консервов и напитков также делают из тонкого стального листа, покрытого оловом.
Взаимодействие воды с некоторыми металлами (рис. 17). 1. Взаимодействие воды с активными металлами в обычных условиях идет очень интенсивно.
При этом протекают реакции замещения
При проведении таких опытов необходимо соблюдать меры предосторожности.
2. При взаимодействии металлов средней активности с водой вместо щелочи выделяется оксид металла:
3. Малоактивные металлы (Cu) с водой не реагируют.
Коррозия, ржавчина, защита от коррозии, белая жесть, алюминиевая фольга, сплав
Свинец — тяжелый голубовато-серый металл, который не ржавеет. Он используется в автомобильных аккумуляторах. Свинцовые экраны защищают людей от опасной радиации. Но свинец токсичен и ядовит для человека.
- Демонстрация №2
- Взаимодействие активных металлов с холодной и горячей водой
- Демонстрацию выполняет учитель, учащиеся наблюдают, делают выводы.
- Цель: узнать, как реагируют активные металлы с холодной и горячей водой.

Обрежьте кусочек натрия скальпелем, высушите фильтровальной бумагой. Высушенный кусочек натрия следует бросить в кристаллизатор с холодной, а затем горячей водой. Наблюдать за ходом реакции через стекло вытяжного шкафа. Такую же реакцию проделать и с металлическим кальцием. Испытать полученные растворы двумя индикаторами.
Взаимодействие металлов с кислотами. ряд активности металлов
Что такое кислоты? Какие кислые вещества вы встречали в природе?
В соответствии с определением кислоты должны вступать в реакции с металлами. Все ли металлы взаимодействуют с кислотами? Это можно проверить на опыте.
В четыре пронумерованные пробирки нальем одинаковое количество раствора соляной кислоты и добавим: в первую пробирку – Mg; во вторую – Zn; в третью – Sn; в четвертую – Cu.
Как видим, не все металлы могут взаимодействовать с кислотами и скорости их взаимодействия различны (рис. 18).
На основании интенсивности взаимодействия металлов с кислотами русским ученым Н.Н. Бекетовым был составлен ряд активности металлов:
Li K Ca Na Mg Al Zn Fe Ni Sn Pb (H2) Cu Hg Ag Au
При использовании ряда химической активности нужно помнить следующие правила:
1) металлы, стоящие в начале этого ряда, химически активны, они могут вытеснить водород из воды. 2) активность металлов в этом ряду снижается слева направо 3) только металлы, стоящие в ряду активности до водорода, вытесняют водород из растворов кислот (рис. 18):
активный металл + кислота —> соль + водород
Протекает реакция замещения. Металлы, стоящие в ряду активности после водорода, не реагируют с разбавленными растворами кислот (табл. 6).
- Лабораторный опыт №3
Взаимодействие металлов с растворами кислот - Цель: исследовать реакции различных металлов с растворами кислот и сделать вывод о существовании химически инертных металлов.
Налейте в четыре пробирки раствор соляной кислоты. В одну из пробирок насыпьте порошка магния, в другую – поместите гранулы цинка, в третью – опилки железа, в четвертую – стружки меди.
Может ли железо не подвергаться коррозии? Да, если оно очень чистое. Например, в Дели (Индия) находится Кутубская колонна высотой 7 м, массой 6,5 т. Она установлена в IX в. до н. э., в ее составе 99,72% Fe. До сих пор эта колонна не подверглась коррозии.
Взаимодействие металлов с растворами солей
Какие соли вы встречали в повседневной жизни?
Химически активные металлы вытесняют менее активные металлы из растворов солей, при этом протекает реакция замещения. Например, из раствора сульфата меди (ІІ) железо вытесняет медь (рис. 19):
Выделение красного налета меди является признаком реакции. Обратная реакция не протекает потому что медь в ряду активности металлов находится после железа, поэтому не вытесняет его.
- Схема реакций замещения выглядит следующим образом:
- соль 4- активный металл = новая соль + новый металл (менее активный)
- Реакции такого типа протекают при следующих условиях: 1) взаимодействующие соли должны быть растворимыми в воде;
- 2) более активный металл вытесняет из соли менее активный металл.
- Демонстрация №3
Вытеснение металлов из растворов солей - Цель: понимать, что более активный металл вытесняет менее активный металл из растворов его солей.
В пробирку поместите гранулы цинка и налейте раствор сульфата меди. В другую пробирку поместите небольшие кусочки железа и налейте раствор сульфата меди. Что наблюдаете? Напишите уравнение реакции. Сделайте вывод.
Практическая работа № 1 Сравнение активности металлов
Цель: Разработать ряд активности металлов. Обобщить результаты и сделать выводы.
Ход работы
В пять пробирок налейте растворы солей по 5 мл, опустите в каждую пробирку стружки меди. Затем такие опыты повторите с другими металлами. Наблюдайте за интенсивностью хода реакций. Заполните таблицу: где идет реакция следует поставить знак “+”, если не идет реакция – знак “–”. По сравнительной интенсивности, т. е. по числу протекающих реакций, составьте ряд активности металлов.
ДЕЛАЕМ ВЫВОДЫ:
- 1. Атомы металлов в реакциях только отдают электроны, образуя положительно заряженные ионы.
- 2. Самопроизвольное разрушение металлов в результате их взаимодействия с веществами окружающей среды называется коррозией.
- 3. Сравнительную активность металлов можно определить с помощью ряда активности, составленного Н. Н. Бекетовым.
- 4. Металлы IA, НА группы очень легко вступают во взаимодействие с кислородом и водой. Многие металлы образуют оксидную пленку, которая препятствует дальнейшему окислению. Благородные металлы вообще не реагируют с кислородом и водой.
Услуги по химии:
- Заказать химию
- Заказать контрольную работу по химии
- Помощь по химии
- Лекции по химии:
- Лекции по неорганической химии:
- Лекции по органической химии:
Активные металлы


Средняя оценка: 4.4
Всего получено оценок: 1074.
Средняя оценка: 4.4
Всего получено оценок: 1074.
Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
Рис. 1. Активные металлы в таблице Менделеева.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.
 Рис. 2. Электрохимический ряд напряжений металлов.
Рис. 2. Электрохимический ряд напряжений металлов.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
| Реакция | Уравнение | Исключение |
| Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом | K + O2 → KO2 | Литий реагирует с кислородом только при высокой температуре |
| Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются | 2Ca + O2 → 2CaO | |
| Реагируют с простыми веществами, образуя соли | – Ca + Br2 → CaBr2; – 2Al + 3S → Al2S3 | Алюминий не вступает в реакцию с водородом |
| Бурно реагируют с водой, образуя щёлочи и водород | – 2Na + 2H2O → 2NaOH + H2; – Ca + 2H2O → Ca(OH)2 + H2 | Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки |
| Реагируют с кислотами, образуя соли |
– Ca + 2HCl → CaCl2 + H2; – 2K + 2HMnO4 → 2KMnO4 + H2 |
|
| Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью |
2Na + CuCl2 + 2H2O: – 2Na + 2H2O → 2NaOH + H2; – 2NaOH + CuCl2 → Cu(OH)2↓ + 2NaCl |
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.
 Рис. 3. Минералы и чистые металлы.
Рис. 3. Минералы и чистые металлы.
К активным металлам относятся элементы I и II групп – щелочные и щелочноземельные металлы, а также алюминий. Их активность обусловлена строением атома – немногочисленные электроны легко отделяются от внешнего энергетического уровня.
Это мягкие лёгкие металлы, быстро вступающие в реакцию с простыми и сложными веществами, образуя оксиды, гидроксиды, соли.
Алюминий находится ближе к водороду и для его реакции с веществами требуются дополнительные условия – высокие температуры, разрушение оксидной плёнки.
Чтобы попасть сюда — пройдите тест.
Средняя оценка: 4.4
Всего получено оценок: 1074.
А какая ваша оценка?
Гость завершил
Тест «Горе от ума»с результатом 13/15
Гость завершил
Тест «Биография Гумилева»с результатом 10/13
Гость завершил
Тест «На дне»с результатом 6/15
Гость завершил
Тест «Тарас Бульба»с результатом 14/16
Гость завершил
Тест «Горе от ума»с результатом 12/15
Гость завершил
Тест «Фауст»с результатом 15/16
Гость завершил
Тест по произведению «12»с результатом 10/10
Гость завершил
Тест «Тарас Бульба»с результатом 12/16
Гость завершил
Тест «Борис Годунов»с результатом 11/15
Не подошло? Напиши в х, чего не хватает!
Большая Рнциклопедия Нефти Рё Газа
Cтраница 1
| Зависимость коэффициента. [1] |
Химическая активность металла определяется сродством его атомов внешним ( валентным) электронам и может быть оценена по ионизационному потенциалу. [2]
Химическая активность металлов этой группы от Zn к Hg уменьшается. [3]
Химическая активность металлов различна.
Такие металлы, как натрий Na, калий К, кальций Са, обладают очень высокой химической активностью, вступая в реакции с неметаллами, водой, кислотами при комнатных условиях.
Есть металлы, которые называются благородными ( золото Аи, платина Pt) из-за их очень слабой химической активности. Благородные металлы с большим трудом реагируют даже с очень сильными окислителями. [4]
Химическая активность металлов в подгруппе хрома уменьшается от хрома к вольфраму. [5]
Химическая активность металлов уменьшается с увеличением количества электронов во внешнем электронном слое. Поэтому в реакциях, протекающих в отсутствие воды, кальций менее активен, чем натрий. [6]
Химическая активность металла определяется, как известно, сродством его атомов к внешним ( валентным) электронам и может быть оценена по величине ионизационного потенциала. [7]
| Некоторые свойства Си, Ag, Аи. [8] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика.
С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании.
При комнатной температур-е Си практически не взаимодействует с фтором вследствие образования прочной защитной пленки фторида.
Хлориды СиСЬ, AgCl, АиС13 также образуются в результате взаимодействия элементных веществ при нагревании. [9]
| Некоторые свойства Си, Ag, Аи. [10] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика.
С кислородом реагирует только медь, благородные ме-рллы Ag и Аи не окисляются кислородом даже при нагревании.
При комнатной температуре Си практически не взаимодействует с фтором вследствие образования прочной защитной пленки фторида.
При нагревании Си и Ag реагируют с серой, образуя Cu2S и AgaS. Хлориды СиСЬ, AgCl, АиС13 также образуются в результате взаимодействия элементных веществ при нагревании. [11]
Химическая активность металлов Си, Ag, Аи сравнительно невелика.
С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании.
При комнатной температуре медь практически не взаимодействует со фтором вследствие образования прочной защитной пленки фторида.
Хлориды CuCl2, AgCl, AuCb также образуются в результате взаимодействия элементных веществ при нагревании. [13]
Химическая активность металлов Си, Ag, Аи сравнительно невелика.
С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании.
При комнатной температуре медь практически не взаимодействует со фторсм вследствие образования прочной защитной пленки фторида.
При нагревании Си и Ag реагируют с серой, образуя сульфиды CujS и AgjS. Хлориды CuClj, AgCl, AuCh также образуются в результате взаимодействия элементных веществ при нагревании. [15]
Страницы: 1 2 3 4
Электрохимический ряд активности металлов | это… Что такое Электрохимический ряд активности металлов?
Электрохимический ряд активности (ряд напряжений, ряд стандартных электродных потенциалов) металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла Men+: Men+ + nē → Me
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительные реакциях в водных растворах.
История
Последовательность расположения металлов в порядке изменения их химической активности в общих чертах была известна уже алхимикам[1]. Процессы взаимного вытеснения металлов из растворов и их поверхностное осаждение (например, вытеснение серебра и меди из растворов их солей железом) рассматривались как проявление трансмутации элементов.
Поздние алхимики вплотную подошли к пониманию химической стороны взаимного осаждения металлов из их растворов.
Так, Ангелус Сала в работе «Anatomia Vitrioli» (1613) пришёл к выводу, что продукты химических реакций состоят из тех же «компонентов», которые содержались в исходных веществах.
Впоследствии Роберт Бойль предложил гипотезу о причинах, по которым один металл вытесняет другой из раствора на основе корпускулярных представлений[2].
В 1793 году Алессандро Вольта, конструируя гальванический элемент («Вольтов столб»), установил относительную активность известных тогда металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. «Сила» гальванического элемента оказывалась тем больше, чем дальше стояли друг от друга металлы в этом ряду («ряд напряжений»). Однако Вольта не связал этот ряд с химическими свойствами металлов.
В 1798 году Иоганн Вильгельм Риттер указал, что ряд Вольта эквивалентен ряду окисления металлов (т. е. последовательности уменьшения их сродства с кислородом). Таким образом, Риттер высказал гипотезу о возникновении электрического тока вследствие протекания химической реакции[3].
В эпоху становления классической химии способность элементов вытеснять друг друга из соединений стала важным аспектом понимания реакционной способности. Й. Берцелиус на основе электрохимической теории сродства построил классификацию элементов, разделив их на «металлоиды» (сейчас применяется термин «неметаллы») и «металлы» и поставив между ними водород.
Последовательность металлов по их способности вытеснять друг друга, давно известная химикам, была в 1860-е и последующие годы особенно основательно и всесторонне изучена и дополнена Н. Н. Бекетовым. Уже в 1859 году он сделал в Париже сообщение на тему «Исследование над явлениями вытеснения одних элементов другими».
В эту работу Бекетов включил целый ряд обобщений о зависимости между взаимным вытеснением элементов и их атомным весом, связывая эти процессы с «первоначальными химическими свойствами элементов – тем, что называется химическим сродством»[4].
Открытие Бекетовом вытеснения металлов из растворов их солей водородом под давлением и изучение восстановительной активности алюминия, магния и цинка при высоких температурах (металлотермия) позволило ему выдвинуть гипотезу о связи способности одних элементов вытеснять из соединений с их плотностью: более лёгкие простые вещества способны вытеснять более тяжёлые («вытеснительный ряд Бекетова»).
Не отрицая значительных заслуг Бекетова в становлении современных представлений об ряде активности металлов, следует считать ошибочным бытующее в отечественной популярной и учебной литературе представление о нём как единственном создателе этого ряда.[5][6].
Многочисленные экспериментальные данные, полученные в конце XIX века, опровергали гипотезу Бекетова. Так, Уильям Одлинг описал множество случаев «обращения активности».
Например, медь вытесняет олово из концентрированного подкисленного раствора SnCl2 и свинец — из кислого раствора PbCl2; она же способна к растворению в концентрированной соляной кислоте с выделением водорода.
Медь, олово и свинец находятся в ряду правее кадмия, однако могут вытеснять его из кипящего слабо подкисленного раствора CdCl2.
Бурное развитие теоретической и экспериментальной физической химии указывало на иную причину различий химической активности металлов. С развитием современных представлений электрохимии (главным образом в работах Вальтера Нернста) стало ясно, что эта последовательность соответствует «ряду напряжений» – расположению металлов по значению стандартных электродных потенциалов.
Таким образом, вместо качественной характеристики — «склонности» металла и его иона к тем или иным реакциям — Нерст ввёл точную количественную величину, характеризующую способность каждого металла переходить в раствор в виде ионов, а также восстанавливаться из ионов до металла на электроде, а соответствующий ряд получил название ряда стандартных электродных потенциалов.
Теоретические основы
Значения электрохимических потенциалов являются функцией многих переменных и поэтому обнаруживают сложную зависимость от положения металлов в периодической системе. Так, окислительный потенциал катионов растёт с увеличением энергии атомизации металла, с увеличением суммарного потенциала ионизации его атомов и с уменьшением энергии гидратации его катионов.
В самом общем виде ясно, что металлы, находящиеся в начале периодов характеризуются низкими значениями электрохимических потенциалов и занимают места в левой части ряда напряжений. При этом чередование (щелочных и щёлочноземельных металлов отражает явление диагонального сходства.
Металлы, расположенные ближе к серединам периодов, характеризуются большими значениями потенциалов и занимают места в правой половине ряда.
Последовательное увеличение электрохимического потенциала (от −3,395 В у пары Eu2+/Eu[источник не указан 228 дней] до +1,691 В у пары Au+/Au) отражает уменьшение восстановительной активности металлов (свойство отдавать электроны) и усиление окислительной способности их катионов (свойство присоединять электроны). Таким образом, самым сильным восстановителем является металлический европий, а самым сильным окислителем — катионы золота Au+.
В ряд напряжений традиционно включается водород, поскольку практическое измерение электрохимических потенциалов металлов производится с использованием стандартного водородного электрода.
Практическое использование ряда напряжений
Ряд напряжений используется на практике для сравнительной оценки химической активности металлов в реакциях с водными растворами солей и кислот и для оценки катодных и анодных процессов при электролизе:
- Металлы, стоящие левее, являются более сильными восстановителями, чем металлы, расположенные правее: они вытесняют последние из растворов солей. Например, взаимодействие Zn + Cu2+ → Zn2+ + Cu возможно только в прямом направлении.
- Металлы, стоящие в ряду левее водорода, вытесняют водород при взаимодействии с водными растворами кислот-неокислителей; наиболее активные металлы (до алюминия включительно) — и при взаимодействии с водой.
- Металлы, стоящие в ряду правее водорода, с водными растворами кислот-неокислителей при обычных условиях не взаимодействуют.
- При электролизе металлы, стоящие правее водорода, выделяются на катоде; восстановление металлов умеренной активности сопровождается выделением водорода; наиболее активные металлы (до алюминия) невозможно при обычных условиях выделить из водных растворов солей.
Таблица электрохимических потенциалов металлов
| Li | Li+ | -3,0401 | реагирует с водой | выделяется водород |
| Cs | Cs+ | -3,026 | ||
| Rb | Rb+ | -2,98 | ||
| K | K+ | -2,931 | ||
| Ra | Ra2+ | -2,912 | ||
| Ba | Ba2+ | -2,905 | ||
| Fr | Fr+ | -2,92 | ||
| Sr | Sr2+ | -2,899 | ||
| Ca | Ca2+ | -2,868 | ||
| Eu | Eu2+ | -2,812 | ||
| Na | Na+ | -2,71 | ||
| Sm | Sm2+ | -2,68 | ||
| Md | Md2+ | -2,40 | реагирует с кислотами | |
| La | La3+ | -2,379 | ||
| Y | Y3+ | -2,372 | ||
| Mg | Mg2+ | -2,372 | ||
| Ce | Ce3+ | -2,336 | ||
| Pr | Pr3+ | -2,353 | ||
| Er | Er3+ | -2,331 | ||
| Ho | Ho3+ | -2,33 | ||
| Nd | Nd3+ | -2,323 | ||
| Tm | Tm3+ | -2,319 | ||
| Sm | Sm3+ | -2,304 | ||
| Pm | Pm3+ | -2,30 | ||
| Fm | Fm2+ | -2,30 | ||
| Dy | Dy3+ | -2,295 | ||
| Tb | Tb3+ | -2,28 | ||
| Lu | Lu3+ | -2,28 | ||
| Gd | Gd3+ | -2,279 | ||
| Es | Es2+ | -2,23 | ||
| Ac | Ac3+ | -2,20 | ||
| Dy | Dy2+ | -2,2 | ||
| Pm | Pm2+ | -2,2 | ||
| Cf | Cf2+ | -2,12 | ||
| Sc | Sc3+ | -2,077 | ||
| Am | Am3+ | -2,048 | ||
| Cm | Cm3+ | -2,04 | ||
| Pu | Pu3+ | -2,031 | ||
| Er | Er2+ | -2,0 | ||
| Pr | Pr2+ | -2,0 | ||
| Eu | Eu3+ | -1,991 | ||
| Lr | Lr3+ | -1,96 | ||
| Cf | Cf3+ | -1,94 | ||
| Es | Es3+ | -1,91 | ||
| Th | Th4+ | -1,899 | ||
| Fm | Fm3+ | -1,89 | ||
| Np | Np3+ | -1,856 | ||
| Be | Be2+ | -1,847 | ||
| U | U3+ | -1,798 | ||
| Al | Al3+ | -1,700 | ||
| Md | Md3+ | -1,65 | ||
| Ti | Ti2+ | -1,63 | конкурирующие реакции: и выделение водорода, и выделение металла в чистом виде | |
| Hf | Hf4+ | -1,55 | ||
| Zr | Zr4+ | -1,53 | ||
| Pa | Pa3+ | -1,34 | ||
| Ti | Ti3+ | -1,208 | ||
| Yb | Yb3+ | -1,205 | ||
| No | No3+ | -1,20 | ||
| Ti | Ti4+ | -1,19 | ||
| Mn | Mn2+ | -1,185 | ||
| V | V2+ | -1,175 | ||
| Nb | Nb3+ | -1,1 | ||
| Nb | Nb5+ | -0,96 | ||
| V | V3+ | -0,87 | ||
| Cr | Cr2+ | -0,852 | ||
| Zn | Zn2+ | -0,763 | ||
| Cr | Cr3+ | -0,74 | ||
| Ga | Ga3+ | -0,560 | ||
| Ga | Ga2+ | -0,45 | ||
| Fe | Fe2+ | -0,441 | ||
| Cd | Cd2+ | -0,404 | ||
| In | In3+ | -0,3382 | ||
| Tl | Tl+ | -0,338 | ||
| Co | Co2+ | -0,28 | ||
| In | In+ | -0,25 | ||
| Ni | Ni2+ | -0,234 | ||
| Mo | Mo3+ | -0,2 | ||
| Sn | Sn2+ | -0,141 | ||
| Pb | Pb2+ | -0,126 | ||
| H2 | H+ | |||
| W | W3+ | +0,11 | низкая реакционная способность | выделение металла в чистом виде |
| Ge | Ge4+ | +0,124 | ||
| Sb | Sb3+ | +0,240 | ||
| Ge | Ge2+ | +0,24 | ||
| Re | Re3+ | +0,300 | ||
| Bi | Bi3+ | +0,317 | ||
| Cu | Cu2+ | +0,338 | ||
| Po | Po2+ | +0,37 | ||
| Тс | Тс2+ | +0,400 | ||
| Ru | Ru2+ | +0,455 | ||
| Cu | Cu+ | +0,522 | ||
| Te | Te4+ | +0,568 | ||
| Rh | Rh+ | +0,600 | ||
| W | W6+ | +0,68 | ||
| Tl | Tl3+ | +0,718 | ||
| Rh | Rh3+ | +0,758 | ||
| Po | Po4+ | +0,76 | ||
| Hg | Hg22+ | +0,7973 | ||
| Ag | Ag+ | +0,799 | ||
| Pb | Pb4+ | +0,80 | ||
| Os | Os2+ | +0,850 | ||
| Hg | Hg2+ | +0,851 | ||
| Pt | Pt2+ | +0,963 | ||
| Pd | Pd2+ | +0,98 | ||
| Ir | Ir3+ | +1,156 | ||
| Au | Au3+ | +1,498 | ||
| Au | Au+ | +1,691 |
Ссылки
Литература
- Корольков Д.В. Основы неорганической химии. — М.:Просвещение, 1982. — 271 с.
Примечания
- ↑ Рабинович В. Л. Алхимия как феномен средневековой культуры. — М.: Наука, 1979
- ↑ Пути познания / Головнер В.Н. Взгляд на мир глазами химика
- ↑ Штрубе В. Пути развития химии: в 2-х томах. Том 2. От начала промышленной революции до первой четверти XX века
- ↑ Беляев А.И. Николай Николаевич Бекетов – выдающийся русский физико-химик и металлург. М., 1953
- ↑ Леенсон И. А. Ряд активности металлов Бекетова: миф или реальность? // Химия в школе. — 2002. — № 9. — С. 90-96.
- ↑ Мчедлов-Петросян Н. О.Труды Н. Н. Бекетова и ряд активности металлов // Вестник Харьковского национального университета. — 2003. — № 596. — Химия. Вып. 10 (33). — С. 221-225.
ПОИСК
Несмотря на общность основных химических свойств, отдельные металлы довольно сильно отличаются друг от друга своей химической активностью. Металлическая природа элементов проявляется тем ярче, чем слабее связаны валентные электроны с ядром в атомах элементов.
Следовательно, наиболее активными являются металлы главных подгрупп I и II групп периодической системы, так называемые щелочные и щелочноземельные металлы. По той же причине среди элементов одной группы металлическая природа ярче выражена у тяжелых и слабее у легких элементов.
По своей химической активности основные металлы можно расположить в ряд активности [c.112] В вертикальных столбцах таблицы — группах располагаются элементы, обладающие одинаковой валентностью в высших солеобразующих оксидах (она указана римской цифрой).
Каждая группа разделена на две подгруппы, одна из которых (главная) включает элементы малых периодов и четных рядов больших периодов, а другая (побочная) образована элементами нечетных рядов больших периодов. Различия между главными и побочными подгруппами ярко проявляются в крайних группах таблицы (исключая VIII).
Так, главная подгруппа I группы включает очень активные щелочные металлы, энергично разлагающие воду, тогда как побочная подгруппа состоит из меди Си,серебра Ag и золота Аи, малоактивных в химическом отношении.
В VII группе главную подгруппу составляют активные неметаллы фтор F, хлор С1, бром Вг, иод I и астат At, тогда как у элементов побочной подгруппы — марганца Мп, технеция Тс и рения Re — преобладают металлические свойства.
VIII группа элементов, занимающая особое положение, состоит из девяти элементов, разделенных на три триады очень сходных друг с другом элементов, и подгруппы благородных газов. [c.
22]
При химических реакциях металлов с кислотами с атомами металлов происходят следующие превращения а) разрыв связей между атомами в кристалле б) отрыв электрона от нейтрального атома в) взаимодействие полученного иона металла с водой (т. е. гидратация иона металла). Следовательно, если активность отдельного (изолированного) атома определяют лишь по энергии ионизации или потенциала ионизации, то активность твердого металла в реакции с кислотой — по алгебраической сумме энергий ионизации, разрушения кристаллической решетки и гидратации. Чем меньше эта сумма, тем активнее металл реагирует с кислотой. Например, для лития она меньше, чем для натрия, рубидия, калия, а для кальция меньше, чем для натрия. [c.173]
Случаи воспламенения химических продуктов (органических красителей и полупродуктов) происходили при ведении процесса сушки вследствие неправильного выбора теплоносителя.
Поэтому при сушке продуктов, имеющих низкую температуру воспламенения, важнейшим условием является правильный выбор теплоносителя, температура которого не должна превышать опасных пределов.
Форма, размеры и материал оборудования должны быть такими, чтобы на их стенки не налипали органические продукты, так как это может привести к локальным перегревам и воспламенению.
Горючие вещества могут воспламениться при воздействии на них концентрированных азотной и серной кислот активные щелочные металлы (натрий и калий) могут воспламениться при воздействии на них воды. Такие металлы нужно хранить в герметичной таре. [c.338]
Дл51 получения калия, бария, рубидия и цезия электролиз расплавов практически не применяется из-за высокой химической активности этих металлов и больиюй их растворимости в расплавленных солях. Метод электролиза широко используется для получения гидроксидов щелочных элементов. Рассмотрим электролиз водного раствора хлорида натрия с целью получения гидроксида натрия. В ходе электролиза на катоде разряжаются ионы водорода и одновременно вблизи катода накапливаются ионы натрия и гидроксид-ионы, т. е. получается гидроксид натрия на аноде выделяется хлор. Очень важно, чтобы продукты электролиза не смешивались, так как гидроксид натрия легко взаимодействует с хлором в результате образуются хлорид и гипохлорит натрия [c.678]
Ванадий, ниобий и тантал взаимодействуют с кислородом,галогенами, азотом, водородом, углеродом и другими веществами — оксидами, кислотами и т. д.
Однако химическая активность этих металлов проявляется только при высоких температурах, когда разрушается защитная пленка, делающая нх пассивными при обычных условиях.
Особенно прочная пленка образуется иа поверхности тантала, который по химической стойкости не уступает платине. [c.276]
Таким образом, в отличие от периодической системы элементов, ряд напряжений металлов не является отражением общей закономерности, на основе которой можно давать разностороннюю характеристику химических свойств металлов.
Ряд напряжений характеризует лишь окислительно-восстановительную способность электрохимической системы металл — ион металла в строго определенных условиях приведенные в нем величины относятся к водному раствору, температуре 25 °С и единичной концентрации (активности) ионов металла. [c.330]
Опыт 4. Сравнение химической активности щелочных металлов. Кусочек натрия пинцетом бросьте в кристаллизатор с водой, к которой добавлен фенолфталеин. Накройте кристаллизатор стеклом. Наблюдайте течение опыта. Аналогичный опыт проведите с литием и калием. Сопоставьте химическую активность по отношению к воде щелочных металлов. [c.106]
Вследствие высокой химической активности щелочноземельные металлы хранят под керосином в запаянных сосудах (кальций обычно в плотно закрывающихся металлических банках). [c.480]
Носители (трегеры) — пористые термостойкие каталитически неактивные или малоактивные материалы, на которые осаждением, пропитыванием или другими методами наносят катализатор.
При этом достигается тонкое диспергирование катализатора, экономия дорогих металлов, создаются большие удельные поверхности при размерах пор, близких к оптимальным, увеличивается термостойкость. Носитель может взаимодействовать с собственно-каталитическим веществом, повышая его активность.
Химическое участие носителя в катализе пытаются объяснить, используя теорию поля лигандов [26—29]. [c.62]
В природе, как правило, встречаются в чистом виде только благородные металлы (платина, золото, серебро и т. д.), а остальные — в виде соединений с неметаллами (минералы, руды). Причина этого — большая химическая активность (сродство) металлов по отношению к кислороду и другим неметаллическим элементам (сере, хлору, фосфору и т. д.).
Свидетельством этого является то, что изобарно-изотермический потенциал у окислов, сульфидов, сульфатов, хлоридов металлов меньше, чем у элементов металла и неметалла, взятых в отдельности. Например, при образовании РегОз из отдельных элементов свободная энергия (в ккал/моль) уменьшается на 177, АЬОз — на 377, 2пО — на 76. [c.
10]
Лабораторное испытание активности Химический состав Анализ следов металлов Измерение поверхности металла по адсорбции газов [c.48]
Восстановительные свойства элементарных металлов под-груипы хрома усиливаются от вольфрама к хрому, однако эти металлы химически менее активны, чем металлы, рассмотренные в [c.281]
Таким образом, химическая активность различных металлов разная. Она определяется способностью атомов металла отдавать валентные электроны. По своей активности все металлы располагаются в определенной последовательности, образуя электрохимический ряд напряжений металлов (см. гл. V, 11). [c.260]
Физические и химические свойства. Бериллий — серебристо-белого цвета, отличается твердостью п хрупкостью. В отличие от многих металлов он — диамагиетнк. На воздухе бериллий покрывается тонким слоем оксида, предохраняющим от коррозии (как и алюминий).
Из элементов ПА-группы бериллий наименее активен, а потому отрицательное значение его стандартного электродного потенциала наименьшее. Следует также отметить близость этой характеристики для Ве ( -=—1,7) и А1 (Е >=—1,67 В), т. е.
по химической активности эти металлы очень близки. Бериллий растворяется в разбавленных щелочах п кислотах, в том числе в HF.
С водородом бериллий непосредственно не взаимодействует, при нагревании реагирует с галогенами, в атмосфере кислорода сгорает, при повышенных температурах взаимодействует с азотом и серой. [c.126]
Мухутдинов Р.Х., Самойлов H.A., Перлов P.A. О химическом взаимодействии каталитически активных оксидов металлов катализаторного покрытия с кремнийорганическим адгезивом // Современные химические технологии очистки воздушной среды. Саратов Изд-во СГУ, 1992. С. 47. [c.243]
При прохождении тяжелых ядер, разогнанных до больших значений энергии, в объеме любых непроводящих материалов образуются треки (в металлах и полупроводниках они не образуются). В частности, в полимерах по пути прохождения частиц разрываются полимерные цепи и появляются активные химические группы.
Не обнаруживаемые даже электронной микроскопией деструктивные изменения можно усилить ультрафиолетовым облучением пленки. Различия в химической активности полимера на поверхности и по траектории частиц проявляются при травлении пленки.
В зависимости от используемого полимера под воздействием щелочи или окислителя в пленке образуются каналы цилиндрической формы. Для облучения полимера используют тяжелые осколки, образующиеся при делении Наиболее совершенная технология получения ядерных фильтров разработана Г. Н. Флеровым с сотр.
, предложившими облучать пленки ускоренными на циклотроне ионами ксенона. Так как все ионы Хе в циклотронном пучке обладают одинаковой энергией, то все поры, образующиеся после травления щелочью или окислителем, должны обладать одинаковыми размерами.
В промышленном масштабе выпускаются поликарбонатные или лавсановые ядерные фильтры с размерами пор от 0,05 до [c.25]
Одинакова ли химическая активность щелочных металлов и от чего она зависит [c.268]
Кажущееся различие между активностью некоторых металлов в ряду напряжений и положением их в периодической системе связано с разной мерой химической активности в том и другом случае (соответственно с изменением ДО в процессе перехода [c.254]
Становится понятным й качественный скачок в свойствах элементов при переходе от периода к периоду. Так, каждый период (кроме первого, сверхмалого) заканчивается инертным элементом со структурой пр .
Следующий же период п + 1) возникает в результате образования нового электронного слоя, причем первым элементом этого периода является более активный щелочной металл с конфигурацией внешнего электронного слоя (п + 1) Последний же член периода имеет конфигурацию (п — — 1) р . Следовательно, переход от младшего периода ( ) к старшему п + 1) характеризуется изменением числа электронных оболочек атомов и их структуры. Это и приводит к скачкообразному изменению химических свойств элементов старшего периода по сравнению с соответствующими элементами младшего периода. [c.54]
Сопоставление рис. ХП.2 и ХП.З показывает, что электронное строение внешней оболочки атомов элементов следующих за неоном в точности повторяет строение атомов, предшествующих ему, т. е. второго периода. Так, натрий имеет во внешнем слое один электрон подобно литию. Химические свойства этих элементов сходны они являются активными одновалентными металла- [c.150]
Как изменяется химическая активность щелочных металлов и склонность к образованию ионных связей [c.89]
Химическая активность этих металлов невелика и уменьшается от меди к золоту. [c.259]
Цинк — активный металл, легко растворяется в кислотах, его соединения слабо амфотерны.
При переходе к ртути основные свойства соединений несколько усиливаются, но химическая активность свободного металла резко падает.
Ртуть интересна тем, что является единственным жидким металлом при нормальных условиях, встречается в самородном виде. Пары кадмия и ртути очень ядовиты. [c.160]
Соединения (1-металлов VII группы с азотом, углеродом, бором и кремнием.
Вследствие устойчивости наполовину законченного подуровня с1 и пониженной химической активности для -металлов УП группы не характерно образование металлообразных соединений. Лишь силициды этих металлов проявляют электронную проводимость.
Проводимость по местам анионных вакансий возможна, так как нитриды, карбиды и другие соединения -металлов обладают значительной широтой области гомогенности. [c.359]
Химическая активность атомов в свободном состоянии зависит от одних причин (заряд ядра, характеристика атомного остова, валентных электронов, наличия вакантных оэбиталей), а для атомов в связанном состоять — еще и от типа химической связи, типа кристаллической реи[етки. Вот почему в различных рядах активности положение отдел ,ных элементов может меня гъся. Например, восстановительная активность щелочных металлов в расплавах изменяется в одной последовательности [c.64]
Учение о периодичности в сочетании с учением о строении вещества позволило раскрыть содержание и определить характер причинно-следственных связей в химии зависимость свойств веществ от их состава и строения. Одним из важнейших свойств элементов является химическая активность.
Как известно, наибольшей химической активностью обладают щелочные металлы, галогены и кислород. Положение указанных элементов в системе и строение их атомов позволило установить причины их высокой активности, а также содержание самого понятия.
В данном случае под активностью подразумевается восстановительная активность щелочных металлов как простых веществ и окислительная активность двухатомных молекул галогенов, кислорода. [c.44]
Очень высокая химическая активность щелочных металлов обусловлена низким ПИ], низкой температурой плавления, рыхлой, легко разрушаемой кристаллической структурой, малой плотностью.
Все эти, а также многие другие характеристики ЩЭ в металлическом состоянии взаимно связаны, и общей причиной уникальных свойств ЩМ, конечно, является их особая электронная структура — наличие только одного электрона на электронной оболочке с главным квантовым числом п и поэтому очень непрочной, легко разрушаемой. [c.12]
Вследствие высокой химической активности щелочные металлы разлагают воду с образованием гидроксидов [c.294]
Химические свойства -металлов VI группы. -Металлы VI группы менее активны, чем металлы III. IV и V групп, однако, особенно [c.343]
Стандартный потенциал растворения является объективной мерой химической активности данного металла. [c.233]
Точных данных о механизме ингибирования нет. Предполагают, что играет роль сорбция ингибитора на активных центрах металла. Одним из первых ингибиторов коррозии был экстракт опийного мака, полученный сотрудниками химического факультета Московского университета в начале Великой Отечественной войны.
Бурый экстракт (ингибитор) добавляли к сильной минеральной кислоте в его присутствии заржавевшие металлические детали очищались от слоя ржавчины, становились блестящими. При этом раст1ворялся только окисел железа, а металл с кислотой не реагировал вследствие ингибирования. [c.
119]
Взаимодействие с элементарными окислителями. Химическая активность 5-металлов ПА-группы заметно ниже, чем 5-металлов 1А-1 руппы, но все металлы ПА-группы сохраняют высокие восстановительные свойства. [c.300]
Однофазные сплавы, представляющие собой химическое соединение или твердый раствор двух различных металлов, ведут себя при анодной поляризации как единое целое.
Активность электроотрицательното металла в таком сплаве, как правило, оказывается ниже, чем в свободном состоянии, а потенциал анодного растворения сплава устанавливается в промежутке между потенциалами оонов ных компонентов (обычно ближе к более отрицательному).
В зависимости от особенностей системы и условий электрошиза установится и соотношение, в кото- [c.407]
Ряд электронофильностн ( благородства , химической активности) избранных металлов [c.303]
Si02. Обычно они встречаются как примеси к другим горным породам. Получению S , Y и La предшествует концентрация сырья, или обогащение. Высокая химическая активность этих металлов затрудняет их получение в свободном виде. Их выделяют электролизом расплавленных галидов. [c.323]






