Металлами называют химические элементы, обладающие в твердом состоянии характерными физическими свойствами: высокой тепло-и электропроводностью, пластичностью, отражающей способностью. «Металлы — суть светлые тела, которые ковать можно» (М.В. Ломоносов).
К металлам относятся 3/4 химических элементов периодической системы Д. И. Менделеева.Чистые металлы обладают сравнительно невысокими прочностью и твердостью, поэтому в технике применяются металлические сплавы.
Сплавами называют металлические тела, состоящие из нескольких металлов (иногда неметаллов).
Металлы и сплавы играли и играют важную роль в развитии техники и цивилизации. Например, изготовление бронзы — сплава меди с оловом — открыло новую эпоху в развитии материальной культуры, которая названа «бронзовым веком». Большинство металлов, находящихся в литосфере, образуют различные химические соединения.
Вопросами извлечения металлов из природного сырья (руды) занимается металлургия.Металлы играют важную роль также и в современной технике, при этом используются практически все металлы, встречающиеся в литосфере.Все металлы и сплавы в твердом состоянии являются кристаллическими телами.
Высокие прочность, теплопроводность, электропроводность, пластичность металлов обусловлены характером химической связи. В кристаллической структуре металла некоторая часть электронов слабо связана с атомами и может перемещаться по металлу (свободные электроны).
Строение металлов может быть представлено моделью, в которой каркас из положительно заряженных атомов погружен в «электронный газ», который компенсирует силы отталкивания между ионами (металлическая связь).
Все металлы и сплавы на их основе подразделяют на черные (железо и сплавы на его основе) и цветные.
К цветным относят все остальные металлы. Цветные (нежелезные) металлы разделяют на группы в зависимости от физических свойств: легкие (литий, магний), тяжелые (медь, свинец, олово), тугоплавкие (вольфрам, молибден), благородные (золото, платина и др.), рассеянные (галлий, индий и др.), редкоземельные (скандий, лантан и др.
), радиоактивные (радий, уран и другие). Лишь немногие металлы содержатся в земной коре в значительном количестве. Кварки металлов (содержание в литосфере в процентах): Al — 8,8 %; Fe — 4,65 %; Mg — 2,1 %; Ti — 0,63 %.
В строительстве применяются сплавы на основе железа (чугун и сталь), а также сплавы на основе меди, алюминия, магния, титана, цинка (бронза, латунь, авиаль, дуралюмин и др.).
Кристаллическая структура металлов
В твердом состоянии металлы и металлические сплавы имеют кристаллическую структуру. Большинство металлов образуют кристаллические структуры: кубическую объемно-центрированную, кубическую гранецентрированную и гексагональную. Многие металлы, в зависимости от условий, образуют две и более кристаллических модификации (полиморфных форм).
Например, железо образует две кристаллические структуры:При повышении температуры или охлаждении железа полиморфные переходы происходят в последовательности:Температуры фазовых переходов определяются методом термического анализа. В расплав вводят термопару и регистрируют изменение температуры при охлаждении или нагревании в системе координат температура — время. Фазовые переходы отражаются на кривых охлаждения (или нагревания) временным замедлением скорости изменения температуры — температурными остановками (рис. 13.1). Рисунок свидетельствует о четырех фазовых переходах при нагревании и охлаждении железа, то есть о полиморфизме железа.Реальные кристаллические структуры отличаются от идеальных тем, что содержат различные дефекты: точечные (вакансии), одномерные (дислокации), двумерные (поверхностные), дефекты зерен, поверхность раздела фаз.Металлы и сплавы, которые применяют в технике, являются телами поликристаллическими, то есть состоящими из большого количества монокристаллов. Свойства металлов зависят не только от физических свойств их атомов, но и от микро- и макроструктуры, поэтому механические свойства металлов могут существенно отличаться от свойств отдельных кристаллов этого металла. Изменение и разнообразие свойств металлов и сплавов, применяемых в технике, достигается путем варьирования фазового состава, морфологии отдельных зерен, расположения зерен, строения межфазовых границ.Как было отмечено, сплавы состоят из нескольких металлов (компонентов сплава). При переходе сплава из жидкого в твердое состояние возможно образование твердых растворов, химических соединений и механических смесей компонентов, содержащихся в расплаве.
Твердые растворы
Твердыми растворами называют сплавы, в которых атомы различных металлов распределены в определенных пределах или неограниченно в общей кристаллической структуре. Растворимость в твердом состоянии характерна для всех кристаллических веществ.Примесные атомы, или атомы легирующего элемента, могут образовывать с матрицей основного кристалла твердые растворы замещения или твердые растворы внедрения. Твердые растворы замещения образуются теми атомами, которые имеют близкие по размерам радиусы (различие не превышает 15 %). Электрохимические твердые растворы внедрения образуются, когда размеры атомов компонентов существенно различаются и возможно внедрение атомов одного компонента в пустоты между атомами другого компонента. Например, углерод образует с железом твердые растворы внедрения, в которых атомы С, имеющие радиус 0,77 А, размещены между атомами Fe (между узлами кристаллической структуры), атомный радиус которого составляет 1,26 А.Химические соединенияОбразуются путем химического взаимодействия компонентов с появлением нового химического соединения (вещества). Соединение образует новую кристаллическую структуру, отличную от структур исходных металлов, и обладает индивидуальными физическими свойствами.
Механические смеси
Образуются при одновременной кристаллизации из расплава нескольких компонентов (механическая смесь или эвтектика). Эвтектики могут состоять из чистых компонентов, твердых растворов, химических соединений.Кристаллизация сплавов, имеющих сложное строение, может идти одновременно по трем названным выше вариантам.
Поведение сплавов при нагревании и охлаждении удобно изучать по диаграммам состояния, которые отражают в обобщенном виде результаты исследования процессов кристаллизации и структурно-фазовых превращений в системе. Диаграммы содержат данные о температурах начала и конца кристаллизации расплава, фазовых превращениях при нагревании и охлаждении и др.
Построение диаграмм состояния производится на основании результатов исследований сплавов методами химического, термического, микроскопического и других анализов.В зависимости от характера протекающих физико-химических процессов различают четыре типа диаграмм состояния двухкомпонентных (бинарных) систем.Методику построения удобно рассматривать на диаграмме состояния 1-го типа (рис.13.3), когда компоненты бинарной системы неограниченно растворяются в жидком состоянии, не растворяются в твёрдом и образуют механическую смесь кристаллов (эвтектику). Система исследуется методом термического анализа. На графиках, отражающих характер изменения температуры при нагревании и охлаждении бинарной системы, имеются две температурных остановки (рис. 13.2). Первая температурная остановка на графике называется температурой начала кристаллизации (а), вторая — температурой конца кристаллизации (b). Если приготовить смеси с различным содержанием компонентов и выполнить термический анализ, то можно увидеть, что температура начала кристаллизации является величиной переменной, она зависит от концентрации компонентов. Температура конца кристаллизации от состава смеси не зависит. Далее полученные температурные остановки (критические точки) следует перенести на диаграмму состояния бинарной системы 1-го типа. Диаграмма строится в системе координат температура — концентрация компонентов. На диаграмме линии (t1 E) и (Е t2) соответствуют температурам начала кристаллизации сплава (линия ликвидуса), а линия (t3 E) — температуре конца кристаллизации (линия солидуса). Сплав, который кристаллизуется при температуре конца кристаллизации называется эвтектическим сплавом, или эвтектикой, и соответствует точке E на диаграмме.Выше линии ликвидуса (t1 E t2) сплав находится в жидком состоянии, ниже линии солидуса (t3 E t3) — кристаллический сплав. Слева от точки E кристаллизация начинается с выделения из расплава кристаллов компонента А. В интервале температур сплав состоит из кристаллов компонента А и жидкой фазы. При понижении температуры содержание компонента А в жидкой фазе понижается по кривой (t1 E). Если перенести точку, соответствующую заданной температуре, на линию ликвидуса и далее на ось концентраций, можно определить состав жидкой фазы. Кристаллизация расплава заканчивается в точке E образованием механической смеси (эвтектики), состоящей из кристаллов компонентов А и В. В твердом состоянии сплав имеет неравномерно-зернистую кристаллическую структуру, содержит сравнительно крупные кристаллы компонента А и мелкокристаллическую эвтектику.Кристаллизация сплава, состав которого находится справа от точки Е, начинается с выделения кристаллов компонента В и заканчивается образованием эвтектики.Кристаллизация эвтектического сплава, соответствующего точке Е, происходит при минимальной для данной системы температуре.На диаграмме (рис. 13.3) t1 и t2 — температуры кристаллизации чистых компонентов А и В.Диаграмма состояния позволяет определить фазовый состав и структуру сплава при заданной температуре.Если компоненты бинарной системы образуют химическое соединение, устойчивое в рассматриваемом интервале температур, то диаграмму можно считать составленной из двух диаграмм 1-го типа, так как химическое соединение можно рассматривать как независимый компонент (рис. 13.4).Диаграмма состояния 2-го типа — компоненты обладают полной растворимостью в жидком и твёрдом состоянии (рис. 13.5). На дианрамме t1 и t2 — температуры плавления чистых компонентов A и В. Выше линии ликвидуса (t1 С t2) сплав находится в жидком состоянии, ниже солидуса (t1 D t2) — в твердом. При охлаждении расплава, соответствующего точке К до температуры t3, начинается выделение кристаллов твердого раствора. Состав кристаллов можно определить, если провести линию параллельную оси абсцисс до линии солидуса, состав кристаллов соответствует точке t4. Следовательно, выделяющиеся кристаллы будут содержать повышенное количество компонента с более высокой температурой плавления. При дальнейшем понижении температуры состав жидкой фазы будет изменяться по кривой (t3 С t1), а состав выделяющихся кристаллов по кривой (t4 D t1), то есть из расплава выделяются кристаллы твердого раствора компонента В в компоненте А переменного состава.Диаграмма состояния 3-го типа — компоненты неограниченно растворяются в жидком состоянии и ограниченно — в твердом (рис. 13.6). Выше линии ликвидуса (t1 E t2) — компоненты находятся в жидком состоянии, ниже линии солидуса (t1 C E D t2) — в твердом. В области II существуют кристаллы твердого раствора компонента В в компоненте А и жидкий сплав; в области III — кристаллы твердого раствора компонента А в компоненте В и жидкий сплав; в области IV — твердые ненасыщенные растворы компонента В в компоненте А и; в области V — твердые ненасыщенные растворы компонента А в компоненте В; в области VI — совместное существование кристаллов твердого насыщенного раствора В в А и эвтектики, смеси кристаллов твердых растворов В в А и А в В; в области VII — совместное существование твердого насыщенного раствора А в В и эвтектики.Максимальная растворимость компонента В в компоненте А в твердом состоянии соответствует точке С, а компонента А в компоненте В — точке D. С понижением температуры растворимость компонента В в компоненте А понижается по линии (С F), поэтому из твердого раствора выделяется компонент В в виде вторичного твердого раствора компонента В в компоненте А. По линии (D К) выпадает вторичный твердый раствор компонента А в компоненте В. В точке E образуется эвтектика — смесь кристаллов твердых растворов В в А и А в В.В системе железо — углерод образуется химическое соединение — Fe3C, карбид железа (цементит). Диаграмма состояния железо — цементит широко используется в практике. По диаграмме можно судить о структуре медленно охлажденных сплавов, а также об изменении структуры в зависимости от температуры и содержания углерода в сплаве (рис. 13.7).Основными структурами и структурными составляющими сплавов в системе Fe — Fe3C являются:
Феррит — твердый раствор углерода в aFe, максимальное содержание углерода при 727 °C — 0,02 %, существует при температуре ниже 911 °C.
Аустенит — твердый раствор углерода в γFe, существует при температуре выше 727 °C; ниже этой температуры распадается на феррит и цементит. Углерод образует твердый раствор внедрения. Максимальная растворимость углерода в γFe — 2,14 % (точка С на диаграмме).Цементит — карбид железа Fe3C, содержит 6,67 % углерода, обладает высокой твердостью и хрупкостью. При медленном охлаждении сплава распадается с образованием феррита и графита.Перлит — эвтектоидная смесь феррита и цементита, образуется при распаде аустенита при температуре 723 °C и содержании углерода — 0,83 %.Ледебурит — эвтектическая смесь аустенита и цементита, образующаяся при 1130 °C и содержании углерода 4,3 % (точка Е). Ледебурит твёрд, хрупок, при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит.Графит — образуется при распаде цементита на феррит и графит. Встречается в серых и ковких чугунах.Диаграмма состояния Fe — Fe3C (рис. 13.7) более всего похожа на диаграмму 3-го типа (рис. 13.6) для компонентов, обладающих ограниченной растворимостью в твердом состоянии.На диаграмме состояния Fe — Fe3C точка А соответствует температуре плавления железа и точка В — температуре плавления цементита. (AEB) -линия ликвидуса, в области I — жидкий сплав. (ACED) — линия солидуса. В области III существуют кристаллы первичного цементита и жидкий сплав, в области II — кристаллы аустенита переменного состава и жидкий сплав. По линии (С E D) кристаллизуется эвтектический сплав состава, соответствующего точке E; ледебурит состоит из кристаллов аустенита (твердого раствора углерода в γFe) и кристаллов первичного цемента, содержание углерода — 4,3 %.При температуре, соответствующей линии солидуса, сплавы можно разделить на три группы:1. 0-2,0 % С — аустенит, область IV на диаграмме (рис. 13.7).2. 2,0-4,3 % С — аустенит + ледебурит (эвтектика), область IX.3. 4,3-6,67 % С — первичный цементит + ледебурит, область X.Превращения в системе Fe — Fe3C, протекающие при дальнейшем понижении температуры (ниже линии солидуса), обусловлены понижением растворимости углерода в γFe и превращением γFe → aFe.По линии (G S) из аустенита выделяется aFe (феррит). Феррит выделяется, когда содержание углерода в сплаве не превышает 0,9 %. При более высоком содержании углерода выделяется цементит по линии (S С) (вторичный цементит). В точке S аустенит распадается на смесь мелких кристаллов феррита (αFe) и цементита, которая называется эвтектоидной смесью (эвтектоидом). Структура, соответствующая эвтектоидной смеси, называется перлитом, содержание углерода — 0,83 %.Сплавы, содержащие до 2 % углерода, называют сталью, сплавы, содержащие от 2 до 6,67 % С, — чугуном. Чугуны и стали обладают различающимися физическими свойствами и областью применения в строительстве.
Лекция № 5. сплавы / материаловедение: конспект лекций
Металлы и их сплавы – основной материал в машиностроении.
Они обладают многими ценными свойствами, обусловленными в основном их внутренним строением. Мягкий и пластичный металл или сплав можно сделать твердым, хрупким, и наоборот. Для того чтобы сознательно изменять свойства металлов, необходимо знать основы их кристаллического строения.
Как известно, все тела состоят из большого количества атомов, которые удерживаются силами сцепления, совершая колебания большой частоты возле точек равновесия. Поскольку атомы разных металлов различны, каждый металл имеет свои определенные свойства. Эти свойства зависят от расположения атомов между собой, характера их связей, от расстояния между ними.
Если изменить расстояние между атомами или порядок их расположения, изменятся и свойства металла. В аморфных телах – смоле, стекле, канифоли и т. п. – атомы расположены беспорядочно. В металлах они находятся в определенном геометрическом порядке, образуя кристаллы, поэтому металлы являются кристаллическими телами.
Металлы различаются не только порядком расположения атомов, но и кристаллической решеткой, которая представляет собой воображаемую пространственную сетку, состоящую из элементарных ячеек, в узлах которой находятся атомы.
Различают следующие кристаллические решетки металлов с плотной упаковкой атомов: кубическую объемно—центрированную, кубическую гранецентрированную и гексагональную.
В ячейке кубической объемно—центрированной решетки атомы расположены в вершинах и центре куба.
Такая ячейка содержит девять атомов (хром, вольфрам, ванадий, молибден, литий, а при определенных температурах – железо и другие металлы).
В ячейке кубической гранецентрированной решетки атомы находятся в вершинах куба и на пересечении диагоналей каждой плоскости. Такая ячейка имеет 14 атомов (свинец, никель, медь, золото, серебро, пластина, железо при определенных температурах и другие металлы).
В ячейке гексагональной кристаллической решетки атомы располагаются в вершинах и в центре шестигранных оснований призмы, а три атома – в средней ее плоскости, при этом такая ячейка содержит 17 атомов (магний, цинк, кадмий, осмий, бериллий и другие металлы).
При определенных условиях некоторые металлы – железо, титан, цирконий, стронций, кобальт, кальций и другие могут перестраиваться из одного вида кристаллической решетки в другой, например из кубической объемно—центрированной – в гранецентрированную и даже гексагональную. Элементарная ячейка отображает только один элемент, или одну ячейку, кристаллической решетки.
Вся кристаллическая решетка в реальном металле состоит из большого числа многократно повторяющихся элементарных ячеек.
Большое значение имеет расстояние между атомами ячейки кристаллической решетки или между параллельными атомными плоскостями, образующими элементарную ячейку. Чем больше это расстояние, тем менее прочен металл.
Расстояние между ними измеряется в ангстремах – 1 А = = 10 –8 см или в нанометрах – 1 А = 0,1 нм.
Из практики известно, что железо прочнее меди, а медь прочнее алюминия.
Порядок расположения атомов – тип кристаллической решетки – природное свойство металла, форма кристаллов и их размеры зависят от процесса перехода металла из жидкого состояния в твердое.
Процесс образования кристаллов при затвердевании металлов называется кристаллизацией. При кристаллизации металлов выделяется тепло, а при переходе металлов из твердого состояния в жидкое происходит поглощение тепла.
Наблюдения с помощью измеряющих температуру проборов за процессом понижения температуры
при переходе металла из жидкого состояния в твердое позволили установить определенную закономерность. Сначала температура понижается равномерно. В начальный период образования кристаллов вследствие выделения скрытой теплоты при формировании кристаллической решетки падение температуры прекращается, и она остается неизменной до полного затвердения металла.
После того как весь металл затвердеет, температура снова начинает понижаться. Температура, соответствующая горизонтальной площадке, называется критической. Кристаллизация металлов подобна кристаллизации солей, и этот процесс состоит из двух элементарных процессов, протекающих одновременно.
Первый заключается в образовании центров кристаллизации, или зародышей кристаллов, второй – в росте кристаллов из этих центров.
Первый этап – появление зародышей кристаллов металла.
Второй этап – по мере остывания металла к зародышам присоединяются все новые и новые атомы жидкого металла, которые группируются в определенном порядке один возле другого, образуя элементарные ячейки кристаллической решетки.
Этот процесс продолжается до тех пор, пока не закончится кристаллизация. Причем кристаллы затвердевшего металла имеют неправильную и весьма разнообразную форму, что объясняется условиями кристаллизации.
В процессе кристаллизации увеличивается количество кристаллов – в 1 мм 3 может образоваться свыше 1000 кристаллов. Кристаллы, имеющие неправильную внешнюю форму, называются кристаллитами, или зернами.
Чистые металлы относительно редко применяются в машиностроении и других отраслях хозяйственного комплекса. Более широко используются сплавы, состоящие из двух и более элементов (из двух металлов, например меди и цинка, или из металла и неметалла, например железа и углерода).
Элементы, входящие в сплав, называются компонентами. В зависимости от расположения атомов в кристаллической решетке различают твердые растворы замещения и твердые растворы внедрения.
В твердом растворе замещения атомы растворимого компонента замещаются атомами растворителя, а в твердом растворе внедрения атомы растворителя размещаются между атомами растворимого компонента в наиболее слабых местах элементов кристаллической решетки.
Сплавы, представляющие собой твердые растворы, отличаются ценными свойствами. Они тверже и прочнее, чем входящие в него компоненты.
Компоненты некоторых сплавов при кристаллизации могут входить в химическую связь, образуя химическое соединение. Химические соединения обладают очень высокой твердостью и хорошим электросопротивлением.
Под диффузией понимают перемещение атомов в кристаллическом теле на расстояния, превышающие средние межатомные расстояния данного металла. Если перемещения атомов не связаны с изменением концентрации в отдельных объемах, то такой процесс называется самодиффузией.
Диффузия, сопровождающаяся изменением концентрации, называется гетеродиффузией. В тех случаях, когда гетеродиффу—зия сопровождается образованием новых фаз, что наиболее часто имеет место при химико—технической обработке, она называется реактивной диффузией.
В основе процесса диффузии лежит атомный механизм, при котором каждый атом совершает более или менее случайные блуждания. Диффузионные превращения в металлах происходят при различных химико—термических обработках – хромировании, цементации, алютировании (алюминирование) и т. д.
Хромирование обеспечивает повышенную жаростойкость стали до 800 °C, высокую коррозионную стойкость в таких средах, как пресная и морская вода, уксусная и фосфорная кислоты, и эрозионную стойкость при низкой и высокой температурах.
Хромирование сталей, содержащих более 0,3–0,4 % углерода, повышает также твердость и износостойкость. При хромировании диффузионный слой состоит из раствора хрома в? – железе, а содержание хрома на поверхности составляет 25–50 %.
При этом процессе в случае применения CrCl 2 протекает следующая реакция:
CrCl 2 + Fe > FeCl 2 + Cr.
При термической обработке стали наблюдаются бездиффузные, или аллотропические, превращения в процессе вторичной кристаллизации. В частности, при температуре +775 °C в стали, содержащей 0,6 % углерода, начинаются аллотропические превращения, т. е. выделение феррита из аустенита (твердого раствора углерода (до 2,14 %)) и других примесей в объеме железа.
Феррит – твердый раствор небольшого количества углерода (до 0,04 %) и других примесей в? – железе – мягкая, пластичная и недостаточно прочная структурная составляющая.
Так как в феррите содержится ничтожное количество углерода, оставшийся аустенит будет постепенно, по мере выделения феррита, обогащаться углеродом.
Когда концентрация углерода в оставшемся аустените достигнет 0,8 %, при температуре +727 °C сталь, содержащая 0,6 % углерода, будет иметь в своем составе феррит и аустенит, а при температурах ниже +727 °C – феррит и перлит, причем структура феррит – перлит сохранится без значительных изменений и при дальнейшем охлаждении стали вплоть до комнатной температуры. Аналогичные превращения характерны для всех доэвтек—тоидных сталей (содержащих менее 0,8 % углерода). Разница будет лишь в температурах начала выделения феррита. Причем, если сталь содержит 0,8 % углерода, ее вторичная кристаллизация будет протекать при постоянной температуре (+727 °C) и сопровождаться только одним процессом – образованием перлита. Это объясняется тем, что в данном случае содержание углерода в стали соответствует эвтектоидному составу – механической смеси кристаллов, выделяющихся из жидкого сплава одновременно. При этом создается мелкозернистая структура сплава.
Сталь и чугун – основные материалы в машиностроении. Они составляют 95 % всех используемых в технике сплавов.
Сталь – это сплав железа с углеродом и другими элементами, содержащий до 2,14 % углерода. Углерод – важнейшая примесь стали. От его содержания зависят прочность, твердость и пластичность стали. Кроме железа и углерода, в состав стали входят кремний, марганец, сера и фосфор. Эти примеси попадают в сталь в процессе выплавки и являются ее неизбежными спутниками.
Чугун – сплав на железной основе. Отличие чугуна от стали заключается в более высоком содержании в нем углерода – более 2,14 %. Наибольшее распространение получили чугуны, содержащие 3–3,5 % углерода. В состав чугунов входят те же примеси, что и в стали, т. е. кремний, марганец, сера и фосфор.
Чугуны, у которых весь углерод находится в химическом соединении с железом, называют белыми (по виду излома), а чугуны, весь углерод которых или большая его часть представляет графит, получили название серых. В белых чугунах всегда имеется еще одна структурная составляющая – ледебурит. Это эвтектика, т. е.
равномерная механическая смесь зерен аустенита и цементита, получающаяся в процессе кристаллизации, в ней 4,3 % углерода. Ледебурит образуется при температуре +1147 °C.
Феррит – твердый раствор небольшого количества углерода (до 0,04 %) и других примесей в? – железе. Практически это чистое железо. Цементит – химическое соединение железа с углеродом – карбид железа.
Перлит – равномерная механическая смесь в сплаве феррита и цементита. Такое название эта смесь получила потому, что шлиф при ее травлении имеет перламутровый оттенок. Так как перлит образуется в результате процессов вторичной кристаллизации, его называют эвтектоидом. Он образуется при температуре +727 °C. В нем содержится 0,8 % углерода.
Перлит имеет две разновидности. Если цементит в нем расположен в виде пластинок, его называют пластинчатым, если же цементит расположен в виде зерен, перлит называют зернистым. Под микроскопом пластинки цементита кажутся блестящими, потому что обладают большой твердостью, хорошо полируются и при травлении кислотами разъедаются меньше, чем пластинки мягкого феррита.
Если железоуглеродистые сплавы нагреть до определенных температур, произойдет аллотропическое превращение ? —железа в ? —железо и образуется структурная составляющая, которая называется аустенитом.
Аустенит представляет собой твердый раствор углерода (до 2,14 %) и других примесей в ? —железе. Способность углерода
растворяться в железе неодинакова при различных температурах. При температуре +727 °C ? —железо может растворять не более 0,8 % углерода. При этой же температуре происходит распад аустенита с образованием перлита. Аустенит – мягкая структурная составляющая. Он отличается большой пластичностью, не обладает магнитными свойствами.
При изучении структурных составляющих железоуглеродистых сплавов установлено, что они при комнатной температуре всегда состоят из двух структурных элементов: мягкого пластичного феррита и твердого цементита, упрочняющего сплав.
Сплавы можно получать при соединении большинства металлов друг с другом, а также с неметаллами. Диаграммы состояния сплавов дают наглядное представление о протекающих в сплавах превращениях в зависимости от их химического состава и температуры.
При построении диаграмм состояния сплавов на оси абсцисс указывают химический состав или концентрацию сплава в процентах. Для этого горизонтальную линию определенной длины делят на сто одинаковых частей и каждое деление принимают за 1 % одного из компонентов сплава.
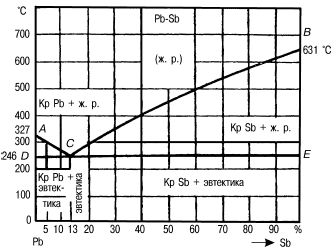
Рис. 5. Диаграмма состояния сплавов системы свинец—сурьма (Pb—Sb)
Точка А соответствует чистому свинцу, а точка В – чистой сурьме. По оси ординат в определенном масштабе указывают температуру. Для того чтобы построить диаграмму состояния сплавов, сначала строят ряд кривых охлаждения сплавов одних и тех же элементов с различной концентрацией.
На основе этих кривых строят диаграмму. Сплавы, компоненты которых при затвердевании образуют только механические смеси, относятся к первой группе.
Диаграмма этих сплавов условно называется диаграммой состояния первого рода. Диаграмма сплавов, образующих при затвердевании только твердые растворы, называется диаграммой состояния второго рода.
Наиболее типичными для диаграмм первого рода являются сплавы свинца с сурьмой.
- Построение диаграммы (первого рода) состояния сплавов Pb—Sb:
- 1) кривые охлаждения доэвтектических сплавов;
- 2) диаграмма состояния сплавов Pb—Sb;
- 3) кривые охлаждения заэвтектических сплавов. Диаграмма построена для пяти видов сплава свинца с сурьмой:
- 1) 5 % сурьмы и 95 % свинца;
- 2) 10 % сурьмы и 90 % свинца;
- 3) 20 % сурьмы и 80 % свинца;
- 4) 40 % сурьмы и 60 % свинца;
- 5) 80 % сурьмы и 20 % свинца.
Все они имеют две критические температуры: верхнюю и нижнюю.
Изучение процессов кристаллизации этих сплавов показывает, что верхняя критическая температура соответствует началу, а нижняя – концу затвердевания сплава.
Таким образом, процесс кристаллизации сплавов Pb—Sb резко отличается от кристаллизации чистых металлов. Сплавы кристаллизуются в интервале температур, а чистые металлы – при постоянной температуре.
Механическая смесь кристаллов, выделяющихся из жидкого сплава одновременно, называется эвтектикой (в переводе с греческого – «хорошо сложенный»). Сплавы указанной концентрации называют эвтектическими.
Линия АСВ на диаграмме называется линией ликвидуса (в переводе с греческого – «жидкий»). Выше этой линии любой сплав свинца с сурьмой находится в жидком состоянии.
Линия ДСВЕ получила название линии солидуса (в переводе с греческого – «твердый»), или эвтектической линии. Точка С показывает состав эвтектики. Сплавы, расположенные левее этой точки, называют доэвтектическими, правее ее – заэвтектическими.
В структуре доэвтектических сплавов, кроме эвтектики, всегда есть некоторое количество свинца, а в заэвтектических, кроме эвтектики, – сурьмы.
3. СТРУКТУРА СПЛАВОВ
Строение металлических сплавов зависит от того, в какие взаимодействия вступают компоненты, их образующие. Под структурой, как уже указано ранее, понимают форму, размеры и характер взаимного расположения фаз в сплаве. Структура сплава выявляется микроанализом.
При полной взаимной растворимости компонентов в твердом состоянии микроструктура всех сплавов представляет собой зерна твердого раствора (рис. 32, а). Сплавы однофазные. Аналогичную структуру будут иметь сплавы, у которых количество
(кликните для просмотра скана)
растворимого компонента не превышает предельной его растворимости при нормальной температуре. При ограниченной растворимости, которая характерна для многих сплавов , могут образовываться структуры, состоящие из смеси двух или более фаз (твердых растворов или твердых растворов и химических соединений). Если в сплаве растворимый компонент присутствует в количестве, превышающем предельную растворимость его в основном металле при данной температуре, то образуется структура, состоящая из матрицы (основного твердого раствора) и выделившихся частиц другого твердого раствора, чаще на базе химического соединения. Такую структуру называют матричной, или гетерогенной. Так, например, при кристаллизации многих сплавов на алюминиевой, магниевой, железной и других основах образуются структуры, состоящие из основного твердого раствора на базе металла растворителя и частиц одного или нескольких химических соединений .
При медленном охлаждении эти фазы выделяются в основном по границам зерен твердого раствора (матрицы) в виде достаточно крупных и нередко равноосных частиц (рис. 32, б).
При ускоренном охлаждении благодаря увеличению числа зародышей новой фазы по границам зерен появляется пограничная оболочка из выделяющейся фазы.
При определенных условиях в процессе кристаллизации возможно образование второй фазы и внутри зерен на имеющихся здесь дефектах (включениях, границах блоков и т. д.). Форма выделения избыточных фаз может быть пластинчатой, игольчатой или сфероидальной.
При так называемой перетектической кристаллизации (см. с. 62) образуется смесь из двух фаз (твердых растворов), в которой фаза, образующаяся первоначально (например, твердый раствор Р), окружена фазой, кристаллизующейся позднее (твердым раствором а) (рис. 32, в).
В сплавах нередко образуется структурная составляющая, получившая название эвтектика (см. с. 56). Эвтектика состоит из двух или более фаз (твердых растворов или твердого раствора а и химического соединения), имеющих форму пластинок, равномерно чередующихся между собой, которые образуют колонии. Иногда обе фазы в колониях непрерывно разветвлены одна в другой (рис. 32, д). Наряду с этой структурой в эвтектике могут присутствовать обособленные кристаллы а- и -твердых растворов (рис. 32, г и е).
При образовании смеси фаз рентгенограммы таких сплавов показывают наличие кристаллических решеток соответствующего числа фаз, образующих его структуру.
Структура сплавов, их фазовый состав, а следовательно, и свойства зависят от состава сплава и той обработки, которую он прошел. Ниже будут рассмотрены формирование различных структур сплавов и влияние структуры (фазового состава) на свойства сплавов.
Металлические сплавы
Металлическим сплавом называется материал, полученный сплавлением двух или более металлов с неметаллами, обладающий металлическими свойствами. Вещества, которые образуют сплав, называются компонентами.
Фазой называют однородную часть сплава, характеризующуюся определенным составом и строением и отделенную от других частей сплава поверхностью раздела. Под структурой понимают форму, размер и характер взаимного расположения фаз в металлах и сплавах.
Структурными составляющими называют имеющие одинаковое строение обособленные части сплава с присущими им характерными особенностями.
Виды сплавов по структуре
По характеру взаимодействия компонентов все сплавы подразделяются на три основных типа: механические смеси, химические соединения и твердые растворы.
Механическая смесь двух компонентов А и В образуется, если они не способны к взаимодействию или взаимному растворению. Каждый компонент при этом кристаллизуется в свою кристаллическую решетку.
Структура механических смесей неоднородна и состоит из отдельных зерен компонента А и компонента В.
Свойства механических смесей зависят от количественного соотношения компонентов: чем больше в сплаве данного компонента, тем ближе к его свойствам свойства смеси.
Химическое соединение образуется, когда компоненты сплава А и В вступают в химическое взаимодействие. При этом соотношение чисел атомов в соединении соответствует его химической формуле А,„В,Г Химическое соединение имеют однородную структуру, состоящую из одинаковых по составу и свойствам зерен. Например, в сплавах железа с углеродом образуется карбид железа, называемый цементитом:
В сплавах алюминия с медью образуется интерметаллическое соединение СиА12.
Твердые растворы образуются, когда атомы одного компонента входят в кристаллическую решетку другого. Твердые растворы
Рис. 1.10. Схемы твердых растворов:
а — замещения; б — внедрения; 1 — атомы основного металла; 2 — атомы растворенного вещества
замещения образуются в результате частичного замещения атомов кристаллической решетки одного компонента атомами второго (рис. 1.10, о).
Твердые растворы внедрения образуются, когда атомы растворенного компонента внедряются в кристаллическую решетку компонента-растворителя (рис. 1.10, б). Твердый раствор имеет однородную структуру, одну кристаллическую решетку.
В отличие от химического соединения твердый раствор существует не при строго определенном соотношении компонентов, а в интервале концентраций.
Обозначают твердые растворы строчными буквами греческого алфавита: а, (3, у, 8 и т. д.
Pereosnastka.ru
- Понятие о структуре металлов и сплавов
- Категория:
- Изготовление форм
Понятие о структуре металлов и сплавов
Все металлы и сплавы имеют кристаллическое, или зернистое, строение.
Их кристаллы состоят из мельчайших частиц — атомов, которые располагаются в строго определенном порядке, образуя мельчайшие кристаллические решетки, которые можно рассмотреть с помощью рентгеновских лучей. Атомы находятся в непрерывном движении.
При нагреве металла движение атомов усиливается, а по достижении температуры плавления кристаллические решетки разрушаются, благодаря чему расплавленный металл приобретает жидкотекучесть. При охлаждении металла кристаллические решетки образуются вновь.
Форма, размеры и расположение зерен характеризуют внутреннее строение —структуру металла, которая наряду с химическим составом оказывает большое влияние на свойства металлов и сплавов: чем меньше зерно, тем плотнее материал, тем выше его механические свойства.
Структуру сплавов определяют в металлографической лаборатории путем рассмотрения шлифа (отшлифованного до зеркального блеска среза кусочка сплава) при увеличении в 100—500 и более раз с помощью металлографического микроскопа. Для выявления отдельных структурных составляющих сплава шлиф обрабатывают растворами кислот.
Железоуглеродистые сплавы в зависимости от содержания углерода подразделяются на две группы — чугуны и стали. Если в железоуглеродистом сплаве содержится до 2% углерода, то его называют сталью, а если больше 2% углерода — то чугуном.
Железоуглеродистые сплавы могут содержать в качестве структурных составляющих графит, феррит, цементит, перлит и др.
Графит —свободный углерод, находящийся в основной массе сплава в виде пластйнок или зерен. Присутствуя в сером чугуне в виде пластин, графит как бы разделяет основную металлическую массу и тем самым снижает прочность и пластичность. Шаровидный графит в меньшей степени нарушает сплошность основной структуры сплава, благодаря чему повышается его прочность и пластичность.
Феррит — почти чистое железо, в котором углерод растворен в небольшом количестве (до 0,04%). Обладает большой вязкостью и пластичностью, низкой прочностью и сопротивляемостью износу.
Цементит — химическое соединение 6,67% углерода и 93,33% железа. Обладает очень большой твердостью и хрупкостью. Значительное количество цементита в белом чугуне делает его хрупким, не -поддающимся механической обработке.
Перлит — смесь тонких, чередующихся между -собой пластин цементита и феррита. Перлит содержит 0,83% углерода и 99,17% железа. Обладает высокой прочностью, твердостью, вязкостью и является основой высококачественных чугунов и сталей.






