- Окрашивание пламени
- Калий — фиолетовое пламя
- Кальций хлористый — красное пламя
- Соляная кислота и медь — зелёное пламя
- Жёлтое пламя — соль
- Секреты сумасшедшего профессора НиколяЦветное пламя
- Цвет пламени при горении соединений, содержащих металлы — стронций, литий, кальций, натрий, железо, молибден, барий, медь, бор, теллур, таллий, селен, мышьяк, индий, цезий, рубидий, калий, свинец, сурьма, цинк. Цвет пламени спирта
- Цветное пламя: проба на окрашивание пламени
- Медный факел
- Цветные свечи
- Библиография
- В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий?
- В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий?
- Калий
- Нахождение в природе
- Месторождения
- Получение
- Физические свойства
- Химические свойства
- Взаимодействие с простыми веществами
- Взаимодействие со сложными веществами
- Соединения с кислородом
- Гидроксид
- Применение
- Важные соединения
- Биологическая роль
- Изотопы
Очень красивый научный эксперимент от профессора Николя «Цветное пламя» позволяет получить пламя четырех разных цветов, используя для этого законы химии.
Набор интереснейший, мы действительно на пламя насмотрелись, удивительное зрелище! Интересно всем: и взрослым, и детям, так что очень рекомендую! Плюс в том, что этот опыт с огнём можно провести и дома, не обязательно выходить на улицу. В наборе есть чашки-плошки, в которых горит таблетка сухого горючего, всё безопасно, и на деревянном полу (или столе) можно поставить. Из серии опытов профессора Николя.
Лучше, конечно, под присмотром взрослых опыт проводить. Даже если дети уже немаленькие. Огонь всё же — штука опасная, но при этом … жутко (тут именно это слово подходит очень точно!) интересная!

- Фото упаковки набора смотрите в галерее в конце статьи.
- Набор 'Цветное пламя' содержит все необходимое для проведения эксперимента. В набор входят:
- иодид калия,
- хлорид кальция,
- раствор соляной кислоты 10%,
- сульфат меди,
- нихромовая проволока,
- медная проволока,
- хлорид натрия,
- сухое горючее, чашка для выпаривания.
Единственное, есть у меня некоторые претензии к производителю — я ожидала найти в коробочке мини-брошюру с описанием химического процесса, который мы здесь наблюдаем, и объяснение, почему пламя становится цветным.
Такого описания здесь не оказалось, так что придётся обратиться к энциклопедии по химии (обзор книг по химии здесь). Если, конечно, будет такое желание.
А желание у старших детей, конечно, возникает! Младшим детям, конечно, никакие объяснения не нужны: им просто очень интересно смотреть, как меняется цвет пламени.
На обратной стороне коробки-упаковки написано, что нужно делать, чтобы пламя стало цветным.
Сначала делали по инструкции, а потом стали просто пламя разными порошками из баночек посыпать (когда убедились, что всё безопасно) — эффект потрясающий.
Всполохи красного пламени в жёлтом, ярко-салатовое пламя, зелёное, фиолетовое… зрелище просто завораживает.
Очень здорово покупать на какой-нибудь праздник, это гораздо интереснее любой петарды. И на новый год будет очень здорово. Мы жгли днём, в темноте было бы ещё эффектнее.
Реактивы у нас после сжигания одной таблетки ещё остались, так что, если взять другую таблетку (купить отдельно), можно повторить опыт. Глиняная чашка отмылась довольно хорошо, так что её на много опытов хватит. А если вы на даче, то порошок можно посыпать и на огонь в костре — он тогда, конечно, быстро кончится, но зрелище будет фантастическое!
Добавляю краткую информацию о реактивах, которые идут в комплекте с опытом. Для любознательных детишек, которым интересно узнать больше.
Окрашивание пламени
- Стандартный способ окрашивания слабосветящегося газового пламени — введение в него соединений металлов в форме легколетучих солей (обычно, нитратов или хлоридов):
- желтое — натрия,
- красное — стронция, кальция,
- зеленое — цезия (или бора, в виде борноэтилового или борнометилового эфира),
- голубое — меди (в виде хлорида).
- В синий окрашивает пламя селен, а в сине-зеленый — бор.
Температура внутри пламени различна и с течение времени она меняется (зависит от притока кислорода и горючего вещества). Синий цвет означает что температура очень высокая до 1400 С, желтый — температура чуть меньше, чем когда синее пламя. Цвет пламени может меняться в зависимости от химических примесей.
Цвет пламени определяется только его температурой, если не учитывать его химический (точнее, элементный) состав. Некоторые химические элементы способны окрашивать пламя в характерный для этого элемента цвет.
В лабораторных условиях можно добиться совершенно бесцветного огня, который можно определить лишь по колебанию воздуха в области горения. Бытовой же огонь всегда «цветной». Цвет огня определяется температурой пламени и тем, какие химические вещества в нём сгорают.
Высокая температура пламени дает возможность атомам перескакивать на некоторое время в более высокое энергетическое состояние. Когда атомы возвращаются в исходное состояние, они излучают свет с определённой длиной волны.
Она соответствует структуре электронных оболочек данного элемента.
Голубой огонек, например, который можно видеть при горении природного газа, обусловлен угарным газом, который и придаёт пламени этот оттенок. Угарный газ, молекула которого состоит из одного атома кислорода и одного атома углерода, является побочным продуктом горения природного газа.
Калий — фиолетовое пламя
Калий (нем. Kalium, франц. и англ. Potassium) — один из важнейших представителей группы щелочных металлов.
Калий — металл наиболее электроположительный после рубидия и цезия.
В чистом сухом воздухе при обыкновенной температуре он не изменяется, в обычном — покрывается слоем едкого калия и углекислой его соли; в свежем разрезе в темноте светится, а в тонких пластинках окисляется столь быстро, что может загореться; расплавленный и нагретый, он также горит; пламя его обладает фиолетовым цветом. Вследствие такой склонности к окислению и является необходимым сохранять его под нефтью.
Открывают присутствие калия по фиолетовой окраске газового беcцветного пламени, которая получается при внесении в пламя его соединений, особенно галоидных, на ушке платиновой проволоки (вот почему в опыте нужно вносить калий в пламя на проволоке — эффект изменения цвета пламени тогда заметнее); в присутствии солей натрия окраску наблюдают через синее кобальтовое стекло или через раствор индиго, помещенный в призматический стеклянный сосуд. Спектр пламени характеризуется двумя линиями — красной и фиолетовой.
Кальций хлористый — красное пламя
При нагревании на воздухе или в кислороде кальций воспламеняется и горит красным пламенем с оранжевым оттенком. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании.
При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
При нагревании в кислороде и на воздухе кальций воспламеняется, сгорая ярко-красным пламенем, при этом образуется основной оксид СаО, который представляет собой белое, весьма огнестойкое вещество, температура плавления которого примерно 2 600 °C. Оксид кальция также известен в технике как негашеная или жженая известь.
Соляная кислота и медь — зелёное пламя
Медь придает пламени зеленый оттенок. При высоком содержании меди в сгораемом веществе пламя имеет яркий зеленый цвет, практически идентичный белому. В зеленый цвет пламя окрашивает борная кислота или медная (латунная) проволока, смоченная в соляной кислоте.
- При смачивании соляной кислотой пламя окрашивается в голубой цвет с зеленоватым оттенком.
- 1) В зеленый цвет пламя окрашивает борная кислота или медная (латунная) проволока, смоченная в соляной кислоте.
- 2) В красный цвет пламя окрашивает мел, смоченный в той же соляной кислоте.
При сильном прокаливании в тонких осколках Ва-содержащие (Барий-содержащие) минералы окрашивают пламя в желто-зеленый цвет. Окрашивание пламени можно усилить, если после предварительного прокаливания смачивать минерал в крепкой соляной кислоте.
Окислы меди (в опыте для зелёного пламени используются соляная кислота и кристаллики меди) дают изумрудно-зеленое окрашивание. Прокаленные Cu-содержащие соединения, смоченные НС1, окрашивают пламя в лазурно-голубой цвет CuС12). Реакция очень чувствительна.
Зеленый цвет и его оттенки огню придают также барий, молибден, фосфор, сурьма.
Азотнокислый и солянокислый растворы меди имеют голубой или зеленый цвет; при прибавлении аммиака цвет раствора изменяется в темно-синий.
Жёлтое пламя — соль
Для желтого пламени требуется добавка поваренной соли, нитрата натрия или хромата натрия.
Попробуйте посыпать на конфорку газовой плиты с прозрачно-голубым пламенем чуть-чуть поваренныой соли — в пламени появятся жёлтые язычки. Такое жёлто-оранжевое пламя дают соли натрия (а поваренная соль, напомним, это хлорид натрия).
Жёлтый цвет — это цвет натрия в пламени. Натрий есть в любом природном органическом материале, поэтому пламя мы обычно и видим жёлтым. А желтый цвет способен заглушить другие цвета — такова особенность человеческого зрения.
Желтые язычки пламени появляются при распадении солей натрия. Такими солями очень богата древесина, поэтому обычный лесной костер или бытовые спички горят желтым пламенем.
Секреты сумасшедшего профессора НиколяЦветное пламя
Цвет пламени при горении соединений, содержащих металлы — стронций, литий, кальций, натрий, железо, молибден, барий, медь, бор, теллур, таллий, селен, мышьяк, индий, цезий, рубидий, калий, свинец, сурьма, цинк. Цвет пламени спирта
|
Проект Карла III Ребане и хорошей компании |
Раздел недели: Плоские фигуры. Свойства, стороны, углы, признаки, периметры, равенства, подобия, хорды, секторы, площади и т.д. |
|||||||||||||||||||||||||||||||||||||||||||||
| Таблицы DPVA.ru — Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Химический анализ. Определение состава химических соединений или их смесей. / / Цвет пламени при горении соединений, содержащих металлы — стронций, литий, кальций, натрий, железо, молибден, барий, медь, бор, теллур, таллий, селен, мышьяк, индий, цезий, рубидий, калий, свинец, сурьма, цинк. Цвет пламени спирта.
Поиск в инженерном справочнике DPVA. Введите свой запрос: |
|||||||||||||||||||||||||||||||||||||||||||||
| Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. Вложите в письмо ссылку на страницу с ошибкой, пожалуйста. | ||||||||||||||||||||||||||||||||||||||||||||||
| Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator |
Цветное пламя: проба на окрашивание пламени
Для химика пламя не только источник тепла, но и инструмент химического анализа. Давно известно, что некоторые химические соединения, введенные в пламя, придают ему характерную окраску. В этом можно убедиться, если в любое пламя внести кусочек поваренной соли.
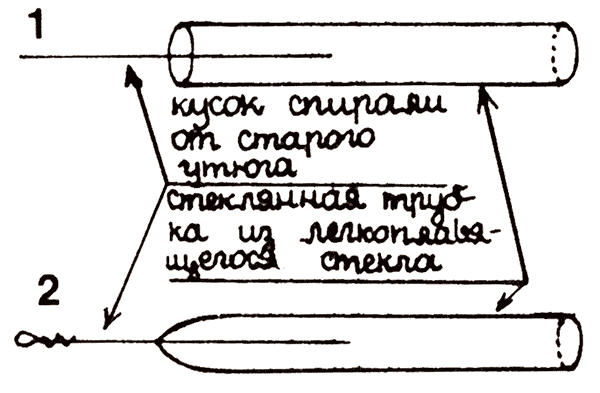
Можно поступить не совсем спортивно и заменить стеклянную трубку корковой пробкой из винной бутылки.
При подведении определенного количества воздуха пламя газовой горелки становиться голубым и не коптит. Отчетливо видны в нем две части. Внутренняя часть называется восстанавливающей. Она голубого цвета и имеет сравнительно низкую температуру. Внешняя часть бесцветная — окисляющая. Температура этой части пламени равно около 1300 °С.
Растворите в нескольких миллилитрах воды, налитых в пробирку щепотку хлористого натрия. Очищенную проволоку погрузите в раствор, а потом введите в окисляющую часть пламени.

Какой великолепный эффект! Пламя в одно мгновение меняет окраску на интенсивно желтую. А теперь проверьте, содержит ли натрии вода, которую вы пьете (этот металл придает пламени желтый цвет). Результат анализа будет положительным. Можете проверить, содержат ли натрий другие вещества. Окажется, что натрий «пронырливый» металл, везде он есть, пламя всегда будет более или менее желтым.
Если вы уже знаете, как меняет окраску пламени натрий, проверьте «поведение» других металлов. Возьмите образцы солей кальция, стронция, бария, калия и меди. Лучше всего взять хлориды или нитраты.
Если у вас их нет, возьмите другие соли, но помните, что сначала проволоку нужно очистить в пламени и соляной кислоте.
После такой очистки опять опускайте проволоку в раствор анализируемого вещества, а затем вводите в окисляющую часть пламени.
При анализе твердых субстанций раскаленную проволоку опускают в анализируемое вещество, которое прилипает к ней и затем сплавляется в пламени горелки, образуя перл. Перл на мгновение опускают в соляную кислоту. Образующиеся при этом хлористоводородные соединения летучие и быстро испаряются с проволоки в пламени, окрашивая его в характерный цвет.
Вероятно вы удивитесь, когда начнете исследовать калий, так как цвет пламени будет такой же как в ходе анализа натрия, и лишь время от времени через желтое пламя будут проскакивать розовые отблески калия.
Это потому, что натрий, содержащийся в воде, употребляемой для растворения образца, не позволяет калию показать себя в полной красоте. В пламени идет „борьба” между натрием и калием, в которой натрий побеждает. Если хотите, можете помочь победить калию. Наблюдайте через так называемое синее кобальтовое стекло.
Это стекло представляет собой фильтр, который задерживает цвет натрия, пропуская цвет калия. Вы, наверное, огорчитесь, что в вашей лаборатории нет кобальтового стекла. Но не падайте духом, вместо него можно взять раствор метилового фиолетового. А если его тоже нет, растворите в воде несколько капель синих чернил.
Если будете наблюдать пламя через этот раствор, увидите фиолетовую вспышку, свидетельствующую о наличии калия.
- А теперь сопоставьте результаты работы:
- Металл Цвет пламени
- барий зеленый
- стронций ало-красный
- кальций кирпично-красный
- медь зелено-синий
- натрий желтый
- калий розово-фиолетовый
- литий красный
Медный факел
Зная, что некоторые металлы окрашивают пламя, сделайте медный «факел». Это необыкновенно интересный опыт. Соберите аппаратуру, показанную на рисунке.
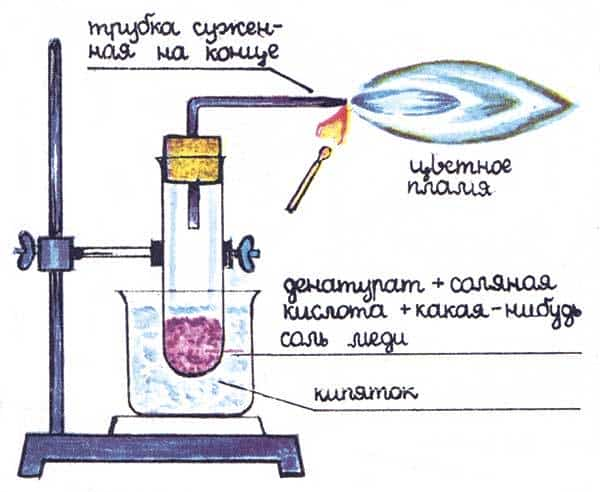
Всыпьте в пробирку несколько криеталликов какой-либо соли меди, например, CuSO4 (медный купорос), и добавьте до 1/3 высоты пробирки денатурат и несколько капель разбавленной соляной кислоты Закупорьте пробирку пробкой, через которую проходит трубка, изогнутая под прямым углом и суженая на конце. Поместите пробирку в химический стакан с горячей водой, денатурат начнет испаряться, увлекая с собой соль меди. Приставьте к выходу трубки горящую спичку: пары денатурата зажгутся, а пламя приобретет зелено-синий цвет. Эффект опыта необыкновенно красив, если его наблюдать в темной комнате.
А теперь модифицируйте опыт, взяв вместо соли меди ранее употреблявшиеся химические соединения, окрашивающие пламя. А если у вас есть бура или борная кислота, проверьте, как окрашивает пламя бор. Борную кислоту можно купите в аптеке. И еще одно: не заливайте пробирку более чем на 1/3 высоты. И ни в коем случае не нагревайте пробирку горелкой!
Цветные свечи
Чтобы получить свечи с разноцветным пламенем надо добавить в расплавленный парафин соль металла, окрашивающего пламя в той или иной цвет.
Синяя свеча. Покрасить парафин в синий цвет можно стеаратом меди. Эту соль получают смешивая растворы сульфата меди и хозяйственного мыла. Пламя свечи тоже будет синим, благодаря ионам меди.
Зеленая свеча. В качестве пигмента используется зеленый оксид хрома (III). Он получается при термическом разложении бихромата аммония (опыт с вулканом). Цвет пламени тоже будет зеленым.
Желтая свеча. Желтый хромат натрия окрасит парафин и пламя свечи в желтый цвет.
Красная свеча. Парафин подкрашивают любым красным пигментом, например гуашью. Чтобы пламя было красным надо добавитькакую-либо соль стронция или лития.
Библиография
- Кшиштоф Кушмерчик, журнал «Горизонты техники для детей» 1989-3
В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий?
В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий?
В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий? Сегодня у нас на календарях суббота 6 марта 2021 года, на Первом канале идет телевикторина Кто хочет стать миллионером? В студии находятся игроки и ведущий Дмитрий Дибров.
В статье мы рассмотрим один из интересных и сложных вопросов сегодняшней игры. На сайте Спринт-Ответ уже готовится к публикации общая, традиционная, статья с полным текстовым обзором телеигры «Кто хочет стать миллионером?» ответы за сегодня 6.03.21.
Пламя — явление горения газа, при котором происходят реакции разложения и горения. Топливом в пламени всегда является газ. Пламя над жидкостью возникает из-за испарения этой жидкости, а пламя над горящим твердым телом указывает на выделение горючего газа из-за разложения топлива (пиролиз).
Цвет пламени может меняться в зависимости от химических примесей, содержащихся в поленьях или другом горючем веществе.
Калий является химическим элементом с атомным номером 19 и атомной массой 39 обозначен символом K. Находится в 1-й, 4-й группах периодической таблицы Менделеева. Атом калия содержит 1 электрон во внешнем электронном слое. Это серебристо-белый мягкий металл, который можно разрезать.
В нормальных условиях он находится в твердом состоянии. Калий электрически и теплопроводен. Его кристаллическая структура объемно-центрированная кубическая. Реагирует бурно с водой и быстро окисляется, поэтому калий нужно следует хранить в масле.
Цвет пламени определяется излучением электронных переходов (например, тепловым излучением) различных возбужденных (как заряженных, так и незаряженных) частиц, образующихся в результате химической реакции между молекулами горючего и кислородом воздуха, а также в результате термической диссоциации. Цвет пламени определяется температурой пламени и тем, какие химические вещества в нём сгорают.
Соединения некоторых металлов при высоких температурах они испаряются, и их пары, под воздействием света, окрашивают пламя горелки характерным образом. Эта окраска является результатом возбуждения атомов металла в пламени, которые возвращаются в основное состояние и излучают квант света со строго определенной длиной волны.
Следует подчеркнуть, что в случае большинства элементов свет излучается только электрически нейтральными атомами, а не ионами.
Например, когда мы вводим ион натрия в пламя, он сначала рекомбинирует со свободным электроном, и только затем, в результате другого столкновения, может произойти возбуждение и релаксация, сопровождающиеся излучением оранжевого света с длиной волны 589 см. нм.
Разность энергий между уровнями для этого перехода невелика и составляет 2,1 эВ, в то время как нижние возбужденные уровни для иона натрия имеют энергию более 30 эВ и недостижимы в пламени.
Свечение ионов в пламени можно наблюдать только у щелочноземельных металлов — хотя в этом случае интенсивность испускания атомов во много раз выше. Во многих случаях этот цвет настолько характерен, что в сочетании с другими аналитическими методами он обеспечивает почти стопроцентную уверенность в присутствии данного металла в образце.
Окрашивание пламени. Летучие (например, хлористые) соли калия окрашивают несветящее газовое пламя в фиолетовый цвет.
Однако при одновременном наличии даже незначительных количеств натрия желтое пламя последнего маскирует фиолетовое пламя калия.
В этом случае рекомендуется смотреть на пламя через синее кобальтовое стекло или индиговую призму, полностью поглощающие желтые лучи. Тогда фиолетовое пламя калия снова становится ясно видимым.
- зеленый
- голубой
- фиолетовый
- желтый
Если в пламя поместить соединение, содержащее калий, то пламя окрасится в фиолетовый цвет. Это правильный ответ на вопрос телевикторины. Игроки решили забрать деньги, сообщает сайт sprintotvet.ru. Выигрыш игроков составил 400 000 рублей.
В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий?
В какой цвет окрасится пламя, если в него поместить соединение, содержащее калий? Игра «Кто хочет стать миллионером?» за 6 марта 2021 года уже идет в эфире страны на Первом канале, ответы на все вопросы игры уже многим известны и их можно найти в интернете, а также узнать на сайте в этой же рубрике. А эта статья с ответом на один из сложных вопросов посвящена игре от 6.03.21.
После того как передача «Кто хочет стать миллионером?» вышла на большие экраны, она собрала большое количество поклонников. Заветным призом являются три миллиона рублей, который можно получить после того, как игроки дадут ответы на все пятнадцать вопросов. В каждой программе участвуют знаменитые, публичные люди.
Пламя бывает разного цвета. Посмотрите в камин. На поленьях пляшут желтые, оранжевые, красные, белые и синие языки пламени. Его цвет зависит от температуры горения и от горючего материала.
Чтобы наглядно себе это представить, вообразите спираль электрической плитки. Если плитка выключена — витки спирали холодные и черные. Допустим, вы решили подогреть суп и включили плитку. Сначала спираль становится темно-красной. Чем выше поднимается температура, тем ярче красный цвет спирали.
Калий — металл наиболее электроположительный после рубидия и цезия. В чистом сухом воздухе при обыкновенной температуре он не изменяется, в обычном — покрывается слоем едкого калия и углекислой его соли; в свежем разрезе в темноте светится, а в тонких пластинках окисляется столь быстро, что может загореться; расплавленный и нагретый, он также горит; пламя его обладает фиолетовым цветом.
Такой металл как калий окрашивает пламя в фиолетовый цвет. Хлорид натрия (поваренная соль), который есть у каждой хозяйки на кухне, горит желтым, по этой же причине все деревья горят желтым цветов, это обусловлено высоким содержанием солей натрия в древесине.
- зеленый
- голубой
- фиолетовый
- желтый
Калий — один из самых распространенных элементов в природе. Он входит в состав как неорганических, так и органических субстратов и объектов. Также он является очень важной частью живых организмов.
Ответ на вопрос: фиолетовый.
Цвет пламени определяется только его температурой, если не учитывать его химический (точнее, элементный) состав. Некоторые химические элементы способны окрашивать пламя в характерный для этого элемента цвет.
Калий
Калий — элемент первой группы (по старой классификации — главной подгруппы первой группы), четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий — мягкий щелочной металл серебристо-белого цвета.
- В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах.
- Очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь.
- Во многих свойствах калий очень близок натрию, но с точки зрения биологической функции и использования клетками живых организмов они антагонистичны.
Соединения калия используются с древнейших времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия K2CO3, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
19 ноября 1807 года в Бейкеровской лекции английский химик Дэви сообщил о выделении калия электролизом расплава едкого кали (KOH)(в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года). Дэви назвал его «потасий» (лат.
potasium; это название (правда, в некоторых языках с двумя буквами s) до сих пор употребительно в английском, французском, испанском, португальском и польском языках. При электролизе влажного едкого кали KOH на ртутном катоде он получил амальгаму калия, а после отгонки ртути — чистый металл.
Дэви определил его плотность, изучил химические свойства, в том числе разложение воды и поглощение водорода.
В 1808 году французские химики Гей-Люссак и Л. Тенар выделили калий химическим путём — прокаливанием KOH с углём.
В 1809 году немецкий физик Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.
Нахождение в природе
Ввиду высокой химической активности калий в свободном состоянии в природе не встречается. Породообразующий элемент, входит в состав слюд, полевых шпатов и т. д.
Также калий входит в состав минералов сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел Биологическая роль).
Кларк калия в земной коре составляет 2,4 % (5-й по распространённости металл, 7-й по содержанию в коре элемент). Средняя концентрация в морской воде — 380 мг/л.
Месторождения
Крупнейшие месторождения калия находятся на территории Канады (производитель PotashCorp), России (ПАО «Уралкалий», г. Березники, г. Соликамск, Пермский край, Верхнекамское месторождение калийных руд), Белоруссии (ПО «Беларуськалий», г. Солигорск, Старобинское месторождение калийных руд).
Получение
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расплавленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
K+ + e− → K 2Cl− → Cl2
При электролизе гидроксида калия на катоде также выделяется расплавленный калий, а на аноде — кислород:
4OH− → 2H2O + O2
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Важное промышленное значение имеют и методы термохимического восстановления:
Na + KOH →N2,380−450oC NaOH + K
и восстановление из расплава хлорида калия карбидом кальция, алюминием или кремнием.
Физические свойства
Калий — серебристый металл с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки, калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет.
Калий активно взаимодействует с водой. Выделяющийся водород воспламеняется, а ионы калия придают пламени фиолетовый цвет. Раствор фенолфталеина в воде становится малиновым, демонстрируя щелочную реакцию образующегося KOH
Калий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,5247 нм, Z = 2.
Химические свойства
Элементарный калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. На воздухе свежий срез быстро тускнеет из-за образования плёнок соединений (оксиды и карбонат).
При длительном контакте с атмосферой способен полностью разрушиться. С водой реагирует со взрывом. Хранить его необходимо под слоем бензина, керосина или силикона, дабы исключить контакт воздуха и воды с его поверхностью.
С Na, Tl, Sn, Pb, Bi калий образует интерметаллиды.
Взаимодействие с простыми веществами
Калий при комнатной температуре реагирует с кислородом воздуха, галогенами; практически не реагирует с азотом (в отличие от лития и натрия). При умеренном нагревании реагирует с водородом с образованием гидрида (200—350 °C):
2K + H2 ⟶ 2KH
с халькогенами (100—200 °C, E = S, Se, Te):
2K + E ⟶ K2E
При сгорании калия на воздухе образуется надпероксид калия KO2 (с примесью K2O2):
K + O2 ⟶ KO2
В реакции с фосфором в инертной атмосфере образуется фосфид калия зелёного цвета (200 °C):
3K + P ⟶ K3P
Взаимодействие со сложными веществами
Калий при комнатной температуре (+20 °C) активно реагирует с водой, кислотами, растворяется в жидком аммиаке (−50 °C) с образованием тёмно-синего раствора аммиаката калия.
2K + 2H2O ⟶ 2KOH + H2↑ 2K + 2HCl ⟶ 2KCl + H2↑ K + 6NH3 ⟶ [K(NH3)]6
Калий глубоко восстанавливает разбавленные серную и азотную кислоты:
8K + 6H2SO4 ⟶ 4K2SO4 + SO2↑ + S↓ + 6H2O 21K + 26HNO3 ⟶ 21KNO3 + NO↑ + N2O↑ + N2↑ + 13H2O
При сплавлении металлического калия со щелочами он восстанавливает водород гидроксогруппы:
2K + 2KOH ⟶ 2K2O + H2↑ (450∘C)
При умеренном нагревании реагирует с газообразным аммиаком с образованием амида (+65…+105 °C):
2K + 2NH3 ⟶ 2KNH2 + H2
Металлический калий реагирует со спиртами с образованием алкоголятов:
2K + 2C2H5OH ⟶ 2C2H5OK + H2↑
Алкоголяты щелочных металлов (в данном случае — этилат калия) широко используются в органическом синтезе.
Соединения с кислородом
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
2K + O2 ⟶ K2O2 K + O2 ⟶ KO2
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
4K + O2 ⟶ 2K2O KO2 + 3K ⟶ 2K2O
Оксиды калия обладают ярко выраженными осно́вными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
K2O2 + 2H2O ⟶ 2KOH + H2O2 4KO2 + 2H2O ⟶ 4KOH + 3O2↑ 4KO2 + 2CO2 ⟶ 2K2CO3 + 3O2↑ Советский изолирующий противогаз ИП-5
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия.
Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
- В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
- Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
- Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
- Также известен озонид калия KO3, оранжево-красного цвета. Получить его можно взаимодействием гидроксида калия с озоном при температуре не выше +20 °C:
4KOH + 4O3 ⟶ 4KO3 + O2 + 2H2O
Озонид калия является очень сильным окислителем, например, окисляет элементарную серу до сульфата и дисульфата уже при +50 °C:
6KO3 + 5S ⟶ K2SO4 + 2K2S2O7
Гидроксид
Основная статья: Гидроксид калия
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого кали при +20 °C в 100 г воды составляет 112 г.
Применение
- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав с составом 12 % натрия, 47 % калия, 41 % цезия обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений. Калий является одним из трёх базовых элементов, которые необходимы для роста растений наряду с азотом и фосфором. В отличие от азота и фосфора, калий является основным клеточным катионом. При его недостатке у растения прежде всего нарушается структура мембран хлоропластов — клеточных органелл, в которых проходит фотосинтез. Внешне это проявляется в пожелтении и последующем отмирании листьев. При внесении калийных удобрений у растений увеличивается вегетативная масса, урожайность и устойчивость к вредителям.
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединения
- Бромид калия применяется в медицине и как успокаивающее средство для нервной системы.
- Гидроксид калия (едкое кали) применяется в щелочных аккумуляторах и при сушке газов.
- Карбонат калия (поташ) используется как удобрение, при варке стекла, как кормовая добавка для птицы.
- Хлорид калия (сильвин, «калийная соль») используется как удобрение.
- Нитрат калия (калийная селитра) — удобрение, компонент чёрного пороха.
- Перхлорат и хлорат калия (бертолетова соль) используются в производстве спичек, ракетных порохов, осветительных зарядов, взрывчатых веществ, в гальванотехнике.
- Дихромат калия (хромпик) — сильный окислитель, используется для приготовления «хромовой смеси» для мытья химической посуды и при обработке кожи (дубление). Также используется для очистки ацетилена на ацетиленовых заводах от аммиака, сероводорода и фосфина.
Кристаллы перманганата калия
- Перманганат калия — сильный окислитель, используется как антисептическое средство в медицине и для лабораторного получения кислорода.
- Тартрат натрия-калия (сегнетова соль) в качестве пьезоэлектрика.
- Дигидрофосфат и дидейтерофосфат калия в виде монокристаллов в лазерной технике.
- Пероксид калия и супероксид калия используются для регенерации воздуха на подводных лодках и в изолирующих противогазах (поглощает углекислый газ с выделением кислорода).
- Фтороборат калия — важный флюс для пайки сталей и цветных металлов.
- Цианид калия применяется в гальванотехнике (серебрение, золочение), при добыче золота и при нитроцементации стали. Чрезвычайно ядовит, один из сильнейших ядов.
- Калий совместно с перекисью калия применяется при термохимическом разложении воды на водород и кислород (калиевый цикл «Газ де Франс», Франция).
- Сульфат калия применяется как удобрение.
Биологическая роль
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий в качестве катиона наряду с катионами натрия является базовым элементом так называемого калиево-натриевого насоса клеточной мембраны, который играет важную роль в проведении нервных импульсов.
Калий содержится большей частью в клетках, до 40 раз больше, чем в межклеточном пространстве. В процессе функционирования клеток избыточный калий покидает цитоплазму, поэтому для сохранения концентрации он должен нагнетаться обратно при помощи натрий-калиевого насоса. Калий и натрий между собой функционально связаны и выполняют следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых — от 1800 до 5000 миллиграммов. Потребность в калии зависит от массы тела, физической активности, физиологического состояния и климата места проживания. Рвота, продолжительные поносы, обильное потение, использование мочегонных повышают потребность организма в калии.
Основными пищевыми источниками являются бобы (в первую очередь белая фасоль), шпинат и капуста кормовая, финики, картофель, батат, сушёные абрикосы, дыня, киви, авокадо, помело, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград. Калия достаточно много в рыбе и молочных продуктах.
Практически все сорта рыбы содержат более 200 мг калия на 100 г. Количество калия в разных видах рыбы различается.
Овощи, грибы и травы также содержат много калия, однако в консервированных продуктах его уровень может быть гораздо меньше. Много калия содержится в шоколаде.
Всасывание происходит в тонком кишечнике. Усвоение калия облегчает витамин B6, затрудняет — алкоголь.
При недостатке калия развивается гипокалиемия. Возникают нарушения работы сердечной и скелетной мускулатуры. Продолжительный дефицит калия может быть причиной острой невралгии.
При избытке калия развивается гиперкалиемия, для которой основным симптомом является язва тонкого кишечника. Настоящая гиперкалиемия может вызвать остановку сердца.
Изотопы
Основная статья: Изотопы калия
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным с периодом полураспада 1,251 миллиарда лет.
Сравнительно малый период полураспада и большая распространённость калия по сравнению с ураном и торием означает, что на Земле ещё 2 млрд лет назад и ранее калий-40 вносил главный вклад в естественный радиационный фон.
В каждом грамме природного калия в секунду распадается в среднем 31,0±0,3 ядра 40K, благодаря чему, например, в организме человека массой 70 кг ежесекундно происходит около 4000 радиоактивных распадов. Поэтому легкодоступные в быту соединения калия (поташ, хлорид калия, калийная селитра и т. д.
) можно использовать как пробные радиоактивные источники для проверки бытовых дозиметров. 40K наряду с ураном и торием считается одним из основных источников геотермальной энергии, выделяемой в недрах Земли (полная скорость энерговыделения оценивается в 40—44 ТВт).
В минералах, содержащих калий, постепенно накапливается 40Ar, один из продуктов распада калия-40, что позволяет измерять возраст горных пород; калий-аргоновый метод является одним из основных методов ядерной геохронологии.
Один из искусственных изотопов — 37K, — с временем полураспада 1,23651 секунды, применяется в экспериментах по изучению Стандартной модели слабого взаимодействия.







