- Page 2
- Page 3
- Гдз по химии 9 класс рябов решебник
- Что входит в состав решебника по химии за 9 класс тесты Рябов УМК (к учебнику Габриеляна)
- Стоит ли использовать решебник по химии за 9 класс тесты М.А. Рябов УМК (к учебнику Габриеляна)
- Современные технологии и ГДЗ
- Гдз решебник по химии 9 класс рябов тесты экзамен
- Химия в 9 классе
- Готовимся к урокам с онлайн-пособием
- Преимущества готовых ответов
- Гдз решебник по химии 9 класс рябов тесты экзамен
- Что узнают ученики на уроках химии
- Полезные качества решебника
- Краткое описание учебника
- Гдз тесты по химии 9 класс рябов умк
- Плюсы овладения дисциплиной с решебником по химии 9 класс тесты Рябов
- Преимущества использования ГДЗ в учебе
- Гдз по химии 9 класс рабочая тетрадь боровских
- Контрольная работа по химии 9 класс тема «Металлы»
Данное пособие содержит решебник (ГДЗ) тесты (металлы) по Химии за 9 класс . Автора: М.А. Рябов Издательство: Экзамен. Полные и подробные ответы к упражнениям на Гитем
Page 2
Page 3
- издательство: Просвещение автор: Крайнева Л.Б.
- издательство: Просвещение авторы: Вишняков Я.В. Могилевский Н.А.
- издательство: Полярная звезда Просвещение авторы: Матвеев А.В. Петрова М.В.
- издательство: Вентана-граф авторы: Преображенская Н.Г. Преображенская И.Ю.
- издательство: Просвещение авторы: Казакевич В.М. Пичугина Г.В.
- издательство: Просвещение авторы: Кондрашова Н.А. Костылева С.В.
- издательство: Просвещение авторы: Сергеева Г.П. Кашекова И.Э.
- издательство: Перспективы образования авторы: Зайцев А.А. Лукьянов С.А.
Гдз по химии 9 класс рябов решебник
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
Химия – дисциплина, которая существенно отличается от других школьных предметов. А для некоторых учеников она может показаться сложной уже с первых уроков. На занятиях будут проводиться не только интересные эксперименты, но и выполняться задачи разного уровня сложности. Наш учебно-методический комплекс пригодится всем, кто задействован в учебном процессе. Школьники могут использовать решебник для более быстрого выполнения домашнего задания и подготовки к следующему уроку. Пособие подарит родителям шанс быстро проверить уроки. Даже преподаватели и репетиторы оценят ГДЗ по достоинству. С ним им будет гораздо проще оценивать работы детей и продумывать планы уроков.
Что входит в состав решебника по химии за 9 класс тесты Рябов УМК (к учебнику Габриеляна)
Школьники обнаружат, что оригинальный сборник содержит около 2600 номеров, задач и проверочных работ. И эти задания охватывают весь пройденный ранее материал. В пособии подробно рассмотрены следующие темы:
- Вещества и их свойства.
- Физические и химические явления.
- Закон сохранения массы.
- Получение кислорода.
- Оксиды и основания.
- Воздух и его состав.
После каждой главы ученики найдут вопросы, задачи и тесты. Работая с подобными номерами с самого начала, школьники разовью навыки, необходимые для сдачи ЕГЭ. В конце учебника собраны типовые задачи, которые помогут закрепить знания и отработать новую информацию.
Стоит ли использовать решебник по химии за 9 класс тесты М.А. Рябов УМК (к учебнику Габриеляна)
Большинство родителей будет против того, чтобы под рукой у их ребенка был сборник с верными ответами. Для них такие пособия – обычные шпаргалки. Но время, когда решебники не приносили особой пользы, давно прошло. Теперь с помощью ГДЗ можно:
- быстрее справиться с объемной домашней работой;
- самостоятельно подготовиться к важной контрольной;
- исправить ошибки в решениях;
- подтянуть успеваемость по предмету;
- чаще отвечать на уроках.
С ГДЗ дети перестанут допускать ошибки в своих работах. Они начнут чаще получать хорошие отметки. Постоянные успехи только подстегнут их мотивацию. Ученики снова полюбят этот предмет и будут с удовольствием посещать занятия.
Современные технологии и ГДЗ
Порой у старшеклассников настолько тяжелые рюкзаки, что еще одно дополнительное пособие им будет только мешать. Поэтому ученики по достоинству оценили возможность открыть пособие онлайн.
Благодаря этому пользоваться ответами к упражнениям можно круглосуточно. Отдельно стоит отметить тот факт, что ключи на страницах портала постоянно модернизируются и обновляются. Все решения написаны подробным языком.
В них смогут разобраться даже те, кто сильно отстал от программы.
Гдз решебник по химии 9 класс рябов тесты экзамен
ГлавнаяГДЗ9 классХимияРябов — Тесты
«ГДЗ по химии за 9 класс, тесты, Рябов (Экзамен)» поможет всем школьникам успешно освоить курс.
В решебнике представлены ценные материалы, которые предназначены для того, чтобы ученик мог готовиться к урокам качественно, не затрачивая при этом много времени и сил.
В отличие от занятий с частными репетиторами, работа с ГДЗ является наиболее эффективной, так как подростки учатся сами справляться с поставленными задачами, а не надеяться на помощь со стороны.
Химия в 9 классе
На уроках выпускники будут проходить следующие темы:
- Свойства алюминия.
- Жесткость воды.
- Металлургия.
- Свойства элемента и простого вещества азота.
- Кислородосодержащие соединения серы.
- Сульфиды.
Помимо изучения новых разделов учебника, школьникам нужно повторить все законы, формулы и прочие материалы за предыдущий год. У некоторых скопился ценный багаж знаний, а у других — пробелы, которые нужно найти и восполнить. Поможет в этом деле данный справочник, выпущенный издательством под названием «Экзамен».
Готовимся к урокам с онлайн-пособием
Одним из главных преимуществ данного сборника верных ответов и решенных заданий является то, что он помогает экономить драгоценные часы.
Ученикам больше не придется тратить много времени на выполнение домашних заданий и подготовку к контрольным и проверочным работам. Все это займет считанные минуты и минимум усилий.
Плюс ко всему они будут уверены в том, что все сделали правильно, так как у них появится уникальный шанс совершать дома самопроверку без чьей-либо помощи. А хорошие и отличные отметки девятиклассникам гарантированы.
Преимущества готовых ответов
«ГДЗ по химии за 9 класс, тесты, Рябов М. А. (Экзамен)» обладает целым рядом плюсов. Среди них хотелось бы отметить следующие:
- доступ с любого современного устройства с выходом в Интернет;
- приятный дизайн;
- простой интерфейс;
- удобная навигация;
- быстрый поиск ответов по номерам заданий.
Школьникам больше не придется загромождать свои рюкзаки дополнительными справочниками. Им достаточно вооружиться любым современным устройством с выходом в Интернет.
Но это не проблема для современных подростков, окруженных всевозможными гаджетами. Воспользоваться материалами они могут как дома, так и в классе.
Это очень удобно, так как выпускник сумеет сразу же заглянуть в ГДЗ, если ему вдруг что-то станет непонятно. Это предотвратит образование пробелов в знаниях.
Предыдущее
Следующее
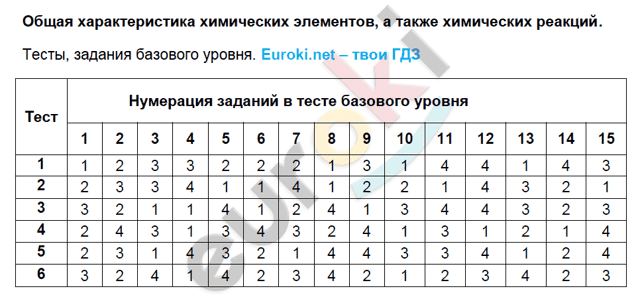 Скачать решение
Скачать решение
Предыдущее
Следующее
Гдз решебник по химии 9 класс рябов тесты экзамен
ГлавнаяГДЗ9 классХимияРябов — Тесты
Химия относится к естественным наукам. Она изучает вещества, их свойства, состав, взаимосвязи, а также процессы превращения и явления возникшие в результате преобразования.
Химическая наука проникла практически во все отрасли промышленности и сельского хозяйства. С её помощью осуществляют переработку ценных ископаемых, производят пластмассы, топливо, а также минеральные удобрения, которые нужны для роста и защиты растений.
Химия играет огромную роль в жизни человека и является жизненно важной наукой.
Что узнают ученики на уроках химии
Девятиклассники начнут новый учебный год с повторения классов неорганических веществ, затем приступят к изучению химических связей и реакций окисления, подробно рассмотрят неметаллы и их свойства, а также познакомятся с органическими соединениями. Школьники научатся:
- Давать характеристику различным веществами и описывать их.
- Правильно применять формулы, и понимать определения.
- Безопасно работать с реагентами и лабораторным оборудованием.
- Применять на практике изученный материал.
Химия развивает интеллектуальные способности, формирует экологическое мышление, а также бережное отношение к окружающей природе.
Полезные качества решебника
Освоение дисциплины сложный и трудоемкий процесс с которым не все ученики справляются успешно. Неудовлетворительные оценки и пробелы в знаниях крайне негативно влияют на успеваемость.
Поможет исправить ситуацию в лучшую сторону «ГДЗ по Химии 9 класс Тесты Рябов (Экзамен)».
Сборник с готовыми и тщательно проработанными онлайн-ответами, которые имеются абсолютно ко всем номерам упражнений учебного издания, поможет:
- проверить правильное выполнение работы заданной на дом;
- заранее подготовиться к предстоящему уроку;
- разобрать и понять особо сложную тему;
- сэкономить время и силы на выполнение домашней работы.
Решебник станет хорошим помощником ученику. Систематическое использование ГДЗ только положительно скажется на результатах учёбы и даст возможность подтянуть свои знания в самые кратчайшие сроки.
Краткое описание учебника
Тестирование – это один из способов проверки предметных навыков и умений. Его осуществляют с помощью специальных пособий. Одно из таких тесты по химии за 9 класс автор Рябов. Работы представлены по всем основным темам и помогут выявить уровень усвояемости пройденного материала, а также выявить пробелы в понимании, и вовремя скорректировать ошибки.
Предыдущее
Следующее
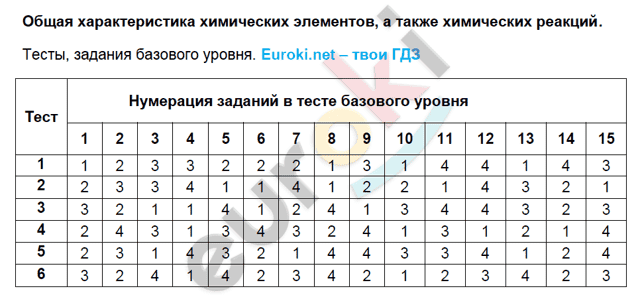 Скачать решение
Скачать решение
Предыдущее
Следующее
Гдз тесты по химии 9 класс рябов умк
Подпишись на группу ВК
Все ГДЗ по Химии 9 класс УМК
«ГДЗ по химии 9 класс тесты Рябов (Экзамен)» является хорошим подспорьем девятиклассникам в освоении раздела естествознания. Учебное пособие разработано в соответствии с требованиями Федерального государственного образовательного стандарта. Решебник включает верные ответы на все номера заданий основного издания.
Учебная нагрузка в девятом классе значительно возрастает из-за предстоящей итоговой аттестации. Поэтому ученики ценят каждую методичку, которая сможет помочь качественной подготовке и сэкономить их время. Данное учебное пособие, в котором собраны самые подробные решения всех номеров, станет твёрдой опорой учащихся в изучении химии.
С решебником у ребят всегда найдутся ответы на вопросы, возникающие в ходе подготовки к урокам и проверочным работам.
Плюсы овладения дисциплиной с решебником по химии 9 класс тесты Рябов
«ГДЗ по химии 9 класс тесты Рябов М. А. (Экзамен)» позволит ученикам систематизировать все знания, полученные от преподавателя, и разобраться во всех темах программы:
- представление о схемах образования веществ с различным типом связи;
- изменение научных теорий о строении атома;
- определение ковалентный полярной связи.
Планомерная подготовка по решебнику способна повысить интерес к изучаемому разделу естествознания, уровень знаний и успеваемость по дисциплине. Ресурс выпущен в онлайн-формате. Простая навигация моментально отправляет к нужному номеру учебника, нумерация которых полностью совпадает с оригинальным изданием.
Преимущества использования ГДЗ в учебе
Онлайн-сборник пригодится отличникам, желающим углубить свои знания по предмету, и троечникам, которые хотят сэкономить время и не испортить оценку в аттестате. Для приобретения фундаментальных знаний необходимо забыть о бездумном списывании готовых ответов.
Онлайн-ресурс нужно применять лишь для проверки самостоятельно выполненных упражнений. Обязательным условием является тщательный разбор допущенных ошибок, который помогает выявить пробелы и наметить темы для более детального рассмотрения учебнику.
Применяя интернет-помощник, школьники получают возможность:
- наверстать пропущенные уроки;
- закрепить пройденный материал;
- разобрать сложные номера;
- планово подготавливаться к итоговой аттестации по предмету.
Желаем успехов в освоении химии – сложного раздела естествознания!
Гдз по химии 9 класс рабочая тетрадь боровских
Авторы: Т. А. Боровских
Издательство: Экзамен
Тип книги: Рабочая тетрадь
ГДЗ рабочая тетрадь Химия. 9 класс. Рабочая тетрадь к учебнику Г. Е. Рудзитиса. ФГОС Т. А. Боровских. Издательство Экзамен. Серия Учебно–методический комплект. Состоит из одной части и 80 страниц.
Продолжая изучении химии в девятом классе, школьники получат знания об основных химических понятиях и определениях, научатся пользоваться химической символикой, овладеют различными умениями и навыками, включающими в себя проведение эксперимента, наблюдение за химическими явлениями, а также проведение расчетов на основе химических формул и уравнений химических реакций. Девятиклассники смогут с новой стороны взглянуть на этот естественно–научный предмет, понять его огромную практическую значимость в современной жизни людей. Они научатся использовать полученные на уроке, а также в ходе практических и лабораторных работ знания в своей повседневной жизни. Рабочая тетрадь имеет в своем составе задания по гидролизу солей, электролитов и неэлектролитов, катализаторам и химическому равновесию, окислительным свойствам азотной кислоты, химическим свойствам металлов и ряду напряжений.
Решебник ГДЗ к рабочей тетради, представленный веб-ресурсом ЯГДЗ, окажет помощь в поиске правильного ответа на вопросы и задания по темам сплавов, одноатомных спиртов, щелочных металлов, положения металлов в Периодической системе Д. И. Менделеева, вычислений по химическим уравнениям.
Урок 1. Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворах
- 1 2 3 4 5 6 7
- Урок 2. Электролитическая диссоциация кислот, щелочей, солей
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14
Урок 3. Сильные и слабые электролиты. Степень диссоциации
- 1 2 3 4 5 6 7
- Урок 4 – 5. Реакции ионного обмена и условия их протекания
- 1 2 3 4 5 6 7 8 9 10
Урок 6-7. Окислительно-восстановительные реакции. Окисление и восстановление
- 1 2 3 4 5 6 7
- Урок 8. Гидролиз солей
- 1 2 3 4
- Урок 9. Решение экспериментальных задач по теме Электролитическая диссоциация)
- 1 2 3 4 5 6 7 8 9
- Урок 10. Проверь свои знания по теме Электролитическая диссоциация
- Урок 11. Положение кислорода и серы в Периодической системе химических элементов, строение их атомов
- 1 2
Урок 12. Сера. Аллотропия серы. Физические и химические свойства серы. Применение
1 2 3 4 5 6 7 8 9 10
Урок 13. Сероводород. Сульфиды
1 2 3 4 5 6 7 8 9
Урок 14. Сернистый газ. Сернистая кислота и ее соли
1 2 3 4 5 6 7 8 9
Урок 15. Оксид серы (VI). Серная кислота и ее соли
- 1 2 3 4 5 6 7 8 9 10 11
- Урок 16. Окислительные свойства концентрированной серной кислоты
- 1 2 3 4 5 6 7 8 9 10
Урок 17. Практическая работа. Решение экспериментальных задач по теме Кислород и сера
1 2 3 4 5 6 7 8
Урок 18. Понятие о скорости химической реакции. Катализаторы. Химическое равновесие
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
- Урок 19. Вычисления по химическим уравнениям
- 1 2 3 4 5 6 7 8 9 10 11 12 13
Урок 20. Положение азота и фосфора в Периодической системе химических элементов, строение атомов. Азот. Свойства, применение
1 2 3 4 5 6
Урок 21.Аммиак. Физические и химические свойства. Получение и применение
1 2 3 4 5 6 7 8 9
Урок 22. Практическая работа. Получение аммиа¬ка и изучение его свойств
- 1 2 3 4 5 6 7 8 9 10
- Урок 23. Соли аммония
- 1 2 3 4 5 6
- Урок 24. Оксид азота (II) и оксид азота (IV)
- 1 2 3 4 5 6
- Урок 25. Азотная кислота и ее соли
- 1 2 3 4 5 6 7 8
- Урок 26. Окислительные свойства азотной кислоты
- 1 2 3 4 5 6 7
Урок 27. Фосфор. Аллотропия фосфора. Свойства фосфора
1 2 3 4 5 6 7 8 9 10 11
Урок 28. Оксид фосфора (V). Ортофосфорная кислота и ее соли. Минеральные удобрения
1 2 3 4 5 6 7 8 9 10
Урок 29. Практическая работа. Определение минеральных удобрений
1 2 3 4 5
Урок 30. Положение углерода и кремния в Перио¬дической системе химических элементов, строение их атомов. Аллотропия углерода
1 2 3 4 5
Урок 31. Химические свойства углерода. Адсорбция
- 1 2 3 4 5 6 7
- Урок 32. Угарный газ, свойства, физиологическое действие
- 1 2 3 4 5 6 7
Урок 33. Углекислый газ. Угольная кислота и ее соли
1 2 3 4 5 6 7 8 9 10 11 12 13 14
Урок 34. Практическая работа. Получение оксида углерода (ІV) и изучение его свойств. Распознавание карбонатов
1 2 3 4 5 6 7 8 9
Урок 35. Кремний и его соединения. Стекло. Цемент
1 2 3 4 5 6 7 8 9 11 13
Урок 36. Проверьте свои знания по темам Кислород и сера, Азот и фосфор, Углерод и кремний. Подготовка к контрольной работе
Урок 37. Положение металлов в Периодической системе химических элементов Д.И. Менделеева. Металлическая связь
1 2 3 4 5 6 7 8
Урок 38. Химические свойства металлов. Ряд напряжений
1 2 3 4 5 6 7
Урок 39. Понятие о металлургии. Способы получе¬ния металлов. Проблемы безотходных производств в металлургии и охрана окружающей среды
- 1 2 3 4 5
- Урок 40. Сплавы
- 1 2 3 4 5
Урок 41. Щелочные металлы. Физические и химические свойства. Нахождение в природе. Применение
1 2 3 4 5 6 7 8 9 10
Урок 42-43. Щелочноземельные металлы. Нахождение в природе. Кальций и его соединения. Жесткость воды и ее устранение
1 2 3 4 5 6 7 8 9 10 11 12
Урок 44-45. Алюминий. Нахождение в природе. Свойства алюминия. Амфотерность оксида и гидроксида алюминия
1 2 3 4 5 6 7 8
Урок 46. Практическая работа. Решение экспериментальных задач по теме Элементы I-III групп Периодической системы Д.И. Менделеева
1 2 3
Урок 47-48. Железо. Железо в природе. Свойства железа. Оксиды и гидроксиды железа. Соли железа (II) и железа (ІІІ)
1 2 3 4 5 6 7
Урок 49. Практическая работа. Решение экспериментальных задач по теме Металлы и их соединения
- 1 2 3 4 5 6
- Урок 50. Проверь свои знания по теме Общие свойства металлов
- Урок 51-52. Первоначальные представления о строении органических веществ
- 1 2 3 4 5 6 7 8 9 10 11 12
Урок 53-56. Предельные углеводороды. Непредельные углеводороды. Ацетилен. Диеновые углеводороды. Природные источники углеводородов
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
Урок 57- 66. Одноатомные спирты. Многоатом¬ные спирты. Муравьиная и уксусная кислоты
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19
Урок 67. Проверь свои знания по органической химии
Контрольная работа по химии 9 класс тема «Металлы»
- 9класс.
- Контрольная работа по теме «Металлы»
- Пояснительная записка
- Цель:
- Осуществление контроля над уровнем усвоения темы учащимися, систематизация и обобщение материала по теме «Металлы»
- Задачи:
- Закрепить представление о положении металлов в периодической системе, зависимости строения их атомов и свойств от положения в периодической системе химических элементов.
- Закрепить навыки в составлении оксидов металлов первых трёх групп химических элементов, а также в составлении уравнений химических реакций.
- Закрепить умение решать задачи на практический выход продукта реакции.
- Ставить перед учащимися предельно конкретную коррекционно-развивающую задачу, учитывая специфику обучения.
- Помочь ребятам со стойкими трудностями в обучении.
Контрольная работа в 9 классе завершает тему «Металлы», она рассчитана на академический час и позволяет проверить качество знаний, умений и навыков у учащихся коррекционных классов.
Работа выполняется по вариантам и по уровням. Она включает в первом уровне три обязательных и одно дополнительное задание, которым можно воспользоваться при не знании какого-либо из заданий.
Во втором уровне обязательными являются все четыре задания.
В первом уровне во втором задании использую приём коррекции и переключения внимания.
Во втором уровне все задания, кроме задачи на коррекцию распределения внимания. При решении задачи в первом и втором уровне использую алгоритм решения.
В заключении хочется ещё раз повторить, что дети, имеющие временную задержку в развитии, ни в коей мере не относятся к умственно отсталым детям, поскольку хорошо воспринимают предлагаемую помощь, сознательно выполняют поставленные перед ними задачи и правильно оперируют теми понятиями, которые они имеют. При своевременной коррекции большинство из них хорошо продвигаются и постепенно выравниваются в знании.
- 9класс.
- Контрольная работа №2 по теме: «Металлы».
- Вариант 1.
- Первый уровень (оценка «3»)
- ЗАДАНИЕ 1
Охарактеризуйте металлы 1 группы периодической системы химических элементов Д.И. Менделеева.
ЗАДАНИЕ 2
Установите соответствие между правой и левой частями уравнений
| 1) NaCl+AgNO3→ | А)Fe(OH)3↓+3NaCl |
| 2)CuSO4+BaCl2→ | Б)Cu↓+FeCl2 |
| 3)Fe+CuCl2→ | B)Fe(OH)2+2NaCl |
| 4)2NaOH+FeCl2→ | Г)NaNO3+AgCl |
| Д)CuCl2+BaSO4↓ |
- ЗАДАНИЕ 3
- Какие физические свойства характерны для металлов?
- Второй уровень (оценка «5»)
- ЗАДАНИЕ 1
- Проведите все возможные реакции Fe с : O2 , Br2, H2, CuCl2, NaOH, HCl, H2O, Cu)
- ЗАДАНИЕ 2
-
Напишите уравнения реакций, соответствующих превращениям, укажите условия их протекания:
-
Рассмотрите реакцию № 1 как ОВР и реакцию № 3 в свете ТЭД
- Ca→ CaO→ Ca(OH)2→ CaSO4→ BaSO4
- ЗАДАНИЕ 3
- Какая масса меди образуется при взаимодействии железа с раствором, содержащим 16г сульфата меди(II)?
- 9класс.
- Контрольная работа №2 по теме: «Металлы».
- Вариант 2.
- Первый уровень (оценка «3»)
- ЗАДАНИЕ 1
Охарактеризуйте металлы 2 группы периодической системы химических элементов Д.И. Менделеева.
ЗАДАНИЕ 2
Установите соответствие между правой и левой частями уравнений
| 1) CaCl2+2NaOH→ | А)FeCl2+H2↑ |
| 2)2K+2H2O→ | Б) FeCl3+H2↑ |
| 3)3NaOH+FeCl3→ | B)Ca(OH)2↓+2NaCl |
| 4)2HCl+Fe→ | Г)3NaCl+Fe(OH)3↓ |
| Д)2KOH+H2↑ |
- ЗАДАНИЕ 3
- Опишите области применения металлов и их соединении.
- Второй уровень (оценка «5»)
- ЗАДАНИЕ 1
- Проведите все возможные реакции Ca с : O2 , Br2, H2, CuCl2, NaOH, HCl, H2O, Cu)
- ЗАДАНИЕ 2
-
Напишите уравнения реакций, соответствующих превращениям, укажите условия их протекания:
-
Рассмотрите реакцию № 1 как ОВР и реакцию № 3 в свете ТЭД
- Al→Al2O3→AlCl3→Al(OH)3→Al(NO3)3
- ЗАДАНИЕ 3
- Какая масса осадка образуется при взаимодействии 4г гидроксида натрия с хлоридом железа (II)?
- 9класс.
- Контрольная работа №2 по теме: «Металлы».
- Вариант 3.
- Первый уровень (оценка «3»)
- ЗАДАНИЕ 1
Охарактеризуйте химический элемент №13 периодической системы Д.И. Менделеева.
ЗАДАНИЕ 2
Установите соответствие между правой и левой частями уравнений
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
|
|
- ЗАДАНИЕ 3
- Расскажите о нахождении металлов в природе.
- Второй уровень (оценка «5»)
- ЗАДАНИЕ 1
- Проведите все возможные реакции Zn с : O2 , Br2, H2, CuCl2, NaOH, HCl, H2O, Cu)
- ЗАДАНИЕ 2
-
Напишите уравнения реакций, соответствующих превращениям, укажите условия их протекания:
-
Рассмотрите реакцию № 1 как ОВР и реакцию № 3 в свете ТЭД
- Mg→MgO →MgCl2→ Mg(OH)2→Mg(NO3)2
- ЗАДАНИЕ 3
- Вычислите массу соли, образующейся при взаимодействии 81 г алюминия с соляной кислотой?
- 9класс.
- Контрольная работа №2 по теме: «Металлы».
- Вариант 4.
- Первый уровень (оценка «3»)
- ЗАДАНИЕ 1
Охарактеризуйте химический элемент №26 периодической системы Д.И. Менделеева.
ЗАДАНИЕ 2
Установите соответствие между правой и левой частями уравнений
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
|
|
- ЗАДАНИЕ 3
- Расскажите историю открытия металлов.
- Второй уровень (оценка «5»)
- ЗАДАНИЕ 1
- Проведите все возможные реакции Mg с : O2 , Br2, H2, CuCl2, NaOH, HCl, H2O, Cu)
- ЗАДАНИЕ 2
-
Напишите уравнения реакций, соответствующих превращениям, укажите условия их протекания:
-
Рассмотрите реакцию № 1 как ОВР и реакцию № 3 в свете ТЭД
Zn→ ZnO→Zn(NO3)2→Zn(OH)2 → ZnO→Zn
ЗАДАНИЕ 3
Определите массу натрия, который потребуется для получения 80 гр. гидроксида натрия.






