- Физические свойства металлов
- Химические свойства металлов
- Механические свойства металлов
- Технологические свойства металлов
- Таблицы свойств металлов
- Таблица «Свойства металлов: Чугун, Литая сталь, Сталь»
- Таблица «Свойства пружинной стали»
- Таблица «Свойства кузовных тонколистовых металлов»
- Таблица «Свойства цветных металлов»
- Таблица «Свойства легких сплавов»
- Таблица «Металлокерамические материалы (PM)1) для подшипников скольжения»
- Таблица «Свойства металлокерамических материалов (РМ)1 для конструкционных деталей»
- Магнитные материалы
- Таблица «Свойства магнитомягких материалов»
- Магнитомягкие металлы
- Таблица «Свойства магнитной листовой и полосовой стали»
- Материалы для преобразователей и электрических реакторов
- Магнитная проницаемость листового сердечника для классов сплавов С21, С22, Е11, Е31 и Е41 для секции тонколистового сердечника EY11
- Материалы для реле постоянного тока
- Таблица «Свойства материалов для реле постоянного тока»
- Металлокерамические материалы для магнитомягких компонентов
- Таблица «Свойства металлокерамических материалов для магнитомягких компонентов»
- Магнитомягкие ферриты
- Таблица «Свойства магнитомягких ферритов»
- Базовые понятия. Запись 7 (физические свойства металлов)
- Видеоурок «Физические свойства металлов»
- Физические свойства металлов
- Общие химические свойства металлов
- 1. РЕАКЦИИ МЕТАЛЛОВ С НЕМЕТАЛЛАМИ
- 2. РЕАКЦИИ МЕТАЛЛОВ С КИСЛОТАМИ
- Физические свойства металлов
- Физические свойства металлов IА группы
- Физические свойства металлов IIА группы
- Физические свойства металлов IIIА группы
- Физические свойства металлов IVА группы
- Физические свойства металлов IVВ группы
- Физические свойства металлов VВ группы
- Физические свойства металлов VIВ группы
- Физические свойства металлов VIIВ группы
- Физические свойства металлов VIIIВ группы

Металлы, это группа элементов, в виде простых веществ, обладающих характерными металлическими свойствами, такими, как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность, ковкость и металлический блеск. В данной статье все свойства металлов будут представлены в виде отдельных таблиц.
Свойства металлов делятся на физические, химические, механические и технологические.
Физические свойства металлов
К физическим свойствам относятся: цвет, удельный вес, плавкость, электропроводность, магнитные свойства, теплопроводность, теплоемкость, расширяемость при нагревании.
Удельный вес металла — это отношение веса однородного тела из металла к объему металла, т.е. это плотность в кг/м3 или г/см3.
Плавкость металла — это способность металла расплавляться при определенной температуре, называемой температурой плавления.
Электропроводность металлов — это способность металлов проводить электрический ток, это свойство тела или среды, определяющее возникновение в них электрического тока под воздействием электрического поля.
Под электропроводностью подразумевается способность проводить прежде всего постоянный ток (под воздействием постоянного поля), в отличие от способности диэлектриков откликаться на переменное электрическое поле колебаниями связанных зарядов (переменной поляризацией), создающими переменный ток.
Магнитные свойства металлов характеризуются: остаточной индукцией, коэрцетивной силой и магнитной проницаемостью.
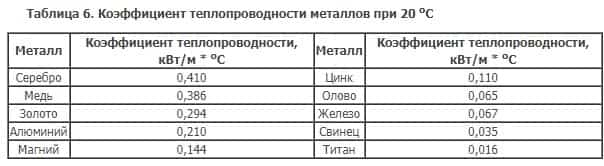
Теплопроводность металлов — это их способность передавать тепло от более нагретых частиц к менее нагретым. Теплопроводность металла определяется количеством теплоты, которое проходит по металлическому стержню сечением в 1см2, длиной 1см в течение 1сек. при разности температур в 1°С.
Теплоемкость металлов — это количество теплоты, поглощаемой телом при нагревании на 1 градус. Отношение количества теплоты, поглощаемой телом при бесконечно малом изменении его температуры, к этому изменению единицы массы вещества (г, кг) называется удельной теплоёмкостью, 1 моля вещества — мольной (молярной).
Расширяемость металлов при нагревании.Все металлы при нагревании расширяются, а при охлаждении сжимаются. Степень увеличения или уменьшения первоначального размера металла при изменении температуры на один градус характеризуется коэффициентом линейного расширения.
Химические свойства металлов
К химическим — окисляемость, растворимость и коррозионная стойкость.
Окисление металлов — это реакция соединения металла с кислородом, сопровождающаяся образованием окислов (оксидов). Если рассмотреть окисляемость шире, то это реакции, в которых атомы теряют электроны и образуются различные соединения, например, хлориды, сульфиды. В природе металлы находятся в основном в окисленном состоянии, в виде руд, поэтому их производство основано на процессах восстановления различных соединений.
Растворимость металлов — это их способность образовывать с другими веществами однородные системы — растворы, в которых металл находится в виде отдельных атомов, ионов, молекул или частиц. Металлы растворяются в растворителях, в качестве которых выступают сильные кислоты и едкие щелочи. В промышленности наиболее часто используются: серная, азотная и соляные кислоты, смесь азотной и соляной кислот (царская водка), а также щелочи — едкий натр и едкий калий.
Коррозионная стойкость металлов — это их способность сопротивляться коррозии.
Механические свойства металлов
- К механическим — прочность, твердость, упругость, вязкость, пластичность.
- Прочностью металла называется его способность сопротивляться действию внешних сил, не разрушаясь.
- Твердостью металлов называется способность тела противостоять проникновению в него другого, более твердого тела.
- Упругость металлов — свойство металла восстанавливать свою форму после прекращения действия внешних сил, вызвавших изменение формы (деформацию).
Вязкость металлов — это способность металла оказывать сопротивление быстро возрастающим (ударным) внешним силам.
Вязкость — свойство обратное хрупкости.
Пластичность металлов — это свойство металла деформироваться без разрушения под действием внешних сил и сохранять новую форму после прекращения действия сил. Пластичность—свойство обратное упругости.
Технологические свойства металлов
- К технологическим — прокаливаемость, жидкотекучесть, ковкость, свариваемость, обрабатываемость резанием.
- Прокаливаемость металлов – это их способность получать закаленный слой определенной глубины.
- Жидкотекучесть металлов — это свойство металла в жидком состоянии заполнять литейную форму и воспроизводить ее очертания в отливке.
- Ковкость металлов —это технологическое свойство, характеризующее их способность к обработке деформированием, например, ковкой, вальцеванием, штамповкой без разрушения.
- Свариваемость металлов — это их свойство образовывать в процессе сварки неразъемное соединение, отвечающее требованиям, обусловленным конструкцией и эксплуатацией производимого изделия.
Обрабатываемость металлов резанием — это их способность изменять геометрическую форму, размеры, качество поверхности за счет механического срезания материала заготовки режущим инструментом. Обрабатываемость металлов зависит от их механических свойств, в первую очередь прочности и твердости.
Современными методами испытания металлов являются механические испытания, химический анализ, спектральный анализ, металлографический и рентгенографический анализы, технологические пробы, дефектоскопия. Эти испытания дают возможность получить представление о природе металлов, их строении, составе и свойствах, а также определить качество готовых изделий.
Таблицы свойств металлов
Таблица «Свойства металлов: Чугун, Литая сталь, Сталь»
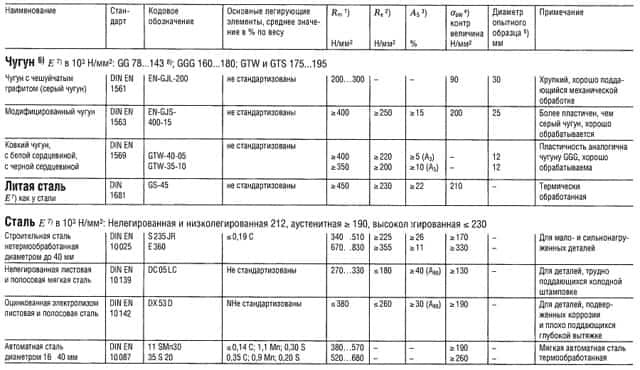
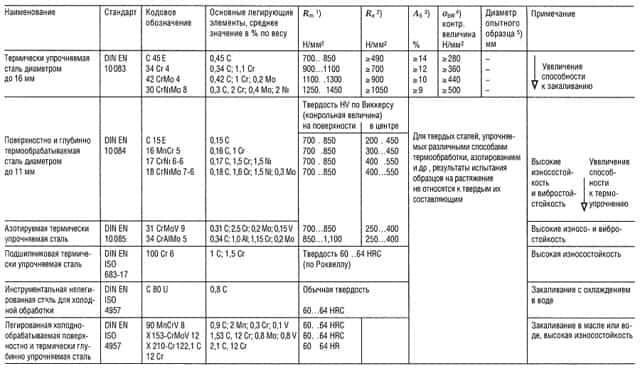
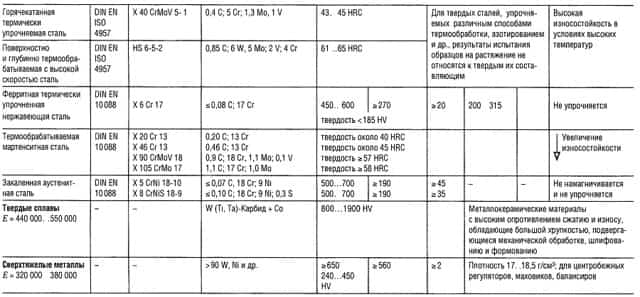
- Предел прочности на растяжение
- Предел текучести (или Rp 0,2);
- Относительное удлинение образца при разрыве;
- Предел прочности на изгиб;
- Предел прочности на изгиб приведен для образца из литой стали;
- Предел усталости всех типов чугуна, зависит массы и сечения образца;
- Модуль упругости;
- Для серого чугуна модуль упругости уменьшается с увеличением напряжения растяжения и остается практически постоянным с увеличением напряжения сжатия.
Таблица «Свойства пружинной стали»
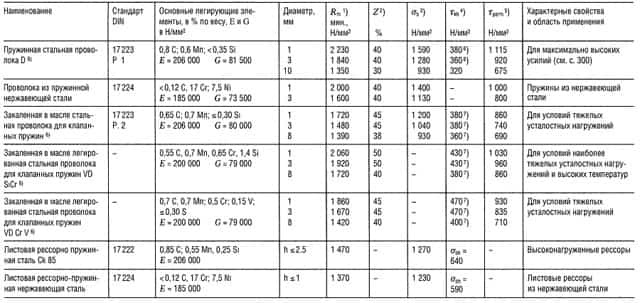
- Предел прочности на растяжение,
- Относительное уменьшение поперечного сечения образца при разрыве,
- Предел прочности на изгиб;
- Предел прочности при знакопеременном циклическом нагружении при N ⩾ 107,
- Максимальное напряжение при температуре 30°С и относительном удлинении 1 2% в течение 10 ч; для более высоких температур см. раздел «Способы соединения деталей»;
- 480 Н/мм2 для нагартованных пружин;
- Приблизительно на 40% больше для нагартованных пружин
Таблица «Свойства кузовных тонколистовых металлов»
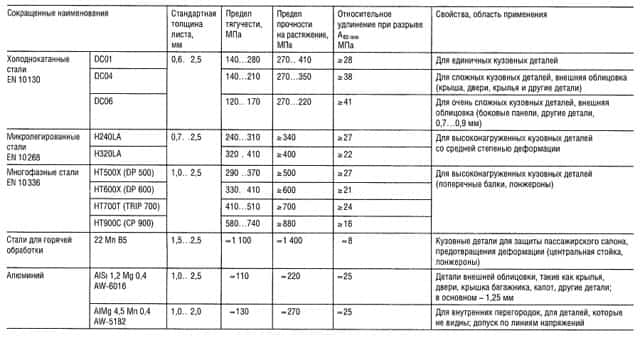
Таблица «Свойства цветных металлов»
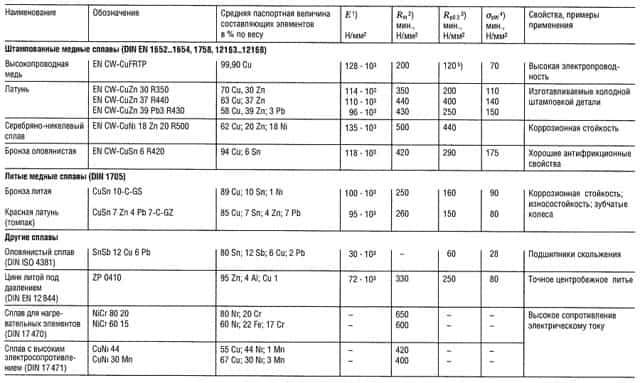
- Модуль упругости, справочные данные;
- Предел прочности на растяжение;
- Предел текучести, соответствующий пластической деформации 0,2%;
- Предел прочности на изгиб;
- Наибольшая величина;
- Для отдельных образцов
Таблица «Свойства легких сплавов»
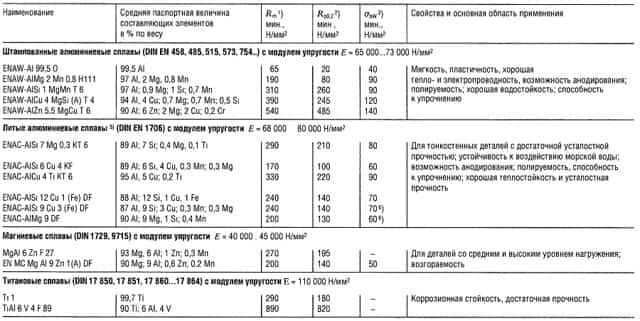
- Предел прочности на растяжение;
- Предел текучести, соответствующий пластической деформации 0,2%;
- Предел прочности на изгиб;
- Наибольшая величина;
- Показатели прочности приведены для образцов и для отливок;
- Показатели предела прочности на изгиб приведены для случая плоского нагружения
Таблица «Металлокерамические материалы (PM)1) для подшипников скольжения»
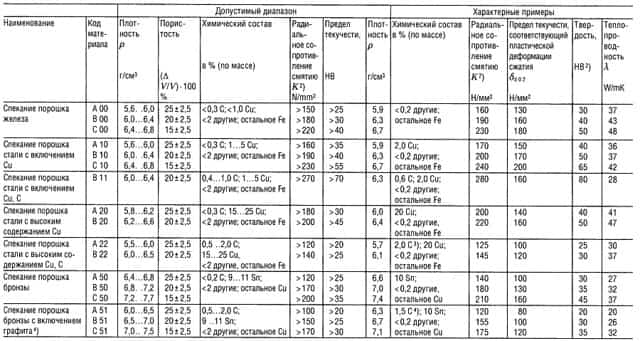
- В соответствии со стандартом DIN 30 910,1990 г. издания;
- Применительно к подшипнику 10/16 г 10;
- Углерод содержится, главным образом, в виде свободного графита;
- Углерод содержится только в виде свободного графита
Таблица «Свойства металлокерамических материалов (РМ)1 для конструкционных деталей»
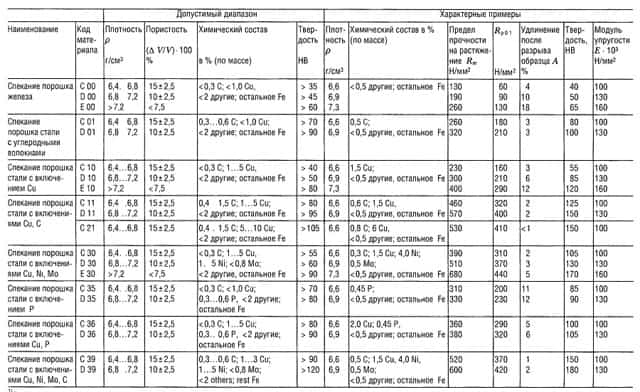
- В соответствии со стандартом DIN 30 910,1990 г. издания;
Магнитные материалы
Таблица «Свойства магнитомягких материалов»
- Данные относятся только к магнитным кольцам.
Магнитомягкие металлы
Таблица «Свойства магнитной листовой и полосовой стали»
Материалы для преобразователей и электрических реакторов
Магнитная проницаемость листового сердечника для классов сплавов С21, С22, Е11, Е31 и Е41 для секции тонколистового сердечника EY11
Материалы для реле постоянного тока
Таблица «Свойства материалов для реле постоянного тока»
Металлокерамические материалы для магнитомягких компонентов
Таблица «Свойства металлокерамических материалов для магнитомягких компонентов»
Магнитомягкие ферриты
Таблица «Свойства магнитомягких ферритов»
- Нормируемые величины;
- Потеря материалом магнитных свойств в зависимости от частоты при низкой плотности магнитного потока (В < 0,1 мТл);
- Потери магнитных свойств при высокой плотности магнитного потока; замеряются предпочтительно при f = 25 кГц, В = 200 мТл, Θ = 100°С;
- Магнитная проницаемость при строго синусоидальном магнитном поле; замеряется при f
Базовые понятия. Запись 7 (физические свойства металлов)
В данной статье ознакомимся с основными физическими свойствами металлов. Вашему вниманию будут представлены пластичность, электропроводность, теплопроводность, металлический блеск, твёрдость, плотность, температура плавления.
Начнём с пластичности.
Пластичность — это свойство вещества изменять форму под внешним воздействием, не разрушаясь, и сохранять принятую форму после прекращения этого воздействия.
Почему у металлов так выходит? Это происходит из-за их строения, виновной выступает кристаллическая решётка. Она состоит из узлов и свободных электронов, которые бегают между углами, никому не принадлежа.
В узлах могут быть атомы, молекулы или ионы. Электроны то присоединяются к ним, то уходят.
Именно взаимосвязью между бегающими по всему веществу электронами и узлами объяснятся свойство пластичности: слои смещаются друг с другом без разрыва.
Как же определить и сравнить пластичность разных металлов? Она определяется при испытании на растяжение. Под действием нагрузки образцы разных металлов в различной степени удлиняются, а их поперечное сечение уменьшается. Чем больше способен образец удлиняться, а его поперечное сечение сужаться, тем пластичнее образец.
Существуют две единицы измерения: относительное удлинение и относительное сужение при разрыв.
- По степени пластичности металлы принято подразделять следующим образом:
- -высокопластичные (относительное удлинение превосходит 40 %) — металлы, составляющие основу большинства конструкционных сплавов (алюминий, медь, железо, титан, свинец) и «легкие» металлы (натрий, калий, рубидий и др.);
- -пластичные (относительное удлинение лежит в диапазоне между 40 и 3%) — магний, цинк, молибден, вольфрам, висмут и др. (наиболее обширная группа);
- -хрупкие (относительное удлинение меньше 3%) — хром, марганец, кобальт, сурьма.
- Электропроводность — свойство проводить электрический ток.
Электрическим током зовём упорядоченное движение частиц. В нашем случае под действие некого поля начинают двигаться в одном направлении все свободные электроны в образце.
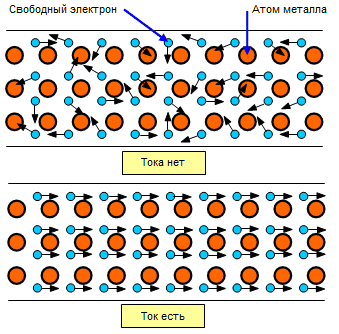
Электропроводность металлов обусловлена концентрацией электронов и их подвижностью. Чем сильнее металл нагрет, тем сильнее прыгающие узлы будут мешать электронам свободно передвигаться в выбранном направлении. Чем больше столкновений, тем сильнее нагревается металл. Данный эффект применяется в нагревательных приборах и в лампах накаливания.
Теплопроводность — свойство металлов переносить энергию от одной части тела к другой.
Оно связано с высокой подвижностью электронов: сталкиваясь с колеблющимися в узлах решётки ионами, атомами, электроны обмениваются с ними энергией. Как видим, данное свойство связано с предыдущим.
Металлический блеск — способность металлов отражать световые лучи.
Данное свойство обуславливается несколькими причинами. Во-первых, от гладкости поверхности, т.е. падающая электромагнитная волна (свет) не застревала в неровностях, а могла отразиться обратно.
Во-вторых, свет попадает на металл, поглощается электронами и через некое малое время излучается обратно, при этом количество энергии, которое может уйти на нагревание, небольшое. Отражённую волну воспринимает наш глаз, цвет волны определяется из величины «длина волны».
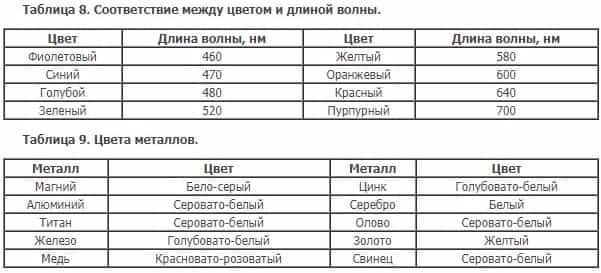
Твёрдость — свойство твёрдого тела сопротивляться проникновению в него другого тела.
Если хотите много теории по данному свойству, то прошу сюда:
- https://libmetal.ru/prop/tverd.htm
Оценка металла по шкале Мооса берёт за основу то, насколько легко образец может быть поцарапан другими металлами.
Например, коэффициент твердости золота — 2,5-3, что значительно ниже коэффициента твердости большинства других материалов.
В то время как графит и некоторые виды пластика стоят на одном конце шкалы, имея значение 1, то на другой её конец ставится алмаз, одно из самых твердых веществ на Земле. Он оценивается в 10 баллов.
Олово: 1.5
Цинк: 2.5
Золото: 2.5-3
Серебро: 2.5-3
Алюминий: 2.5-3
Медь: 3
Медь: 3
Бронза: 3
Никель: 4
Платина: 4-4.5
Сталь: 4-4.5
Железо: 4.5
Палладий: 4.75
Родий: 6
Титан: 6
Укрепленная сталь: 7-8
Вольфрам: 7.5
- Карбид вольфрама: 8.5-9
- Плотность — это отношение массы на объём.
Тяжело расшифровать определение, но я попробую. Оно значит, что при равном объёме разные металлы будут проявлять разную инерцию. Конечно, если и стало понятнее, то на чуток.
- -лёгкие (плотность не более 5 г/см3) — магний, алюминий, титан и др.:
- -тяжёлые — (плотность от 5 до 10 г/см3) — железо, никель, медь, цинк, олово и др. (это наиболее обширная группа);
- -очень тяжёлые (плотность более 10 г/см3) — молибден, вольфрам, золото, свинец и др.
- Таблицы с плотностями:
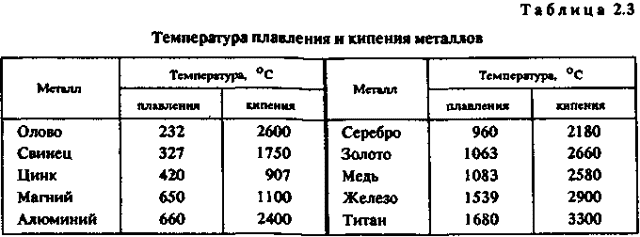
- Температура плавления — температура, при которой осуществляется процесс перехода вещества из твёрдого состояния в жидкое.
При увеличении внутренней энергии начинают сильнее колебаться узлы, решётка теряет свою структуру, нарушаются связи. Примерно такой процесс можно назвать переходом в жидкое состоянии.
- Делят металлы на несколько групп:
- -легкоплавкие (температура плавления не превышает 600 oС) — цинк, олово, свинец, висмут и др.;
- -среднеплавкие (от 600 oС до 1600 oС) — к ним относятся почти половина металлов, в том числе магний, алюминий, железо, никель, медь, золото;
- -тугоплавкие ( более 1600 oС) — вольфрам, молибден, титан, хром и др.
- Больше про плавление написано здесь:
Дополнительная общая ссылка:
- https://examer.ru/ege_po_himii/teoriya/svojstva_prostyx_veshhestv
Большое спасибо за внимание!
Видеоурок «Физические свойства металлов»
Содержание:
§ 1 Свойства металлов 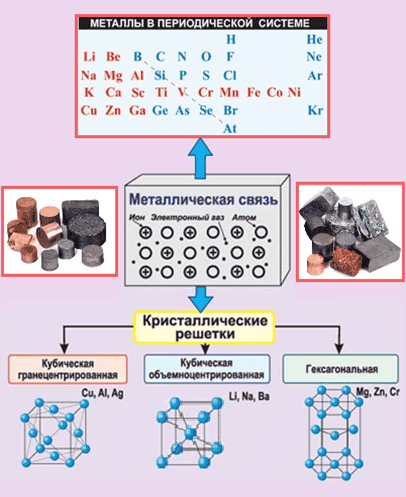
Физические свойства металлов объясняются особенностями строения их кристаллических решеток. В узлах решеток располагаются или положительно заряженные ионы металлов, или их атомы, а между ними перемещаются свободные электроны. Связь, между свободными электронами и ионами металла в кристаллической решетке, называется металлической.
Для металлов характерны как общие физические свойства, так и индивидуальные свойства. Металлический блеск, пластичность и ковкость, теплопроводность и электропроводность – это свойства, характерные для всех металлов, по ним отличают их от неметаллов. Температура плавления, плотность, твердость для каждого металла свои, в этом они отличаются друг от друга.
§ 2 Общие физические свойства металлов
Пластичность– способность металла изменять форму под действием внешних сил без разрушения и сохранять ее после прекращения воздействия. При воздействии на металлическую кристаллическую решетку происходит смещение слоев атом-ионов металла относительно друг друга без разрыва связей, поэтому для них характерна высокая пластичность.
Наиболее пластичные металлы: золото, серебро, медь, олово, свинец. Например из 1 г золота можно получить тончайшую проволоку длиной около 3 км или же лист, способный покрыть потолок трехкомнатной квартиры площадью около 50 м2.
Тончайшие листы золота, толщиной от 1 мкм до 3 мкм, называют сусальным золотом. Его применяют для декоративной отделки изделий, изготовленных в основном из дерева.
Листочками сусального золота оклеивают резные деревянные рельефы, предназначенные для украшения интерьеров дворцов, храмов, дорогой мебели.
- Электропроводность – свойство вещества проводить электрический ток.
- В металлической кристаллической решетке присутствуют свободные электроны, которые при обычных условиях двигаются в беспорядке, а при попадании в электрическое поле начинают двигаться направлено, в результате чего возникает электрический ток.
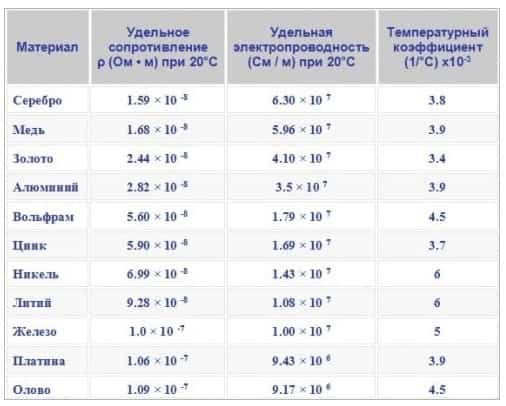
- Наибольшей электропроводностью обладают серебро, медь, золото, алюминий, железо;
а наименьшей – свинец, марганец, вольфрам и ртуть.
При повышении температуры электропроводность металлов уменьшается, это объясняется усилением колебательного движения атомов-ионов металлов, что затрудняет направленное движение электронов.
При понижении температуры электропроводность увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Медь и алюминий наиболее доступные металлы, поэтому их используют в виде проводников электрического тока.
Теплопроводность – способность металла передавать теплоту от более нагретых его частей менее нагретым. Это свойство металлов также объясняется подвижностью свободных электронов, они при движении сталкиваются с колеблющимися в узлах решетки ионами и обмениваются с ними энергией.
При повышении температуры колебания одних ионов передаются другим ионам с помощью электронов, и температура всего металлического предмета быстро выравнивается. Теплопроводность металлов изменяется в той же последовательности, что и электропроводность.
Наибольшей теплопроводностью обладают серебро, медь, золото, алюминий, железо; а наименьшей – свинец, марганец, вольфрам и ртуть.
Если одновременно в горячую воду опустить например чайные ложки, изготовленные из серебра, меди, золота, алюминия, железа, то быстрее нагреется ложка из серебра, так как ее теплопроводность выше теплопроводности других металлов, затем медная, золотая, алюминиевая и затем железная ложки.
§ 3 Отличительные особенности металлов
Твердость – способность твердого тела сопротивляться проникновению в него другого более твердого тела. Все металлы, за исключением ртути, при обычных условиях являются твердыми веществами.
По твердости металлы сравнивают с алмазом, твердость которого принята за 10.
Самыми мягкими являются щелочные металлы (цезий, рубидий, калий, натрий) их можно резать ножом, а самым твердым является хром, он царапают стекло.
Плотность – величина, определяемая отношением массы тела к его объему.
По плотности металлы делятся на легкие (с плотностью менее 5 г/см3) и тяжелые (с плотностью более 5 г/см3). К легким металлам относятся щелочные (литий, натрий), щелочноземельные (кальций, магний) и алюминий. К тяжелым – цинк, железо, никель, медь, серебро, свинец, ртуть, золото, платина. Самый легкий металл – литий (0,53 г/см3), а самый тяжелый – осмий (22,6 г/см3).
Плавкость металлов – это процесс перехода вещества из твердого в жидкое состояние. По температуре плавления металлы можно разделить на легкоплавкие и тугоплавкие.
К легкоплавким относятся металлы, температура плавления которых ниже 10000 С. Это ртуть, галлий, цезий, калий, олово, свинец, цинк, магний, алюминий.
Если температура плавления выше температуры плавления железа 15390 С, то металл является тугоплавким. К ним относятся: титан, хром, ванадий, цирконий, гафний, ниобий, молибден, вольфрам.
Самая низкая температура плавления у ртути – 390 С, поэтому это единственный металл, который при комнатной температуре находится в расплавленном состоянии. Самая высокая температура плавления у вольфрама 34200 С, из этого металла изготавливают нити накаливания электрических ламп.
§ 4 Краткие итоги по теме урока
К физическим свойствам металлов относятся: металлический блеск, пластичность и ковкость, теплопроводность и электропроводность, твердость, плотность, плавкость. Свойства металлов зависят от особенностей строения их кристаллических решеток.
Все металлы обладают металлическим блеском, электропроводностью, теплопроводностью, пластичностью.
Твердость, плотность и температура плавления и кипения металлов отличаются, на эти показатели влияют расположение атомов и ионов в узлах кристаллической решетки и их атомные радиусы.
Список использованной литературы:
- Габриелян О.С. Химия. 9 класс: учебник для общеобразовательных учреждений / М.: Дрофа, 2010.
- Химия. 9 класс: Настольная книга учителя / О.С. Габриелян, И.Г. Остроумов. – М.: Дрофа, 2003
- Рудзитис Г.Е., Фельдман Ф.Г. Химия: Неорган. химия. Орган. химия: Учеб. для 9 кл. общеобразоват. учреждений. – М.: Просвещение, 1999
Использованные изображения:
Физические свойства металлов
- Общие физические свойства металлов
- Благодаря наличию свободных электронов (“электронного газа”) в кристаллической решетке все металлы проявляют следующие характерные общие свойства:
- 1) Пластичность – способность легко менять форму, вытягиваться в проволоку, прокатываться в тонкие листы.
2) Металлический блеск и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл светом.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т.к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение “электронного газа”.
4) Теплопроводность. Обусловлена высокой подвижностью свободных электронов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность – у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и больше радиус атома. Самый легкий – литий (ρ=0,53 г/см3); самый тяжелый – осмий (ρ=22,6 г/см3). Металлы, имеющие плотность менее 5 г/см3 считаются “легкими металлами”.
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т.пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C). Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
Общие химические свойства металлов
Сильные восстановители: Me0 – nē → Men+
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
1. РЕАКЦИИ МЕТАЛЛОВ С НЕМЕТАЛЛАМИ
- 1) С кислородом:2Mg + O2 → 2MgO
- 2) С серой:Hg + S → HgS
- 3) С галогенами:Ni + Cl2 –t°→ NiCl2
- 4) С азотом:3Ca + N2 –t°→ Ca3N2
- 5) С фосфором:3Ca + 2P –t°→ Ca3P2
- 6) С водородом (реагируют только щелочные и щелочноземельные металлы):2Li + H2 → 2LiH
- Ca + H2 → CaH2
2. РЕАКЦИИ МЕТАЛЛОВ С КИСЛОТАМИ
- 1) Металлы, стоящие в электрохимическом ряду напряжений до H восстанавливают кислоты-неокислители до водорода:
- Mg + 2HCl → MgCl2 + H2
- 2Al+ 6HCl → 2AlCl3 + 3H2
- 6Na + 2H3PO4 → 2Na3PO4 + 3H2
- 2) С кислотами-окислителями:
- При взаимодействии азотной кислоты любой концентрации и концентрированной серной с металлами водород никогда не выделяется!
Физические свойства металлов
Всем металлам присущи металлический блеск (однако In и Ag отражают свет лучше других металлов), твердость (самый твердый металл – Cr, самые мягкие металлы – щелочные), пластичность (в ряду Au, Ag, Cu, Sn, Pb, Zn, Fe наблюдается уменьшение пластичности), ковкость, плотность (самый легкий металл – Li, самый тяжелый – Os), тепло – и электропроводность, которые уменьшаются в ряду Ag, Cu, Au, Al, W, Fe.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип > 1000С) и легкоплавкие (Tкип < 1000С). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Физические свойства металлов IА группы
Металлы, расположенные в IA группе, называют щелочными. Все щелочные металлы легкие (обладают небольшой плотностью), очень мягкие (за исключением Li легко режутся ножом и могут быть раскатаны в фольгу), имеют низкие температуры кипения и плавления (с ростом заряда ядра атома щелочного металла происходит понижение температуры плавления).
- В свободном состоянии Li, Na, K и Rb – серебристо-белые металлы, Cs – металл золотисто-желтого цвета.
- Щелочные металлы хранят в запаянных ампулах под слоем керосина или вазелинового масла, поскольку они обладают высокой химической активностью.
- Щелочные металлы обладают высокой тепло- и электропроводностью, что обусловлено наличием металлической связи и объемоцентрированной кристаллической решетки
Физические свойства металлов IIА группы
Металлы, расположенные в IIA группе, называют щелочноземельными. В свободном состоянии Be – металл серо-стального цвета, обладающий плотной гексагональной кристаллической решеткой, достаточно твердый и хрупкий. На воздухе Be покрывается оксидной пленкой, что придает ему матовый оттенок и снижает его химическую активность.
Магний в виде простого вещества представляет собой белый металл, который, также, как и Be, при нахождении на воздухе приобретает матовый оттенок за счет образующейся оксидной пленки. Mg мягче и пластичнее бериллия. Кристаллическая решетка Mg – гексагональная.
Ca, Ba и Sr в свободном виде – серебристо-белые металлы. При нахождении на воздухе мгновенно покрываются желтоватой пленкой, которая представляет собой продукты их взаимодействия с составными частями воздуха. Кальций – достаточно твердый металл, Ba и Sr – мягче.
Ca и Sr имею кубическую гранецентрированную кристаллическую решетку, барий – кубическую объемоцентрированную кристаллическую решетку.
Все щелочноземельные металлы характеризуются наличием металлического типа химической связи, что обуславливает их высокую тепло- и электропроводность. Температуры кипения и плавления щелочноземельных металлов выше, чем щелочных металлов.
Физические свойства металлов IIIА группы
Металлы, находящиеся в IIIA группе – Al, Ga, In, Tl – в свободном виде представляют собой металлы серебристого цвета с характерным металлическим блеском, обладающие высокими значениями тепло- и электропроводности. За счет образования оксидной пленки при пребывании на воздухе Tl темнеет.
При переходе от Al к Tl, т.е. с ростом заряда ядра атома химического элемента, происходит уменьшение температур кипения и плавления простых веществ.
Физические свойства металлов IVА группы
Металлы, находящиеся в IVA группе – Ge, Sn, Pb. В свободном виде Ge представляет собой металл серебристо-белого цвета, Pb – металл сине-серого цвета. Для олова характерно явление аллотропии, так, различают белое и серое олово, различающиеся строением кристаллической решетки (тетрагональная у белого олова и кубическая у серого).
Физические свойства металлов IVВ группы
В эту группу входят Ti, Zr и Hf, которые в свободном состоянии и в виде слитков представляют собой металлы серебристо-белого цвета, характеризующиеся ковкостью и пластичностью, хотя присутствие примесей, даже незначительное резко изменяет их характеристики – твердые и хрупкие. Для этих металлов характерна гексагональная плотноупакованная кристаллическая решетка, низкие температуры плавления (тугоплавкие металлы) и кипения, а также невысокая электропроводность.
Физические свойства металлов VВ группы
Ванадий, ниобий и тантал – представители металлов VВ группы. В свободном виде V, Nb, Ta – металлs бледно-серого («стального») цвета. Для ванадия характерны: твердость, пластичность, высокая плотность, легкость, высокая температура плавления. Твердость, ковкость и тугоплавкость – основные характеристики Nb и Ta.
Физические свойства металлов VIВ группы
Для металлов VIB группы характерны высокая электропроводность и твердость, они являются парамагнетиками и в свободном виде представляют собой светло-серые металлы. При переходе от Cr к W, т.е.
с увеличением заряда ядра атома химического элемента, значения температур плавления и кипения, а также плотности увеличиваются.
Cr, Mо и W обладают объемно-центрированной кубической кристаллической решеткой.
Физические свойства металлов VIIВ группы
Металлы, входящие в VIIВ группу – Mn, Tc и Re – в свободном виде – серебристо-белые металлы, для них, как и для металлов VIВ группы с увеличением заряда ядра атома химического элемента характерно увеличение значений температур плавления и кипения, а также плотности. Для технеция и рения характерна плотная гексагональная кристаллическая решетка. Tc – хрупкий металл, Re – более пластичен.
Для марганца характерно несколько модификаций, в зависимости от структуры кристаллической решетки: сложная кубическая – α-марганец, примитивная кубическая – β- марганец, гранецетрированная кубическая – γ- марганец, объемно-центрированная кубическая – δ- марганец.
Физические свойства металлов VIIIВ группы
Металлы, входящие в состав VIII группы – Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt – условно разделяют на 2 подгруппы: элементы подгруппы железа (Fe, Co, Ni) и элементы подгруппы платины (Ru, Rh, Pd, Os, Ir, Pt).
Железо – металл серебристо-белого цвета, кобальт и никель – металлы серовато-белого цвета. Для железа характерны 4 модификации, для кобальта – две, для никеля – одна, в зависимости от структуры кристаллической решетки и температуры, до которой нагревают эти металлы.
Выделяют α- (объемно-центрированная кристаллическая решетка, характерны ферромагнитные свойства, T






