Кристаллизация — процесс выстраивания атомов и молекул в жесткую кристаллическую решетку с хорошо определенной энергетически устойчивой структурой. Мельчайший структурный элемент кристаллической решетки — ячейка. Она способна принимать атомы и молекулы, и благодаря этому свойству формируется макроскопический кристалл.
В процессе кристаллизации атомы и молекулы соединяются между собой под определенными углами, образуя характерную форму кристалла с гладкими поверхностями и гранями. Хотя кристаллизация происходит в природе, у нее также есть широкое промышленное применение.
Она используется на этапе разделения и очистки при производстве фармацевтических и химических продуктов.
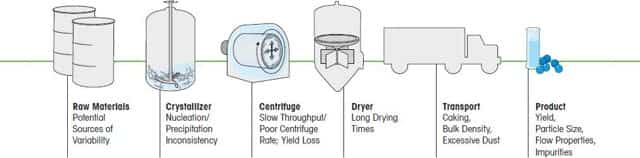
Условия процесса кристаллизации напрямую влияют на размер и форму кристаллов и чистоту кристаллического продукта. Важно понимать сущность процесса кристаллизации и правильно подбирать его параметры.
Это позволит получать однородные кристаллы нужного размера, формы и чистоты, а также предотвратить проблемы на последующих этапах, такие как слишком долгое время фильтрации или недостаточная сушка.
Кристаллизация широко применяется для производства различных необходимых нам продуктов — начиная от пищи и лекарств и заканчивая топливом.
Большинство продуктов агрохимической и фармацевтической промышленности в ходе разработки и производства подвергается нескольким этапам кристаллизации. С помощью этого процесса получают такие ключевые пищевые ингредиенты, как лактоза и лизин.
Однако нежелательная кристаллизация может быть опасна — например, кристаллизация газовых гидратов в глубоководных трубопроводах.
- Кристаллизация— это процесс образования твердой фазы в виде кристаллов из растворов или расплавов.
- Кристалл— тело, частицы которого (атомы, ионы или молекулы) расположены в трехмерной периодической структуре, принимающей естественную форму многогранника.
- Осаждение— синоним кристаллизации, однако этот термин чаще всего употребляется в отношении кристаллизации, которая происходит очень быстро в результате химической реакции.
- Растворимость— свойство вещества, его количество, которое способно раствориться в данном растворителе при данной температуре.
Насыщенный раствор— раствор, содержащий максимальное количество вещества, которое способно раствориться в данном растворителе при данной температуре. Кристаллизация происходит в насыщенном растворе. Количество растворенного на тот момент вещества определяется его растворимостью.
Пересыщение— разница между реальной и равновесной концентрациями растворенного вещества при данной температуре.
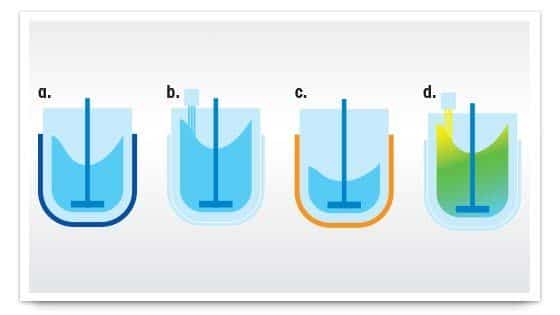
- Кристаллизация происходит, когда растворимость вещества в растворе понижается каким-либо способом. Стандартные методы снижения растворимости:
- a) охлаждение;
- b) добавление антирастворителя;
- c. испарение;
- d) реакция (осаждение).
- Выбор метода кристаллизации зависит от имеющегося оборудования, целей процесса кристаллизации, растворимости и стабильности растворенного вещества в выбранном растворителе.
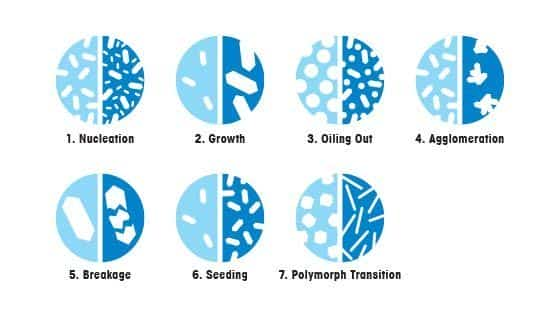
Кристаллизация происходит за счет нескольких взаимосвязанных процессов, на протекание которых влияют выбранные параметры. Основные этапы:
Данные процессы, которые часто протекают в скрытом виде, оказывают ключевое влияние на результат кристаллизации.
- Выберите подходящий растворитель. Ключевые моменты, на которые нужно обратить внимание, — количество вещества, которое можно в нем растворить (растворимость), и безопасность работы с растворителем.
- Повышая температуру, полностью растворите продукт в растворителе. Нерастворенные примеси можно удалить из горячего раствора с помощью фильтрования.
- Чтобы уменьшить растворимость, используйте охлаждение, добавление антирастворителя, испарение или реакцию осаждения. Раствор станет пересыщенным.
- Кристаллизируйте продукт. При уменьшении растворимости до определенной точки начинается нуклеация и рост кристаллов. В ходе этого процесса формируются кристаллы продукта высокой степени чистоты. Примеси останутся в растворе.
- Позвольте системе достигнуть равновесия после охлаждения (или применения другого метода кристаллизации).
- Проведите фильтрацию и сушку готового продукта.
- Ознакомьтесь с подборкой статей по теме кристаллизации:
- Классическая работа по нуклеации кристаллов из растворовJaroslav Nývlt, Kinetics of nucleation in solutions, Journal of Crystal Growth, Volumes 3–4, 1968.
- Исследование механизмов выращивания кристаллов из раствораCrystal Growth Kinetics, Material Science and Engineering, Volume 65, Issue 1, July 1984.
Описание причин, по которым в системах «растворенное вещество — растворитель» вместо кристаллизации происходит образование новой жидкой фазыKiesow et al., Experimental investigation of oiling out during crystallization process, Journal of Crystal Growth, Volume 310, Issue 18, 2008.
Подробное исследование причин агломерации кристаллов в процессе кристаллизацииBrunsteiner et al., Toward a Molecular Understanding of Crystal Agglomeration, Crystal Growth & Design, 2005, 5 (1), pp 3–16.
Исследование механизмов распада агломератов в процессе кристаллизацииFasoli & Conti, Crystal breakage in a mixed suspension crystallizer, Volume 8, Issue 8, 1973, Pages 931–946.
Обзор алгоритмов разработки эффективных процессов кристаллизации в высокотехнологичных сегментах химической промышленностиPaul et al., Organic Crystallization Processes, Powder Technology, Volume 150, Issue 2, 2005.
Технологии, которые гарантируют получение нужной полиморфной формы в процессе кристаллизацииKitamura, Strategies for Control of Crystallization of Polymorphs, CrystEngComm, 2009,11, 949–964.
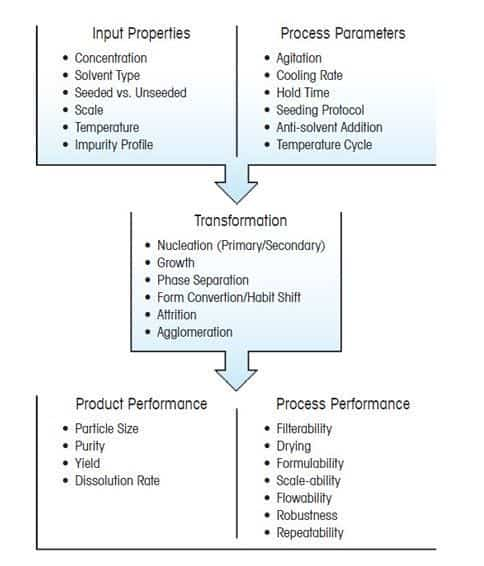
Кристаллы обладают множеством характеристик, но, пожалуй, важнейшая из них — это распределение кристаллов по размерам. От этого параметра в значительной степени зависят качество конечного продукта и эффективность процесса его получения.
Размер и форма кристаллов непосредственно влияют на основные технологические этапы, следующие за кристаллизацией, — фильтрацию и сушку. Конечный размер кристаллов также определяет качество кристаллического продукта.
Например, биологическая доступность и эффективность фармацевтических составов тем выше, чем мельче получаемые кристаллы, так как они лучше растворяются.
Оптимизировать дисперсность кристаллов можно путем тщательного подбора условий и параметров процесса кристаллизации. Чтобы кристаллический продукт приобрел нужные свойства, важно понимать, как параметры процесса влияют на основные превращения в ходе кристаллизации — образование зародышей (нуклеацию), рост и распад кристаллов.
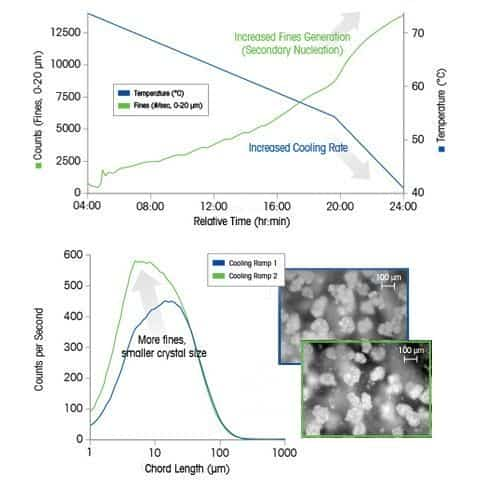
В этом примере охлаждение в конце цикла вызывает вторичную нуклеацию, которая приводит к образованию множества мелких частиц. Исследование проведено с использованием анализаторов размера частиц.
Увеличение скорости охлаждения раствора ведет к более быстрому пересыщению, в результате скорость образования зародышей кристаллов будет выше скорости их роста. Следовательно, чтобы получить нужное распределение кристаллов по размеру, чрезвычайно важно контролировать скорость охлаждения.
Дисперсность кристаллов льда, например, влияет на вкус и консистенцию мороженого: так, кристаллы размером менее 50 мкм предпочтительнее кристаллов, которые больше 100 мкм. Она влияет и на технологические свойства распыляемых агрохимикатов: их частицы должны быть малы настолько, чтобы не засорять сопла при распылении, но при этом достаточно большими, чтобы их не уносило на соседние поля.
При масштабировании получить кристаллический продукт нужного размера и формы с наименьшими издержками возможно лишь в случае понимания всех нюансов кристаллизации.

Рабочая станция кристаллизации позволяет ученым получать максимум информации из каждого эксперимента с помощью централизованного программного решения. Средства процессно-аналитической технологии (PAT):
- Автоматизированные реакторы EasyMax, OptiMax и RX-10, а также реакционный калориметр RC1 обеспечивают непрерывное (24/7) и точное регулирование и регистрацию параметров процесса, включая значения энтальпии кристаллизации, благодаря чему ученые могут точно определять критические параметры процесса (CPP).
- EasyViewer — это зондовый прибор для получения изображений с высоким разрешением и их анализа. EasyViewer рассчитывает характеристики дисперсий кристаллов, частиц и капель в том естественном виде, в каком они находятся в технологической среде.
- ParticleTrack — анализатор размера и количества частиц. Полученная с его помощью статистически достоверная характеристика свойств дисперсных систем способствует успешному масштабированию процесса от лаборатории до производства при полном соблюдении требований ATEX.
- ReactRaman — рамановская спектроскопия in situ позволяет получать информацию химического и структурного характера, которая необходима для комплексного изучения полиморфных систем и выбора параметров процесса, обеспечивающих получение кристаллов требуемой формы.
- ReactIR — спектроскопия ИКФС в режиме реального времени предоставляет важные сведения о концентрации и уровне пересыщения, ширине зоны метастабильности, кинетике снятия пересыщения и конечной точке кристаллизации. Эти данные необходимы для обеспечения повторяемости процесса кристаллизации и гарантированного достижения заданной конечной точки.
- Программное обеспечение iC — обеспечивает взаимодействие между всеми средствами PAT. Все датчики и реакторы могут обмениваться информацией, а все аналитические данные (размер, форма, пересыщение и т. д.) могут быть использованы в качестве контрольных параметров процесса.
В дисперсных системах такие параметры, как температура, интенсивность перемешивания или режим дозирования, непосредственно влияют на качество процесса и конечного продукта. Приборы EasyMax, OptiMax, RC1 и RX-10 обеспечивают точное регулирование и регистрацию условий процесса для гибкого конструирования дисперсных систем.
- Регистрируются все данные: начиная от порядка добавления ингредиентов, программы дозирования и подъема температуры до регулирующих воздействий в ходе процесса.
- Информацию, собранную с помощью средств PAT (ReactIR, ReactRaman, EasyViewer и ParticleTrack), можно сопоставить с графиками изменения параметров процесса, чтобы выявить механизмы формирования частиц.
- Точность автоматического управления позволяет ученым и инженерам уверенно запускать процессы без участия оператора.
Размер, форма и концентрация — это важнейшие свойства частиц на каждой стадии процесса кристаллизации и на всех этапах масштабирования, поэтому они считаются критическими показателями качества (CQA). Анализаторы размера частиц оперативно отображают и количественно характеризуют частицы и важнейшие механизмы их формирования, что существенно облегчает разработку процессов кристаллизации.
- Свойства частиц и механизмы их формирования регистрируются автоматически для последующего анализа.
- Обмен данными между автоматизированными реакторами и системами ParticleTrack и EasyViewer способствует созданию замкнутых автоматических систем. В такой системе ученые могут регулировать режим охлаждения или добавление антирастворителя в зависимости от размера или количества частиц, чтобы избежать формирования нежелательных фракций, например слишком мелких.
- Интуитивно понятная функция «Мастер запуска эксперимента» позволяет ученым быстро накапливать высококачественные данные о свойствах дисперсных систем.
Такие характеристики среды, как концентрация раствора, степень пересыщения и кристаллическая (полиморфная) модификация, часто связаны между собой и в совокупности определяют успех разработки технологического процесса кристаллизации. Системы ReactIR и ReactRaman анализируют состояние раствора и дисперсии для безошибочного достижения заданной конечной точки процесса.
- Они непрерывно контролируют состав раствора и форму отдельных частиц, регистрируют и отображают результаты в режиме реального времени.
- Сочетание спектроскопических средств PAT, таких как ReactIR и ReactRaman, с автоматизированными реакторами позволяет ученым использовать степень пересыщения в качестве параметра регулирования. Процессы кристаллизации проводятся при постоянном пересыщении для достижения более равномерного распределения частиц по размерам.
- Аналитические функции One Click автоматически находят и наглядно отображают химическую и структурную информацию, предоставляя фактические данные для быстрого принятия решений.

Кристаллизация металлов
Любое вещество может находиться в одном из четырех агрегатных состояний: твердом, жидком, газообразном и плазменном. Агрегатное состояние определяется энергией взаимодействия атомов.
Стабильным (равновесным) при определенных внешних условиях является состояние вещества, при котором оно обладает минимумом свободной энергии. Свободная энергия — часть внутренней энергии вещества.
Внутренняя энергия вещества — это сумма потенциальной энергии (энергии взаимодействия) и кинетической энергии частиц (тепловые колебания). Часть внутренней энергии, высвобождающаяся при переходе вещества из одного состояния в другое,называется свободной энергией.
Чем больше высвободится свободной энергии, тем меньшей энергией будет обладать вещество, тем более стабильно его состояние. Свободную энергию можно представить как аналог потенциальной энергии (рис. 1).
В положении 1 шарик имеет максимальную потенциальную энергию. Это положение не является устойчивым, шарик скатывается в положение 2, при котором его потенциальная энергия будет равна 0. Вещество может находиться в метастабильном состоянии (закаленная сталь). Такое состояние не обладает минимумом свободной энергии, но является достаточно устойчивым (стабильным).
Вещество в метастабильном состоянии может находиться бесконечно долго при условии постоянства внешних факторов.Первичная кристаллизация металлов и сплавов. Кристаллизация — это переход металла из жидкого состояния в твердое с образованием кристаллического строения.
Это первичная кристаллизация (в отличие от вторичной, когда кристаллы металлических фаз выделяются из твердого вещества).
Рассмотрение кристаллизации для металлов и сплавов на их основе связано с тем, что эти материалы получают методом литья, тогда как многие неметаллические материалы производят другими способами.
Ряд неметаллических материалов существует в природном виде (углерод), многие химические соединения получают путем химических реакций: карбиды — карбидизацией, нитриды — азотированием и т.п. Процесс кристаллизации (затвердевания) обусловлен стремлением системы к переходу в более устойчивое термодинамическое состояние.
При изменении внешних условий, например температуры, свободная энергия системы меняется различно для жидкого и твердого (кристаллического) состояния (рис. 2). Выше температуры Ts более стабильным
является жидкое состояние, так как металл в этом состоянии имеет меньший запас свободной энергии. Ниже температуры Ts меньшим запасом свободной энергии обладает металл в твердом состоянии.
При температуре величины свободных энергий твердого и жидкого состояний равны. Это означает, что металл может находиться в обоих состояниях бесконечно долго, так как переход из одного состояния в другое не будет сопровождаться уменьшением свободной энергии.
Температура Ts получила название теоретической температуры кристаллизации.
Для начала кристаллизации необходимо, чтобы свободная энергия металла в твердом состоянии стала меньше свободной энергии жидкого состояния. Это становится возможным при охлаждении жидкости ниже Ts.
Температура, при которой фактически начинается процесс кристаллизации, называется фактической температурой кристаллизации (Тк).
Охлаждение жидкого металла ниже теоретической температуры кристаллизации называется переохлаждение, а разность между теоретической и фактической температурой кристаллизации — степенью переохлаждения (ΔТ):
ΔТ=Тs — Тk
Степень переохлаждения зависит от скорости охлаждения жидкого металла. С увеличением скорости охлаждения понижается фактическая температура кристаллизации и, следовательно, возрастает степень переохлаждения.
Процесс кристаллизации можно описать с помощью кривых охлаждения, построенных в координатах «температура — время» (рис. 3).
Охлаждение в жидком состоянии сопровождается плавным понижением температуры (участок 1 кривой охлаждения), при достижении температуры кристаллизации на кривой охлаждения появляется горизонтальная площадка (участок 2 кривой охлаждения), т.е. охлаждение (понижение температуры) останавливается.
Это вызвано тем, что отвод тепла компенсируется выделяющейся в процессе кристаллизации скрытой
теплотой кристаллизации. После полного перехода металла из жидкого состояния в твердое температура вновь начинает плавно снижаться (участок 3 кривой охлаждения). Увеличение скорости охлаждения от V1 до V3 приводит к увеличению степени
переохлаждения (см. рис. 3).
Кристаллизация начинается с образования в жидком металле центров кристаллизации и продолжается за счет роста их числа и размеров (рис. 4). Процесс кристаллизации можно охарактеризовать двумя параметрами: числом центров кристаллизации (ЧЦК),

образующихся в единицу времени в единице объема (1 см3/с), и скоростью роста кристаллов (СК ) [мм /с]. Эти параметры зависят от степени переохлаждения, а следовательно, от скорости охлаждения при кристаллизации металла.
В соответствии с законом Таммана для каждой степени переохлаждения указанные параметры могут иметь только одно значение (рис. 5).
При теоретической температуре кристаллизации ( Ts) значения ЧЦК и СК равны 0 и кристаллизация происходить не может.
При повышении степени переохлаждения значения ЧЦК и СК возрастают, процесс кристаллизации идет быстро. Это объясняется тем, что при высоких температурах, близких к Тs подвижность атомов велика.
При определенных степенях переохлаждения значения ЧЦК и СК достигают максимума, после чего снижаются вследствие уменьшения подвижности атомов при низких температурах.
Размер образовавшихся в процессе кристаллизации зерен зависит от соотношения величин ЧЦК и СК, т.е. определяется степенью переохлаждения (скоростью охлаждения
металла в процессе кристаллизации).
При малых степенях переохлаждения (низкой скорости охлаждения металла) образуется малое число центров кристаллизации, которые
растут с большой скоростью,—- АТ' (см. рис. 5). В этом случае структура металла после окончания кристаллизации будет крупнозернистой.
При больших степенях переохлаждения, напротив, ЧЦК велико, а СК мала (ДГ» — АТ”'), поэтому структура металла получается мелкозернистой.
Если степень переохлаждения настолько велика, что значения ЧЦК и СК близки к пулю, кристаллизации не происходит.
При этом образуется твердое тело, имеющее не кристаллическое строение с «правильным» расположением атомов, а аморфное — с хаотическим расположением атомов — «твердая жидкость». Аморфное состояние
характерно для неметаллических материалов (стекла, полимеры). Для получения аморфного состояния у металлических материалов требуется очень большая скорость охлаждения 106… 107 °С/с.
Процесс кристаллизации металлов
Кристаллизацией называется переход из жидкого в твердое состояние с образованием кристаллических решеток или кристаллов. В реальных металлических телах кристаллизация расплавов заканчивается образованием структуры сложно переплетенных кристаллов — дендритов. Их морфология определяет свойства материалов. При образовании кристаллов их развитие идет в основном в направлении, перпендикулярном плоскостям с максимальной плотностью упаковки атомов. Это приводит к тому, что первоначально образуются длинные ветви, так называемые оси первого порядка. Одновременно с удлинением осей первого порядка на их ребрах зарождаются и растут перпендикулярные к ним такие же ветви второго порядка. в свою очередь на них растут оси третьего порядка и т.д. Образуются кристаллы древовидной — дендритной формы. Преимущественный рост кристалла происходит в направлении отвода тепла. Ветви дендритов разделены очень тонкими прослойками нерастворимых в жидком и особенно в твердом состоянии примесей и мельчайшими полостями и порами, возникшими в результате уменьшения объема при переходе металла из жидкого состояния в твердое. При tпл, определенной для каждого металла, твердый металл переходит в жидкий. Многие свойства при этом меняются незначительно. Например, плотность падает на 5-7% , электропроводность и теплопроводность возрастают. Характер внутренних сил не изменяется. Металлическая жидкость по своему строению близка к твердому телу. Кристаллическая решетка сохраняется до температуры плавления. После расплавления решетка разрушается, но сохраняется динамический ближний порядок. Затвердевание происходит при температуре tзатв, она меньше tпл. Существует переохлаждение и перенагрев.
При температуре Тп величины свободных энергий жидкого и твердого состояния равны. Процесс кристаллизации протекает при температуре, меньшей Тп. Для начала затвердевания необходимо переохлаждение (разность энергий). Переохлаждение тем больше, чем больше скорость изменения.
Процесс кристаллизации происходит в два этапа: образование зародышей кристаллов; рост образовавшихся кристаллов.
В реальных металлах центрами кристаллизации являются тугоплавкие частицы и стенки литейной формы.
В чистых металлах центрами кристаллизации служат области с дальним порядком расположения атомов (кластеры), т.е. их строение близко к строению кристаллической решетки.
Чем больше скорость охлаждения (степень переохлаждения), тем более мелкозернистая структура образуется. Если скорость охлаждения порядка 105-106 градусов в секунду, получается аморфная структура.
5.Строение металлического слитка. Особенности строения литого и деформированного металла.
Кристаллизация стального слитка идет в три стадии. Сначала на поверхности слитка образуется зона мелких кристаллов за счет влияния холодных стенок формы, которые обеспечивают в начальный момент времени высокую скорость охлаждения. Затем растут большие кристаллы, вытянутые по направлению отвода теплоты (столбчатые кристаллы).
В середине слитка, где наблюдается наименьшая степень переохлаждения, образуются большие равновесные кристаллы. При некоторых условиях (перегретый жидкий металл, малое содержание примесей) зона крупных равновесных кристаллов почти исчезает. Структура слитка состоит практически из одних столбчатых кристаллов — транскристаллическая.
Зона столбчатых кристаллов обладает наибольшей плотностью, но в местах стыка столбчатых кристаллов собираются нерастворимые примеси, и такие слитки часто расьтрескиваются при обработке давлением.
В верхней части слитка, затвердевающей в последнюю очередь, концентрируется усадочная раковина. Там содержится много количества усадочных пор. Слиток имеет неоднородный состав.
По направлению от поверхности к центру и снизу вверх увеличивается концентрация углерода и вредных примесей: серы и фосфора. Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией.
Она отрицательно влияет на механические свойства.
Пластическая деформация металлов и сплавов как тел поликристаллических, имеет некоторые особенности по сравнению с пластической деформацией монокристалла. Деформация поликристаллического тела складывается из деформации отдельных зерен и деформации в приграничных объемах.
Плоскости скольжения зерен произвольно ориентированны в пространстве, поэтому под влиянием внешних сил напряжения в плоскостях скольжения отдельных зерен будут различны.
Деформация начинается в отдельных зернах, в плоскостях скольжения которых возникают максимальные касательные напряжения. Соседние зерна будут разворачиваться и постепенно вовлекаться в процесс деформации.
Деформация приводит к изменению формы зерен: зерна получают форму, вытянутую в направлении наиболее интенсивного течения металла (поворачиваются осями наибольшей прочности вдоль направления деформации.
Металл приобретает волокнистое строение. Волокна с вытянутыми вдоль них неметаллическими включениями являются причиной неодинаковости свойств вдоль и поперек волокон. Одновременно с изменением формы зерен в процессе пластической деформации происходит изменение ориентировки в пространстве их кристаллической решетки.
Деформированный металл находится в неравновесном состоянии. Переход к равновесному состоянию связан с уменьшением искажений в кристаллической решетке, снятием напряжений, что определяется возможностью перемещения атомов.
- При повышении температуры металла в процессе нагрева после пластической деформации диффузия атомов увеличивается и начинают действовать процессы разупрочнения, приводящие металл в более равновесное состояние – возврат и рекристаллизация.
- Возврат. Небольшой нагрев вызывает ускорение движения атомов, снижение плотности дислокаций, устранение внутренних напряжений и восстановление кристаллической решетки
- Рекристаллизация – процесс зарождения и роста новых недеформированных зерен при нагреве наклепанного металла до определенной температуры.
Нагрев металла до температур рекристаллизации сопровождается резким изменением микроструктуры и свойств. Нагрев приводит к резкому снижению прочности при одновременном возрастании пластичности. Также снижается электросопротивление и повышается теплопроводность.
1 стадия – первичная рекристаллизация (обработки) заключается в образовании центров кристаллизации и росте новых равновесных зерен с неискаженной кристаллической решеткой. Новые зерна возникают у границ старых зерен и блоков, где решетка была наиболее искажена. Количество новых зерен постепенно увеличивается и в структуре не остается старых деформированных зерен.
Движущей силой первичной рекристаллизации является энергия, аккумулированная в наклепанном металле. Система стремится перейти в устойчивое состояние с неискаженной кристаллической решеткой.
2 стадия – собирательная рекристаллизация заключается в росте образовавшихся новых зерен.
Движущей силой является поверхностная энергия зерен. При мелких зернах поверхность раздела большая, поэтому имеется большой запас поверхностной энергии. При укрупнении зерен общая протяженность границ уменьшается, и система переходит в более равновесное состояние.
Основными факторами, определяющими величину зерен металла при рекристаллизации, являются температура, продолжительность выдержки при нагреве и степень предварительной деформации
С повышением температуры происходит укрупнение зерен, с увеличением времени выдержки зерна также укрупняются. Наиболее крупные зерна образуются после незначительной предварительной деформации 3…10 %. Такую деформацию называют критической. И такая деформация нежелательна перед проведением рекристаллизационного отжига.
Практически рекристаллизационный отжиг проводят дпя малоуглеродистых сталей при температуре 600…700oС, для латуней и бронз – 560…700oС, для алюминевых сплавов – 350…450oС, для титановых сплавов – 550…750oС.
Кристаллизация металла
Кристаллизация металла – процесс изменения жидкого состояния металла на твердое. Этот переход возможен при понижении температуры, и сопряжен с определенными затратами энергии на образование границы раздела – жидкость-кристалл. Кристаллизация, как физический процесс представляет собой образование центров кристаллизации с последующим ростом в них непосредственно самих кристаллов.
Этим же закономерностям подчиняется кристаллизация не только чистых металлов, но и их сплавов. Основным условием протекания процесса является то, что система должна стремиться к состоянию, в котором значение свободной энергии будет минимальным.
Особенности процесса
- Центры образуются случайно, без привязки друг к другу. На начальной стадии они имеют правильную форму, но впоследствии из-за столкновения и соединения нескольких центров в один, форма их становится неправильной. Число центров напрямую зависит от температуры переохлаждения.
- В начале процесса кристаллизация идет более быстро – объем жидкой фазы велик и в ней активно образуются кристаллы. Когда их объемное количество превышает половину всего тела, из-за столкновения кристаллов скорость процесса замедляется.
Важно понимать, что кристаллизация одного и того же металла может проходить по-разному и результат процесса, а именно размер кристаллов – будет различным. В частности, речь идет о зависимости от числа центров и скорости роста кристаллов. Если центров много, а скорость процесса кристаллизации невысокая, образуется твердый металл с мелкими зернами кристаллов. Если число центров небольшое, но скорость их роста высокая – образуется крупнозернистый металл.
Эту особенность используют на металлургическом производстве. Так, для литья тонкостенных изделий и обеспечения их прочности, используют процесс мелкозернистой кристаллизации. Если же необходимо отлить деталь с толстыми стенками, подойдет метод крупнозернистой кристаллизации.
Важно: если температура жидкого металла становится ниже температуры переохлаждения (то есть жидкий металл быстро и сильно переохладить), не выполняется основное условие кристаллизации – нет центров, и не растут кристаллы, то есть процесс кристаллизации не происходит. Жидкий металл, минуя твердую форму, сразу переходит в аморфное состояние.
Кристаллизация металлов
Эмпирически доказано, что при небольшом давлении с уменьшением температуры все вещества (исключение — гелий) превращаются в твердые тела, то есть кристаллизуются.
Если давление достаточно высоко, то большое количество веществ превращается из жидкостей в твердые вещества. Вещества, называемые аномальными, сохраняют свою жидкую фазу вплоть до $T=0K$ при большом давлении.
К таким веществам относят те вещества, плотность которых уменьшается при переходе от жидкости к твердому состоянию. Температура плавления таких веществ уменьшается при росте давления.
К аномальным веществам относят, например:
Определение 1
Кристаллизацией называют переход из состояния жидкости в твердое состояние при определенных температуре и давлении.
В процессе кристаллизации выделяется теплота, которую именуют теплотой кристаллизации.
Кристаллизация – это фазовый переход первого рода. Она происходит при давлении ниже тройной точки.
- Соотношение давления и температуры в фазовом переходе первого рода задает уравнение Клапейрона — Клаузиуса:
- $frac{dp}{dT}=frac{L}{T(V_1-V_2)} (1),$
- где $L$ — скрытая теплота кристаллизации; $V_2$ — удельный объем вещества в твердом состоянии; $V_1$ — удельный объем этого же вещества в виде жидкости.
У большого количества веществ удельный объем в процессе перехода из жидкого состояния в твердое, становится меньше, соответственно плотность растет. Получается, что для этих веществ давление в состоянии фазового перехода $p$ при увеличении температуры увеличивается, поскольку $frac {dp}{dT}>0$.
Металлы могут находиться в трех состояниях:
- в виде газа;
- жидкости;
- твердом состоянии,
- это зависит от температуры и давления.
- Химически чистые металлы обладают температурой плавления, при которой они переходят из твёрдого состояния в жидкость, и температурой кипения, при которой они становятся газами.
- Температуры плавления металлов могут колебаться:
- от $-38,9^0 C$ у ртути;
- до $+3410^0C$ у вольфрама.
Возникновения кристаллической решетки идет в процессе перехода металла из состояния жидкости в состояние твердого тела.
Если условия в этом процессе являются идеальными, то результатом этого перехода атомы расположатся в геометрически верной структуре, между ними будут определенные расстояния, то есть атомы составят кристаллическую решетку.
Так, в процессе медленного охлаждения получают монокристаллы, масса которых достигает 200 грамм и больше. Эти кристаллы используют, например, в полупроводниковой технике.
Кривые охлаждения расплавов
Остывание расплавленного металла при уменьшении температуры происходит плавно (рис.1), кривая $A$.
Однако, если достигается температура кристаллизации $T_k$, возникает горизонтальный отрезок, который связывают с наличием выделения скрытой теплоты кристаллизации, компенсирующей отвод теплоты.
При дальнейшем уменьшении температуры металл становится твердым, и его температура продолжает уменьшаться.
Рисунок 1. Кривые охлаждения расплавов. Автор24 — интернет-биржа студенческих работ
В реальной действительности кривая кристаллизации несколько иная (рис.1 $B$). Это происходит потому, что металл в состоянии жидкости, способен существовать при температуре более низкой ($T_p$), чем температура кристаллизации. Температуру $T_p$ называют температурой переохлаждения ($T_p$ В процессе кристаллизации металлов можно выделить две стадии:
- Возникновение центов кристаллизации.
- Рост кристаллов.
Существует несколько схем, которые объясняют процесс кристаллизации жидких металлов. В расплаве возникают центы кристаллизации.
При уменьшении температуры ниже, чем $T_p$ (или $T_k$) за короткий отрезок времени в веществе возникают новые центры кристаллизации, они растут.
При свободном процессе кристаллизации появляется первичная ось, потом возникают вторичные оси и оси высших порядков. Кристаллы обретают древовидную (дендритную) форму.
В настоящих условиях кристаллизация протекает поначалу с большой скоростью, но при взаимном столкновении увеличивающихся кристаллов скорость процесса уменьшается.
До тех пор, пока кристалл находится в жидкости, он обладает правильной формой. Когда кристаллы сталкиваются между собой, они срастаются, правильная форма их нарушается.
Так появляются кристаллы с неправильной формой, называемые зернами (кристаллитами).
Факторы, влияющие на кристаллизацию
На прохождение процесса кристаллизации оказывают основное влияние:
- Наличие температуры переохлаждения.
- Скорость и направление отвода теплоты.
- Наличие примесей в металле, которые являются центрами кристаллизации.
Отметим, что в направлении отвода тепла в процессе кристаллизации, кристалл растет существенно быстрее, чем в других направлениях. Это ведет к возникновению неправильной формы кристаллов.
Рассмотрим кристаллизацию стали. Слитки стали создают в металлических изложницах. В этих емкостях металл не способен кристаллизоваться одновременно во всем объеме, поскольку теплота отводится от вещества не равномерно.
Процесс затвердевания начинается у стенок и дна емкости, так как эти части имеют более низкую температуру, чем вещество внутри.
Твердая сталь имеет более высокую плотность, чем ее расплав, в этой связи в слитке в верхней части, в результате уменьшения объема возникает усадочная раковина.
По химическому составу вещество будет неоднородным. Оси растущего кристалла имеют больше легкоплавких элементов, затвердевающих медленнее.
Процесс формирования слитка можно описать так:
- Расплав стали соприкасается со стенками сосуда, в котором она находится, при этом в начальный момент времени возникают мелкие центры кристаллизации, обладающие разной ориентацией.
- Скорость кристаллизации уменьшается, кристаллы увеличиваются. При этом они ориентируются по направлениям отвода тепла. Возникает зона слитка, которая состоит из ориентированных столбчатых и древовидных кристаллитов.
- Внутренняя часть слитка составлена из неориентированных, крупных равновесных кристаллитов.
- В верхней части слитка имеется усадочная раковина, около нее обычно располагаются мелкие газовые раковины.
Процесс кристаллизации расплавов металлов
Кристаллизация — переход металла (сплава) из жидкого состояния в твердое — происходит в условиях, когда расплав переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией (свободная энергия кристалла меньше свободной энергии жидкой фазы).
Влияние температуры на свободную энергию жидкой (Gж) и твердой фазы (Gт) показано на рис. 1а.
При температуре плавления Тпл жидкая и твердая фазы существуют одновременно. Реальный процесс кристаллизации протекает при переохлаждении металла ниже теоретической температуры кристаллизации Тпл. Величина ?Т= Тпл — Ткр называется степенью переохлаждения.
Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, приведены на рис. 1 б (v— скорость охлаждения, v1 < v2 < v3).
Вначале, когда металл находится в жидком состоянии, температура системы уменьшается плавно. При достижении температуры Тпл на кривой охлаждения появляется горизонтальная площадка, так как отвод теплоты в окружающую среду компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации.
По окончании кристаллизации температура вновь уменьшается плавно. При медленном охлаждении (v1) степень переохлаждения мала, и кристаллизация протекает при температуре, близкой к теоретической температуре кристаллизации Тпл. С увеличением скорости охлаждения степень переохлаждения возрастает, и кристаллизация происходит при более низких температурах.
Рисунок 1. Охлаждение расплава и начало кристаллизации
а — изменение свободной энергии (G) в жидком (G Ж) и твердом (G т) состоянии в зависимости от температуры: Ткр — температура начала кристаллизации; Тпл — температура, при которой жидкая и твердая фазы существуют одновременно; ?T — степень переохлаждения; б — кривые охлаждения металлов при кристаллизации: ?T1, ?T2, ?T3 — степень переохлаждения при скорости охлаждения v1, v2, v3 соответственно.
Чем «чище» жидкий металл, тем выше температура переохлаждения.
Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров.
С повышением степени переохлаждения увеличиваются число зародышей и скорость кристаллизации. Но при дальнейшем повышении степени переохлаждения скорость роста зародышей и скорость кристаллизации уменьшаются.
Рост кристаллов заключается в присоединении к зародышам все новых атомов из жидкой фазы (рис. 2 а). Центры кристаллизации — зародыши (черные квадраты) — самопроизвольно возникают при переохлаждении металла.
Очень маленькие зародыши неустойчивы, возникнув, они растворяются. Чем больше степень переохлаждения, тем устойчивее зародыши, тем меньше их критический размер.
Далее зародыши увеличиваются в размере, одновременно появляются новые зародыши.
Пока число зародышей невелико, кристаллы растут свободно и сохраняют правильную геометрическую форму. В местах соприкосновения отдельных кристаллов рост их отдельных граней прекращается, развиваются грани в тех местах, где есть свободная жидкость. В результате кристаллы не имеют правильной геометрической формы.
Такие кристаллы называются кристаллитами. Чем больше центров кристаллизации, тем больше образуется кристаллов в данном объеме, тем мельче окончательный размер кристаллов.
Однако уменьшение скорости зарождения числа зародышей при критических температурах ограничивает возможность регулирования их размера повышением скорости охлаждения.
С целью регулирования размеров зерен часто применяют искусственное введение в расплав веществ, создающих центры кристаллизации (модифицирование). В технических металлах в качестве центров кристаллизации часто выступают инородные включения (например, шлаковые включения, частички футеровки печи, оксиды металлов).
Рис. 2. Схема кристаллизации металла
а — схема роста кристаллов; б — структура дендрита; в — схема образования дендрита; ¦ — зародыши; 1, 2, 3 — оси кристаллизации.
В большинстве случаев кристаллизация металлов происходит с большой скоростью (кристаллизация при заливке металла в изложницу, кристаллизация расплава при литье в металлические формы).
При ускоренном охлаждении металла кристаллы растут неравномерно.
Рост зародышей по одной из осей (в направлении наибольшего градиента температур) значительно опережает рост по другим осям, происходит так называемая дендритная кристаллизация.
Д.К.Чернов, описывая рост дендрита (рис. 2 б), ввел понятие «порядок осей кристаллизации». После образования зародыша его развитие (рис. 2 в) идет в направлении наибольшего градиента температур (ось первого порядка).
Увеличение размеров осей первого порядка происходит не только в длину, одновременно увеличивается и ее ширина.
В дальнейшем от осей первою порядка под определенными углами начинают расти новые оси, называемые осями второго и третьего порядка.
По мере роста осей более высокого порядка (четвертого, пятого и т.д.) постепенно заполняются все промежутки, ранее занятые жидким металлом, — дендритная кристаллизация замедляется.
Дендритная кристаллизация отчетливо выражена в условиях недостатка жидкого металла для заполнения пространства (поверхностные слои, усадочная раковина) и при наличии примесей и посторонних атомов в расплаве (кристаллизация реальных сплавов).






