- Что такое удельная теплоемкость?
- Зависимость удельной теплоемкости от температуры
- Дифференциальная сканирующая калориметрия
- Метод непосредственного расчета
- Изотермическая ступенчатая ДСК
- ТМДСК со стационарным режимом
- ТМДСК
- TOPEM®
- IsoStep™
- TOPEM®
- Для чего нужно знать удельную теплоемкость?
- Какие преимущества при определении удельной теплоемкости дает метод с температурной модуляцией по сравнению с методом с использованием сапфира?
- Количество теплоты. Удельная теплоёмкость – FIZI4KA
- Примеры заданий
- Часть 1
- Удельная теплоемкость вещества — формулы, определение, обозначение
- Виды теплопередачи
- Теплопроводность
- Конвекция
- Излучение
- Удельная теплоемкость: понятие и формула для расчета
- Таблица удельных теплоемкостей
- Удельная теплоемкость металлов при различных температурах
Что такое удельная теплоемкость?

Теплоемкость — это физическая характеристика вещества, определяемая как количество теплоты, которое требуется для увеличения его температуры на заданную величину.
Удельная теплоемкость, или отношение теплоемкости материала к массе — это количество теплоты, необходимое для увеличения температуры одного грамма материала на один градус шкалы Цельсия (или Кельвина).
Эта физическая характеристика используется в разных целях, в том числе при оптимизации технологических процессов и для оценки термических рисков. Единицей измерения удельной теплоемкости является Дж/г·К.
- Для расчета теплоемкости материала используются следующие уравнения:
- Cp = q / (m ∙ ∆ T),
- где cp = удельная теплоемкость; m = масса в граммах; q = количество полученной или потерянной теплоты; ∆T = изменение температуры.
Зависимость удельной теплоемкости от температуры
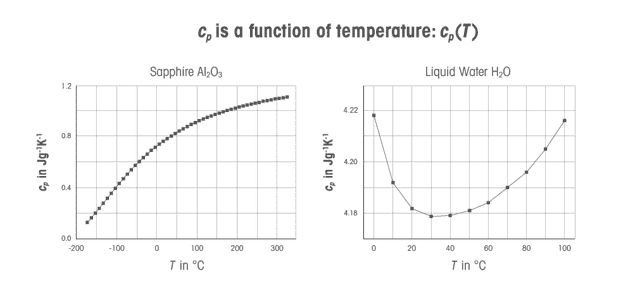
Удельная теплоемкость вещества зависит от температуры. На графике видно, что удельная теплоемкость сапфира возрастает с температурой, что характерно для большинства веществ. Вода отличается исключительно большой удельной теплоемкостью около 4 Дж/г·К с аномальной температурной зависимостью: минимум теплоемкости приходится на температуру около 35 °C.
Чтобы получить дополнительную информацию, посмотрите вебинар «Определение удельной теплоемкости методом ДСК»:
Вещества реагируют на нагревание по-разному. На практике эта разница лучше всего заметна в поведении металла и воды под воздействием прямого солнечного света. Металл, в отличие от воды, нагревается быстро. Это означает, что теплоемкость воды выше теплоемкости металла.
Значения удельной теплоемкости твердых веществ и жидкостей находятся в диапазоне от 0,1 до 5 Дж/г·К. Удельная теплоемкость большинства веществ возрастает вместе с температурой. По этой причине теплоемкость измеряют, как правило, в относительно большом температурном диапазоне. В таблице приведены значения для 25 °C.
| Вещество | Корунд | Алюминий | Свинец | Полистирол | Вода |
| cp (Дж г–1·K–1) | 0,895 | 0,776 | 0,129 | 1,3 | 4,18 |
Дифференциальная сканирующая калориметрия
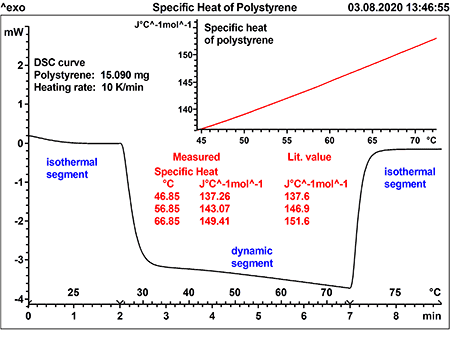
Дифференциальная сканирующая калориметрия (ДСК) — универсальный метод, который применяется во многих научных, испытательных и производственных лабораториях. Этот метод основан на измерении теплового потока в образце, который нагревается, охлаждается или выдерживается в изотермических условиях (при постоянной температуре).
ДСК — распространенный метод определения удельной теплоемкости благодаря своей простоте, короткому циклу измерения и достижимой точности в пределах ± 2 % (в зависимости от варианта осуществления метода; см. следующий раздел).
Обычные приборы для ДСК позволяют выполнять измерения при температуре до 700 °C. Выше 700 °C можно получить хорошие результаты с помощью систем ТГА/ДСК МЕТТЛЕР ТОЛЕДО.
На графике видно, что удельная теплоемкость полистирола в выбранном диапазоне линейно растет с увеличением температуры.
Расчет удельной теплоемкости на основании кривой теплового потока, полученной методом ДСК, может быть выполнен несколькими способами. В программном обеспечении STARe МЕТТЛЕР ТОЛЕДО поддерживаются следующие методы:
Метод непосредственного расчета
| Метод непосредственного расчета |
| Метод с использованием сапфира |
Изотермическая ступенчатая ДСК
| Изотермическая ступенчатая ДСК |
ТМДСК со стационарным режимом
| ТМДСК со стационарным режимом |
ТМДСК
| ТМДСК |
TOPEM®
| TOPEM® |
Метод непосредственного расчета и метод с использованием сапфира реализуются с помощью обычных приборов ДСК и линейной температурной программы. Обычный прибор ДСК измеряет только общий тепловой поток (один сигнал). Однако существуют две составляющие теплоемкости: явная теплоемкость (обратимый тепловой поток) и скрытая теплоемкость (необратимый тепловой поток):
Cp = cp, явная + cp, скрытая
Скрытая теплоемкость связана с физико-химическими переходами (плавлением, кристаллизацией) или химическими реакциями. Эти тепловые эффекты наблюдаются на кривой ДСК в виде эндотермических и экзотермических пиков. Скрытая теплоемкость положительна в случае эндотермических эффектов и отрицательна в случае экзотермических.
Явная теплоемкость связана с количеством тепла, поглощаемого за счет перегруппировки и общего движения молекул. Эта составляющая теплоемкости всегда положительна. На кривой ДСК видно, что в отсутствие тепловых эффектов явная теплоемкость прямо связана с измеренным тепловым потоком. Для многих физико-химических переходов явная теплоемкость составляет базовую линию соответствующего пика.
Температурно-модулированная ДСК (ТМДСК) отличается от обычной ДСК тем, что позволяет разделить общий тепловой поток на обратимую и необратимую часть. Это повышает точность измерения в тех случаях, когда перекрываются разные тепловые эффекты, например стеклование (обратимый процесс) и релаксация энтальпии (необратимый процесс).
Температурные программы ТМДСК намного сложнее программ, используемых в обычном анализе ДСК. МЕТТЛЕР ТОЛЕДО предлагает три методики выполнения измерений ДСК с температурной модуляцией. Ниже указаны их основные особенности.
IsoStep™
- Точное измерение cp с использованием сапфирового эталона.
- Отличает кинетические эффекты от изменений теплоемкости.
- Разделение перекрывающихся эффектов на одной частоте.
TOPEM®
- Уникальная многочастотная методика.
- Разделение перекрывающихся эффектов.
- Наиболее точное измерение cp.
Многочастотная, квазистатическая

Так как удельная теплоемкость является функцией температуры, необходима калибровка (проверка) по температуре в диапазоне измерения. Отклонения следует скорректировать. В методе ДСК наиболее заметной причиной плохой воспроизводимости измерений является передача тепла между датчиком и тиглем и между тиглем и образцом. Способ коррекции изотермического дрейфа описан в стандарте DIN 51007.
Точность измерения повышается за счет надлежащей настройки прибора ДСК с помощью сертифицированных эталонов, например эталонов LGC (Великобритания), NIST (США) или PTB (Германия). Если используется метод непосредственного расчета, тепловой поток должен быть правильно отрегулирован для конкретного температурного диапазона и используемых тиглей.
Более подробно о калибровке приборов МЕТТЛЕР ТОЛЕДО для термического анализа, настройке теплового потока и температуры:
Количественная оценка теплоемкости является методически сложной задачей для ДСК. Тем не менее этот метод широко используется благодаря следующим преимуществам: доступность приборов ДСК, несложная подготовка образцов, относительно короткое время измерения, хорошая точность и наличие коммерческого программного обеспечения для обработки результатов.
Методические советы:
- Стабилизируйте прибор перед измерением.
- Не используйте данные, полученные в первом же эксперименте после включения прибора.
- Проверьте воспроизводимость с помощью повторных измерений.
- Для повышения точности усредняйте результаты нескольких измерений.
- Вычитайте «холостые» значения (кроме TOPEM).
- Точно размещайте тигли на датчике.
- Используйте одни и те же тигли для всех трех измерений. Если это невозможно, используйте тигли с минимальной разницей в массе (
- При большей разнице между тиглями требуется коррекция результатов.
- Рекомендация для органических материалов: используйте тигли 40 мкл и образцы массой от 10 до 20 мг.
- Используйте скорость нагрева от 5 до 10 K/мин.
- Взвешивайте образец после измерения. При значительной потере массы качество измерения cp снижается. В приборах синхронного термического анализа (ТГА/ДСК) потеря массы регистрируется автоматически.
- Для повышения точности, прежде всего в методах без модуляции:
- Используйте образцы большой массы, Cp (образца) >>Cp (эталона).
- Обеспечьте хороший тепловой контакт между образцом и тиглем.
Теплоемкость Cp — свойство образца (не связанное с его массой). Удельная теплоемкость Cp — свойство материала (связанное с массой).
Удельная теплоемкость cp — это сумма явной и скрытой теплоемкости.
Для чего нужно знать удельную теплоемкость?
- Для оптимизации технологических процессов, например литья под давлением, сушки распылением, кристаллизации.
- Для расчета конструкции химических реакторов и обеспечения их безопасности
- Для расчета других термодинамических величин, таких как энтальпия, энтропия, свободная энергия Гиббса.
- Для анализа и интерпретации экспериментальных кривых ДСК.
В диапазоне высоких температур удельную теплоемкость можно измерить с помощью прибора синхронного термического анализа (ТГА/ДСК).
Какие преимущества при определении удельной теплоемкости дает метод с температурной модуляцией по сравнению с методом с использованием сапфира?
- Методы с температурной модуляцией отличаются меньшим дрейфом и достигают точности ± 2 %. Теплоемкость можно также определять в изотермических условиях методами изотермической ступенчатой ДСК, ТМДСК и TOPEM.
- Перекрывающиеся тепловые эффекты, связанные, например, с процессами стеклования и кристаллизации, можно разделять.
Количество теплоты. Удельная теплоёмкость – FIZI4KA
ОГЭ 2018 по физике ›

1. Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством теплоты.
Количеством теплоты называется изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество теплоты обозначают буквой ( Q ). Так как количество теплоты является мерой изменения внутренней энергии, то его единицей является джоуль (1 Дж).
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
2. Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде.
Таким образом, чем больше масса тела, тем большее количество теплоты требуется ему для нагревания. То же самое и с охлаждением: тело большей массы при охлаждении отдаёт большее количество теплоты.
Эти тела сделаны из одного и того же вещества и нагреваются они или охлаждаются на одно и то же число градусов.
[ Qsim m ]
3. Если теперь нагревать 100 г воды от 30 до 60 °С, т.е. на 30 °С, а затем до 100 °С, т.е.
на 70 °С, то в первом случае на нагревание уйдёт меньше времени, чем во втором, и, соответственно, на нагревание воды на 30 °С, будет затрачено меньшее количество теплоты, чем на нагревание воды на 70 °С.
Таким образом, количество теплоты прямо пропорционально разности конечной ( (t_2,^circ C) ) и начальной ( (t_1,^circ C) ) температур: ( Qsim(t_2-t_1) ).
4.
Если теперь в один сосуд налить 100 г воды, а в другой такой же сосуд налить немного воды и положить в неё такое металлическое тело, чтобы его масса и масса воды составляли 100 г, и нагревать сосуды на одинаковых плитках, то можно заметить, что в сосуде, в котором находится только вода, температура будет ниже, чем в том, в котором находятся вода и металлическое тело. Следовательно, чтобы температура содержимого в обоих сосудах была одинаковой нужно воде передать большее количество теплоты, чем воде и металлическому телу. Таким образом, количество теплоты, необходимое для нагревания тела зависит от рода вещества, из которого это тело сделано.
5. Зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К), называется удельной теплоёмкостью вещества.
Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой ( c ). Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Удельная теплоёмкость свинца 140 Дж/кг °С. Это значит, что для нагревания 1 кг свинца на 1 °С необходимо затратить количество теплоты 140 Дж. Такое же количество теплоты выделится при остывании 1 кг воды на 1 °С.
Поскольку количество теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты ( Q ), необходимое для нагревания тела массой ( m ) от температуры ( (t_1,^circ C) ) до температуры ( (t_2,^circ C) ), равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
[ Q=cm(t_2{}^circ-t_1{}^circ) ]
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
6. Пример решения задачи. В стакан, содержащий 200 г воды при температуре 80 °С, налили 100 г воды при температуре 20 °С. После чего в сосуде установилась температура 60 °С. Какое количество теплоты получила холодная вода и отдала горячая вода?
При решении задачи необходимо выполнять следующую последовательность действий:
- записать кратко условие задачи;
- перевести значения величин в СИ;
- проанализировать задачу, установить, какие тела участвуют в теплообмене, какие тела отдают энергию, а какие получают;
- решить задачу в общем виде;
- выполнить вычисления;
- проанализировать полученный ответ.
1. Условие задачи.
Дано:
( m_1 ) = 200 г
( m_2 ) = 100 г
( t_1 ) = 80 °С
( t_2 ) = 20 °С
( t ) = 60 °С
______________
( Q_1 ) — ? ( Q_2 ) — ?
( c_1 ) = 4200 Дж/кг · °С
2. СИ: ( m_1 ) = 0,2 кг; ( m_2 ) = 0,1 кг.
3. Анализ задачи. В задаче описан процесс теплообмена между горячей и холодной водой. Горячая вода отдаёт количество теплоты ( Q_1 ) и охлаждается от температуры ( t_1 ) до температуры ( t ). Холодная вода получает количество теплоты ( Q_2 ) и нагревается от температуры ( t_2 ) до температуры ( t ).
4.
Решение задачи в общем виде. Количество теплоты, отданное горячей водой, вычисляется по формуле: ( Q_1=c_1m_1(t_1-t) ).
Количество теплоты, полученное холодной водой, вычисляется по формуле: ( Q_2=c_2m_2(t-t_2) ).
5. Вычисления.
( Q_1 ) = 4200 Дж/кг · °С · 0,2 кг · 20 °С = 16800 Дж
( Q_2 ) = 4200 Дж/кг · °С · 0,1 кг · 40 °С = 16800 Дж
6. В ответе получено, что количество теплоты, отданное горячей водой, равно количеству теплоты, полученному холодной водой.
При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха.
В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
Содержание
- Примеры заданий
- Ответы
Примеры заданий
Часть 1
1. Удельная теплоёмкость серебра 250 Дж/(кг · °С). Что это означает?
- 1) при остывании 1 кг серебра на 250 °С выделяется количество теплоты 1 Дж
2) при остывании 250 кг серебра на 1 °С выделяется количество теплоты 1 Дж
3) при остывании 250 кг серебра на 1 °С поглощается количество теплоты 1 Дж - 4) при остывании 1 кг серебра на 1 °С выделяется количество теплоты 250 Дж
2. Удельная теплоёмкость цинка 400 Дж/(кг · °С). Это означает, что
- 1) при нагревании 1 кг цинка на 400 °С его внутренняя энергия увеличивается на 1 Дж
2) при нагревании 400 кг цинка на 1 °С его внутренняя энергия увеличивается на 1 Дж
3) для нагревания 400 кг цинка на 1 °С его необходимо затратить 1 Дж энергии - 4) при нагревании 1 кг цинка на 1 °С его внутренняя энергия увеличивается на 400 Дж
3. При передаче твёрдому телу массой ( m ) количества теплоты ( Q ) температура тела повысилась на ( Delta t^circ ). Какое из приведённых ниже выражений определяет удельную теплоёмкость вещества этого тела?
1) ( frac{mDelta t^circ}{Q} )
2) ( frac{Q}{mDelta t^circ} )
3) ( frac{Q}{Delta t^circ} )
4) ( QmDelta t^circ )
4.
На рисунке приведён график зависимости количества теплоты, необходимого для нагревания двух тел (1 и 2) одинаковой массы, от температуры. Сравните значения удельной теплоёмкости (( c_1 ) и ( c_2 )) веществ, из которых сделаны эти тела.
1) ( c_1=c_2 )
2) ( c_1>c_2 )
3) ( c_1
Удельная теплоемкость вещества — формулы, определение, обозначение
Эти два процесса знакомы каждому. Вот нам захотелось чайку, и мы ставим чайник, чтобы нагреть воду. Или ставим газировку в холодильник, чтобы охладить.
Логично предположить, что нагревание — это увеличение температуры, а охлаждение — ее уменьшение. Все, процесс понятен, едем дальше.
Но не тут-то было: температура меняется не «с потолка». Все завязано на таком понятии, как количество теплоты. При нагревании тело получает количество теплоты, а при нагревании — отдает.
Количество теплоты — энергия, которую получает или теряет тело при теплопередаче.
Обнаружено новое непонятное слово — теплопередача. Минуточку, давайте закончим с количеством теплоты.
В процессах нагревания и охлаждения формулы для количества теплоты выглядят так:
|
В этих формулах фигурирует и изменение температуры, о котором мы сказали выше, и удельная теплоемкость, речь о которой пойдет дальше.
А вот теперь поговорим о видах теплопередачи.
Виды теплопередачи
Теплопередача — процесс передачи теплоты (обмена энергией).
Здесь все совсем несложно, видов всего три: теплопроводность, конвекция и излучение.
Теплопроводность
Тот вид теплопередачи, который можно охарактеризовать, как способность тел проводить энергию от более нагретого тела к менее нагретому.
Речь о том, чтобы передать тепло с помощью соприкосновения. Признавайтесь, грелись же когда-нибудь возле батареи. Если вы сидели к ней вплотную, то согрелись вы благодаря теплопроводности. Обниматься с котиком, у которого горячее пузо, тоже эффективно.
Порой мы немного перебарщиваем с возможностями этого эффекта, когда на пляже ложимся на горячий песок. Эффект есть, только не очень приятный. Ну а ледяная грелка на лбу дает обратный эффект — ваш лоб отдает тепло грелке.
Конвекция
Когда мы говорили о теплопроводности, мы приводили в пример батарею. Теплопроводность — это когда мы получаем тепло, прикоснувшись к батарее. Но все вещи в комнате к батарее не прикасаются, а комната греется. Здесь вступает конвекция.
Дело в том, что холодный воздух тяжелее горячего (холодный просто плотнее). Когда батарея нагревает некий объем воздуха, он тут же поднимается наверх, проходит вдоль потолка, успевает остыть и спуститься обратно вниз — к батарее, где снова нагревается. Таким образом, вся комната равномерно прогревается, потому что все более горячие потоки сменяют все менее холодные.

Излучение
Пляж мы уже упоминали, но речь шла только о горячем песочке. А вот тепло от солнышка — это излучение. В этом случае тепло передается через волны.
Если мы греемся у камина, то получаем тепло конвекцией или излучением?????
Обоими способами. То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
Удельная теплоемкость: понятие и формула для расчета
Формулы количества теплоты для нагревания и охлаждения мы уже разбирали, но давайте еще раз:
|
В этих формулах фигурирует такая величина, как удельная теплоемкость. По сути своей — это способность материала получать или отдавать тепло.
С точки зрения математики удельная теплоемкость вещества — это количество теплоты, которое надо к нему подвести, чтобы изменить температуру 1 кг вещества на 1 градус Цельсия:
|
Также ее можно рассчитать через теплоемкость вещества:
|
Величины теплоемкость и удельная теплоемкость означают практически одно и то же. Отличие в том, что теплоемкость — это способность всего вещества к передаче тепла. То есть формулу количества теплоты для нагревания тела можно записать в таком виде:
|
Онлайн-курсы физики в Skysmart не менее увлекательны, чем наши статьи!
Таблица удельных теплоемкостей
Удельная теплоемкость — табличная величина. Часто ее указывают в условии задачи, но при отсутствии в условии — можно и нужно воспользоваться таблицей. Ниже приведена таблица удельных теплоемкостей для некоторых (многих) веществ.
| Газы | C, Дж/(кг·К) |
| Азот N2 | 1051 |
| Аммиак NH3 | 2244 |
| Аргон Ar | 523 |
| Ацетилен C2H2 | 1683 |
| Водород H2 | 14270 |
| Воздух | 1005 |
| Гелий He | 5296 |
| Кислород O2 | 913 |
| Криптон Kr | 251 |
| Ксенон Xe | 159 |
| Метан CH4 | 2483 |
| Неон Ne | 1038 |
| Оксид азота N2O | 913 |
| Оксид азота NO | 976 |
| Оксид серы SO2 | 625 |
| Оксид углерода CO | 1043 |
| Пропан C3H8 | 1863 |
| Сероводород H2S | 1026 |
| Углекислый газ CO2 | 837 |
| Хлор Cl | 520 |
| Этан C2H6 | 1729 |
| Этилен C2H4 | 1528 |
| Металлы и сплавы | C, Дж/(кг·К) |
| Алюминий Al | 897 |
| Бронза алюминиевая | 420 |
| Бронза оловянистая | 380 |
| Вольфрам W | 134 |
| Дюралюминий | 880 |
| Железо Fe | 452 |
| Золото Au | 129 |
| Константан | 410 |
| Латунь | 378 |
| Манганин | 420 |
| Медь Cu | 383 |
| Никель Ni | 443 |
| Нихром | 460 |
| Олово Sn | 228 |
| Платина Pt | 133 |
| Ртуть Hg | 139 |
| Свинец Pb | 128 |
| Серебро Ag | 235 |
| Сталь стержневая арматурная | 482 |
| Сталь углеродистая | 468 |
| Сталь хромистая | 460 |
| Титан Ti | 520 |
| Уран U | 116 |
| Цинк Zn | 385 |
| Чугун белый | 540 |
| Чугун серый | 470 |
| Жидкости | Cp, Дж/(кг·К) |
| Азотная кислота (100%-ная) NH3 | 1720 |
| Бензин | 2090 |
| Вода | 4182 |
| Вода морская | 3936 |
| Водный раствор хлорида натрия (25%-ный) | 3300 |
| Глицерин | 2430 |
| Керосин | 2085…2220 |
| Масло подсолнечное рафинированное | 1775 |
| Молоко | 3906 |
| Нефть | 2100 |
| Парафин жидкий (при 50С) | 3000 |
| Серная кислота (100%-ная) H2SO4 | 1380 |
| Скипидар | 1800 |
| Спирт метиловый (метанол) | 2470 |
| Спирт этиловый (этанол) | 2470 |
| Топливо дизельное (солярка) | 2010 |
- Задача
- Какое твердое вещество массой 2 кг можно нагреть на 10 ˚C, сообщив ему количество теплоты, равное 7560 Дж?
- Решение:
- Используем формулу для нахождения удельной теплоемкости вещества:
- c= Q/m(tконечная — tначальная)
- Подставим значения из условия задачи:
- c= 7560/2*10 = 7560/20 = 378 Дж/кг*˚C
- Смотрим в таблицу удельных теплоемкостей для металлов и находим нужное значение.
| Металлы и сплавы | C, Дж/(кг·К) |
| Алюминий Al | 897 |
| Бронза алюминиевая | 420 |
| Бронза оловянистая | 380 |
| Вольфрам W | 134 |
| Дюралюминий | 880 |
| Железо Fe | 452 |
| Золото Au | 129 |
| Константан | 410 |
| Латунь | 378 |
| Манганин | 420 |
| Медь Cu | 383 |
| Никель Ni | 443 |
| Нихром | 460 |
| Олово Sn | 228 |
| Платина Pt | 133 |
| Ртуть Hg | 139 |
| Свинец Pb | 128 |
| Серебро Ag | 235 |
| Сталь стержневая арматурная | 482 |
| Сталь углеродистая | 468 |
| Сталь хромистая | 460 |
| Титан Ti | 520 |
| Уран U | 116 |
| Цинк Zn | 385 |
| Чугун белый | 540 |
| Чугун серый | 470 |
Ответ: латунь
Удельная теплоемкость металлов при различных температурах
Представлена таблица значений массовой удельной теплоемкости металлов при различных температурах и постоянном давлении. Теплоемкость металлов в таблице указана при отрицательных и положительных температурах (от -253 до 3422°С). Определить удельную теплоемкость металла можно как величину, численно равную количеству теплоты, которое необходимо подвести к единице массы металла для увеличения его температуры на один градус.
Какова удельная теплоемкость металла? При средних и высоких температурах абсолютные значения и температурные зависимости удельной теплоемкости металлов различаются достаточно сильно.
Так, при комнатных температурах наибольшей удельной теплоемкостью отличается литий — она равна 3390 Дж/(кг·град) при температуре 20°С.
Также к металлам с высокой теплоемкостью при средних (до 350°С) температурах можно отнести такие металлы, как магний, алюминий, бериллий, натрий, плутоний.
Наименьшим значением теплоемкости обладают металлы с высокой атомной массой, например торий и уран. Удельная теплоемкость этих металлов равна, соответственно 113 и 116 Дж/(кг·град).
Несмотря на столь большой диапазон изменения этой величины, имеют место некоторые схожие значения, наиболее хорошо прослеживающиеся для металлов одной подгруппы, что является следствием периодической системы Менделеева.
Следует отметить, что при низких отрицательных температурах металлы также имеют широкий диапазон значений теплоемкости.
Например, при температуре -173°С по данным таблицы минимальной теплоемкостью обладает вольфрам. Теплоемкость вольфрама при этой температуре равна всего 87 Дж/(кг·град).
Металлом с самой высокой теплоемкостью при отрицательных температурах является все тот же литий, имеющий низкую атомную массу.
| Алюминий Al | -173…27…127…327…527…661…727…1127…1327 | 483…904…951…1037…1154…1177…1177…1177…1177 |
| Барий Ba | -173…27…127…327…527…729…927…1327 | 177…206…249…290…316…300…292…278 |
| Бериллий Be | -173…27…127…327…527…727…927…1127…1287…1327 | 203…1833…2179…2559…2825…3060…3281…3497…3329…3329 |
| Ванадий V | 27…127…327…527…727…927…1127…1527…1947 | 484…503…531…557…585…617…655…744…895 |
| Висмут Bi | 27…127…272…327…527…727 | 122…127…146…141…135…131 |
| Вольфрам W | -173…27…127…327…727…1127…1527…2127…2527…3127…3422 | 87…132…136…141…148…157…166…189…208…245…245 |
| Гадолиний Gd | 27…127…327…527…727…1127…1312 | 236…179…185…196…207…235…179 |
| Галлий Ga | -173…27…30…127…327…527…727 | 266…384…410…394…382…378…376 |
| Гафний Hf | 27…127…327…527…727…927…1127…1527…2127…2233 | 144…147…156…165…169…183…192…211…202…247 |
| Гольмий Ho | 27…127…327…527…727…927…1127…1327…1470…1527 | 165…169…172…176…193…218…251…292…266…266 |
| Диспрозий Dy | 27…127…327…527…727…927…1127…1327…1409…1527 | 173…172…174…188…210…230…274…296…307…307 |
| Европий Eu | 27…127…327…527…727…826…1127 | 179…184…200…217…250…251…251 |
| Железо Fe | -173…27…127…327…527…727…1127…1327…1537 | 216…450…490…572…678…990…639…670…830 |
| Золото Au | 27…127…327…527…727…927…1105…1127 | 129…131…135…140…145…155…170…166 |
| Индий In | -223…-173…27…127…157…327…527…727 | 162…203…235…250…256…245…240…237 |
| Иридий Ir | 27…127…327…527…727…927…1127…1327…2127…2450 | 130…133…138…144…153…161…168…176…206…218 |
| Иттербий Yb | 27…127…427…527…727…820…927 | 155…159…175…178…208…219…219 |
| Иттрий Y | 27…127…327…527…727…1127…1327…1522 | 298…305…321…338…355…389…406…477 |
| Кадмий Cd | 27…127…321…327…527 | 231…242…265…265…265 |
| Калий K | -173…-53…0…20…63…100…300…500…700 | 631…690…730…760…846…817…775…766…775 |
| Кальций Ca | -173…27…127…327…527…727…842…1127 | 500…647…670…758…843…991…774…774 |
| Кобальт Co | 27…127…327…527…727…1127…1327…1497…1727 | 421…451…504…551…628…800…650…688…688 |
| Лантан La | 27…127…327…527…727…920 | 195…197…200…218…238…236 |
| Литий Li | -187…20…100…300…500…800 | 2269…3390…3789…4237…4421…4572 |
| Лютеций Lu | 27…127…327…527…727…1127…1327…1650 | 153…153…156…163…173…207…229…274 |
| Магний Mg | -173…27…127…327…527…650…727…1127 | 648…1025…1070…1157…1240…1410…1391…1330 |
| Марганец Mn | -173…27…127…327…527…727…1127…1246…1327 | 271…478…517…581…622…685…789…838…838 |
| Медь Cu | 27…127…327…527…727…927…1085…1327 | 385…398…417…433…451…481…514…514 |
| Молибден Mo | 27…127…327…527…727…1127…1327…1527…1727…2127…2623 | 250…262…276…285…294…320…337…357…379…434…418 |
| Мышьяк As | -253…-233…-193…-123…-23…127…327…727 | 15…75…175…275…314…339…354…383 |
| Натрий Na | -173…-53…-13…20…100…300…500…700 | 977..1180…1200…1221…1385…1280…1270…1275 |
| Неодим Nd | 27…127…327…527…727…927…1024…1127 | 190…200…223…253…291…309…338…338 |
| Нептуний Np | 127 | 147 |
| Никель Ni | -173…-50…20…100…300…500…800…1000…1300…1455 | 423…442…457…470…502…530…565…580…586…735 |
| Ниобий Nb | 27…127…327…527…727…1127…1327…1527…1727…2127…2477 | 263…274…285…293…301…322…335…350…366…404…450 |
| Олово Sn | -173…27…127…232…327…527…727 | 187…229…244…248…242…236…235 |
| Осмий Os | 27…127…327…527…727…1127…1327…1527…1727…1927 | 130…132…136…140…144…152…156…160…164…168 |
| Палладий Pd | 27…127…327…527…727…927…1127…1527 | 244…249…256…264…277…291…306…343 |
| Платина Pt | 27…127…327…527…727…1127…1527…1772 | 133…136…141…147…152…163…174…178 |
| Плутоний Pu | 27…127…327…527…727 | 134…586…1500…2430…3340 |
| Празеодим Pr | 27…127…327…527…727…935 | 184…202…224…253…287…305 |
| Радий Ra | 950 | 136 |
| Рений Re | 27…127…327…527…727…927…1127…1327…1527…1927 | 136…139…145…151…157…163…168…174…180…192 |
| Родий Rh | 27…127…327…527…727…1127…1327…1727 | 243…253…273…293…311…342…355…376 |
| Ртуть Hg | -223…-173…-73…-39…27…127…227…327 | 99…121…136…141…139…137…136…135 |
| Рубидий Rb | -173…-73…20…40…127…327…527…727 | 299…321…356…364…361…356…359…368 |
| Рутений Ru | 27…127…327…527…727…1127…1327…1527…1727…1927…2334 | 238…241…251…265…278…306…325…346…367…389…414 |
| Самарий Sm | 27…127…327…527…727…1078…1227 | 197…221…272…293…300…313…334 |
| Свинец Pb | -223…-173…-73..27…127…227…328…527…727 | 103…117…123…128…133…138…146…143…140 |
| Серебро Ag | 27…127…327…527…727…962…1127 | 235…239…250…256…277…310…310 |
| Скандий Sc | 27…127…327…527…727…1127…1541…1627 | 568…586…611…647…694…815…978…978 |
| Стронций Sr | -173…27…127…327…527…768…1127 | 268…306…314…343…377…411…411 |
| Сурьма Sb | -223…-173…27…127…327…527…630…927 | 100…163…209…213…224…234…275…275 |
| Таллий Tl | -173…27…127…303…727 | 120…129…134…149…141 |
| Тантал Ta | 27…127…327…527…727…1127…1527…2127…2327…2727…3022 | 140…144…150…154…157…160…162…177…187…219…243 |
| Тербий Tb | 27…127…327…527…727…1127…1357 | 182…179…189…207…226…272…292 |
| Технеций Tc | 27…127…327…527…727…1127…1327…2127…2200 | 210…211…225…256…290…324…318…297…290 |
| Титан Ti | 27…127…327…527…727…1127…1327…1527…1671…1727 | 531…556…605…637…647…664…729…800…989…989 |
| Торий Th | -173…27…127…327…527…727…1127…1327…1750…1927 | 98…113…117…124…132…140…155…163…198…198 |
| Тулий Tm | 27…127…327…527…727…1127…1327…1545 | 159…161…163…175…186…204…213…244 |
| Уран U | -173…27…127…327…527…727…842…1127 1135…1327…1927 | 93…116…125…146…175…178…161…161…201…203…209 |
| Хром Cr | 25…127…327…527…727…1127…1327…1527…1727…1907 | 453…482…517…558…614…764…849…936…1020…962 |
| Цезий Cs | -173…27…29…127…327…527…727 | 194…244…246…241…226…219…225 |
| Церий Ce | 27…127…327…527…727…804…927 | 292…202…228…246…268…269…269 |
| Цинк Zn | 27…127…327…420…527…727 | 389…403…436…480…480…480 |
| Цирконий Zr | 27…127…327…527…727…1127…1327…1527…1727…1860 | 279…295…321…345…367…325…341…360…381…467 |
| Эрбий Er | 27…127…327…527…727…1127…1327…1505 | 168…169…174…181…192…220…238…231 |
Зависимость удельной теплоемкости металлов от температуры различна. Наиболее сильную зависимость теплоемкости от температуры имеют плутоний и бериллий.
Для многих металлов увеличение температуры приводит к постоянному росту их теплоемкости. У других металлов теплоемкость при нагревании увеличивается, а при достижении температуры плавления снижается или остается практически постоянной.
Удельная теплоемкость металлов в жидком (расплавленном) состоянии практически не меняется.
Металлы в таблице расположены в алфавитном порядке, величина теплоемкости соответствует указанным температурам, допускается интерполяция значений. Например, удельную теплоемкость алюминия при температуре 90°С можно определить по таблице следующим образом: 904+(951-904)/(127-27)*90=946,3 Дж/(кг·град).
Источники:






