- СТРУКТУРА
- СВОЙСТВА
- Запасы и добыча
- ПРОИСХОЖДЕНИЕ
- ПРИМЕНЕНИЕ
- КЛАССИФИКАЦИЯ
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
- Вольфрам – полезные свойства и особенности металла
- Что представляет собой
- Как был открыт
- Старатели
- Наука
- Как представлен в природе
- Физико-химические характеристики
- Месторождения, добыча
- Технология получения
- Как используется
- Соединения
- Другие формы
- Значение для человека
- Цены
- Вольфрам — свойства и область применения — Портал о ломе, отходах и экологии
- Основные характеристики вольфрама
- Сплавы, содержащие вольфрам
- Область применения вольфрама
- Вольфрам: свойства, температура плавления, плотность, история открытия. Применение, продукция из вольфрама
- Тугоплавкий металл вольфрам
- Что такое вольфрам?
- История открытия
- Основные характеристики
- Вольфрам обладает важными химическими свойствами:
- Какие марки существуют?
- Преимущества и недостатки
- Где используется?
- Применение вольфрама и сплавов востребовано в разных сферах:
- Виды продукции
- Вольфрам | это… Что такое Вольфрам?
- История и происхождение названия
- Нахождение в природе
- Месторождения
- Получение
- Физические свойства
- Химические свойства
- Применение
- Металлический вольфрам
- Соединения вольфрама
- Другие сферы применения
- Рынок вольфрама
- Биологическая роль
- Изотопы
- Интересные факты
- Примечания
 Вольфрам — самый тугоплавкий из металлов. Более высокую температуру плавления имеет только неметаллический элемент — углерод. При стандартных условиях химически стоек. Название Wolframium перешло на элемент с минерала вольфрамит, известного ещё в XVI в. под названием лат. Spuma lupi («волчья пена») или нем. Wolf Rahm (“волчьи сливки”, “волчий крем”). Название было связано с тем, что вольфрам, сопровождая оловянные руды, мешал выплавке олова, переводя его в пену шлаков («пожирает олово как волк овцу»).
Вольфрам — самый тугоплавкий из металлов. Более высокую температуру плавления имеет только неметаллический элемент — углерод. При стандартных условиях химически стоек. Название Wolframium перешло на элемент с минерала вольфрамит, известного ещё в XVI в. под названием лат. Spuma lupi («волчья пена») или нем. Wolf Rahm (“волчьи сливки”, “волчий крем”). Название было связано с тем, что вольфрам, сопровождая оловянные руды, мешал выплавке олова, переводя его в пену шлаков («пожирает олово как волк овцу»).
СТРУКТУРА
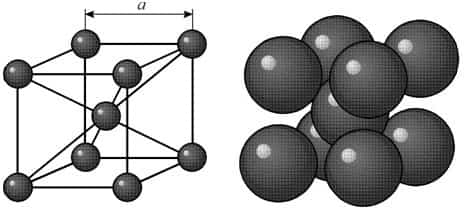 Кристалл вольфрама имеет объемноцентрированную кубическую решетку. Кристаллы вольфрама на холоду отличаются малой пластичностью, поэтому в процессе прессования порошка они практически почти не изменяют своей основной формы и размеров и уплотнение порошка происходит главным образом путем относительного перемещения частиц.
Кристалл вольфрама имеет объемноцентрированную кубическую решетку. Кристаллы вольфрама на холоду отличаются малой пластичностью, поэтому в процессе прессования порошка они практически почти не изменяют своей основной формы и размеров и уплотнение порошка происходит главным образом путем относительного перемещения частиц.
В объемно-центрированной кубической ячейке вольфрама атомы располагаются по вершинам и в центре ячейки, т.е. на одну ячейку приходится два атома. ОЦК-структура не является плотнейшей упаковкой атомов. Коэффициент компактности равен 0,68. Пространственная группа вольфрама Im3m.
СВОЙСТВА

Вольфрам является одним из наиболее тяжелых, твердых и самых тугоплавких металлов. В чистом виде представляет собой металл серебристо-белого цвета, похожий на платину, при температуре около 1600 °C хорошо поддается ковке и может быть вытянут в тонкую нить.
Запасы и добыча
 Кларк вольфрама земной коры составляет (по Виноградову) 1,3 г/т (0,00013 % по содержанию в земной коре). Его среднее содержание в горных породах, г/т: ультраосновных — 0,1, основных — 0,7, средних — 1,2, кислых — 1,9.
Кларк вольфрама земной коры составляет (по Виноградову) 1,3 г/т (0,00013 % по содержанию в земной коре). Его среднее содержание в горных породах, г/т: ультраосновных — 0,1, основных — 0,7, средних — 1,2, кислых — 1,9.
Процесс получения вольфрама проходит через подстадию выделения триоксида WO3 из рудных концентратов и последующем восстановлении до металлического порошка водородом при температуре около 700 °C.
Из-за высокой температуры плавления вольфрама для получения компактной формы используются методы порошковой металлургии: полученный порошок прессуют, спекают в атмосфере водорода при температуре 1200—1300 °C, затем пропускают через него электрический ток.
Металл нагревается до 3000 °C, при этом происходит спекание в монолитный материал. Для последующей очистки и получения монокристаллической формы используется зонная плавка.
ПРОИСХОЖДЕНИЕ
 Вольфрам встречается в природе главным образом в виде окисленных сложных соединений, образованных трехокисью вольфрама WO3 с оксидами железа и марганца или кальция, а иногда свинца, меди, тория и редкоземельных элементов. Промышленное значение имеют вольфрамит (вольфрамат железа и марганца nFeWO4 * mMnWO4 — соответственно, ферберит и гюбнерит) и шеелит (вольфрамат кальция CaWO4). Вольфрамовые минералы обычно вкраплены в гранитные породы, так что средняя концентрация вольфрама составляет 1—2 %.
Вольфрам встречается в природе главным образом в виде окисленных сложных соединений, образованных трехокисью вольфрама WO3 с оксидами железа и марганца или кальция, а иногда свинца, меди, тория и редкоземельных элементов. Промышленное значение имеют вольфрамит (вольфрамат железа и марганца nFeWO4 * mMnWO4 — соответственно, ферберит и гюбнерит) и шеелит (вольфрамат кальция CaWO4). Вольфрамовые минералы обычно вкраплены в гранитные породы, так что средняя концентрация вольфрама составляет 1—2 %.
Наиболее крупными запасами обладают Казахстан, Китай, Канада и США; известны также месторождения в Боливии, Португалии, России, Узбекистане и Южной Корее.
Мировое производство вольфрама составляет 49—50 тысяч тонн в год, в том числе в Китае 41, России 3,5; Казахстане 0,7, Австрии 0,5. Основные экспортёры вольфрама: Китай, Южная Корея, Австрия.
Главные импортёры: США, Япония, Германия, Великобритания.
Также есть месторождения вольфрама в Армении и других странах.
ПРИМЕНЕНИЕ

Вольфрам используют в качестве электродов для аргоно-дуговой сварки. Сплавы, содержащие вольфрам, отличаются жаропрочностью, кислотостойкостью, твердостью и устойчивостью к истиранию. Из них изготовляют хирургические инструменты (сплав «амалой»), танковую броню, оболочки торпед и снарядов, наиболее важные детали самолетов и двигателей, контейнеры для хранения радиоактивных веществ. Вольфрам — важный компонент лучших марок инструментальных сталей. Вольфрам применяется в высокотемпературных вакуумных печах сопротивления в качестве нагревательных элементов. Сплав вольфрама и рения применяется в таких печах в качестве термопары.
Для механической обработки металлов и неметаллических конструкционных материалов в машиностроении (точение, фрезерование, строгание, долбление), бурения скважин, в горнодобывающей промышленности широко используются твёрдые сплавы и композитные материалы на основе карбида вольфрама (например, победит, состоящий из кристаллов WC в кобальтовой матрице; широко применяемые в России марки — ВК2, ВК4, ВК6, ВК8, ВК15, ВК25, Т5К10, Т15К6, Т30К4), а также смесей карбида вольфрама, карбида титана, карбида тантала (марки ТТ для особо тяжёлых условий обработки, например, долбление и строгание поковок из жаропрочных сталей и перфораторное ударно-поворотное бурение крепкого материала). Широко используется в качестве легирующего элемента (часто совместно с молибденом) в сталях и сплавах на основе железа. Высоколегированная сталь, относящаяся к классу «быстрорежущая», с маркировкой, начинающейся на букву Р, практически всегда содержит вольфрам. ( Р18, Р6М5. от rapid – быстрый, скорость).
Сульфид вольфрама WS2 применяется как высокотемпературная (до 500 °C) смазка. Некоторые соединения вольфрама применяются как катализаторы и пигменты. Монокристаллы вольфраматов (вольфраматы свинца, кадмия, кальция) используются как сцинтилляционные детекторы рентгеновского излучения и других ионизирующих излучений в ядерной физике и ядерной медицине.
Дителлурид вольфрама WTe2 применяется для преобразования тепловой энергии в электрическую (термо-ЭДС около 57 мкВ/К). Искусственный радионуклид 185W используется в качестве радиоактивной метки при исследованиях вещества.
Стабильный 184W используется как компонент сплавов с ураном-235, применяемых в твердофазных ядерных ракетных двигателях, поскольку это единственный из распространённых изотопов вольфрама, имеющий низкое сечение захвата тепловых нейтронов (около 2 барн).
Вольфрам (англ. Tungsten) – W
КЛАССИФИКАЦИЯ
Физические свойства
Оптические свойства
Кристаллографические свойства
Вольфрам – полезные свойства и особенности металла
Название этого элемента сразу вызывает ассоциации с электрической лампочкой. Нить накаливания, которая светится внутри стеклянной колбы, сделана из этого материала. Это вольфрам.

Что представляет собой
Вольфрам – это металл, химический элемент, занимающий ячейку периодической системы Менделеева № 74.
По блеску и сероватому цвету схож с платиной.
Относится к металлам «туговскипающей» и «тугоплавкой» групп. По тугоплавкости уступает только жидкому углероду. Данное свойство позволяет отличить его от других металлов.
Международное обозначение – W (Wolframium).
Как был открыт
Знакомство людей с вольфрамом датируется эпохой Средневековья.
Старатели
Вольфрам получали еще европейские старатели при восстановлении олова. Но его считали «мусором», засоряющим ценный элемент. Под влиянием вольфрамовой руды в процессе восстановления часть олова превращалась в шлак, уменьшая долю чистого вещества.
Отсюда присказка, которая появилась у старателей: «Вольфрам сжирает олово, как волк овечку».
Наука
История открытия вольфрама связана с несколькими учеными-химиками:
- В середине 18 века швед Аксель Фредерик Кронштедт открыл тяжелый металл, названый им Tung Sten (по-шведски – тяжелый камень).
- Через 30 лет за дело взялся его соотечественник, член академии наук страны Карл Шееле. Свободное от работы в аптеке время он отдавал экспериментам в домашней лаборатории. Его считают «отцом» не только вольфрама. В списке также барий, марганец, кислород, хлор. Из вольфрамовой руды (тунгстена) он выделил соль кислоты, не числящейся в реестрах.
- Дальнейшую работу над соединением доверил испанским коллегам братьям Элюар. Которые и получили новый элемент.
Название и символ металла – Wolframium и W – предложил Йенс Якоб Берцелиус.
Этимология названия вольфрама имеет немецкие корни: Wolf Rahm («волчий крем/сливки»).
А тунгстен переименовали в честь ученого – в шеелит.
Как представлен в природе
Самородный цветной металл вольфрам на планете не встречается. Он представлен в виде руды либо минералов.
Руды состоят из соединений вольфрама с железом, марганцем, кальцием, иногда другими элементами, включая редкоземельные.
Минералы – это вкрапления в граниты (до 2%). Из них промышленное значение имеют вольфрамит (вольфрам с железом и марганцем) и шеелит (с кальцием).
Каждая тонна земной коры содержит 1,30 г вольфрама.
Физико-химические характеристики
Чистый вольфрам – в числе первых по плотности, твердости, первый по температуре плавления и кипения среди металлов. Эти физические свойства дополняет химическая стойкость даже при запредельных температурах.
| Вольфра́м / Wolframium (W), 74 |
| 183,84(1) а. е. м. (г/моль) |
| [Xe] 4f14 5d4 6s2 |
| 137 пм |
| 170 пм |
| (+6e) 62 (+4e) 70 пм |
| 2,3 (шкала Полинга) |
| W ← W3+ 0,11 В W ← W6+ 0,68 В |
| +2, +3, +4, +5, +6 |
| 769,7 (7,98) кДж/моль (эВ) |
| 19,25 г/см³ |
| 3695 K (3422 °C, 6192 °F) |
| 5828 K (5555 °C, 10031 °F) |
| 285,3 кДж/кг 52,31 кДж/моль |
| 4482 кДж/кг 824 кДж/моль |
| 24,27 Дж/(K·моль) |
| 9,53 см³/моль |
| кубическая объёмноцентрированная |
| 3,160 Å |
| 310 K |
| (300 K) 162,8 Вт/(м·К) |
| 7440-33-7 |
При 1580°C легко куется, вытягивается до тонкой проволоки.
Данные преимущества создает структура вещества.
 Тугоплавкий прочный металл, светло-серого цвета – вольфрам
Тугоплавкий прочный металл, светло-серого цвета – вольфрам
На воздухе с относительной влажностью менее 60% сопротивление металла коррозии стопроцентное.
Месторождения, добыча
Месторождения вольфрамовой руды на планете не редкость, запасы оцениваются миллионами тонн.
Крупнейшими залежами располагают КНР, Казахстан, Канада, США. Меньше сырья у России, Португалии, Узбекистана, других стран.
Глобальные объемы производства – 48-51 тысяча тонн вольфрама ежегодно. Безусловный лидер Китай (80%).
Добыча ведется закрытым либо карьерным способом.
Технология получения
Вольфрамовые руды из разных мест добычи содержат 0,3-2,5% оксида металла. Поэтому промышленное получение продукта из руды начинается на обогатительных предприятиях.
Это многоступенчатый процесс:
- Дробление руды.
- Шлифовка.
- Флотация.
- Обжиг.
Содержание полезных компонентов увеличивается до 60%:
- Чистоту концентрата повышают, расщепляя примеси гидроксидом натрия и задействуя метод ионообменной экстракции.
- До порошка восстанавливают при 650-700°C в водородистой среде.
Тугоплавкость оказалась недостатком, исключающим классическую плавку.
Твердые формы создают методом порошковой металлургии:
- Порошок спрессовывают.
- Спекание проводят при 1250-1300°C в водороде.
- Воздействуют электричеством.
- Нагревают до 3000°C, добиваясь монолитного спекания.
 Вольфрамовый порошок
Вольфрамовый порошок
- Дополнительно металл очищают зонной плавкой.
- На основе вольфрама или с его участием металлурги выплавляют продукт десятков наименований и марок.
- Среди самых распространенных – чистый вольфрам (ВЧ) и сплав с рением (ВР).
- Классификация марок вольфрама основывается на составе присадок:
| Название марки | Вид присадки |
| ВА | Алюминий + кремнистая щелочь |
| ВМ | Торий + кремнистая щелочь |
| ВИ | Окись иттрия |
| ВТ | Окись тория |
| ВЛ | Окись лантана |
Как используется
Свойства вольфрама обозначили главного потребителя. Это металлургия. Она создает конечный продукт и исходники для других отраслей промышленности.
Порошковый вольфрам – основа либо компонент твердых, жаропрочных износоустойчивых сплавов, премиальных марок сталей.
Из тугоплавкого металла и сплавов создают широкий ассортимент продукции:
- Узлы и детали авиационных, ракетных двигателей.
- Элементы электровакуумных приборов (кинескопы, нити накаливания).
 Нить накаливания из вольфрама
Нить накаливания из вольфрама - Нагреватели вакуумных печей.
- Электроды для аргонно-дуговой сварки. Они не плавятся, создают прочный сварной шов. Пригодны для материалов любого состава (цветные металлы, легированные стали, другие).
- Емкости для радиоактивных продуктов. Здесь решающими оказались преимущества металла перед свинцом.
- Хирургический инструментарий.
Характеристики металла подошли оборонному комплексу: танковая, торпедная броня, крупнокалиберные снаряды, пули. А также суперскоростные роторы гироскопов, контролирующих траекторию полета баллистических ракет.
 Вольфрам в слитках
Вольфрам в слитках
Соединения
Обширен спектр применения вольфрамовых соединений:
- Без дителлурида невозможно преобразование тепла в электричество.
- Карбид – основа сплавов и композитов для механической обработки металлов и неметаллов. У горнодобытчиков, нефтяников, газовиков – для бурения скважин.
- Сульфид – термостойкая (до 500°C) смазка.
- Трехокись – материал для создания электролита топливных элементов, работающих при повышенных температурах.
Соединения вольфрама закупают производители лаков, красок, текстиля.
Другие формы
Изотоп W184 – компонент сплавов с изотопами урана. Из них делают ракетные двигатели на ядерном топливе.
Радионуклид искусственного происхождения (W185) востребован как детектор излучений (включая рентгеновское) ядерным сегментом физики и медицины.
Значение для человека
Тугоплавкий металл не имеет значения для человека как биологического организма.
Опасность представляет лишь вдыхание вольфрамовой пыли.
Цены
На рынке торгуют металлическим вольфрамом (чистота 99%) и полуфабрикатами (пруток, проволока, полоска).
Порядок цены на металл – 50 500$ за тонну. Полуфабрикаты дороже вдвое-втрое.
Проверить совместимость мужчины и женщины по Знаку Зодиака
Вольфрам — свойства и область применения — Портал о ломе, отходах и экологии
Из всех известных сегодня металлов вольфрам самый тугоплавкий. Он занимает 74-ю позицию периодической системы, имеет ряд схожих свойств с молибденом и хромом, находящимися с ним в одной группе. На вид вольфрам представляет твердое вещество серого цвета, с характерным серебристым блеском.
Основные характеристики вольфрама
Для практического применения наиболее важны высокие показатели следующих характеристик:
- электрическое сопротивление;
- коэффициент линейного расширения;
Чистый вольфрам обладает высокой пластичностью, не растворяется в специальном кислотном растворе без предварительного нагрева хотя бы до 5000С.
Он легко вступает в реакцию с углеродом, следствием которой является образование карбида вольфрама известного высокой прочностью. Также металл известен своими оксидами, наиболее распространенный из них вольфрамовый ангидрид.
Его главное преимущество над остальными, возможность восстановления порошка к состоянию компактного металла, с побочным образованием низших оксидов.

Режущие пластины фирмы Sandvik Coromant с применением карбида вольфрама
Среди основных характеристик, делающих применение вольфрама затруднительным называют следующие:
- ломкость и склонность к окислению при низких температурах.
Кроме того, высокая температура кипения, а также точка испарения затрудняют добычу компактного материала.
Сплавы, содержащие вольфрам
Сегодня различают однофазные сплавы вольфрама. Это подразумевает внедрение одного или нескольких элементов. Наиболее известны соединения вольфрама с молибденом. Легирование этим элементом повышает прочность вольфрама при его растяжении. Также к однофазным сплавам относятся системы: вольфрам-титан/цирконий, ниобий, гафний.
Однако большей пластичности придает вольфраму рений, сохраняя остальные показатели на характерном ему высоком уровне. Но практическое применение таких соединений ограничено трудностями при добыче Re.
Поскольку вольфрам наиболее тугоплавкий материал, получить его сплавы трудно традиционным способом. При температуре плавления вольфрама другие металлы уже кипят или даже переходят в газообразную фазу.
Современные технологии позволяют получать ряд сплавов с помощью электролиза.
Например, вольфрам — никель — кобальт, который используется не для изготовления целых деталей, а с целью нанесения защитного слоя на менее прочные металлы.
Также в промышленности все еще остается актуальным способ получения вольфрамовых сплавов, используя методы порошковой металлургии. При этом требуется создание особых условий технологического процесса, который включает в себя наличие вакуума.
Особенности взаимодействия металлов с вольфрамом делают предпочтительными соединения не парного характера, а с использованием 3, 4-х и более компонентов.
Такие сплавы отличаются особенной твердостью, однако малейшее отклонение от процентного содержания того или иного элемента приводит к повышению хрупкости готового сплава.
Вольфрам, как многие другие элементы редкой группы, не встречается в природе. Поэтому добыча металла не сопровождается строительством крупных промышленных комплексов. Сам процесс получения материала условно делят на такие этапы:
- Добыча руды, содержащей редкий металл.
- Создание условий для возможного выделения вольфрама от перерабатываемой массы.
- Концентрирование материала в виде раствора или осадка.
- Очищение полученного химического соединения.
- Получение чистого вещества.

Вольфрамовая руда
Более сложным оказывается процесс изготовления компактного металла, к примеру, вольфрамовой проволоки. Основная трудность заключается в том, что нельзя допустить даже малейшего попадания примесей, резко ухудшающих плавкие и прочностные свойства.
Область применения вольфрама
С помощью этого металла изготавливают нити накаливания, рентгеновские трубки, нагреватели, экраны вакуумных печей, предназначающихся для использования в высокотемпературном режиме.
Рентгеновская трубка с нитью из вольфрама
Сталь, легированная вольфрамом имеет высокие прочностные качества.
Продукция из таких видов сплава используется для изготовления инструментов широкого предназначения: медицина, бурение скважин, изделия для обработки материалов в машиностроении (режущие пластины, как на фото выше).
Преимуществом соединения считается устойчивость к истиранию, маловероятность появления трещин в процессе эксплуатации. Наиболее известная в строительстве марка стали с использованием вольфрама называется «победит».

Лом вольфрама
Химическая промышленность также нашла применение вольфраму. Из него делают краски, катализаторы, пигменты.
Атомная промышленность использует тигли из этого металла, а также специальные контейнера для хранения радиоактивных отходов.
О нанесении покрытий из вольфрама уже вкратце упоминалось. Оно применяется для нанесения на материалы, работающие при высоких температурах в восстановительных и нейтральных средах, как защитная пленка.
Также известны прутки, используемые при дуговой сварке. Поскольку вольфрам неизменно остается тугоплавким металлом при выполнении сварочных работ он используется с присадочными проволоками.
Вольфрам: свойства, температура плавления, плотность, история открытия. Применение, продукция из вольфрама

Тугоплавкий металл вольфрам
Среди всех металлов, которые известны сегодня, вольфрам является наиболее тугоплавким. Характеризуется высокой химической стойкостью.
Вольфрамовые свойства нашли применение в разных сферах, которые имеют связь с повышенными температурными режимами, особенно в металлургии.
Температура плавления вольфрама очень высокая, что дает возможность сделать его компонентом для получения сплавов и жаропрочных сталей, обладающих высокой прочностью.
Что такое вольфрам?
Вольфрам в периодической системе Д.И. Менделеева стоит в 4 группе, имеет номер атома 74, его атомная масса составляет 183,85. Для обозначения используется символ «W» (Wolframium).
В чистом виде в естественных условиях бывает редко, как правило, это сложные окисленные соединения, образующие трехокись вольфрама с оксидами таких веществ, как железо, марганец, а также калий, свинец, медь, торий.
Самые крупные запасы на планете сегодня сосредоточены в таких странах, как Казахстан, Китай, Канада, Америка, Россия. Промышленность использует шеелит и вольфрамит.
История открытия
Рудокопы Саксонии в XIV-XVI вв. заметили, что после обработки оловянных руд остается много шлака. Работники в здешних копальнях называли его побочным продуктом, который «пожирает» олово, сравнивали с «волком, пожирающим овцу». Так и сформировалось название шлака «wolfrahm» («волчья пена» с немецкого языка).
Когда химик Карл Шееле обработал азотной кислотой «tungsten» («тяжелый камень» в переводе со шведского языка), удалось выделить новый метал, получивший такое же название. Событие произошло в 1781 г. Позже провели ряд анализов, которые показали, что шведскому химику удалось открыть не сам вольфрам, а его оксид. Поэтому минерал переименовали на «шеелит».
Через два года после открытия, сделанного Карлом Шееле, химики из Испании братья Элюар заявили, что смогли выделить из вольфрамита рудников Саксонии чистый вольфрам. Нужно отметить, что ни Шееле, ни братья Элюар не настаивали на том, что именно они стали первооткрывателями вольфрама.
До начала ХХ века химический элемент назывался «tungsten», его обозначали символом «Tu». Термин «вольфрам» и символ «W» был утвержден только в середине прошлого века.
Основные характеристики
Кроме самой высокой тугоплавкости, одно из наиболее тяжелых и твердых веществ. В Чистый вольфрам имеет серебристо-белый окрас. Отлично поддается ковке (при 1600 °С). В условиях вакуума характеризуется отличной устойчивостью.
- Физические свойства:
- • плавится при достижении показателя температуры 3422 °С;
- • закипает при температуре 5555 °С;
- • плотность вольфрама – 19,25 г/см3;
- • сопротивление – 55⋅10−9 Ом•м (20°С);
- • магнитная восприимчивость – 0,32⋅10−9;
- • твердость (по Бринеллю) – 488 кг/мм2.
Вольфрам обладает важными химическими свойствами:
- • стойкий к кислотам в обычных условиях;
- • легче взаимодействует с окислителями, чем с тяжелыми металлами;
- • реагирует со многими элементами, в результате чего образуются различные по сложности соединения;
- • незначительно растворяется в щелочах при нагревании;
- • валентность в соединениях 2-6 (чем выше валентность, тем более устойчивы).

Какие марки существуют?
Вольфрам может быть чистым, с присадками, в составе сплава, куда входят и другие металлы.
Для обозначения чистого вольфрама используется маркировка ВЧ. Для маркировки сплава вольфрама и рения применяется обозначение ВР.
- На наличие разных видов присадок указывают следующие комбинации букв:
- • ВА – кремнещелочной и алюминия;
- • ВМ – кремнещелочной и тория;
- • ВТ – окиси тория;
- • ВЛ – окиси лантана.
- Указанные марки вольфрама используются наиболее часто в промышленности.
Преимущества и недостатки
- Преимущества обусловлены высокими показателями:
- • плавления (очень высокий температурный режим);
- • прочности (лидер среди всех существующих металлов);
- • плотности;
- • электропроводности.
- Кроме этого, вольфрам стойкий к воздействию коррозийных процессов, имеет низкий коэффициент теплового расширения.
- Недостатками вольфрама можно считать хрупкость и возможность разрушения при ударе.
Где используется?
Применение вольфрама и сплавов востребовано в разных сферах:
- • металлургии;
- • судостроении;
- • медицине;
- • текстильном производстве;
- • электротехнической, радиоэлектронной, химической, атомной, горнодобывающей и ряде других отраслей промышленности.
- Из него получают сверхтвердые стали и сплавы, которые применяются, чтобы обрабатывать металлы механическим путем, в бурении скважин, для изготовления деталей, из которых собираются двигатели самолетов.
- Вольфрамовые электроды предназначаются для аргонодуговой сварки.
- В ядерной физике и медицине нашли применение монокристаллы вольфраматов.
- Элемент необходим для нитей накаливания и элементов электровакуумных приборов, артиллерийских снарядов, роторов гироскопов (сверхскоростных) и др.
Виды продукции
Свойства вольфрама дают возможность изготавливать такие виды продукции:
• Электроды. Для работы с материалами разного состава, цветными металлами, высоколегированными сталями. Не плавятся, шов прочный и долговечный.
• Проволока. Используется в лампах накаливания, благодаря сопротивлению вольфрама (нагреватели, спирали).
• Порошок. Основа для сплавов и сталей.
• Прутки. Изделия для изготовления вольфрамовых электродов.
• Листы. Изделия из металла вольфрама необходимы для тепловых экранов, подставок и других элементов крепления для высокотемпературных печей.

Голосование:
2516
13 января 2021
Вольфрам | это… Что такое Вольфрам?
| 74 | Вольфрам |
| 4f145d46s2 |
Вольфра́м — химический элемент с атомным номером 74 в периодической системе, обозначается символом W (лат. Wolframium), твёрдый серый переходный металл.
Вольфрам — самый тугоплавкий металл (элемент) среди природных элементов. При стандартных условиях химически стоек.
История и происхождение названия
Название Wolframium перешло на элемент с минерала вольфрамит, известного ещё в XVI в. под названием «волчья пена» — «Spuma lupi» на латыни, или «Wolf Rahm» по-немецки. Название было связано с тем, что вольфрам, сопровождая оловянные руды, мешал выплавке олова, переводя его в пену шлаков («пожирает олово как волк овцу»).
В настоящее время в США, Великобритании и Франции для вольфрама используют название «tungsten» (швед. tung sten — «тяжелый камень»).
В 1781 знаменитый шведский химик Шееле , обрабатывая азотной кислотой минерал шеелит, получил жёлтый «тяжелый камень».
В 1783 испанские химики братья Элюар сообщили о получении из саксонского минерала вольфрамита жёлтой окиси нового металла, растворимой в аммиаке. При этом один из братьев, Фаусто, был в Швеции в 1781 и общался с Шееле.
Шееле не претендовал на открытие вольфрама, а братья Элюар не настаивали на своём приоритете.
Нахождение в природе
Кларк вольфрама земной коры составляет (по Виноградову) 1,3 г/т(0.0013 % по содержанию в земной коре). Его среднее содержание в горных породах, г/т: ультраосновных — 0,1, основных — 0,7, средних — 1,2, кислых — 1,9.
Вольфрам встречается в природе главным образом в виде окисленных сложных соединений, образованных трехокисью вольфрама WO3 с оксидами железа и марганца или кальция, а иногда свинца, меди, тория и редкоземельных элементов.
Промышленное значение имеют вольфрамит (вольфрамат железа и марганца nFeWO4 * mMnWO4 — соответственно, ферберит и гюбнерит) и шеелит (вольфрамат кальция CaWO4).
Вольфрамовые минералы обычно вкраплены в гранитные породы, так что средняя концентрация вольфрама составляет 1-2 %.
Месторождения
Наиболее крупными запасами обладают Казахстан, Китай, Канада и США; известны также месторождения в Боливии, Португалии, России и Южной Корее.
Мировое производство вольфрама составляет 49-50 тысяч тонн в год, в том числе в Китае 41, России 3,5; Казахстане 0,7, Австрии 0,5. Основные экспортёры вольфрама: Китай, Южная Корея, Австрия.
Главные импортёры: США, Япония, Германия, Великобритания.
Также есть месторождения вольфрама в Армении и других странах.
Получение
Вольфрамовый порошок
Процесс получения вольфрама проходит через подстадию выделения триоксида WO3 из рудных концентратов и последующем восстановлении до металлического порошка водородом при температуре ок. 700 °C. Из-за высокой температуры плавления вольфрама для получения компактной формы используются методы порошковой металлургии: полученный порошок прессуют, спекают в атмосфере водорода при температуре 1200—1300 °C, затем пропускают через него электрический ток. Металл нагревается до 3000 °C, при этом происходит спекание в монолитный материал. Для последующей очистки и получения монокристаллической формы используется зонная плавка.
Физические свойства
Вольфрам — светло-серый металл, имеющий самые высокие доказанные температуры плавления и кипения (предполагается, что сиборгий ещё более тугоплавок, но пока что об этом твёрдо утверждать нельзя — время существования сиборгия очень мало).
Некоторые физические свойства приведены в таблице (см. выше). Другие физические свойства вольфрама:
Вольфрам является одним из наиболее тяжелых, твердых и самым тугоплавким металлом. В чистом виде представляет собой металл серебристо-белого цвета, похожий на платину, при температуре около 1600 °C хорошо поддается ковке и может быть вытянут в тонкую нить.
Химические свойства
Проявляет валентность от 2 до 6. Наиболее устойчив 6-валентный вольфрам. 3- и 2-валентные соединения вольфрама неустойчивы и практического значения не имеют.
Вольфрам имеет высокую коррозионную стойкость: при комнатной температуре не изменяется на воздухе; при температуре красного каления медленно окисляется в оксид вольфрама (VI). Вольфрам в ряду напряжений стоит сразу после водорода, и в соляной, разбавленной серной и плавиковой кислотах почти не растворим. В азотной кислоте и царской водке окисляется с поверхности.
Легко растворяется в смеси азотной и плавиковой кислот[2]:
Реагирует с расплавленными щелочами в присутствии окислителей[3]:
Поначалу, данные реакции идут медленно, однако при достижении 400 °C (500 °C для реакции с участием кислорода) вольфрам начинает саморазогреваться и реакция протекает достаточно бурно, с образованием большого количества тепла.
В смеси азотной и плавиковой кислоты растворяется, образуя гексафторвольфрамовую кислоту H2[WF6].
Из соединений вольфрама наибольшее значение имеют: триоксид вольфрама или вольфрамовый ангидрид, вольфраматы, перекисные соединения с общей формулой Me2WOX, а также соединения с галогенами, серой и углеродом.
Вольфраматы склонны к образованию полимерных анионов, в том числе гетерополисоединений с включением других переходных металлов.
Применение
Главное применение вольфрама — как основа тугоплавких материалов в металлургии.
Металлический вольфрам
Нить накаливания
- Тугоплавкость и пластичность вольфрама делают его незаменимым для нитей накаливания в осветительных приборах, а также в кинескопах и других вакуумных трубках.
- Благодаря высокой плотности вольфрам является основой тяжёлых сплавов, которые используются для противовесов, бронебойных сердечников подкалиберных и стреловидных оперенных снарядов артиллерийских орудий, сердечников бронебойных пуль и сверхскоростных роторов гироскопов для стабилизации полёта баллистических ракет (до 180 тыс. об/мин).
- Вольфрам используют в качестве электродов для аргоно-дуговой сварки.
- Сплавы вольфрама, ввиду его высокой температуры плавления, получают методом порошковой металлургии. Сплавы, содержащие вольфрам, отличаются жаропрочностью, кислотостойкостью, твердостью и устойчивостью к истиранию. Из них изготовляют хирургические инструменты (сплав «амалой»), танковую броню, оболочки торпед и снарядов, наиболее важные детали самолетов и двигателей, контейнеры для хранения радиоактивных веществ. Вольфрам — важный компонент лучших марок инструментальных сталей.
- Карбид вольфрама (зачастую наряду или вместо карбида титана) используют как наполнитель в твёрдых сплавах — керметах (победит), где матрицей служит кобальт (5-16 %).
- Вольфрам применяется в высокотемпературных вакуумных печах сопротивления в качестве нагревательных элементов. Сплав вольфрама и рения применяется в таких печах в качестве термопары.
Соединения вольфрама
- Для механической обработки металлов и неметаллических конструкционных материалов в машиностроении (точение, фрезерование, строгание, долбление), бурения скважин, в горнодобывающей промышленности широко используются твёрдые сплавы и композитные материалы на основе карбида вольфрама (например, победит, состоящий из кристаллов WC в кобальтовой матрице; широко применяемые в России марки — ВК2, ВК4, ВК6, ВК8, ВК15, ВК25, Т5К10, Т15К6, Т30К4), а также смесей карбида вольфрама, карбида титана, карбида тантала (марки ТТ для особо тяжёлых условий обработки, например, долбление и строгание поковок из жаропрочных сталей и перфораторное ударно-поворотное бурение крепкого материала). Широко используется в качестве легирующего элемента (часто совместно с молибденом) в сталях и сплавах на основе железа. Высоколегированная сталь, относящаяся к классу «быстрорежущая», с маркировкой, начинающейся на букву Р, практически всегда содержит вольфрам.
- Сульфид вольфрама WS2 применяется как высокотемпературная (до 500 °C) смазка.
- Некоторые соединения вольфрама применяются как катализаторы и пигменты.
- Дителлурид вольфрама WTe2 применяется для преобразования тепловой энергии в электрическую (термо-ЭДС около 57 мкВ/К).
Другие сферы применения
Искусственный радионуклид 185W используется в качестве радиоактивной метки при исследованиях вещества. Стабильный 184W используется как компонент сплавов с ураном-235, применяемых в твердофазных ядерных ракетных двигателях, поскольку это единственный из распространённых изотопов вольфрама, имеющий низкое сечение захвата тепловых нейтронов (около 2 барн).
Рынок вольфрама
Цены на металлический вольфрам чистотой около 99 % на конец 2010 года составляли около 40-42 долларов США за килограмм, в мае 2011 года составляли около 53-55 долларов США за килограмм. Полуфабрикаты от 58 USD (прутки) до 168 (тонкая полоса)[4].
Биологическая роль
Вольфрам не играет значительной биологической роли. У некоторых архебактерий и бактерий имеются ферменты, включающие вольфрам в своем активном центре.
Существуют облигатно-зависимые от вольфрама формы архебактерий-гипертермофилов, обитающие вокруг глубоководных гидротермальных источников.
Присутствие вольфрама в составе ферментов может рассматриваться как физиологический реликт раннего архея — существуют предположения, что вольфрам играл роль в ранних этапах возникновения жизни[5].
Пыль вольфрама, как и большинство других видов металлической пыли, раздражает органы дыхания.
Изотопы
Основная статья: Изотопы вольфрама
Природный вольфрам состоит из пяти изотопов (180W, 182W, 183W, 184W и 186W). Искусственно созданы и идентифицированы ещё 30 радионуклидов. В 2003 открыта[6] чрезвычайно слабая радиоактивность природного вольфрама (примерно два распада на грамм элемента в год), обусловленная α-активностью 180W, имеющего период полураспада 1,8·1018 лет[7].
Интересные факты
Вольфрам — самый тугоплавкий металл. Температура плавления 3380 °C, кипения 5900 °C. Примерно такую же температуру имеет фотосфера Солнца[8].
Плотность вольфрама почти равняется плотности золота: 19,30 г/см³ против 19,32 г/см³ соответственно.
Примечания
- ↑ Редкол.:Кнунянц И. Л. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1988. — Т. 1. — С. 418. — 623 с. — 100 000 экз.
- ↑ Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — С. 347.
- ↑ Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — С. 348.
- ↑ Цены на вольфрам
- ↑ Федонкин М. А. Сужение геохимического базиса жизни и эвкариотизация биосферы: причинная связь — Палеонтологический журнал — 2003 — № 6 — с. 33-40
- ↑ F. A. Danevich et al. (2003). «α activity of natural tungsten isotopes». Phys. Rev. C 67. DOI:10.1103/PhysRevC.67.014310.
- ↑ C. Cozzini et al. (2004). «Detection of the natural α decay of tungsten». Phys. Rev. C 70. DOI:10.1103/PhysRevC.70.064606.
- ↑ Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.






