- Краткие сведения
- Физические свойства, особенности
- Разновидности карбидов
- Применение материалов
- Основные металлические карбиды
- Карбид гафния
- Карбиды хрома
- Карбид титана
- Карбиды вольфрама
- Карбид кальция
- Карбид циркония
- Заключение
- Твердые сплавы
- Характеристика
- Классификация
- Вольфрамо-кобальтовые
- Титановольфрамовокобальтовые
- Титанотанталовольфрамокобальтовые твердые сплавы
- Безвольфрамовые сплавы
- Свойства
- Примеры маркировки твердых сплавов
- Применение и продукция из твердых сплавов
- КАРБИДЫ
В природе металлы активно вступают в химические реакции с кислотами, щелочами и атмосферным кислородом. В большинстве случаев для этого не требуется дополнительная обработка (химическая, термическая).
При сильном нагреве металлы начинают активно вступать в реакцию с углеродом, что приводит к образованию сложных соединений под названием карбиды. Эти соединения отличаются рядом необычных свойств — высокая прочность, тугоплавкость, химическая инертность.
Какие бывают карбиды металлов? Как эти соединения применяются в промышленности? Какие вещества получили наибольшее применение?
Краткие сведения
Карбиды — это химические соединения, которые состоят из углерода (C) и другого элемента. Обычно в качестве второго элемента выступают металлы — это может быть железо (Fe), титан (Ti), хром (Cr), гафний (Hf) и другие.
В карбидных соединениях углерод более высокой электроотрицательностью (в сравнении со вторым элементом). Поэтому карбиды нельзя отнести к оксидам, галогенидам и другим химическим соединениям.
Карбиды металлов — в основном твердые тугоплавкие вещества, которые отличаются очень высокой прочностью и почти не вступают в реакции с химически активными веществами.
Благодаря этим необычным свойствам карбиды часто применяют в качестве абразивов для обработки различных сплавов (это может быть чугун, сталь, соединения на основе алюминия).
Из них делают электроды для сварки, огнеупорные стержни, элементы электрических систем. Первые карбиды на основе калия, железа и магния были открыты и получены совсем недавно — в XIX веке.
Однако со временем были получены и новые карбидные соединения — на основе хрома, титана, гафния, вольфрама, кальция.
Физические свойства, особенности
Карбидные материалы обладают рядом характерных свойств, особенностей. Перечислим их:
- Высокая твердость. Атомы углерода и металлов образуют твердую кристаллическую решётку, для разрушения которой потребуется большое механическое усилие. Поэтому с помощью ударов разрушить карбидные вещества будет крайне сложно. Благодаря высокой твердости материалы нашли широкое распространение в различных технических сферах (от военного машиностроения до строительства).
- Высокая температура плавления. Плотная кристаллическая решетка обеспечивает устойчивость вещества при сильном нагреве или охлаждении. Средняя температура плавления карбидов находится в пределах от 1500 до 2000 градусов. Поэтому такой материал без проблем выдержит длительное воздействие экстремальных температур (скажем, его можно использовать в печах, металлургических ковшах для расплавления других материалов).
- Устойчивость к химическим веществам и коррозии. Внешние электронные оболочки веществ-карбидов являются полностью заполненными. Поэтому такой материал будет редко вступать в химические реакции с другими веществами (он устойчив к воздействию кислот, щелочей, солей). Вещества не вступают в реакцию с водой и атмосферным кислородом, поэтому они не покрываются ржавчиной, что обеспечивает их высокий срок годности.
- Повышенная износоустойчивость. Изделия на основе карбидов долгое время сохраняют свою форму даже в случае удара, деформации или воздействия высоких температур. Поэтому они обладают повышенной износоустойчивостью, что делает их срок годности большим. Благодаря повышенной устойчивости материал часто применяют для изготовления абразивных и шлифовальных изделий, которыми можно пользоваться в течение большого срока.
Стоит обратить внимание, что далеко не все карбидные соединения обладают перечисленными свойствами. Скажем, карбид золота (I) чрезвычайно взрывоопасен (тогда как большинство других карбидов металлов — нет).
Он может взорваться даже в случае неаккуратного пересыпания вещества на бумажную поверхность.
Поэтому при рассмотрении физических и химических свойства карбидов нужно по отдельности рассматривать каждое соединение, поскольку карбидные материалы могут обладать уникальными необычными свойствами.
Разновидности карбидов
Различают несколько разновидностей карбидов в зависимости от конфигурации кристаллической решетки. Тип решетки определяет ряд физико-химических свойства материала, что нужно учитывать при их применении. Рассмотрим основные разновидности кристаллических решеток карбидов:
- Материалы с ковалентной решеткой. Вещества с таким способом связи возможны только в том случае, если в качестве второго элемента выступает бром или кремний. На атомарном уровне соединение образуется за счет sp, sp-2 или sp-3 гибридизации. В веществе атомарный металл заменяет собой углерод, что позволяет формировать прочное устойчивое вещество, которое устойчиво к механическим ударам, высоким температурам, химическим веществам. С точки зрения электропроводности вещество является полупроводником (хотя использование карбидов в качестве полупроводниковых элементов невыгодно с практической точки зрения).
- Металлоподобные материалы. В эту группу входят соединения, у которых металлических элемент является железом, кобальтом, никелем либо относится к переходной группе (IV-VII). У таких карбидных соединений металлические атомы располагаются не на месте атомов углерода, а в различных пустотах кристаллических решеток (поэтому часто такие вещества называют карбидами внедрения). Такое необычное расположение делает вещество устойчивым, крепким, надежным, оно не будет разрушаться под воздействием высоких температур или при воздействии химически активных веществ (кислоты, щелочи, соли и другие).
- Материалы с ионной связью. В эту группу входит множество карбидов, у которых в качестве металлического элемента выступает алюминий, редкоземельные металлы либо элементы I или II группы периодической таблицы. По химической структуре вещества похожи на соединения с ковалентной решеткой с той лишь разницей, что здесь металлы обычно теряют один или несколько электронов на внешнем уровне, что приводит к образованию веществ-ионов. По химико-физическим свойствам ионные карбиды аналогичны стандартным соединениям — отличная прочность, высокая температура плавления. Единственное крупное отличие — вещества активно взаимодействуют с кислотами (обычно с образованием металла или подобных веществ).

Применение материалов
Карбиды металлов применяются производстве (в основном — в тяжелом). Перечислим основные варианты применения:
- Простые карбидные соединения на основе железа могут добавлять в металлический сплав (чугун, сталь, чистое железо), чтобы улучшить его физико-химические свойства. Дополнительные компоненты улучшают прочность, повышают химическую инертность, минимизируют риск коррозии под действием воды или атмосферного воздуха. Еще одно полезное свойство — увеличение температуры плавления, что удобно в случае изготовления тугоплавких запчастей или деталей.
- Карбиды на основе титана или вольфрама отличаются сверхвысокой прочностью, а плавятся они при сверхвысоких температурах. Поэтому из них делают режущие и абразивные инструменты, которые отличаются высоким сроком годности. Подобные соединения можно использовать в качестве огнеупорных материалов (скажем, при производстве печей), для изготовления сварочных стержней.
- Карбид кальция обладает необычным свойством — при контакте с водой происходит ряд химических реакций, что в конечном счете приводит к образованию ацетилена. Это вещество широко применяется для кислородной сварки, резки или напайки. Поэтому такое карбидное соединение может использоваться для изготовления соответствующих деталей (электроды для сварочных инструментов, напайка и другие). Ацетилен при горении выделяет большое количество тепла, поэтому к работам нужно подойти осторожно.
Основные металлические карбиды
На практике широко применяется множество карбидных соединений. Рассмотрим основные из них.
Карбид гафния
Встречается в виде только одного вещества — HfC. В нормальных условиях обладает кристаллической структурой, окрашено в серый цвет. плавится при температуре 3900 градусов — интересно, что его закипание происходит уже при температуре 4160 градусов.
Поэтому к расплавлению нужно подходить аккуратно, чтобы не испарить его. При нагреве до 2000 градусов начинает взаимодействовать с металлами (молибден, вольфрам).
Вещество не обладает полной химической инертностью — оно вступает в реакцию с кислотами (в азотной или серной кислоте оно способно полностью раствориться).
Карбиды хрома
Встречается в виде нескольких веществ; основные — Cr23C6, Cr3C2, Cr7C3. Отличаются высокой химической инертностью (хотя могут реагировать с цинком при сильном нагреве).
Не вступают в контакт с водой, атмосферным воздухом, кислотами, щелочами, солями, другими карбидными соединениями. Температура плавления не слишком высокое — большинство соединений плавятся уже при температуре 1500-1700 градусов.
У соединения Cr7C3 при нагреве до 800 градусов происходит ряд эндотермических реакций и превращений, что приводит к превращению вещества в Cr23C6.
Карбид титана
Встречается в виде одного стабильного соединения — TiC. При нормальных условиях обладает серым цветом с характерным металлическим блеском. Плавится при температуре 3100 градусов, кипит — при 4305 градусах. Обладает высокой устойчивостью, прочностью.
Химическая инертность средняя — в нормальном состоянии может вступать в реакцию с кислотами и щелочами (хотя реакция идет слабо). При нагреве до 2500 градусов может вступать в реакцию с азотом (в том числе — атмосферным).
При нагреве до 1200 градусов может окисляться и/или вступать в реакцию с углекислым газом.
Карбиды вольфрама
Встречается в виде двух устойчивых соединений — WC и W2C. Оба карбида отличаются приблизительно одинаковыми химико-физическими свойствами. Вид — мелкий порошок серовато-черного цвета (со слабым металлическим блеском или без него).
Вещества плавятся при температуре около 2720 градусов, однако при более низких температурах начинается их активных контакт с атмосферным воздухом, азотом или углекислым газом.
Соединения легко растворяются в разогретых до температуре кипения серных и азотных кислотах.
Карбид кальция
Основное устойчивое соединение — CaC2. Вид — крупные прозрачные кристаллы, которые могут обладать светло-голубым оттенком.
При наличии примесей может окрашиваться в другие цвета — серый, желтый, коричневый, черный и другие (в зависимости от типа примеси и ее концентрации).
Соединение плавится при температуре порядка 2500 градусов, однако при комнатной температуре оно активно вступает в реакцию с водой с активным выделением ацетилена. Поэтому вещество нуждается в особых безопасных способах хранения (ацетилен является токсичным для человека).
Карбид циркония
Основное соединение — ZrC. Стандартное состояние — небольшие кристаллы серого цвета, обладающие металлическим блеском.
Температура плавления — 3530 градусов, однако при нагреве до 1200 градусов вещество начинает активно вступать в реакцию с атмосферным кислородом, что приводит к образованию оксидов.
Вещество слабо реагирует с кислотами, щелочами и солями, однако может вступать в реакцию с атомизированным азотом в составе сложных веществ, что приводит к образованию нитритов. Поэтому вещество нуждается в особых способах хранения.

Заключение
Подведем итоги. Карбиды металлов — соединения, в состав которых входит углерод и какой-либо дополнительный металл. Это может быть железо, хром, цирконий, вольфрам и другие.
Соединение может образовывать сложную прочную кристаллическую решетку (ковалентную, металлическую, ионную). Карбиды из-за особенностей своего строения отличаются высокой прочностью, устойчивостью к механической деформации, химической инертностью.
Вещества обычно не вступают в реакцию с кислотами, щелочами, солями, атмосферными газами (кислород, азот, углекислый газ).
Из карбидов делают абразивные или шлифовальные инструменты, поскольку они не деформируются, не портятся со временем, могут деформировать другие прочные соединения.
Из них делают электроды для сварочных инструментов, термоустойчивые стержни, элементы электрических инструментов. Некоторые виды карбидов могут проявлять необычные свойства.
Скажем, карбид золота взрывается при легком контакте, а карбид кальция может вступать в реакцию с водой при комнатной температуре с образованием ацетилена.
Используемая литература и источники:
- Статья на Википедии
- Самсонов Г. В., Косолапова Т. Я., Домасевич Л. Т. Свойства, методы получения и области применения тугоплавких карбидов и сплавов на их основе. Киев, 1974
- Gusev A. I., Rempel A. A. Nanocrystalline Materials. — Cambridge: Cambridge International Science Publishing, 2004.
- Вальков Ф. А. Неорганическая химия, учебник для педагогических вузов. — М.: Государственное учебно-педагогическое издательство, 1963.
Твердые сплавы
Металлы, отличающиеся повышенной твёрдостью и износостойкостью — это твердые сплавы. Изготавливаются, как правило, из карбидов металлов (титана, хрома, вольфрама и прочих), что делает их особенно стойкими к высоким температурам и механическим воздействиям. Такие сплавы невероятно прочные, а потому, пригодные для различных производств.
Характеристика
Помимо прочности и износостойкости к полезным свойствам данных материалов можно отнести тугоплавкость. При нагреве до 900 — 1150°C твердый сплав сохраняет все свои качества.
Существует специальная маркировка, которая указывает свойства и характеристики сплава. В основе принципа маркирования – буквы, указывающие на наличие того или иного металла и цифры, показывающие его количество в %. Необходимо точно понимать их значение, так как от данных показателей зависит пригодность материала для проведения необходимых работ.
Классификация
Как и любые металлические материалы, твердые сплавы имеют собственную классификацию, которая помогает подобрать наиболее подходящий материал для своих целей.
В зависимости от способа получения, сплавы бывают:
Как видно из названия, литые сплавы изготавливают технологией литья.
Среди них: стеллиты (которые состоят из хрома, вольфрама, углерода и никеля; как связка используется кобальт), сормайты (состоящие из хрома, углерода и никеля на железной основе), а также твердые сплавы, в которых в качестве основы использован никель.
Чаще всего, в процессе литья применяется технология пресса, которая позволяет получить изделия высокого качества, требующие минимальной обработки перед использованием (однако, чаще всего необходимо проведение термической постобработки).
Спеченные сплавы (или металлокерамические), в свою очередь, производятся по технологии порошковой металлургии.
Она представляет собой высокоточное производство, благодаря чему, получаемый на выходе материал имеет максимально высокую степень качества и не требует дополнительной обработки.
Максимум, что может потребоваться – небольшая шлифовка полученного изделия. Металлокерамическими данные сплавы называют, потому что способ их производства схож с производством керамических изделий.
По химическому составу различают:
- ВК – однокарбидные, вольфрамо-кобальтовые;
- ТК – двухкарбидные, титано-вольфрамо-кобальтовые;
- ТТК – трехкарбидные, титано-тантало-вольфрамо-кобальтовые;
- ТН — безвольфрамовые.
Вольфрамо-кобальтовые
Сплавы на основе карбида вольфрама – наиболее распространённые представители данной группы. К ним относятся BK6 и BK8, упомянутые выше.
Сплавы можно разделить ещё на две группы, в зависимости от их состава: содержащие в своём составе вольфрам – как уже говорилось ранее, такие сплавы состоят из карбида вольфрама и ещё минимум одного металла, играющего роль связки (чаще всего таковым является кобальт).
В основном сплавы группы ВК используют для изготовления режущего инструмента. Это резцы, пластины.
Состав и характеристики сплавов ВК
| Сплав | Состав сплава, % | Характеристика физико-механических свойств | ||||
| WC | TaC | Co |
|
|
HRA, не менее | |
| ВК3 | 97 | — | 3 | 1176 | 15,0-15,3 | 89,5 |
| ВК3-М | 97 | — | 3 | 1176 | 15,0-15,3 | 91,0 |
| ВК4 | 96 | — | 4 | 1519 | 14,9-15,2 | 89,5 |
| ВК6 | 94 | — | 6 | 1519 | 14,6-15,0 | 88,5 |
| ВК6-М | 94 | — | 6 | 1421 | 14,8-15,1 | 90,0 |
| ВК6-ОМ | 92 | 2 | 6 | 1274 | 14,7-15,0 | 90,5 |
| ВК8 | 92 | — | 8 | 1666 | 14,4-14,8 | 87,5 |
| ВК10 | 90 | — | 10 | 1764 | 14,2-14,6 | 87,0 |
| ВК10-М | 90 | — | 10 | 1617 | 14,3-14,6 | 88,0 |
| ВК10-ОМ | 88 | 2 | 10 | 1470 | 14,3-14,6 | 88,5 |
| ВК10-ХОМ | 88 | — | 10 | 1500 | 14,3-14,6 | 89,5 |
* Буква М означает, что сплав является мелкозернистым, ОМ — особо мелкозернистый.
Из таких материалов получаются высококачественные инструменты, которые используются в промышленности, различных производствах и в быту, изготовление деталей различных конструкций. Это могут быть детали для автомобилей, механических предметов, приборов и любых механизмов. изготовление деталей, требующих высокой жаростойкости.
Титановольфрамовокобальтовые
Группа сплавов ТК производится для иструментов, выполняющих резание сталей, дающих сливную стружку. В основе состава карбид титана и карбид вольфрама. В связке идёт кобальт. Титан дает снижение адгезии со сталью, благодаря этому сплавы группы ТК более износостойкие при обработки сталей. При увеличении карбидов титана повышается твердость и износостойкость, но прочностьснижается.
| Сплав | Состав сплава, % | Характеристика физико-механических свойств | ||||
| WC | TiC | Co |
|
|
HRA, не менее | |
| T30K4 | 66 | 30 | 4 | 980 | 9,5-9,8 | 92,0 |
| T15K6 | 79 | 15 | 6 | 1176 | 11,1-11,6 | 90,0 |
| T14K8 | 78 | 14 | 8 | 1274 | 11,2-11,6 | 89,5 |
| T5K10 | 85 | 6 | 9 | 1421 | 12,4-13,1 | 88,5 |
| T5K12 | 83 | 5 | 12 | 1666 | 13,1-13,5 | 87,0 |
Титанотанталовольфрамокобальтовые твердые сплавы
По ГОСТ 3882-74 имеется 5 марок. Титан в составе улучшает свойства и эксплуатационные показатели, выражающиеся в повышении прочности при обычной и повышенной температуре. Благодаря карбиду тантала в составе улучшается износостойкость при резании
| Сплав | Состав, % | Характеристика физико-механических свойств | |||||
| WC | TiC | TaC | Co | σизг , Мпа, не менее |
|
HRA, не менее | |
| TT7K12 | 81 | 4 | 3 | 12 | 1666 | 13,0-13,3 | 87,0 |
| TT8K6 | 84 | 8 | 2 | 6 | 1323 | 12,8-13,3 | 90,5 |
| TT10K8-Б | 82 | 3 | 7 | 8 | 1617 | 13,5-13,8 | 89,0 |
| ТТ20К9 | 67 | 9,4 | 14,1 | 9,5 | 1470 | 12,0-13,0 | 91,0 |
| Т8К7 | 85 | 7,5 | 0,5 | 7 | 1519 | 12,8-13,1 | 90,5 |
Безвольфрамовые сплавы
Такие сплавы в СССР появились в 1970 гг. ввиду дефицита вольфрама. По ГОСТ 26530-85 существует две марки безвольфрамовых сплавов на основе карбидов, карбонитридов титана с никель-молибденовой связкой.
| Сплав | Содержание основных компонентов в %(по массе) |
|
|||||
| TiC | TiCN | Ni | Mo | σизг , Мпа, не менее |
|
HRA, не менее | |
| TH20 | 79 | — | 15,0 | 6,0 | 1050 | 5,5-6,0 | 90,0 |
| KHT16 | — | 74 | 19,5 | 6,5 | 1200 | 5,5-6,0 | 89,0 |
Эти марки обладают меньшей прочностью и теплостойкости они не могут заменить традиционные вольфрамовые. Сплав КНТ16 хорошо подходит для прерывистого резания. А марка ТН20 может эффективно заменить Т30К4 и Т15К6. Им можно проводить чистовую и получистовую обработку незакаленной стали.
Так или иначе, благодаря своим свойствам сплавы массово применяются во многих производствах.
По классификации ИСО, твердые сплавы делят по областям применения при обработке резанием:
- Р — для стальных отливок, дающих сливную стружку;
- М — труднообрабатываемые стали, сплавы;
- К — обработка чугуна;
- N — обработка алюминия и других цветных металлов и их сплавов;
- S — для обработки жаропрочных сплавов и сплавов на основе титана;
- H — для закаленной стали.
Сплавы группы Р маркируются синим цветом, М — желтым и К — красным цветом
Свойства
Основные свойства твёрдых сплавов: твердость; жаростойкость; прочность; износостойкость;
Однако, стоит понимать, что данные характеристики зависят от соотношения элементов, из которых изготовлен сплав. Так, например, материалы, в названии которых используется сочетание букв «BK» напрямую зависимы от размера от карбида вольфрама.
При уменьшении зерна карбида, сплав становится более твёрдым. При этом, велика вероятность уменьшения его прочности. При увеличении зерна происходит обратный процесс – прочность увеличивается, но сплав получается менее твёрдый.
Поэтому при закупке данного материала важно понимать значение маркировок, так они напрямую говорят о его свойствах.
Титаносодержащие сплавы более твердые и жаростойкие. Температура их плавления выходит за пределы 1200°C. Кроме того, они меньше подвержены окислению.
Из недостатков можно отметить худшую теплопроводность, по сравнению с материалами группы «BK», а также слабую прочность при изгибаниях.
Однако эта проблема решается добавлением в состав карбида тантала – сплавы, маркированные как «TTK» гораздо более прочны при работе.
Активному использованию в различных производствах способствует также и тот факт, что твердые металлы, как ни странно, весьма пластичны. Поэтому работать с ними можно как при высоких, так и при низких температурах.
Однако, резать, гнуть и проводить прочую механическую работу следует с большой осторожностью в связи с большой ломкостью и слабой прочностью при изгибах. При обработке материала необходимо знать его плотность, так как от этого зависит его прочность.
Так, например плотность вольфрамовых сплавов варьируется от 14 до 15 г/см³; титаносодержащих – от 9 до 13,5 г/см³; материала с примесью тантала – от 12 до 13,6г/см³.
От всех перечисленных свойств зависит, где и каким образом могут применяться твердые сплавы.
Примеры маркировки твердых сплавов
По принципу маркировки твердые сплавы делят согласно химическому составу:
- ВК — в составе карбид вольфрама и кобальт. Цифра означает содержание кобальта в процентах. Например это сплав ВК8, ВК10, ВК6
- ТК. Титаносодержащие сплавы, содержащие карбид титана, карбид вольфрама, кобальт. Обозначение буквами ТК. Цифра после буквы Т означает содержание карбида титана в процентах, а после буквы К — процент содержания кобальта. Это сплавы Т5К10, Т14К8, Т15К6, ТЗ0К4
- ТТК. Титано-тантало-вольфрамовые. Сплав включает в себя сразу три металла: титан, вольфрам и тантал и кобальт. Маркируется буквами ТТК. Цифра после ТТ, например «7» указывает на содержание карбидов титана и тантала, цифра после «К» , например «12» — процент кобальта. Марки ТТ7К12, ТТ20К9;
- ТН. Безвольфрамовые. ТНМ20, ТНМ25, ТНМ30.
Применение и продукция из твердых сплавов
Материал широко распространен в современной промышленности. Развивается и технология производства самих сплавов, улучшается их качество, меняется состав, появляются новые маркировки. Но помимо изменения самого материала, меняются и принципы работы с ним. Появляются новые типы соединений, наносимые на изделия, благодаря чему, они приобретают новые функции и роли в промышленности.
На сегодняшний день твёрдые сплавы применяются:
- В производстве режущего инструмента. Изготовленные из высокопрочных материалов инструменты позволяют повысить качество производства, ускорить его и снизить затраты на брак и закупку материалов. Высокая жаростойкость и прочность позволяют работать на предельных скоростях. Поэтому сплавы гораздо более ценны в производстве инструмента, нежели простая сталь. В их производстве зачастую используют алмазные заготовки, значительно повышающую качество материала и его свойства. К примерам таких инструментов можно отнести резцы, свёрла и т.д.;
- В изготовлении высокопрочных деталей для механических изделий, производственных машин, автомобилей и техники, ножей и лезвий для грейдеров – в механизмах, испытывающих высокие перегрузки и усилия;
- В производстве оборудования, предназначенного для больших нагрузок. Например, рудодобывающее оборудование, буровые установки. Сплавы применяются в опорах промышленных весов и в прочих механизмах, рассчитанных на большие усилия и давления;
- При изготовлении мелких, но ключевых деталей различных механизмов. Например, из данного материала производятся подшипники, клеммы, различные защитные напыления и прочее.
- В производстве различных форм и матриц, при отливке стальных изделий как простых, так и имеющих сложную форму.
- Для механической постобработки сложных материалов (сталь, чугун, цветные металлы, жаростойкие материалы и т.д.).
- При штамповании различных изделий.
Перед закупкой инструмента, деталей или просто исходного материала, в составе которого есть сплавы, необходимо тщательно изучить к какому классу они относятся и какими свойствами обладают.
В этом поможет понимание значений маркировок, которые указывают на состав изделия и, как следствие, на его способность выдерживать те или иные нагрузки.
Каждый класс материала предназначен для применения в конкретной сфере производства и может быть абсолютно не пригоден для иной, что также следует учитывать.
КАРБИДЫ
КАРБИДЫ (от латинского carbo – уголь) – соединения углерода с металлами, а также с бором и кремнием. Эти соединения обладают удивительным разнообразием физических и химических свойств.
Так, карбид золота Au2C2 взрывается уже при попытке пересыпать его с листочка фильтровальной бумаги, на котором он был высушен.
С другой стороны, карбиды некоторых элементов (например, бора и тантала) не разлагаются даже при температуре белого каления и настолько химически инертны, что на них не действует царская водка, а по твердости они приближаются к алмазу!
Впервые необычное соединение металла с углеродом (К2С2) получил в 1809 знаменитый английский химик Гемфри Дэви. В 1863 французский химик Марселен Бертло изучил свойства другого карбида – очень неустойчивого и легко взрывающегося карбида одновалентной меди Cu2C2. В 1878 немецкий металлург Ф.Мюллер, растворив образцы стали в разбавленной серной кислоте, выделил карбид железа Fe3C.
Но только в конце 19 в. французский химик Анри Муассан, прославившийся получением фтора, синтезировал многие из этих необычных соединений и изучил их свойства. Он получал карбиды, нагревая до очень высокой температуры смеси древесного угля с разными металлами, их оксидами или карбонатами. Для этого он использовал жар вольтовой дуги в электрической печи собственной конструкции.
Карбиды, как оказалось, можно получить не только в лаборатории. Еще до работ Муассана австрийский ученый Э.
Вайнсхенк в 1889 открыл в метеоритах минерал когенит, представляющий собой смешанный карбид железа, кобальта и никеля состава (FeNiCo)3C.
А сам Муассан в 1904 обнаружил в метеорите, привезенном из каньона Диабло в штате Аризона, темно-зеленый минерал, представляющий собой карбид кремния SiC. Этот минерал в честь ученого назвали муассанитом.
Раньше карбиды классифицировали по их устойчивости к действию воды и кислот, а также по тому, какие газы выделяются при их разложении.
Современная классификация учитывает тип химической связи между атомами в карбидах – именно от этого зависят в основном физические и химические свойства.
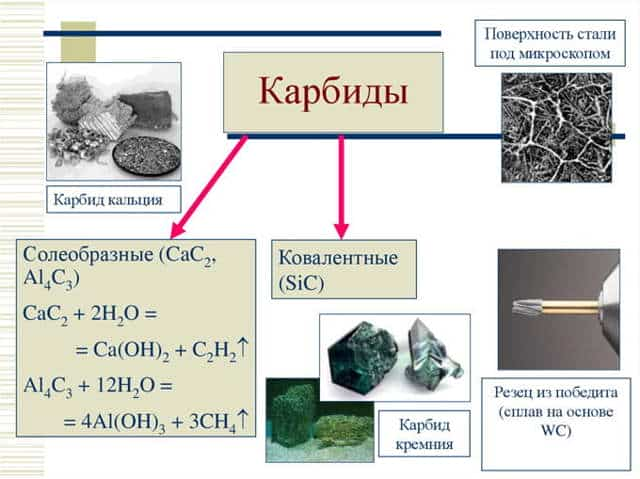
В соответствии с этой классификацией, карбиды можно разделить на три группы, которые довольно сильно отличаются по своим свойствам.
К первой группе относятся так называемые солеобразные карбиды с ионной связью. Эти карбиды образуют щелочные и щелочноземельные металлы, алюминий, редкоземельные элементы, а также актиноиды. Их состав иногда соответствует типичным валентностям металлов (Al4C3), а иногда – нет (Ве2С).
Многие ионные карбиды можно получить непосредственно из элементов (Са + 2С ® СаС2) или восстановлением оксидов углеродом (СаО + 3С ® СаС2 + СО). Ионный характер связи приводит к высокой температуре плавления; например, карбид кальция СаС2 плавится при 2300°С, карбид тория ThC2 – при 2655°С.
Водой или разбавленными кислотами ионные карбиды легко разлагаются – гидролизуются. При этом образуются различные углеводороды и гидроксид металла. Самый известный пример – получение ацетиленагидролизом карбида кальция: СаС2 + 2Н2О ® Ca(OH)2 + С2Н2. Ацетилен выделяется также при гидролизе Na2C2, К2С2 и др.
Поэтому такие карбиды можно рассматривать как производные ацетилена, в которых атомы водорода замещены атомами металла. При этом катионы металла и анионы С2–2 размещаются в соответствующих узлах кристаллической решетки. Солеобразный характер этих карбидов подтверждается возможностью их электролиза в расплавленном состоянии.
Интересно отметить, что чистый карбид кальция – бесцветные кристаллы, хотя увидеть их непросто, так как обычный технический продукт имеет цвет от бурого до черного.
Взаимодействие карбидов щелочных металлов с водой протекает исключительно бурно. Так, если карбид калия просто облить водой, произойдет бурная реакция, которая сопровождается взрывом такой силы, что выделяющийся ацетилен сразу же разлагается с выделением угля. Чтобы провести реакцию К2С2 + 2Н2О ® 2КОН + С2Н2, надо медленно пропускать над карбидом водяной пар.
В ряде случаев карбиды ионного типа образуются непосредственно при пропускании ацетилена через растворы солей металлов. Так карбиды серебра, меди(I), золота и ртути, которые чаще называют ацетиленидами. Ацетилениды щелочных металлов можно получить действием ацетилена на свободные металлы. В сухом виде ацетилениды тяжелых металлов легко разлагаются со взрывом.
Гидролиз ионных карбидов других металлов показывает, что они «происходят» из других углеводородов. Например, при гидролизе карбида алюминия выделяется метан: Al4C3 + 12H2O ® 4Al(OH)3 + 3CH4 (так же гидролизуется карбид бериллия Ве2С), а при гидролизе карбида магния получается метилацетилен: Mg2C3 + 4H2O ® 2Mg(OH)2+ НС≡С–СН3.
Интересно, что карбид магния другого состава, MgC2, дает при гидролизе только ацетилен. Иногда при гидролизе ионных карбидов углеводороды выделяются совместно с водородом, который частично гидрирует непредельные углеводороды. С выделением почти равных количеств водорода и метана разлагается карбид марганца: Mn3C + 6H2O ® 3Mn(OH)2 + CH4 + H2.
Карбиды редкоземельных металлов и тория при разложении разбавленными кислотами выделяют не чистый ацетилен, а его смесь с метаном, этиленом и другими углеводородами.
Например, при гидролизе карбида церия СеС2 получается смесь ацетилена с метаном в соотношении 4:1, а также немного этилена и жидких и твердых углеводородов (состав продуктов зависит от условий проведения реакции). Еще больше жидких и твердых углеводородов дает при гидролизе карбид урана.
Выделение углеводородов при гидролизе карбидов позволило Д.И.Менделееву выдвинуть так называемую карбидную теорию происхождения нефти в глубинах Земли из неорганических веществ.
По представлению Менделеева, в глубинах земного шара должны быть расплавленные металлы, в основном железо, которое с углеродом дает карбид. Во время горообразования в земной коре образуются трещины, по которым в глубины проникает вода.
Воздействуя на карбид железа и карбиды других металлов, вода (в виде пара) образует углеводороды, например: 2FeC + 3H2O ® Fe2O3 + C2H4. Газообразные углеводороды по тем же трещинам поднимаются ближе к поверхности, где скапливаются в пористых пластах. Однако когда в 60-е гг. 20 в.
был подробно изучен состав углеводородов нефти, оказалось, что смесь «искусственных углеводородов», образующихся при гидролизе карбидов, по своему составу резко отличается от природной смеси.
Кроме того, все нефти, полученные неорганическим путем, оптически неактивны, тогда как природная нефть оптически активна. На основании этих, а также ряда других фактов неорганическая теория происхождения нефти была подвергнута критике, и в настоящее время многие ученые полагают, что нефть имеет биологическое происхождение.
Ко второй группе относятся карбиды, которые образуют переходные металлы IV–VII групп, а также кобальт, железо и никель. Это металлоподобные соединения с другой структурой. В них атомы углерода, имеющие небольшие размеры, не связаны друг с другом и располагаются в пустотах между атомами металлов.
Различная упаковка атомов металла в кристаллической решетке приводит к разному составу карбидов даже для одного и того же металла; например, хром образует карбиды состава Cr3C2, Cr4C, Cr7C3 и др. Эти карбиды (их называют карбидами внедрения) часто отличаются большой твердостью и очень высокими температурами плавления.
Например, карбиды тантала и гафния TaC и HfC – наиболее тугоплавкие из известных веществ (плавятся при 3985 и 3890°С соответственно).
Металлоподобные карбиды обладают высокой электропроводностью и очень высокой химической стойкостью к агрессивным средам (многие из них не растворяются даже в царской водке).
Они используются для упрочнения чугуна и стали (карбиды железа, хрома, вольфрама, молибдена), а также для производства очень твердых сплавов, которые применяют для обработки металлов резанием (карбиды WC, TiC, TaC, VC, Cr3C2).
Например, твердые наконечники резцов, сверл делают из победита – спеченного порошка карбида вольфрама WC с добавкой металлического кобальта. Очень важную роль играет карбид железа Fe3C (цементит) – твердые кристаллы, входящие в структуру чугуна и стали.
Карбид вольфрама WC используют также для изготовления буровых коронок, деталей аппаратуры для производства синтетических алмазов, для нанесения износостойких покрытий на поверхности металлов.
Карбид титана интересен ярким проявлением нестехиометрии: состав этого соединения выражается формулой TiCх, где х колеблется в пределах от 0,49 до 1 (см. СТЕХИОМЕТРИЯ).
Это вещество, как и карбид вольфрама, используют как компонент жаропрочных, жаростойких и твердых сплавов, для получения износостойких покрытий, для изготовления тугоплавких тиглей, в которых можно плавить почти любые металлы (сам карбид плавится при 3257°С). Карбидом титана выкладывают внутренние стенки высокотемпературных печей.
К третьей группе относятся ковалентные карбиды. Их образуют кремний и бор – соседи углерода по периодической таблице, близкие к нему как по размеру атомов, так и по электроотрицательности.
Карбид кремния SiC (техническое название – карборунд) в чистом виде – бесцветные кристаллы, но примеси часто окрашивают его в различные цвета, вплоть до черного.
По своей структуре это соединение аналогично алмазу; решетку карбида кремния можно получить, если в немного расширенной решетке алмаза заменить половину атомов углерода на атомы кремния.
Это вещество обладает очень высокой твердостью; помимо этого оно имеет свойства полупроводника. Из него делают шлифовальные бруски и круги, огнеупорные материалы для печей и литейных машин, нагревательные элементы для электропечей, полупроводниковые диоды.
Бор образует по два карбида с точно известной структурой – В4С и В13С2.
Наибольшее значение имеет первый из них – черные блестящие кристаллы, которые по твердости уступают лишь алмазу и нитриду бора BN.
Этот карбид применяют для изготовления абразивных и шлифовальных материалов и в качестве полупроводника. Карбид, обогащенный изотопом 10В, используется как поглотитель нейтронов в ядерных реакторах.
Илья Леенсон






