- Описание
- Пирометаллургические методы
- Общие способы получения металлов
- Пирометаллургия
- Гидрометаллургия
- Электрометаллургия
- Пирометаллургический метод получения металлов
- Пирометаллургия
- Гидрометаллургия
- Электрометаллургия
- Промышленные способы получения металлов
- Основные способы получения металлов
- Как получают металл в промышленности
- 4.2.1. Понятие о металлургии: общие способы получения металлов
- ПОИСК
Современная металлургия обладает большим количеством способов получения чистого металла. Одним из них является пирометаллургия. Она включает целую совокупность технологических процессов, которые протекают при высоких температурах. С его помощью получают различные металлы: чёрные (сталь, чугун) и цветные (медь, никель, титан и многие другие).

Описание
Основу технологического процесса пирометаллургии составляет плавка, которая протекает при достаточно высоких температурах. Необходимая величина температуры зависит от степени плавления элемента, который необходимо получить. Они делят на три большие категории:
- легкоплавкие (с температурой плавления до 600 °С);
- среднеплавкие (не более 1600 °С, к ним относятся: никель сурьма, кальций);
- тугоплавкие (их температура плавления превышает 1600 °С).
Сырьём в пирометаллургии служит: руда, содержащая необходимый металл, концентраты, различные добавки. При обработке первичного сырья получают два компонента: металл и шлак.
В некоторых процессах получают так называемый штейн и шлак.
Получение необходимой температуры обеспечивается за счёт применения естественного топлива (угля, газа, продуктов нефтепереработки), температуры химических реакций, электрического нагрева.
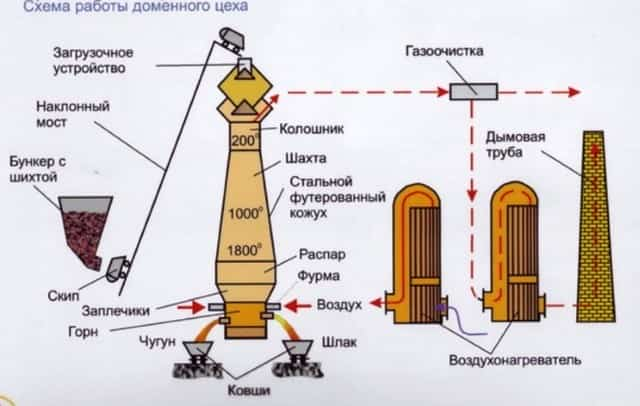
В черной пирометаллургии характерным примером получения стали служит доменная плавка. С её помощью получают сталь различных марок.
В цветной металлургии каждый металл обладает своими специфическими особенностями. Поэтому для получения используют свои специфические приёмы, которые подходят только для конкретного элемента. Например, для получения меди или никеля предварительно производят плавку на штейн. Потом из него получают черновой материал.
- Современная пирометаллургия обладает большим количеством разнообразных конструкций плавильных печей. Они бывают вертикальные и горизонтальные, периодические и непрерывные, с различным способом нагрева, со специфическими процессами (ликвация, электроннолучевая плавка, зонная и другие)
- Большую популярность такие процессы получили для получения многих тугоплавких металлов: молибдена, титана, ванадия.
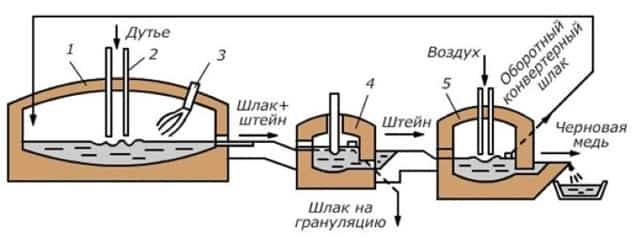
На завершающем этапе пирометаллургии выделяют чистый материал различными приёмами. Получения алюминия осуществляется проведением электролиза. В качестве сырья применяется глинозём.
Процесс протекает при температуре,более 1000 °С. Чистый элемент собирают на угольном катоде. Для этой технологической операции существует специальная ванна.
Приведенный пример показывает, что у цветных металлов проведение электролиза необходимо для выделения чистой фракции.
Пирометаллургические методы
Основными методами (способам) такого извлечения металлов является восстановление. К ним относятся:
- металлотермия;
- силикатотермия;
- восстановление различными элементами или химическими соединениями.
Любой пирометаллургический метод предполагает высокотемпературное протекание процесса. Первый из перечисленных пирометаллургических способов предполагает ускорение реакции восстановления за счёт свойств более активных металлов. Например, алюминия, магния, натрия.

Второй метод пирометаллургии – это восстановление необходимого элемента с помощью кремния. Остальные способы реализовываются за счёт применения различных химических элементов (например, водорода,углерода) или соединениями (например, гидритами различных металлов, монооксидом углерода).
Применение углерода и его монооксида в пирометаллургии считается целесообразным, когда отсутствуют высокие требования к чистоте получаемого материала и не допускаются высокие затраты на проведение реакции.
Обычно углеродом восстанавливают следующие элементы:
- железо из двух его соединений с кислородом: оксид железа (III) и четырёхмерного оксида железа (магнетита);
- олова из касситерита;
- меди из куприта.
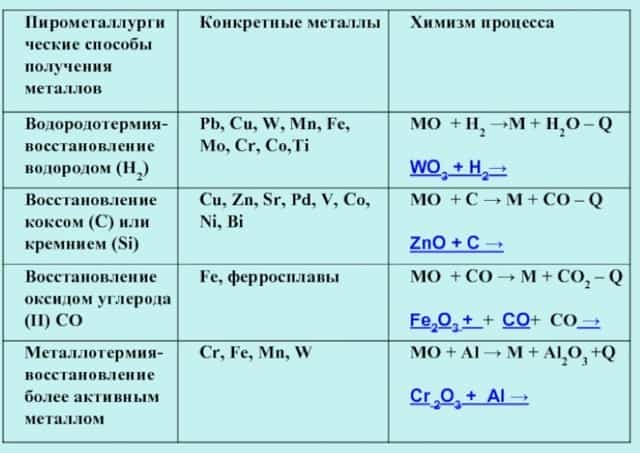
Методы с применением углерода объединяются одним термином – карбометрия. Кроме перечисленных технологий к современной пирометаллургии относят так называемую хлорную металлургию.
Она обеспечивает выделение материала при хлорировании сырья с добавлением, так называемого восстановителя. На завершающем этапе производят переработку полученных хлоридов. Этот метод обладает определёнными преимуществами перед классической пирометаллургией.
К ним относятся: практически полное извлечение необходимого содержимого, более высокая скорость реакции.
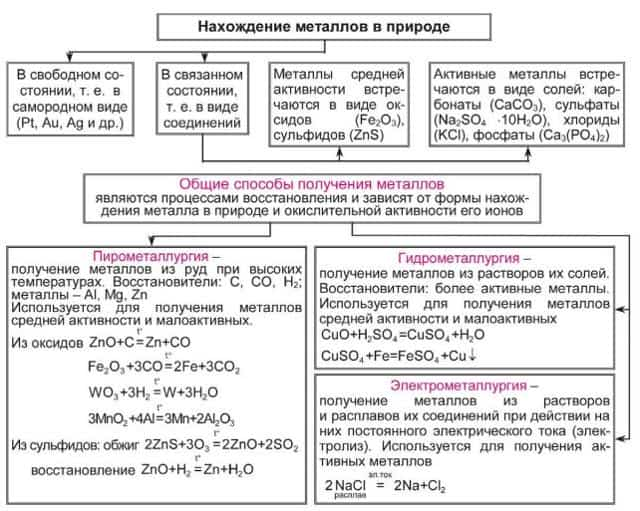
Общие способы получения металлов
Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
- Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами .
- Получение металлов из руд — задача металлургии.
- Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
- Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
- М n+ + ne−→M
- Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
-

- В соответствии с этим существуют следующие способы получения металлов:
- • пирометаллургический;
- • гидрометаллургический;
- • электрометаллургический.
Пирометаллургия
- Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
- Например, олово восстанавливают из касситерита СнО 2 , а медь — из куприта Cu 2 O
- прокаливанием с углем (коксом):
- SnО 2 + 2С = Sn + 2СО ↑; Cu 2 O + С = 2Cu+ СО ↑
- Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
- 2ZnS + 30 2 = 2ZnО + 2SO 2 ↑; ЗнО + С = Zn + СО ↑ сфалерит (цинковая обманка)
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
- FeСO3 = FеО + СO 2 ↑ ; FеО + С = Fе + СО ↑ сидерит (шпатовый железняк)
- Восстановлением углем можно получить Фе, Су, Zn, Сд, Ge, Sn, Рб и другие металлы, не образующие прочных карбидов (соединений с углеродом).
- В качестве восстановителя можно применять водород или активные металлы:
- 1) МоO 3 + ЗН 2 = Мо + ЗН 2 O (водородотермия)
- К достоинствам этого метода относится получение очень чистого металла.
- 2) TiO 2 + 2Мg = Тi + 2МgO (магнийтермия)
- ЗМnO 2 + 4Аl = ЗМn + 2Аl 2 O 3 (алюминотермия)
- Чаще всего в металлотермии используют алюминий, теплота образования оксида
которого очень велика (2А1 + 1,5 O 2 = Аl 2 O 3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
- Q= Σ Q 1 — Σ Q 2 ,
- где Q 1 — теплота образования продукта, Q 2 -теплота образования исходного вещества.
- Доменный процесс (производство чугуна): C + O 2 = CO 2 , CO 2 + C ↔ 2CO 3Fe 2 O 3 + CO = 2(Fe 2 Fe 3 2 )O 4 + CO 2 (Fe 2 Fe 3 2 )O 4 + CO= 3FeO + CO 2 FeO + CO= Fe + CO 2 (чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe 3 C);
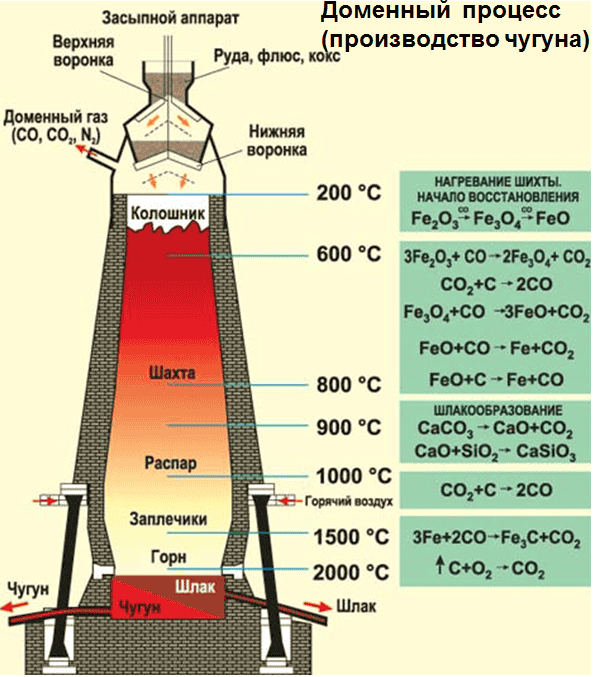 Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (CO 2 , SO 2 ), либо связываются в легко отделяемый шлак – смесь Ca 3 (PO 4 ) 2 и CaSiO 3 . Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (CO 2 , SO 2 ), либо связываются в легко отделяемый шлак – смесь Ca 3 (PO 4 ) 2 и CaSiO 3 . Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
- Гидрометаллургия — это восстановление металлов из их солей в растворе.
- Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СуО, ее обрабатывают разбавленной серной кислотой:
- СуО + Н 2 SО 4 = СuSO 4 + Н 2
- Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
- СuSO 4 . + Fе = Сu + FеSO 4
- Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
- Примеры:
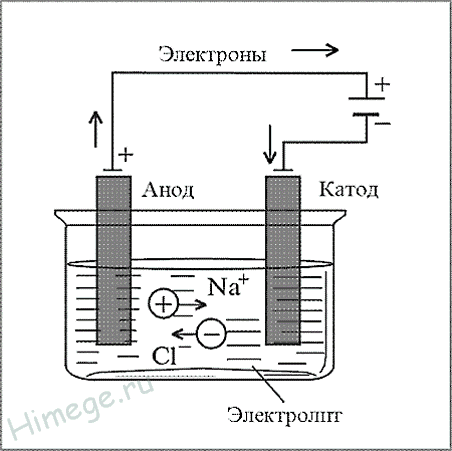 а) NaCl (электролиз расплава) → 2Na + Cl 2
а) NaCl (электролиз расплава) → 2Na + Cl 2 - б) CaCl 2 (электролиз расплава) → Ca + Cl↑ в) 2Al 2 O 3 (электролиз расплава) → 2Al + 3O 2 ↑ г) 2Cr 2 (SO 4 ) + 6H 2 O(электролиз) → 4Cr↓ + 3O 2 ↑ +6H 2 SO 4 д) 2MnSO 4 + 2H 2 O (электролиз) → 2Mn↓ + O 2 ↑+2H 2 SO 4 е) FeCl 2 (электролиз раствора) → Fe↓ + Cl 2 ↑
-
Пирометаллургический метод получения металлов

Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
- Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
- Получение металлов из руд — задача металлургии.
- Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
- Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
- М n+ + ne−→M
- Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
- В соответствии с этим существуют следующие способы получения металлов:
- • пирометаллургический;
- • гидрометаллургический;
- • электрометаллургический.
Пирометаллургия
- Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
- Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
- прокаливанием с углем (коксом):
- SnО2+ 2С = Sn + 2СО ↑; Cu2O + С = 2Cu+ СО ↑
- Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
- 2ZnS + 302 = 2ZnО + 2SO2 ↑; ZnО + С = Zn + СО ↑сфалерит (цинковая обманка)
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
FeСO3 = FеО + СO2 ↑ ; FеО + С = Fе + СО ↑сидерит (шпатовый железняк)
Восстановлением углем можно получить Fе, Сu, Zn, Сd, Ge, Sn, Рb и другие металлы, не образующие прочных карбидов (соединений с углеродом).
- В качестве восстановителя можно применять водород или активные металлы:
- 1) МоO3 + ЗН2 = Мо + ЗН2O (водородотермия)
- К достоинствам этого метода относится получение очень чистого металла.
- 2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
- ЗМnO2 + 4Аl = ЗМn + 2Аl2O3 (алюминотермия)
- Чаще всего в металлотермии используют алюминий, теплота образования оксида
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
Q= Σ Q1 — Σ Q 2 ,
Обмеднение металла в домашних условиях
- где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
- Доменный процесс (производство чугуна):C + O2 = CO2, CO2 + C ↔ 2CO3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2(Fe2Fe32)O4+ CO= 3FeO + CO2FeO + CO= Fe + CO2
- (чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов.
При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
- Гидрометаллургия — это восстановление металлов из их солей в растворе.
- Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
- СuО + Н2SО4 = СuSO4 + Н2
- Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
- СuSO4. + Fе = Сu + FеSO4
- Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
- Примеры:а) NaCl (электролиз расплава) → 2Na + Cl2
- б) CaCl2 (электролиз расплава) → Ca + Cl↑в) 2Al2O3(электролиз расплава) → 2Al + 3O2↑г) 2Cr2(SO4) + 6H2O(электролиз) → 4Cr↓ + 3O2↑ +6H2SO4д) 2MnSO4 + 2H2O (электролиз) → 2Mn↓ + O2↑+2H2SO4
- е) FeCl2(электролиз раствора) → Fe↓ + Cl2↑
- Источник: http://himege.ru/obshhie-sposoby-polucheniya-metallov/
Промышленные способы получения металлов

Существует несколько способов получения металлов в промышленности. Их применение зависит от химической активности получаемого элемента и используемого сырья. Некоторые металлы встречаются в природе в чистом виде, другие же требуют сложных технологических процедур для их выделения. Добыча одних элементов занимает несколько часов, другие же требуют многолетней обработки в особых условиях. Общие способы получения металлов можно разделить на следующие категории: восстановление, обжиг, электролиз, разложение.
Есть также специальные методы получения редчайших элементов, которые подразумевают создание специальных условий в среде обработки.
Сюда может входить ионная декристаллизация структурной решетки или же наоборот, проведение контролируемого процесса поликристаллизации, которые позволяют получать определенный изотоп, радиоактивное облучение и другие нестандартные процедуры воздействия.
Они используются довольно редко ввиду высокой дороговизны и отсутствия практического применения выделенных элементов. Поэтому остановимся подробнее на основных промышленных способах получения металлов. Они довольно разнообразны, но все основаны на использовании химических или физических свойств определенных веществ.
Основные способы получения металлов
Одним из основных способов получения металлов является их восстановление из оксидов. Это одно из самых распространенных соединений металлов, которые встречаются в природе.
Процесс восстановления протекает в доменных печах под воздействием высоких температур и при участии металлических или неметаллических восстановителей.
Из металлов используют элементы с высокой химической активностью, например, кальций, магний, алюминий.
Нагартованный металл это
Среди неметаллических веществ применяются оксид углерода, водород и коксующиеся угли.
Суть процедуры восстановления заключается в том, что более активный химический элемент или соединение вытесняет металл из оксида и вступает в реакцию с кислородом.
Таким образом, на выходе образуется новый оксид и чистый металл. Это самый распространенный способ получения металлов в современной металлургии.
Обжиг является лишь промежуточным методом получения чистого элемента. Он предполагает сжигание сульфида металла в кислородной среде, в результате чего образуется оксид, который затем подвергается процедуре восстановления.
Этот метод также применяется довольно часто, так как сульфидные соединения широко распространены в природе. Прямое получение чистого металла из его соединений серой не используют по причине сложности и дороговизны технологического процесса.
Гораздо проще и быстрее провести двойную обработку, как было указано выше.
Электролиз, как способ получения металлов подразумевает пропускание тока через расплав металлического соединения. В результате процедуры чистый металл оседает на катоде, а остальные вещества — на аноде. Такой способ применим к солям металлов. Но он не является универсальным для всех элементов. Подходит способ для получения щелочных металлов и алюминия.
Это связано с их высокой химической активностью, которая под воздействием электрического тока позволяет с легкостью нарушать установленные в соединениях связи. Иногда электролитический способ получения металлов применяют к щелочноземельным элементам, но они уже не так хорошо поддаются данной обработке, а некоторые и вовсе не разрывают полностью связь с неметаллом.
Последний способ — разложение происходит под воздействием высоких температур, которые позволяют разорвать связи между элементами на молекулярном уровне.
Для каждого соединения потребуется свой температурный уровень, но в целом метод не содержит каких-либо хитростей или особенностей.
Единственный момент: полученный в результате обработки металл, может потребовать проведения процедуры спекания.
Но этот способ позволяет получить практически на 100% чистый продукт, так как для его проведения не применяются катализаторы и другие химические вещества. В металлургии способы получения металлов называют пирометаллургическим, гидрометаллургическим, электрометаллургическим и термическим разложением.
Это четыре приведенных выше способа, только названные не по химической, а по промышленной терминологии.
Как получают металл в промышленности
Способ производства металла во многом зависит от его распространения в недрах земли. Добыча в основном происходит в виде руды с определенным процентным содержанием элементов. Богатые руды могут содержать до 90% металла. Бедные руды, которые содержат всего 20-30% вещества, перед обработкой отправляют на обогатительную фабрику.
В чистом виде в природе встречаются только благородные металлы, которые добывают в виде самородков различного размера.
Химически активные элементы встречаются либо в виде простых солей, либо в виде полиэлементных соединений, которые имеют очень сложное химическое строение, но в основном достаточно просто разлагаются на составляющие при определенном воздействии.
Металлы средней и малой активности в природных условиях образуют оксиды и сульфиды. Реже их можно встретить в составе сложных кислотно-металлических соединений.
Как определить серебро от другого металла?
Перед получением чистого металла зачастую производится одна или несколько процедур разложения сложных веществ на более простые.
Гораздо проще выделять один продукт из двухэлементного соединения, чем из многоэлементного сложного образования.
К тому же технологический процесс требует тщательного контроля, который очень сложно обеспечить, когда речь идет о большом количестве примесей с разными свойствами.
Что касается экологической стороны вопроса, то самым чистым можно признать электрохимический способ получения металлов, так как при его проведении в атмосферу не выделяется никаких веществ. В остальном же металлургия является одним из самых вредных для природы производств, поэтому в современном мире уделяется большое внимание проблеме создания безотходного оборудования.
Уже сейчас многие заводы отказались от использования мартеновских печей в пользу более современных электрических моделей. Они потребляют гораздо больше энергии, но не выбрасывают в атмосферу продукты сгорания топлива. Очень важной является и вторичная переработка металлов.
Для этого во всех странах оборудованы специальные пункты приема, в которых можно сдавать вышедшие из эксплуатации детали из черных и цветных металлов, которые затем отправятся на переработку.
В будущем из них изготовят новую продукцию, которую можно будет использовать в соответствии с назначением.
| Сталь – это железоуглеродистый сплав, который содержит около 1,5% углерода, если его содержание увеличивается, то значительно повышается хрупкость и твердость стали. Основной исходный материал для производства стали — стальной лом и передельный чугун…. |
| Если говорить об общем объеме, то на долю пирометаллургических способов производства меди приходится более трех четвертей выпуска этого металла. Наряду с большинством цветных металлов, медь с каждым годом становится все более дефицитной, а основная добыча материала… |
| По распространенности кремний в земной коре занимает 2-ое пространство следуя за кислорода, сталкивается основным образом в повторяющемся виде кислородных синтезов (силикаты, кварц и т.д.). Высочайшей частоты кремний применяется в полупроводниковых техниках… |
| Под воздействием высоких температур удается получить металлы из оксидов. Процесс осуществляется в доменных печах с использованием металлических и неметаллических восстановителей, которые вступая в реакцию с кислородом, вытесняют металл из… |
| Для получения металла высшей пробы с минимальным количеством примесей используется электролитический способ добычи. С момента открытия месторождения и до завершающей стадии переплавки сырья в готовое …… |
| По сравнению со сталью чугун является более хрупким материалом, однако его литейные свойства более высокие. Производство чугуна осуществляется в домнах, которые работают по принципу противотока. Уменьшив содержание таких элементов, как углерод марганец, фосфор и… |
Источник: https://promplace.ru/dobycha-i-poluchenie-metallov-staty/sposoby-polucheniya-metallov-1539.htm
4.2.1. Понятие о металлургии: общие способы получения металлов
- Металлургия — это комплексная отрасль промышленности, которая занимается производством металлов.
- Поскольку большинство металлов в природе существует в виде различных соединений, то химическая суть металлургических процессов заключается в восстановлении металлов:
- Me+n + nē → Me0
- В зависимости от того, какой используется восстановитель и каковы условия, при которых проводят процессы восстановления различают пиро-, гидро-, электро- и биометаллургию.
Пирометаллургия (от греч. огонь и металлургия) представляет собой все химические способы восстановления металлов из руд, осуществляемые с применением высоких температур.
В качестве восстановителей в пирометаллургии используют уголь (кокс), оксид углерода (II), водород, активные металлы, кремний.
Оксидные руды чаще всего восстанавливают коксом или оксидом углерода (II) — этот процесс носит название карботермия:
Для извлечения металлов пирометаллургическим способом из сульфидных руд их сначала подвергают предварительному отжигу:
А затем, полученный оксид восстанавливают коксом:
Тугоплавкие металлы, например, молибден и вольфрам, восстанавливают водородом:
Если восстановителями химически активные металлы, то этот пирометаллургический способ называют металлотермия. В зависимости от природы металла-восстановителя различают алюминотермию, или алюмотермию, — восстановление алюминием и магнийтермию — восстановление магнием. Способ металлотермии позволяет восстанавливать металлы не только из оксидов, но и с галогенидов:
Известен способ восстановления металлов кремнием, называемый силикотермией:
Гидрометаллургия представляет собой метод получения металлов, заклющийся в преобразовании природных соединений металлов в растворимую форму с последующим восстановлением металла из раствора.
О возможности применения гидрометаллургических процессов для извлечения металлов еще в 1763 г.. Говорил М. В. Ломоносов.
Гидрометаллургического способами добывают благородные (золото, серебро, платину), цветные (медь, никель, цинк, кобальт), редкие (цирконий, гафний, тантал) и другие металлы:
NiSO4 + Zn = Ni + ZnSO4
К преимуществам данного способа относится возможность его использования для получения металлов при их малом содержании в руде, которую невозможно перерабатывать обычными способами; снижение во многих случаях загрязнения окружающей среды, например, при обжиге сульфидных руд.
Электрометаллургия — это способ получения металлов с применением электрического тока — электролиза. Электролизом расплавов получают самые активные металлы (от лития до марганца в ряду активности), электролизом водных растворов — менее активные (Zn, Cu, Ni, Cr и т.д.).
Биометалургия основана на биохимических процессах, протекающих при использовании микроорганизмов. Известно, что микроорганизмы типа литотрофы (с лат.
– «поедающие камни») могут преобразовывать нерастворимые сульфиды металлов в растворимые сульфаты.
Сейчас с применением микроорганизмов добывают медь (в США данный метод достигает 10% от общего ее производства), уран, рений, серебро, никель, свинец, а также некоторые редкие металлы.
ПОИСК
В пирометаллургии используют также способность сульфидов металлов восстанавливать их оксиды, что приводит к самовосстановлению металлов из смеси их соединений. Это происходит при получении меди и свинца из их сульфидных руд. [c.
295]
Методы извлечения металлов из руд определяются химическим составом последних. Извлечение металлов производится при высоких температурах, в отсутствие воды (пирометаллургия) или в водной среде, т. е. в растворах (гидрометаллургия).
С химической точки зрения реакции получения металлов по существу сводятся к реакциям окисления — восстановления. [c.228]
Пирометаллургия занимает ведущее место в металлургии. Она охватывает способы получения металлов из руд с помощью реакций восстановления, проводимых при высоких температурах. В качестве восстановителей применяют уголь, активные металлы, оксид углерода (И), водород, метан. Так, например, уголь и оксид углерода (И) восстанавливают медь из красной медной руды (куприта) СпаО [c.231]
Применяя водород, с помощью пирометаллургии получают металлы высокой чистоты. Например [c.394]
Пирометаллургия охватывает способы получения металлов из руд с помощью реакций восстановления, проводимых при высоких температурах. В основе пирометаллургии лежат реакции восстановления металлов из их окислов. В тех случаях, когда руда представляет собой соль, например сульфид цинка, ее предварительно переводят в окисел [c.319]
В последние годы в пирометаллургии цинка достигнуты большие успехи.
Освоены нОвые процессы получения цинка дистилляция в вертикальных ретортах, восстановление в электротермических печах, плавка цинковых концентратов В1 шахтных печах В связи с тем что потребности отдельных отраслей промышленности могут быть удовлетворены более дешевым дистилляционным цинком, в ряде зарубежных стран получают развитие новые пирометаллургические процессы (СШД, Англия). [c.413]
Пирометаллургия является наиболее старым и распространенным видом металлургии тяжелых металлов. Ее главнейшие операции [c.228]
Реакция образования фосгена протекает при наличии катализатора (активированного угля) и при комнатной температуре. Способность оксида углерода восстанавливать многие оксиды металлов широко используется в пирометаллургии.
Эти реакции лежат в основе промышленного производства таких металлов, как Ре, Со, N1, Си, Ag, Мп, Мо н др. Условия восстановления определяются природой оксида металла. Температуры восстановления металлических оксидов варьируют от 300 до 1500 °С.
В доменном процессе суммарная реакция представлена уравнением [c.186]
ПИРОМЕТАЛЛУРГИЯ — область металлургии, связанная с получением и очисткой металлов (сплавов) при высоких температурах (обжиг, плавка и др.). К П. относится производство чугуна, стали, меди, свинца, никеля и других металлов. [c.192]
Пирометаллургия — восстановление металлов при высоких температурах. [c.376]
В обычных условиях оксид углерода (II) химически весьма инертен. При нагревании проявляет восстановительные свойства, что широко используется в пирометаллургии (см. стр. 265). При 700°С окись углерода сгорает синим пламенем, выделяя большое количество тепла (282 кдж/моль) [c.460]
Пирометаллургия — это получение металлов из их соединений при высоких температурах с помощью различных восстановителей углерода, оксида углерода (II), водорода, металлов (алюминия, магния) и др. Например [c.277]
В зависимости от способов получения металлов различают пирометаллургию, гидрометаллургию и электрометаллургию. [c.319]
Гидрометаллургия, как и пирометаллургия, состоит из собственно гидрометаллургии, в которой реакции выделения металлов осуществляются в водных растворах без нагревания и в отсутствие электрического тока, и гидроэлектрометаллургии, где выделение металлов производится электролизом водных растворов. [c.229]
Восстановление металлов газообразными СО и Нз в п р и-сутствии твердого углерода. Восстановление оксидов металлов этими восстановителями идет только при высоких температурах — пирометаллургия. Процесс идет в газообразной фазе и присутствие углерода смещает равновесие в сторону восстановления металла, поэтому различают два метода ведения процесса [c.286]
Методом пирометаллургии получают большое количество различных металлов. [c.287]
Пиримидиновые основания 658 Пирит 305 Пирокатехин 549 Пиролиз 457 Пирометаллургия 277 Пиросерная кислота 370 Пирофосфорная кислота 401 Пиррол 655 [c.707]
В пирометаллургии цветных металлов реакциями, ведущими к получению металла, часто являются восстановление оксидов окисью углерода, водородом или углеродом. [c.110]
Пирометаллургаей называется способ получения металла из руд, основанный на их нагревании, например, в печах, продуваемых воздухом. Этот способ используется в двух из трех восстановительных процессов, приведенных в таблице.
Нагрев при этом происходит либо на воздухе (обжиг), либо в присутствии восстановителя. Обычно используются уголь (кокс) или моноксид углерода, поскольку они недороги и доступны. Если оба этих вещества не годятся, в качестве восстановителя можно использовать более активный металл.
Пирометаллургия — наиболее важный и старейший способ получения металлов из руд. [c.153]
Некоторые металлы извлекают из руд в основном способами пирометаллургии, и только конечная стадия — получение чистого металла осуществляется так называемым электролитическим рафинированием (табл.
УИМ), которое предусматривает анодное растворение пирометаллургического, загрязненного различными примесями металла и катодное его осаждение в том же электролизере в более чистом виде.
При этом товарными являются металлы, получаемые как в результате пирометаллургиче-ской переработки (металлы пониженной чистоты), так и рафинирования (чистые металлы). [c.232]
В противоположность щелочноземельным металлам цинк и кадмий в свободном состоянии можно получить химическим восстановлением или электролизом растворов их соединений. Пирометаллурги-ческое получение 2п и Сс1 из их сернистых руд проводится в две стадии. Сначала руды подвергаются окислительному обжигу, затем полученные оксиды восстанавливают углем [c.581]
Получение черновой меди пирометаллурги-ческим методом из халькопирита описывается суммарным уравнением (не забудьте подобрать коэффициенты) [c.267]
С кислородом углерод образует два оксида — монооксид СО и диоксид СО2. Монооксид углерода используется в пирометаллургии как сильный восстановитель (переводит металлы из их оксидов в свободное состояние). Для СО характерны и реакции присоединения, такие как образование карбонилкомплексов типа [Ре(С0)5]. [c.203]
Пирометаллургия занимает ведущее место в металлургической промышленности. Суть метода заключается получении металлов из руд с помощью восстановителей при высоких температурах.
В качестве восстановителей используют уголь, активные металлы, водород, метан, рксид углерода (II).
Например, один из способов получения олова из оловянного камня (касситерита) ЗпОа заключается в восстановлении олова из оксида Зп(1У) углем [c.143]
Пирометаллургия включает собственно пирометаллургию, использующую химические реакции, идущие при высоких температурах, и пироэлектрометаллургию, в которой высокие температуры достигаются действием электрического тока (получаемый металл выделяется на катоде). [c.228]
Восстановление металлов из их соединений требует больших затрат энергии, равноценных теплотам образования этих соединений.
Для протекания восстановительного процесса его необходимо проводить либо при высокой температуре, либо в растворе. Металлургические процессы, осуществляемые при сильном нагревании, называются пирометаллург и ческими (от греч.
piros — огонь), а если они приводятся в растворах, то —гидрометаллу р г и ч е с к и м и. [c.294]
Пирометаллургия объединяет методы, основанные на восстановле-нин металлов нз руд при высоких температурах с помощью угля или оксида углерода (II) иногда в этих целях используют алюминий, кремний и водород. [c.262]
Наряду с обычным получением меди путем процессов, проводимых при высоких температурах (пирометаллургия), большое значение имеют методы ее извлечения, основанные на обработке руд теми или иными жидкостями (гидрометаллургия).
Для извлечения меди из особенно пригодных для гидрометаллургической переработки окисленных руд часто пользуются р тбав-ленным раствором серной кислоты. Медь сульфидных руд может быть переведена в раствор по схеме СигЗ + 2Рб2(504)з = 4Ре304 + 2Си504 + 8.
Из образующегося разбавленного раствора медной соли металл выделяют затем либо электролизом, либо действием металлического железа. [c.419]
Химия (1986) — [ c.286 ]
- Неорганическая химия (1987) — [ c.262 ]
- Химия для поступающих в вузы 1985 (1985) — [ c.231 ]
- Учебник общей химии (1981) — [ c.419 ]
- Химия (1979) — [ c.264 ]
- Пособие по химии для поступающих в вузы 1972 (1972) — [ c.289 ]
- Общая химия (1987) — [ c.192 ]
Общая и неорганическая химия Изд.3 (1998) — [ c.680 ]
Общая химическая технология (1964) — [ c.385 , c.402 , c.411 ]
Курс химии Часть 1 (1972) — [ c.274 ]
Общая химия и неорганическая химия издание 5 (1952) — [ c.326 , c.327 ]
Общая химия 1982 (1982) — [ c.539 ]
Общая химия 1986 (1986) — [ c.522 ]
Общая химическая технология (1970) — [ c.435 , c.436 , c.438 , c.451 ]
- Неорганическая химия (1978) — [ c.241 ]
- Химия (1975) — [ c.247 ]
- Химия германия (1967) — [ c.362 ]
- Общая химия Издание 18 (1976) — [ c.533 ]
- Общая химия Издание 22 (1982) — [ c.539 ]
- Неорганическая химия (1969) — [ c.572 ]
- Общая и неорганическая химия (1981) — [ c.243 ]
Основы общей химической технологии (1963) — [ c.161 , c.162 ]
- Общая химическая технология Том 2 (1959) — [ c.124 ]
- Основы общей химии Том 2 Издание 3 (1973) — [ c.252 ]
- Основы общей химии Том 3 (1970) — [ c.47 ]






