- Практическая работа по материаловедению на тему "Расшифровка марок цветных металлов и сплавов"
- Практическая работа «Цветные металлы: расшифровка марок цветных металлов; применение цветных металлов." — Практикум по материаловедению
- Пахомов Ю. | Сборник практических работ по химии | Журнал «Химия» № 42/2003
- 9 КЛАСС
- Практическая работа 20. Сплавы
- Сплавы железа – чугун
- Практическая работа 21. Коррозия металлов и методы защиты
- Виды коррозии Химическая (газовая) коррозия
- Электрохимическая коррозия
- Основные методы защиты металлов от коррозии
Цель работы: изучение микроструктуры и свойств цветных металлов и сплавов и установление связи между структурой сплава и соответствующей диаграммой состояния.
Алюминий и его сплавы.Алюминий кристаллизуется в гранецентрированной кубической решетке. Наиболее характерные свойства его – малый удельный вес (g = 2,7), низкая температура плавления (657 оС), высокая тепло- и электропроводность, высокая пластичность.
Алюминий – один из важнейших промышленных металлов. Он находит широкое применение в электротехнике, в химическом аппаратостроении, в быту и других областях. Применение его как конструкционного материала в технике ограничено низкой прочностью (sВ = 8–10 кг/мм2).
Алюминий значительно упрочняется путем введения различных легирующих элементов, что позволяет получить сплавы с высокими прочностными свойствами.
Применяющиеся в технике алюминиевые сплавы делятся на деформируемые и литейные.
Деформируемые сплавы. Сплавы этого класса подразделяются на неупрочняемые термической обработкой и упрочняемые.
К сплавам первой группы относятся АМг1,5…, АМц2. В связи с низким содержанием легирующих элементов (магния или марганца) они представляют собой однофазные твердые растворы, обладающие высокой пластичностью, свариваемостью, но низкими прочностью и твердостью.
Повысить их прочность можно за счет наклепа, возникающего при холодной пластической деформации.
Для сплавов этой группы характерна широкая область применения: трубные конструкции, различные емкости для жидкостей (баки, цистерны), радиаторы охлаждения, элементы строительных конструкций (окна, двери), посуда и т. д.
К сплавам второй группы относятся Д1, Д18…, АК6, АК8…, В93, В95.
Наиболее распространенным представителем этой группы является дюралюминий (Д1, Д16), который, кроме алюминия, содержит около 4 % Cu, 1 % Mg, 1 % Mn и менее 0,7 % Fe и Si.
Основными легирующими элементами являются медь и магний, поэтому этот материал может быть причислен к сплавам системы Al–Cu–Mg. Кремний и железо являются постоянными примесями, попадающими в сплав вследствие применения недостаточно чистого алюминия.
Марганец вводится в дюралюминий главным образом для повышения коррозионной стойкости.
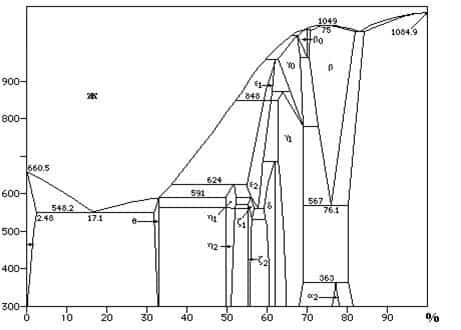
Перечисленные компоненты образуют ряд растворимых соединений CuAl, CuMgAl2 (S-фаза), Mg2Si, вызывающих упрочнение сплава в процессе термической обработки, заключающихся в закалке от 500 оС в воде с последующим естественным старением в течение 5–7 суток. Железистые и марганцовистые соединения в процессе закалки не растворяются. Диаграмма состояния Al–Cu представлена на рисунке 16.1.
Структура дюралюминия в отторженном состоянии состоит из твердого раствора и вторичных включений различных интерметаллических соединений; в закаленном – из пересыщенного твердого раствора и нерастворимых железистых и марганцовистых соединений. В процессе старения из пересыщенного твердого раствора выделяется высокодисперсная вторичная фаза (например, CuAl2II), которая является препятствием для движения дислокаций и приводит к упрочнению сплава в 3 – 4 раза.
Литейные сплавы. В качестве литейных сплавов на основе алюминия широкое распространение имеют силумины – алюминиевокремистые сплавы (5–14 % Si). Диаграмма состояния системы Al–Si представлена на рисунке 16.2.
Силумины обладают высокой жидкотекучестью, малой усадкой, удовлетворительной коррозионной стойкостью и применяются для получения отливок сложной формы.
Типичным силумином является эвтектический сплав (11–12 % Si), структура которого имеет игольчатую эвтектику (основа сплава), состоящую из твердого раствора кремния в алюминии a и небольшого количества грубых игольчатых включений Si (рисунок 16.3, а).
-
-
- Рисунок 16.1 – Диаграмма состояния Al–Cu
Повышение прочности и пластичности силумина достигается модифицированием – введением в расплав перед разливкой незначительного количества натрия и его солей. При этом изменяется структура сплава: кристаллы кремния вместо игольчатых становятся округлыми.
Введение модификатора вызывает смещение линии начала кристаллизации кремния в сторону более высокого содержания кремния и более низких температур. Эвтектический сплав с 11–12 % Si в этом случае становится доэвтектическим (рисунок 16.3, б).
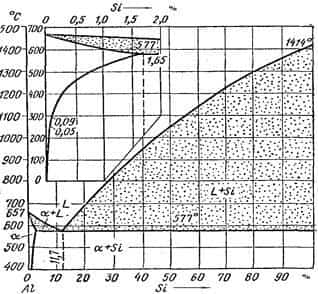
- Рисунок 16.2 – Диаграмма состояния Al–Si
- а) б)
- а – немодифицированный; б – модифицированный
- Рисунок 16.3 – Микроструктура силумина АЛ2
При более высоких требованиях к прочностным свойствам применяют специальные силумины – доэвтектические сплавы с 4–10 % Si с добавками меди, магния, марганца. Эти сплавы способны упрочняться при термической обработке. Маркировка сплавов АЛ: буквы указывают, что это алюминиевый (А), литейный (Л) сплав; цифры – порядковый номер в ГОСТе.
Медь и ее сплавы.Медь имеет гранецентрированную кубическую решетку. Удельный вес меди 8,94 г/см3, температура плавления 1083 оС. Она обладает высокой теплопроводностью, электропроводностью, пластичностью в горячем и холодном состояниях и широко применяется в различных областях техники. Кроме того, медь является основой важнейших сплавов – латуней и бронз.
Сплавы меди с цинком (латуни). Практическое применение имеют сплавы с содержанием цинка до 45 %, которые называются латунями. Равновесная диаграмма состояния для этой системы приведена на рисунке 16.4. По структуре латуни делятся на две группы:
– сплавы с содержанием цинка до 39 % являются однофазными со структурой твердого раствора цинка и меди (a);
– сплавы с содержанием цинка более 39 % имеют двухфазную структуру (a+b); b-твердый раствор на базе соединения CuZn с электронным типом связи имеет кубическую объемно-центрированную решетку (рисунок 16.5).
Рисунок 16.4 – Диаграмма состояния Cu–Zn
Цинк до определенного предела повышает прочность и пластичность сплавов. Максимальной пластичностью обладают материалы со структурой однофазного твердого раствора.
Переход через границу однофазной области (39 % Zn) приводит к резкому снижению пластичности, повышению прочностных и литейных свойств. Максимальной прочностью обладает b-латунь при содержании цинка 45 %.
Однако пластичность ее относительно низка.
Рисунок 16.5 – Микроструктура литой двухфазной латуни
Литейные свойства двухфазных латуней характеризуются хорошей жидкотекучестью, малой склонностью к ликвации, способностью к образованию концентрированной усадочной раковины.
Латуни легко поддаются пластической деформации, поэтому их используют для производства листов, лент, профилей.
Причем для прокатки в холодном состоянии применяют латуни с содержанием цинка до 30 % ( a-латуни), а для прокатки в горячем состоянии наиболее пригодны латуни со структурой a + b (при температуре обработки давлением их структура состоит из одной – b-фазы).
Кроме простых латуней – сплавов меди и цинка, применяются специальные, в которые для придания тех или иных свойств дополнительно вводят различные элементы: свинец – для улучшения обрабатываемости, олово – для повышения сопротивления коррозии в морской воде, алюминий и никель – для повышения механических свойств. Марки латуней начинаются с буквы Л, далее следуют буквы, указывающие наличие определенных легирующих элементов, цифры отображают концентрацию меди и легирующих элементов.
Бронзы. Бронзами называются сплавы меди с другими элементами (за исключением цинка). В зависимости от основного легирующего элемента бронзы разделяются на оловянистые, алюминиевые, бериллиевые, марганцовистые и т. д.
Марки бронз начинаются с букв Бр. Далее следуют буквы, показывающие наличие определенных легирующих элементов, и цифры, указывающие их содержание. Бронзы применяют для получения отливок и поковок.
Дорогостоящие и дефицитные оловянистые бронзы в настоящее время заменяются алюминиевыми.
Алюминиевая бронза. Наиболее распространены алюминиевые бронзы, содержащие 5–11 % Al. Сплавы с содержанием алюминия до 9,8 % имеют однофазную структуру твердого раствора алюминия в меди (a) (рисунок 16.6).
При больших концентрациях алюминия у сплавов двухфазная структура, состоящая из твердого раствора (a) и эвтектоида (a + g¢).
Фаза g является твердым раствором на основе электронного соединения Cu32Al19 со сложной кубической решеткой (рисунок 16.7).
Алюминиевые бронзы среди медных сплавов выделяются высокими механическими, коррозионными и антифрикционными свойствами, в связи с чем их широко применяют в машиностроении для деталей конструкционного назначения.
Наряду с простыми алюминиевыми бронзами используют сложные. При введении железа до 4 % происходит измельчение a-фазы, повышение твердости и прочности бронзы за счет его растворения в меди.
Легирование никелем приводит к повышению жаропрочности бронз.
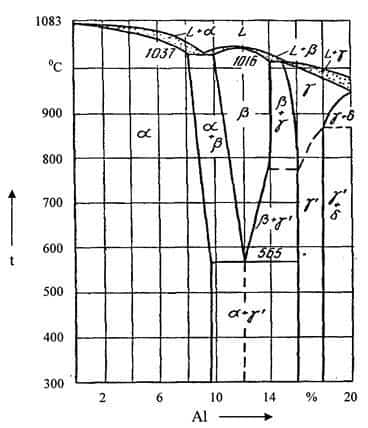
Рисунок 16.6 – «Медный» участок диаграммы состояния Cu–Al
Бериллиевая бронза обладает исключительно ценными качествами (диаграмма состояния этой системы приведена на рисунке 16.8). Она имеет высокую прочность и твердость, повышенный предел упругости и усталости. Бериллиевая бронза является ценным пружинным материалом и с успехом применяется для изготовления деталей, работающих на износ. Этот материал не дает искр при ударе.
- Рисунок 16.7 – Микроструктура литой бронзы БрА10
-
0 10 20 30 40 50 60 70 80 % 100 - Be
- Рисунок 16.8 – Диаграмма состояния Cu–Be
Наиболее высокие механические свойства имеют сплавы с 2,0–2,5 % бериллия. Как видно из диаграммы состояния, они являются дисперсионно-твердеющими. Растворимость бериллия в меди при комнатной температуре не превышает 0,2 %.
Закалка с 800 оС фиксирует пересыщенный раствор бериллия в меди.
Последующее искусственное старение при 300–350 оС приводит к резкому повышению твердости и прочности, которое связано с выделением из твердого раствора g (CuBeII) – фазы в форме дисперсных включений.
Широкому распространению бериллиевой бронзы препятствует ее высокая стоимость и дефицитность.
Легкоплавкие подшипниковые сплавы (баббиты). Подшипниковыми сплавами называются материалы, из которых изготавливаются вкладыши подшипников скольжения. При применении очень мягких легкоплавких сплавов (баббитов) гарантируется минимальный износ шейки вала. Кроме того, они имеют минимальный коэффициент трения со сталью и хорошо удерживают смазку.
По условиям работы подшипниковый сплав должен иметь гетерогенную структуру и состоять из мягкой основы и твердых включений.
Мягкая основа обеспечивает хорошую прирабатываемость подшипника к валу, твердые включения служат опорными точками для трущихся частей вала.
Небольшая поверхность соприкосновения вала и вкладыша уменьшает трение, а имеющиеся промежутки между валом и мягкой основой обеспечивают хорошую смазку.
В качестве баббитов применяются сплавы системы Pb–Sb (диаграмма состояния которой приведена на рисунке 16.9), Sn–Sb, Pb–Sn–Sb, а также баббиты на основе цинка с добавками Cu, Al и баббиты на основе алюминия с добавками Cu, Sb, Ni.
Широкое применение в промышленности получили заэвтектические сплавы системы свинец-сурьма (БС), содержащие 16–18 % Sb. Мягкой основой в этом сплаве является эвтектика (a + b), твердость которой составляет 7–8 НВ. Твердость включений сурьмы 30 НB. Микроструктура баббита БС, содержащего 16–18 % Sb, приведена на рисунке 16.10.
Двойные заэвтектические сплавы системы свинец-сурьма сильно ликвируют. Кристаллы b (твердый раствор свинца в сурьме) при отливке всплывают наверх. Для предотвращения ликвации b-кристаллов в сплав вводится медь (1–2 %), которая образует с сурьмой химическое соединение Сu3Sb.
Это соединение, кристаллизуясь первым, образует скелет, на котором задерживаются b-кристаллы. В системе олово-сурьма (Sn–Sb) олово имеет низкую твердость 5 HВ.
Для подшипников скольжения наиболее подходящим является сплав, состоящий из 10–13 % Sb и 87 % Sn, имеющий двухфазную структуру a + b¢, где a-твердый раствор на основе олова (мягкая составляющая); b¢-твердый раствор на базе интерметаллического соединения SnSb (твердые включения).
Практическая работа по материаловедению на тему "Расшифровка марок цветных металлов и сплавов"
- Практическая работа № 1
- Тема: Маркировка цветных металлов и сплавов
- Цель: расшифровать
буквы и цифры в названии марок цветных металлов и сплавов. - Оборудование:
мультимедийный проектор - Ход
урока: - 1. Организационный момент (проверить готовность к уроку, отметить отсутствующих, объявить тему и
цель урока, порядок выполнения работы)
Порядок выполнения работы
1. Изучить характеристики и расшифровку марок
алюминия и его сплавов, меди и её сплавов, изложенных в теоретической части
работы.
2. Произвести
расшифровку предложенных марок материалов таблицы 1, полученные результаты
записать в таблицу 2.
- 3. Оформить отчёт
работы - Задание
- Произвести расшифровку марок цветных металлов
и их сплавов из таблицы 1 - 2. Теоретическая основа работы
- Классификация цветных сплавов.
- Алюминий и алюминиевые сплавы
- Медь
и медные сплавы - Титан, магний и их сплавы
- Олово, свинец, цинк и их сплавы
- Алюминий
и его сплавы
Алюминий — легкий
металл, обладающий высокими тепло- и электропроводностью, стойкий к коррозии.
В
зависимости от степени частоты первичный алюминий согласно ГОСТ 11069-74 бывает
особой (А999), высокой (А995, А95) и технической чистоты (А85, А7Е, АО и др.).
Алюминий маркируют буквой А и цифрами, обозначающими доли процента свыше 99,0%
Al; буква «Е» обозначает повышенное содержание железа и пониженное
кремния.
А999 — алюминий особой чистоты, в котором
содержится не менее 99,999% Al;
А5 — алюминий технической чистоты в котором
99,5% алюминия. Алюминиевые сплавы разделяют на деформируемые и литейные. Те и
другие могут быть не упрочняемые и упрочняемые термической обработкой.
Деформируемые алюминиевые сплавы хорошо
обрабатываются прокаткой, ковкой, штамповкой. Их марки приведены в ГОСТ4784-74.
К деформируемым алюминиевым сплавам не упрочняемым термообработкой, относятся
сплавы системы Al-Mn и AL-Mg:Aмц; АмцС; Амг1; АМг4,5; Амг6.
Аббревиатура
включает в себя начальные буквы, входящие в состав сплава компонентов и цифры,
указывающие содержание легирующего элемента в процентах.
К деформируемым
алюминиевым сплавам, упрочняемым термической обработкой, относятся сплавы
системы Al-Cu-Mg с добавками некоторых элементов (дуралюны, ковочные сплавы), а
также высокопрочные и жаропрочные сплавы сложного хим.состава. Дуралюмины
маркируются буквой «Д» и порядковым номером, например: Д1, Д12, Д18,
АК4, АК8.
Чистый деформируемый алюминий обозначается
буквами «АД» и условным обозначением степени его чистоты: АДоч
(>=99,98% Al), АД000(>=99,80% Аl), АД0(99,5% Аl), АД1 (99,30% Al),
АД(>=98,80% Аl).
Литейные алюминиевые сплавы (ГОСТ 2685-75)
обладает хорошей жидко-текучестью, имеет сравнительно не большую усадку и
предназначены в основном для фасонного литья. Эти сплавы маркируются буквами
«АЛ» с последующим порядковым номером: АЛ2, АЛ9, АЛ13, АЛ22, АЛЗО.
Иногда маркируют по составу: АК7М2; АК21М2,
5Н2,5; АК4МЦ6. В этом случае «М» обозначает медь. «К» —
кремний, «Ц» — цинк, «Н» — никель; цифра — среднее %
содержание элемента.
Из алюминиевых антифрикционных сплавов (ГОСТ 14113-78)
изготовляют подшипники и вкладыши как литьем так и обработкой давлением.
Такие
сплавы маркируют буквой «А» и начальными буквами входящих в них
элементов: А09-2, А06-1, АН-2,5, АСМТ.
В первые два сплава входят в указанное
количество олова и меди (первая цифра-олово, вторая-медь в %), в третий
2,7-3,3% Ni и в четвертый медь сурьма и теллур.
Медь и её сплавы
Технически чистая медь обладает высокими
пластичностью и коррозийной стойкостью, малым удельным электросопротивлением и
высокой теплопроводностью. По чистоте медь подразделяют на марки (ГОСТ 859-78).
После обозначения марки указывают способ
изготовления меди: к — катодная, б — бес кислородная, р — раскисленная. Медь
огневого рафинирования не обозначается.
МООк — технически чистая катодная медь,
содержащая не менее 99,99% меди и серебра.
МЗ — технически чистая медь огневого
рафинирования, содержит не менее 99,5%меди и серебра.
Медные сплавы разделяют на бронзы и латуни.
Бронзы- это сплавы меди с оловом (4 — 33% Sn хотя бывают без оловянные бронзы),
свинцом (до 30% Pb), алюминием (5-11% AL), кремнием (4-5% Si), сурьмой и
фосфором (ГОСТ 493-79 , ГОСТ 613-79, ГОСТ 5017-74, ГОСТ 18175-78).
Латуни — сплавы меди с цинком (до 50% Zn) и
небольшими добавками алюминия, кремния, свинца, никеля, марганца (ГОСТ
15527-70, ГОСТ 17711-80). Медные сплавы предназначены для изготовления деталей
методами литья, называют литейными, а сплавы, предназначенные для изготовления
деталей пластическим деформированием — сплавами, обрабатываемыми давлением.
Медные сплавы обозначают начальными буквами их
названия (Бр или Л), после чего следуют первые буквы названий основных
элементов, образующих сплав, и цифры, указывающие кол-во элемента в процентах.
Приняты следующие обозначения компонентов сплавов:
| А — алюминий | Су — сурьма |
| Мц — марганец | К — кремний |
| С — свинец | Н — никель |
| Б — бериллий | Т — титан |
| Мг — магний | Кд — кадмий |
| Ср — серебро | О — олово |
| Ж — железо | Ф — фосфор |
| Мш — мышьяк | Х — хром |
| Ц — цинк |
- Примеры БрА9Мц2Л — бронза, содержащая 9% алюминия, 2% Mn, остальное Cu
(«Л»' указывает, что сплав литейный); - ЛЦ40Мц3Ж — латунь, содержащая 40% Zn, 3% Mn,
~l% Fe, остальное Cu; - Бр0Ф8,0-0,3 — бронза на ряду с медью
содержащая 8% олова и 0,3% фосфора; - ЛАМш77-2-0,05 — латунь содержащая 77% Cu, 2%
Al, 0,055 мышьяка, остальное Zn (в обозначении латуни, предназначенной для
обработки давлением, первое число указывает на содержание меди). - В несложных по составу латунях указывают
только содержание в сплаве меди:Л96 — латунь содержащая 96% Cu и ~4% Zn
(томпак); - Лб3 — латунь содержащая 63% Cu и -37% Zn.
- Марки меди и её применение
- 1. Практическая
часть работы - Порядок составление отчета
- 1. Записать
название работы - 2. Нарисовать
таблицу 2 - 3. Провести
расшифровку марок стали из таблицы 1, полученные результаты записать в таблицу
2 - 4. Ответить на
контрольные вопрос - Таблица
1
| 1) БСт3кп | 9) БрАЖНЮ-4-4 |
| 2) АЛ 9 | 10) БрА7Мц15ЖЗН2Ц2 |
| 3) БрОФ4-0 | 11) ЛЦ23АбЖЗМц2 |
| 4) БрСуЗНЗЦЗС20Ф | 12) БрКМцЗ-1 |
| 5) ЛЦ40МцЗА | 13) Бр06Ц6СЗ |
| 6) ЛЖМц59-1-1 | 14) ЛАНКМц75-2-2 |
| 7) ЛС59-1 | 15) АК4М4.ВТ22 |
 Л68 Л68 |
16) АК 9 |
|
17)ЛК80-3 18)ЛН65-5 |
Таблица
2
| № | Марка | Химические элементы и их содержание, применение |
| 1 | Пример ЦАМ10-5Л | содержит 9,0-12,4%Al, 4,0-5,5% Cu, 0,03-0,06% Mg, временное сопротивление не менее 250 МПа, пластичность не менее 0,4%, твердость -не менее 100HB. Из сплава изготавливают подшипники и втулки металлообрабатывающих станаков, прессов, работающих под давлением до200-10000 Па. |
| 1 | АЛ 9 | |
| 3 | ||
| 4 | ||
| 5 |
Контрольные вопросы для самостоятельной
работы
1. Опишите
основные свойства меди.
2. Какие примеси меди значительно снижают пластичность и
электропроводность?
3. Как влияет кислород, висмут, сера на структуру и свойства меди?
4. Опишите влияние цинка на свойства латуней.
5. Опишите влияние легирующих элементов на свойства бронз.
6. Какие принципы
положены в основу маркировки латуней и бронз?
7. Как по
маркировке отличить алюминиевые сплавы для литья (силумины) от сплавов для
пластического деформирования (дюралюмины)? Всегда ли это возможно?
Практическая работа «Цветные металлы: расшифровка марок цветных металлов; применение цветных металлов." — Практикум по материаловедению
- Цветные металлы:
расшифровка марок цветных металлов; - применение
цветных металлов». - Цели работы:
- — изучить цветные металлы;
- — научиться определять химический
состав цветных металлов по их маркам; - — применение цветных металлов.
- В современном машиностроении,
энергетике, радиоэлектронике и других отраслях народного хозяйства широкое
применение находят цветные металлы и сплавы на их основе. - Цветные металлы и их сплавы обладают
различными физико-химическими, механическими и технологическими свойствами,
благодаря которым они нашли широкое применение: высокой устойчивостью против
коррозии, электро- и теплопроводностью, способностью подвергаться различным
видам обработки.
Медь.
По ГОСТ
859-2001 первичная техническая медь выпускается в виде катодов, слитков,
полуфабрикатов, прутков, которые перерабатываются в круглые, квадратные,
шестигранные горячекатаные и тянутые ленты, труб, проволоки электротехнической,
фольги медной и рулонной и электролитической и медных порошков.
Медь в этой
продукции в зависимости от массовой доли примесей выпускается следующих марок:
М00А, М00БК, М0А, М0, МБ, М1, М2, М2Р, М3, М3Р, М4. В маркировке первичной технической меди приняты
следующие обозначения: М – медь; цифры от 00 до 4 – массовая доля естественных
примесей от 0,01 до 1,00 %; Б – бескислородная, Р – раскисленная, А – анодная,
К – катодная.
Латуни.
Сплавы меди с цинком называются латунями.
- По сравнению с медью латунь обладает
более высокой прочностью, твердостью, упругостью, коррозионной стойкостью,
меньшей пластичностью и высокими технологическими свойствами (литейными
свойствами, деформируемостью и обрабатываемостью резанием). - По ГОСТ 15527-70 латунь выпускается в
виде проволоки, лент, полос, полос, труб, тянутых и прессованных изделий в
отожженном и нагартованном состоянии. - Простые латуни состоят из меди и
цинка.
Марки простых латуней: Л96, Л90,
Л85, Л80, Л70, Л68, Л63, Л60. Латуни маркируются буквой Л – латунь, после
которой стоят цифры, указывающие содержание в ней меди в процентах. Например,
Л63 означает, что латунь состоит из 63% меди и 37% цинка.
Сложные латуни состоят из меди,
цинка, алюминия, железа, марганца, никеля, олова, свинца и других химических
элементов.
По ГОСТ 15527-70 выпускаются следующие марки сложных латуней:
ЛА77-2, ЛАЖ60-1-1, ЛАМш59-3-2, ЛАНКМц75-2-2,5-0,5-0,5, ЛЖМц59-1-1, ЛЖС58-1-1,
ЛН65-5, ЛЖц58-2, ЛМцА57-1-1, ЛО90-1, ЛО70-1, ЛО62-1, ЛО60-1, ЛС63-3, ЛС74-3, ЛС74-3,
ЛС64-3, ЛС60-1, ЛС59-1, ЛС59-3, ЛС74-3, ЛМш68-0,05.
Сложные латуни маркируются буквой Л
– латунь, после которой следуют буквы, обозначающие легирующие элементы: А –
алюминий, Ж – железо, Мц – марганец, К – кремний, С – свинец, О – олово, Мш –
мышьяк, Н – никель.
Первые цифры, стоящие за буквами, обозначают массовую долю
меди в процентах, последующие цифры – массовую долю компонентов в процентах в
той последовательности, в какой они приведены в буквенной части условного
обозначения. Количество цинка определяется по разности.
Например, латунь марки ЛС60-1
имеет следующее содержание компонентов: 60% меди, 1% свинца, 39% цинка.
Приведенные марки сложных латуней
обрабатываются давлением. Кроме того, выпускается большая группа литейных
латуней в виде чушек (ГОСТ 1020-77) следующих марок: ЛС, ЛСД, ЛС1, ЛОС, ЛК,
ЛК1, ЛК2, ЛКС, ЛМцС, ЛМцЖ, ЛЖ, ЛАЖМц.
Бронзы.
Бронзами называются сплавы меди с оловом и другими химическими элементами. По
способу переработки различают литейные и деформируемые бронзы, по химическому
составу – оловянистые и безоловянистые.
Оловянистые бронзы (ГОСТ 613-79)
выпускаются в виде чушек следующих марок: БрО3Ц12С5, БрО3ЦТС5Н1, БрО4Ц4С17, БрО5Ц5С5,
БрО5С25, БрО6Ц6С3, БрО8Ц4, БрО10Ф01, БрО10Ц2, БрО10С10, БрО4Ц7С5.
Безоловянистые бронзы (ГОСТ493-79)
выпускаются в виде чушек для последующего литья следующих марок: БрА9Мц2Л,
БрА10Мц2Л, БрА9ЖЗЛ, БрА10Ж3Мц2, БрА10Ж4Н4Л, БрА11Ж6Н6, БрА9Ж4Н4Мц1, БрС30,
БрА71Мц15Ж3Н2Ц2, БрСу3НЦ3С20Ф.
Маркируют бронзы буквами Бр –
бронза, за которыми следуют буквы, обозначающие легирующие элементы, введенные
в бронзу: А – алюминий, Ж – железо, Н – никель, С – свинец, Су – сурьма, Ц –
цинк, Ф – фосфор, и далее цифры, показывающие содержание этих элементов в
процентах. Количество меди определяется по разности.
Алюминий.
По ГОСТ 11069-2001 в зависимости от химической чистоты выпускается первичный
алюминий трех групп: особой чистоты (А999), высокой чистоты (А995, А99, А97,
А95), технической чистоты (А85, А8, А7, А7Е, А6, А5, А5Е, АО).
В маркировке
первичного алюминия цифры соответствуют массовой доле чистого алюминия.
Например, марка алюминия А999 означает, что массовая доля чистого алюминия
составляет 99,999%, примесей не более 0,001%.
- По ГОСТ 2685-75 литейные алюминиевые
сплавы выпускаются следующих групп и марок: - — сплавы на основе системы алюминий
– кремний — АЛ2, АЛ4, АЛ4-1, АЛ-9,
АЛ9-1, АЛ-34, АК9, АК7; - — сплавы на основе системы алюминий
– кремний – медь – АЛ3, АЛ5, АЛ5-1, АЛ6, АЛ32 и др.; - — сплавы на основе системы алюминий
– медь – АЛ7, АЛ19, АЛ33; - — сплавы на основе системы алюминий
– магний – АЛ8, АЛ13, АЛ22, АЛ23, АЛ23-1, АЛ27, АЛ27-1, АЛ28; - — сплавы на основе системы алюминий
и прочие компоненты – АЛ1, АЛ11, АЛ21, АЛ24, АЛ25, АЛ30 и др.
Литейные алюминиевые сплавы идут на
изготовление фасонных отливок, работающих при различных нагрузках: корпусов
приборов, кронштейнов, блоков цилиндров, головок цилиндров, поршней и т.д.
Разновидностью деформируемых
алюминиевых сплавов являются силумины, которые иногда также применяются в
качестве литейных сплавов.
Сплавы в чушках используются для подшихтовки при
выплавке деформируемых сплавов, сплавы в слитках – для обработки давлением и в
виде готовых изделий, полученных обработкой давлением в горячем и холодном
состоянии: прутки, фасонные профили, трубы, листы, ленты, полосы, поковки,
штамповки и проволока.
Деформируемые алюминиевые сплавы,
неупрочняемые термической обработкой (ММ, М, ДМН, АМ4С, АМг1, АМг2, АМг3, АМг4,
АМг4,5, АМгВС, АМг5, АМг6), — это группы сплавов системы алюминий – марганец и
сплавы системы алюминий – магний, так называемые сплавы АМг.
Дюралюминий (Д1, Д16, В65, Д18, В95
и др.) – это наиболее распространенный представитель деформируемых алюминиевых
сплавов, упрочняемых термической обработкой.
Алюминиевые сплавы для поковок и
штамповок (АК4, АК4-1, АК5, АК6, АК8) обладают высокой прочностью, твердостью,
а также пластичностью в горячем состоянии.
Магний.
В зависимости от массовой доли примесей по ГОСТ 804-95 выпускается первичный
магний следующих марок: Мг96 (99,96% магния), Мг95 (99,95% магния), Мг90
(99,90% магния). В состав примесей входят такие химические элементы, как
железо, алюминий, марганец, кремний, никель, медь.
По ГОСТ 2856-79 выпускаются
следующие магниевые сплавы для производства фасонных отливок в виде чушек: МЛ3,
МЛ4, МЛ4пч, МЛ5, МЛ5пч, МЛ6, МЛ8, МЛ9, МЛ10, МЛ11, МЛ12, МЛ15, МЛ19 (пч –
повышенной чистоты).
Из этих сплавов получают фасонные
отливки сложной формы.
Литейные магниевые сплавы применяют
для изготовления деталей в самолетостроении и приборостроении (арматура, штурвалы, корпуса приборов и др.).
- К деформируемым магниевым сплавам
относятся сплавы на основе алюминия, цинка, марганца, циркония с различной
степенью легирования. - По ГОСТ 14957-76 выпускаются
следующие марки магниевых деформируемых сплавов: МА1, МА2, МА5, МА8, МА11,
МА13, МА14, ВМД1. - Магниевые деформируемые сплавы идут
на изготовление различных деталей в авиационной, автомобильной промышленности и
станкостроении: масло- и бензобаки, арматура топливных, гидравлических и
масляных систем, обшивка самолетов, детали грузоподъемных машин, автомобилей и
др.
Титан.
В зависимости от массовой доли примесей выпускают технический титан следующих
марок: ВТ1-00, ВТ1-0, ВТ1 (ГОСТ 19807-74).
Титановые литейные сплавы выпускают
следующих марок: ВТ1, ВТ5Л, ВТ3-1Л, ВТ1Л, ВТ21Л. Титановые литейные идут на изготовление фасонных
отливок различной формы и труб.
- Задания к практической работе.
- 1.
Определите
химический состав: - простых латуней
по маркам: Л63, Л85, Л90, Л96; - сложных латуней:
ЛАЖ60-1-1Л, ЛА77-2, ЛО70-1, ЛМцЖ52-4-1, ЛА67-2,5. - 2.
Определите
химический состав бронз по их маркам: - БрОЦСН3-7-5-1,
БрАЖ9-4, БрАЖН10-4-4Л, БрАЖМц10-3-1, БрОС8-12, БрБН1-7, БрКМц3-1. - 3. Выбрать применение цветных металлов и
сплавов
4. Преимущества
цветных металлов.
5. Задания
3,4 оформить в виде таблице.
Пахомов Ю. | Сборник практических работ по химии | Журнал «Химия» № 42/2003
9 КЛАССПродолжение. См. № 34, 35, 36, 37, 38, 39, 40, 41/2003 Практическая работа 20. СплавыЦели. Рассмотреть образцы коллекции сплавов, повторить и закрепить понятия о сплавообразовании, обсудить причины огромного значения сплавов в современной технике. Сплавы – системы, состоящие из двух или нескольких металлов или металлов и неметаллов, обладающие характерными для металлического состояния свойствами. Сплавы являются основой технического могущества страны, т. к. по некоторым свойствам значительно превосходят чистые металлы – обладают большей прочностью, коррозионной стойкостью и твердостью, лучшими литейными свойствами, магнетизмом, электросопротивлением, сверхпроводимостью и т. д. Основа сплавообразования – металлическая связь и способность металлов перестраивать свои кристаллические решетки. Распределение электронов и изменение их энергии – факторы, определяющие кристаллическое строение и все свойства металлов и сплавов. Если атомы двух металлов не взаимодействуют, то они распределяются статистически равномерно и напоминают раствор двух жидкостей, инертных к химическому взаимодействию (а). Если атомы разных металлов притягиваются сильнее однородных, то образуется упорядоченный твердый раствор (б), возникает сверхструктура. При значительном электронно-химическом различии компонентов сплавов (радиус атома, электроотрицательность, тип кристаллической решетки и др.) могут возникнуть интерметаллические соединения. (Отметим, что с С, S, О, Cl металлы образуют чисто химические соединения.) При более слабом притягивании разнородных компонентов сплава по сравнению с однородными образуются равновесные структуры-смеси (в). В каком-то зерне такого сплава больше одного компонента, а в каком-то – другого. Части сплава отличаются составом, структурой, свойствами, это – гетерогенные сплавы. Разница в размерах атомов до 8% роли не играет, но более 12% делает образование сплава невозможным. Сплавы могут быть растворами замещения (близкие радиусы атомов) или внедрения (когда радиус внедряющегося атома мал и соответствует размеру пор). Если между узлами кристаллической решетки поры малы, то образуется более сложная кристаллическая структура. Например, при образовании цементита (Fe3С) объемно-центрированная решетка железа превращается в объемно-центрированную тетрагональную. Сплавы железа – чугун
Практическая работа 21. Коррозия металлови методы защиты Цели. Повторить и закрепить сущность процессов химической и электрохимической коррозии металлов, понятие о гальваническом элементе, основные методы антикоррозионной защиты (конкретные примеры, эксперимент в лабораторных условиях). Оборудование и реактивы. Наждачная бумага (для зачистки), щипцы тигельные, тигель для расплавления гранул цинка, муфельная печь, спиртовка, спички, держатель для пробирок, штатив с пробирками, стеклянная воронка, U-образная трубка, очищенный железный гвоздь – электрод с пробкой, угольный электрод с пробкой, медный соединительный проводник, санитарная склянка; Zn (2 гранулы), Сu (тонкая проволока без изоляции), Н2SO4 ( = 10%), HCl (разб.), растворы CuSO4, NaCl, K3[Fe(CN)6] (красная кровяная соль), Fe (мелкие стружки или очищенная мелкая проволока в кусочках), стальные пластинки (2 шт.), уротропин (1/2 таблетки), фенолфталеин (спиртовой р-р). Коррозия (от лат. «corrosio») – разрушение металлов и их сплавов в результате воздействия на них окружающей среды. Виды коррозии Химическая (газовая) коррозияВзаимодействие металлов и сплавов с кислородом и другими агрессивными газами (галогенами, SO2, H2S, СО2, водяными парами, окcидами азота и др.), разрушающее действие жидких неэлектролитов и металлических расплавов, т. е. окислительно-восстановительный процесс взаимодействия металлов и сплавов с веществами окружающей среды. Например, на железе уже при t > 200 °С образуется видимая пленка окалины (FеО, Fe2О3, Fe3О4), содержащая трещины, поры и не защищающая металл от дальнейшего разрушения. Задание 1. С целью оценки экологической опасности для окружающей среды и разрушающего действия на аппаратуру, состоящую большей частью из сплавов железа, был проведен анализ состава воздуха на химическом предприятии. При повышенной температуре в воздухе обнаружены водяные пары, сера, хлор, пары соляной и серной кислот. Уравнениями реакций показать сущность химической коррозии. Задание 2. На воздухе соли Fe2+ приобретают бурую окраску. Закончить уравнения реакций на основе электронного баланса: 3FeСl2 + O2 + H2O = 2FeCl3 + Fe(OH)3, … ; 3FeSO4 + O2 + H2O = 2Fe2(SO4)3 + Fe(OH)3, … . Электрохимическая коррозияКоррозия возникает при взаимодействии металлов и сплавов с растворами электролитов, электропроводными органическими соединениями и расплавами солей. Коррозия – окислительно-восстановительный процесс, возникающий при контакте двух проводников с различной восстановительной активностью в среде электролита (взаимодействие гальванических пар). Например, что будет происходить, если во влажной нейтральной среде на алюминиевую пластину поставлены медные заклепки?
Fe2O3•nH2O – бурая ржавчина. Если рН среды меньше 7, то происходит и водородная деполяризация катода (с выделением H2). Задание 3. Какие из перечисленных ниже условий будут: 1) способствовать электрохимической коррозии; 2) препятствовать электрохимической коррозии? а) неоднородность сплава; б) чистые поверхности металла; в) влажность окружающего воздуха; г) погружение в раствор NaCl; д) наличие на поверхности металла плотной оксидной пленки; е) присутствие в воздухе SO2; ж) покрытие поверхности металла жировым слоем. |
(Ответ дать в следующей форме: 1–а и т. д.)
Основные методы защиты металлов от коррозии
| Нанесение металлических покрытий (лужение, меднение, хромирование, серебрение…) | Ингибирование (введение веществ, замедляющих коррозию металлов) | Протекторная защита (протектор – металл с большей электрохимической активностью – разрушаетсяв первую очередь) | Металлы – медь, титан, хром, никель |
| Неметаллические покрытия (смазка, крашение, лакирование, эмалирование, фосфатирование, оксидирование…) | Удаление агрессивных веществ, очистка среды, контактирующейс металлом | Kатодная защита (металлическое сооружение, подключенноек источнику тока, – катод, заземление – анод; анод разрушаетсяв первую очередь) | Сплавы железа (нержавеющая сталь), меди (латунь, олово), алюминия, титана и др. |
| Собрать прибор (по схеме). В оба колена U-образной трубки через воронку залить раствор NаСl, осторожно в левое колено добавить несколько капель красной кровяной соли (реактив на Fe2+), в правое – спиртовой раствор фенолфталеина. Закрыть отверстия трубки пробками с электродами, соединив последние медным проводником. | Объяснить происходящие изменения соответствующими схемами и уравнениями реакций. | … |
| Установку отставить в сторону и наблюдать в течение всего занятия | Kакой вид коррозии происходит в данном случае? | … |
| В две пробирки поместитьпо грануле цинка и прилить равные объемы разбавленной H2SO4. Обратить внимание на скорость реакции. В одну из пробирок добавить несколько капель раствора СuSO4, в другой – прикоснуться медной проволокой к грануле Zn. Наблюдать | Kак влияет на скорость химической реакциидобавление раствора сульфата меди(II)? Объяснить, обосновать соответствующими уравнениями реакций и схемой. K каким последствиям приводит контакт цинка с медью в среде электролита? Обосновать | … |
| Расплавить 1–2 гранулы цинка и опустить в расплав тщательно очищенную железную проволоку. Наблюдать покрытие цинком поверхности железа. Железную проволоку без цинка и с осажденным цинком поместить в 10%-й раствор Н2SO4, наблюдать не менее 10 мин | Объяснить наблюдаемые превращения. Kакое название носит подобная защита железа? | … |
| В две пробирки налить по 1,5–2 мл соляной кислоты и в одну из них внести полтаблетки уротропина. Затем в каждую пробирку внести очищенные тонкие кусочки железной (стальной) проволочки. Наблюдать | Сравнить скорость реакции в присутствии и в отсутствие уротропина, объяснить наблюдаемое. Kакова в данном случае роль уротропина? | … |
| Очистить две стальные пластинки наждачной бумагой и одну из них нагреть до появления следов «побежалости» (т.е. следов оксидной пленки). Затем нанести по капле раствора СuSO4 на оба образца. Наблюдать | По скорости появления темного пятна на образцах оценить защитные свойства оксидной пленки.Составить уравнения происходящих реакций | … |






