- Строение «электронных» оболочек атомов
- Распределение электронных зарядов по уровням
- Электронные формулы химических элементов
- Заключение
- Электронные конфигурации атомов
- Литий
- Бериллий
- Бор
- Правило Гунда
- Энергетические ячейки
- Урок 6. Простые ионы – HIMI4KA
- Ионная химическая связь
- Положительные и отрицательные ионы
- Степень окисления веществ
- Валентность химических элементов
- Название ионов
- Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов
- Запись по электронным оболочкам (схема электронного строения)
- Запись с обозначением энергетических уровней и подуровней
- Электронная конфигурация атомов 1 и 2 периодов
- Электронная конфигурация атомов 3 периода
- Электронная конфигурация атомов 4 периода
- Электронная конфигурация ионов
- Основное и возбуждённое состояния атома
- Ион
- Число электронов в ионе
- Энергия ионизации
- Энергия сродства электрону
- Катионы и анионы
- Какой заряд будет у атома?
- Пример
В химии есть очень увлекательный, но сложный раздел – электронная конфигурация атомов и ионов.
Молекулу любого из элементов таблицы Менделеева можно изучить с точки зрения как физики, так и химии.
Дивный молекулярный мир на атомном уровне отличается от привычного. Разберем подробно, как образуется электронная формула элементов.
Строение «электронных» оболочек атомов
Для лучшего понимания электронных окружающих ядро оболочек, нужно знать об ионе – частице, в основе которой, кроме электронов, присутствуют так называемые протоны.

Если число протонов больше числа электронов, то такой атом называется катионом (положительный заряд). В противном случае атом называется анионом (заряд отрицательный).
Каждый из электронов занимает свой собственный уровень относительно ядра.
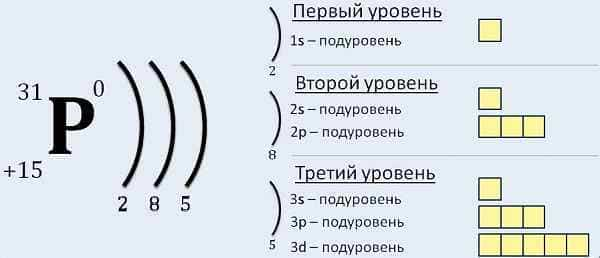
Конфигурация электронов для отдельно взятого атома может строиться в порядке атомных чисел. В качестве первоначального элемента выбирается водород, а далее продолжается добавление одного протона к ядру согласно с подсхемой и местом в периодической таблице, пока не опишутся все химические элементы.
Такая процедура называется принципом Aufbau (Ауфбау). Название принципа происходит от немецкого слова и переводится «построить».
Можно сделать вывод, что появление ионов связано с моментом, когда атомы получают или теряют заряды. Катион (положительно заряженный ион) образуется, когда один или несколько зарядов удаляются из «родительского атома».
Распределение электронных зарядов по уровням
Как уже говорилось выше, молекула любого элемента периодической таблицы – это своеобразный микрокосмос, где в разные стороны (спины) двигаются заряженные частицы (лептон). По-английски spin означает «вращение». Их полуцелые «спины» были описаны Вольфгангом Паули в 1925 году.
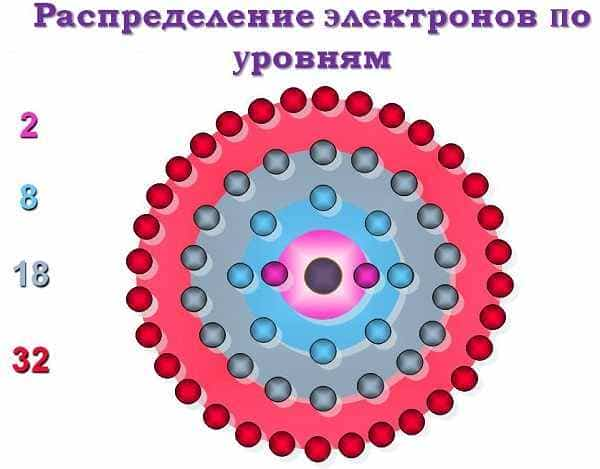
Всего принципов построения графических распределительных схем существует три:
- Принцип ограничений, который сформирован швейцарским физиком В. Паули. На одном электронном уровне ядра может быть два лептона с разным направлением вращения (если один вращается против часов стрелки, то другой по часовой). Опыты в адронном коллайдере доказали этот факт.
- Второй строительный принцип говорит, что лептоны стремятся занять уровни по мере возрастания энергетического запаса.
- Третий гласит, что любой электрон «любит» только себя и плохо переносит «соседей» по орбитали. Иными словами, сначала электроны занимают свободные клетки (в графическом исполнении формулы), а уже по второму кругу занимают свободные места.
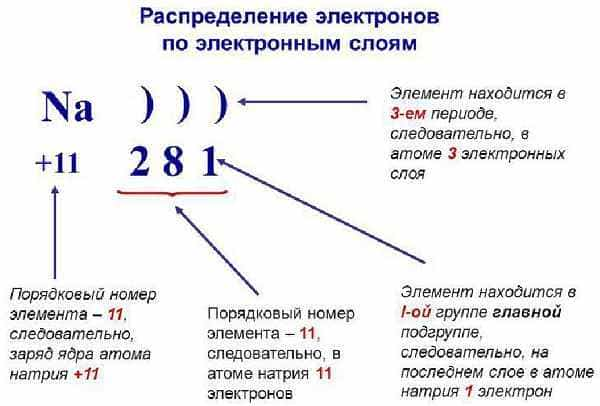
Теперь рассмотрим состав «квартир» для лептонов. В зависимости от уровня и энергии, орбитальные места можно разделить на четыре формы:
- Эс (s) имеет форму круга и способен на одном уровне вместить только два заряда ядра.
- Пи (p) готов предоставить три «места» для шести лептонов.
- Де (d) предоставляет пять «мест» – 10 заряженных частиц.
- Эф (f) самый щедрый на «места», их число равно семи – соответственно 14 парных частиц.
Электронные формулы химических элементов
Здесь приводится таблица-подсказка для некоторых химических элементов.
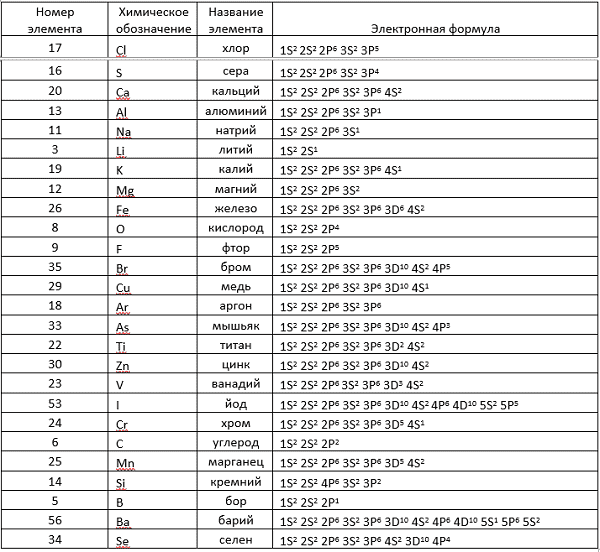
Теперь, руководствуясь данными таблицы, разберем электронные записи элементов на примере «аргона» (Ar).
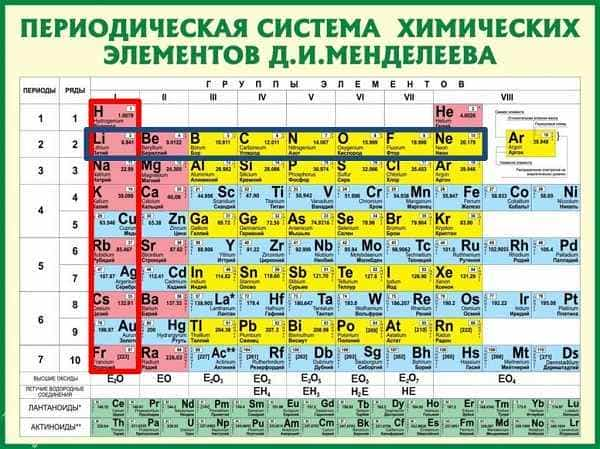
В таблице Менделеева его номер восемнадцать. Руководствуясь описанным выше, высчитываем количество частиц (всего их 18).

Ещё до построения электронно-графической формулы Аргона, вспомним, как формируются орбитали и строятся ячейки:
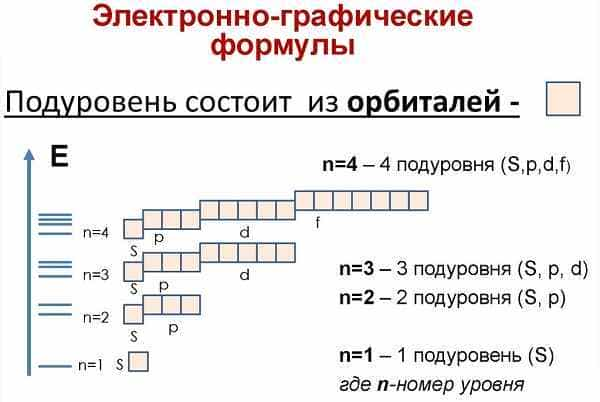
Начинаем распределять электроны Ar:
- a) поскольку аргон находится в третьем периоде, то у него три подуровня. Смотрим в учебник химии и находим, что это p-элемент,
- b) запишем формулу: 1 s, 2 s, 2 p, 3 s, 3 p,
- c) теперь рисуем орбитальные ячейки и заполняем их.
- Графическое изображение формулы аргона
- Важно знать: непарные заряды во внешних орбиталях, называемые валентными зарядами, отвечают за большинство химических и физических проявлений элементов.
Заключение
Чтобы немного отстранится от научных теорий, стоит пофантазировать. Представьте атомное ядро и окружающие его заряды вселенной. Ядро – это солнце, а заряды планеты. Формула наглядно описывает положение подобных «планет» в космосе (атомного вещества). Чтобы перейти с одного уровня на другой, потребуется большая энергия.
В квантовой физике некоторые специалисты выдвинули теорию о том, что при вмешательстве в структуру атома можно сделать объект невидимым. Ведь если подумать, то фотон (мельчайшая частица света) может не вступать в связь с электронами атома и, не встречая сопротивления, преодолевать объект.
Впечатляет? Химическая формула элемента очень важна для физики. Благодаря труду Менделееву и его таблице, нам стали доступны современные технологии. Химические формулы и эксперименты скучны и сложны, хочется верить, что эта статья сделала их более понятными.
Электронные конфигурации атомов
Заполнение орбиталей в не возбужденном атоме осуществляется таким образом, чтобы энергия атома была минимальной (принцип минимума энергии). Сначала заполняются орбитали первого энергетического уровня, затем второго, причем сначала заполняется орбиталь s-подуровня и лишь затем орбитали p-подуровня.
В 1925 г. швейцарский физик В. Паули установил фундаментальный квантово-механический принцип естествознания (принцип Паули, называемый также принципом запрета или принципом исключения).
В соответствии с принципом Паули:
в атоме не может быть двух электронов, имеющих одинаковый набор всех четырех квантовых чисел.
Электронную конфигурацию атома передают формулой, в которой указывают заполненные орбитали комбинацией цифры, равной главному квантовому числу, и буквы, соответствующей орбитальному квантовому числу. Верхним индексом указывают число электронов на Данных орбиталях.
Электронная конфигурация атома водорода 1s1, а гелия 1s2. Атом водорода имеет один неспаренный электрон, а атом гелия — два спаренных электрона. Спаренные электроны имеют одинаковые значения всех квантовых чисел, кроме спинового. Атом водорода может отдать свой электрон и превратиться в положительно заряженный ион — катион Н+ (протон), не имеющий электронов (электронная конфигурация 1s0). Атом водорода может присоединить один электрон и превратиться в отрицательно заряженный ион Н- (гидрид-ион) с электронной конфигурацией 1s2.
Литий
Три электрона в атоме лития распределяются следующим образом: 1s21s1. В образовании химической связи участвуют электроны только внешнего энергетического уровня, называемые валентными.
У атома лития валентным является электрон 2s-подуровня, а два электрона 1s-подуровня — внутренние электроны. Атом лития достаточно легко теряет свой валентный электрон, переходя в ион Li+, имеющий конфигурацию 1s22s0.
Обратите внимание, что гидрид-ион, атом гелия и катион лития имеют одинаковое число электронов. Такие частицы называются изоэлектронными. Они имеют сходную электронную конфигурацию, но разный заряд ядра.
Атом гелия весьма инертен в химическом отношении, что связано с особой устойчивостью электронной конфигурации 1s2. Незаполненные электронами орбитали называют вакантными. В атоме лития три орбитали 2p-подуровня вакантные.
Бериллий
Электронная конфигурация атома бериллия — 1s22s2. При возбуждении атома электроны с более низкого энергетического подуровня переходят на вакантные орбитали более высокого энергетического подуровня. Процесс возбуждения атома бериллия можно передать следующей схемой:
1s22s2 (основное состояние) + hν → 1s22s12p1 (возбужденное состояние).
Сравнение основного и возбужденного состояний атома бериллия показывает, что они различаются числом неспаренных электронов. В основном состоянии атома бериллия неспаренных электронов нет, в возбужденном их два.
Несмотря на то что при возбуждении атома в принципе любые электроны с более низких по энергии орбиталей могут переходить на более высокие орбитали, для рассмотрения химических процессов существенными являются только переходы между энергетическими подуровнями с близкой энергией. Это объясняется следующим. При образовании химической связи всегда выделяется энергия, т. е.
совокупность двух атомов переходит в энергетически более выгодное состояние. Процесс возбуждения требует затрат энергии. При распаривании электронов в пределах одного энергетического уровня затраты на возбуждение компенсируются за счет образования химической связи.
При распаривании электронов в пределах разных уровней затраты на возбуждение столь велики, что не могут быть компенсированы образованием химической связи. В отсутствие партнера по возможной химической реакции возбужденный атом выделяет квант энергии и возвращается в основное состояние — такой процесс называется релаксацией.
Бор
Пять электронов в атоме бора распределяются по орбиталям следующим образом: 1s22s22p1. Как следует из приведенной электронной конфигурации, атом бора имеет в основном состоянии один неспаренный электрон (на p-подуровне).
При возбуждении один из электронов с 2s-подуровня переходит на вакантную орбиталь 2p-подуровня, в результате чего в атоме появляются три неспаренных электрона.
Бор — пример электронодефицитного атома: число электронов в нем меньше числа орбиталей заполняемого энергетического подуровня.
Правило Гунда
Заполнение в невозбужденных атомах p, d- и f-подуровней осуществляется таким образом, чтобы мультиплетность атома была максимальной (правило Гунда).
Мультиплетность определяется числом неспаренных электронов: если такие электроны отсутствуют, то считают, что мультиплетность равна 1, и такое состояние атома называют синглетным; если имеется 1 неспаренный электрон, то мультиплетность равна 2 — дублетное состояние.
Триплетному состоянию (мультиплетность равна 3) соответствует наличие двух неспаренных электронов. Правило Гунда используют для определения электронных конфигураций некоторых атомов, начиная с атома углерода.
Энергетические ячейки
Электронную конфигурацию атомов часто представляют в форме энергетических ячеек. В этом случае чертой (или квадратом) обозначают каждую орбиталь. Чаще всего так обозначают только те орбитали, на которых находятся или могут находиться валентные электроны.
Электроны обозначают с помощью стрелок, направленных вверх (s = +½) или вниз (s = -½)- Неспаренный электрон и спаренные электроны изображают так:
Без учета правила Гунда для основного состояния атома углерода можно предложить два варианта электронной конфигурации, отвечающих и принципу минимума энергии, и принципу Паули:
В соответствии с правилом Гунда основному состоянию атома углерода отвечает триплет. Таким образом, спаривание электронов возникает только после того, как на каждой орбитали данного подуровня уже находится по одному электрону.
При возбуждении атома углерода электрон с 2s-подуровня переходит на 2p-подуровень:
Атом фтора имеет электронную конфигурацию [He]2s22p5. Имея только один неспаренный электрон, фтор может быть только одновалентным. Атом фтора легко присоединяет один электрон, превращаясь во фторид-ион с конфигурацией [He]2s22p6. Такую электронную конфигурацию имеет атом неона — благородного газа. Восьмиэлектронная оболочка 2s22p6 отвечает очень устойчивому состоянию. До настоящего времени не получено ни одного соединения неона.
Электронные конфигурации атомов элементов 3-го периода Периодической системы элементов будут в определенной степени аналогичны приведенным выше (нижним индексом указан атомный номер):
11Na [Ne]3s1
12Mg [Ne]3s2
13Al [Ne]3s23p1
14Si [Ne]2s22p2
15P [Ne]2s23p3
Однако аналогия не является полной, так как третий энергетический уровень расщепляется на три подуровня и у всех перечисленных элементов имеются вакантные d-орбитали, на которые могут при возбуждении переходить электроны, увеличивая мультиплетность. Особо это важно для таких элементов, как фосфор, сера и хлор.
Максимальное число неспаренных электронов в атоме фосфора может достигать пяти:
Этим объясняется возможность существования соединений, в которых валентность фосфора равна 5. Атом азота, имеющий конфигурацию валентных электронов в основном состоянии такую же, как и атом фосфора, образовать пять ковалентных связей не может.
Аналогичная ситуация возникает при сравнении валентных возможностей кислорода и серы, фтора и хлора. Распаривание электронов в атоме серы приводит к появлению шести неспаренных электронов:
[Ne]3s23p4 (основное состояние) → [Ne]3s13p33d2 (возбужденное состояние).
Это отвечает шести валентному состоянию, которое для кислорода недостижимо. Максимальная валентность азота (4) и кислорода (3) требует более детального объяснения, которое будет приведено позднее.
Максимальная валентность хлора равна 7, что соответствует конфигурации возбужденного состояния атома [Ne]3s13p3d3.
Наличие вакантных Зd-орбиталей у всех элементов третьего периода объясняется тем, что, начиная с 3-го энергетического уровня, происходит частичное перекрывание подуровней разных уровней при заполнении электронами.
Так, 3d-подуровень начинает заполняться только после того, как будет заполнен 4s-подуровень.
Запас энергии электронов на атомных орбиталях разных подуровней и, следовательно, порядок их заполнения, возрастает в следующем порядке:
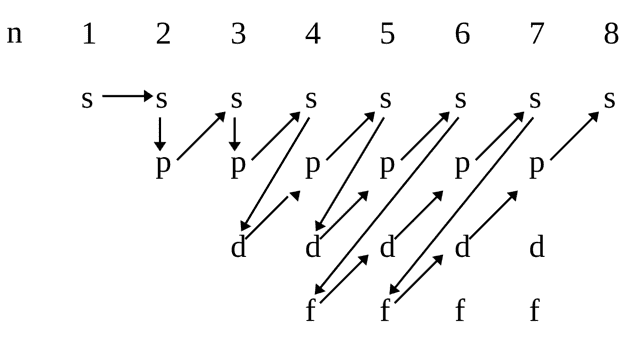
Раньше заполняются орбитали, для которых сумма первых двух квантовых чисел (n + l) меньше; при равенстве этих сумм сначала заполняются орбитали с меньшим главным квантовым числом.
Эту закономерность сформулировал В. М. Клечковский в 1951 г.
Элементы, в атомах которых происходит заполнение электронами s-подуровня, называются s-элементами. К ним относятся по два первых элемента каждого периода: водород, гелий, все элементы IА (щелочные металлы) и IIА (бериллий, магний и щелочноземельные металлы) групп.
Элементы, в атомах которых происходит заполнение электронами p-подуровня, называются p-элементами. К ним относятся в каждом периоде (кроме первого) по шесть последних элементов, образующих группы IIIА — VIIIА.
Первый d-элемент — скандий — имеет электронную конфигурацию [Ar]4s23d1.
Электронные конфигурации следующих двух d-элементов не выходят за рамки общих представлений о строении электронных оболочек: 22Ti [Ar]4s23d2 и 23V[Ar]4s23d3.
Максимальная валентность титана, равная 4, объясняется переходом в возбужденное состояние за счет распаривания электронов: [Ar]4s23d2 → [Ar]4s13d3. Аналогично для ванадия: [Ar]4s23d3 → [Ar]4s13d4 (максимальная валентность 5).
Однако уже у следующего d-элемента — хрома — наблюдается некоторое «отклонение» в расположении электронов по энергетическим уровням в основном состоянии: вместо ожидаемых четырех неспаренных электронов на 3d-подуровне в атоме хрома имеются пять неспаренных электронов на 3d-подуровне и один неспаренный электрон на s-подуровне: 24Cr [Ar]4s13d5.
Явление перехода одного s-электрона на d-подуровень часто называют «проскоком» электрона. Это можно объяснить тем, что орбитали заполняемого электронами d-подуровня становятся ближе к ядру вследствие усиления электростатического притяжения между электронами и ядром.
Вследствие этого состояние [Ar]4s13d5 становится энергетически более выгодным, чем [Ar]4s23d4. Таким образом, наполовину заполненный d-подуровень (d5) обладает повышенной стабильностью по сравнению с иными возможными вариантами распределения электронов.
Электронная конфигурация, отвечающая существованию максимально возможного числа распаренных электронов, достижимая у предшествующих d-элементов только в результате возбуждения, характерна для основного состояния атома хрома. Электронная конфигурация d5 характерна и для атома марганца: [Ar] 4s23d5.
У следующих d-элементов происходит заполнение каждой энергетической ячейки d-подуровня вторым электроном: 26Fe [Ar]4s23d6; 27Co [Ar]4s23d7; 28Ni [Ar]4s23d8.
У атома меди достижимым становится состояние полностью заполненного d-подуровня (d10) за счет перехода одного электрона с 4s-под-уровня на 3d-подуровень: 29Cu [Ar]4s13d10. Последний элемент первого ряда d-элементов имеет электронную конфигурацию 30Zn [Ar]4s23d10.
Общая тенденция, проявляющаяся в устойчивости d5 и d10 конфигурации, наблюдается и у элементов ниже лежащих периодов.
Молибден имеет электронную конфигурацию, аналогичную хрому: 42Mo [Kr]5s14d5, а серебро — меди: 47Ag[Kr]5s0d10.
Более того, конфигурация d10 достигается уже у палладия за счет перехода обоих электронов с 5s-орбитали на 4d-орбиталь: 46Pd [Kr]5s0d10. Существуют и другие отклонения от монотонного заполнения d-, а также f-орбиталей.
Урок 6. Простые ионы – HIMI4KA
Архив уроков › Основные законы химии
В уроке 6 «Простые ионы» из курса «Химия для чайников» познакомимся с простыми ионами и выясним, чему равен его заряд; также рассмотрим как образуется ионная химическая связь; научимся определять степень окисления и валентность элементов. Данный урок очень важный, и чтобы его лучше понять, обязательно просмотрите прошлые уроки, особое внимание уделяя уроку 1 «Схема строения атомов», а также уроку 3 «Схема образования молекул».
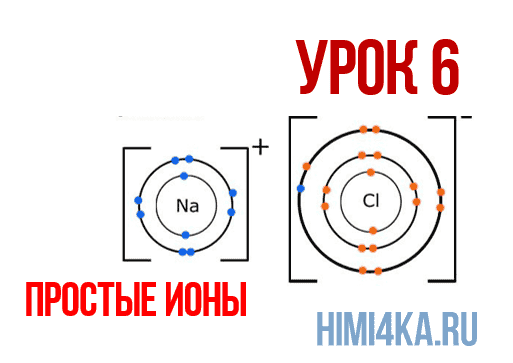
Ионная химическая связь
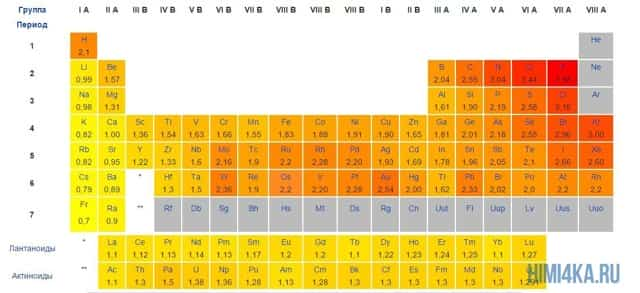
Мы уже кратко рассматривали ковалентную полярную химическую связь, в которой из-за незначительного различия в электроотрицательности атомов (0.4-2.0) электронная пара распределяется между ними не равномерно. Для тех, кто забыл, напоминаю, что электроотрицательность — это способность атомов притягивать к себе электроны.
Однако, если электроотрицательность атомов различается больше чем на 2 по таблице электроотрицательности, то электронная пара полностью переходит к более электроотрицательному атому, и в результате образуется ионная химическая связь. Ионная химическая связь образуется только между атомами типичных металлов (т.к. они легко теряют внешние электроны) и неметаллов (т.к. они обладают большой электроотрицательностью).
Положительные и отрицательные ионы
Наглядным примером ионной химической связи может служить обычная поваренная соль NaCl, которая присутствует на каждой кухне. Атомы натрия (и вообще всех металлов) слабо удерживают внешние электроны, тогда как атомы хлора напротив, обладают очень большой способностью притягивать к себе электроны, т.е обладают большой электроотрицательностью.
Поэтому при образовании молекулы NaCl каждый атом Na теряет один электрон (e—), образуя положительный ион натрия Na+, а каждый атом Cl, наоборот, приобретает этот потерянный электрон натрия, образуя отрицательный ион хлора Cl—. Это записывается в виде двух реакций:
- Na → Na+ + e— и ½Cl2 + e— → Cl—
Записать ½Cl2 пришлось потому, что газообразный хлор в природе состоит из двухатомных молекул, а не из свободных одиночных атомов хлора.
На рисунке выше, изображена кристаллическая решетка NaCl, где каждый хлорид-ион Cl— окружен со всех сторон соседними положительными ионами натрия Na+; ионы натрия Na+ точно также окружены ближайшими хлорид-ионами Cl—. Подобное расположение ионов обладает высокой устойчивостью.
Положительно заряженные ионы называются катионами. К ним в основном относятся металлы, так как они легко отдают от одного до трех электронов. Ниже приведены примеры катионов:
Анионами являются неметаллы, поскольку с радостью присоединяют к себе электроны, превращаясь в отрицательно заряженные ионы. Примеры анионов:
Степень окисления веществ
Заряд простого, одноатомного иона, например Mg2+ или F2-, называется его степенью окисления. Степень окисления — это такое число электронов, которое необходимо прибавить (восстановить) к иону или отнять (окислить) у него, чтобы он превратился обратно в нейтральный атом.
- Реакция восстановления: Mg2+ + 2e— → Mg
- Реакция окисления: F2- → F + 2e—
Процесс присоединения электронов к атому или просто их смещение в сторону данного атома называется реакцией восстановления, а оттягивание электронов от атома или их полное удаление называется реакцией окисления. Вот вам отличная шпаргалка со степенями окисления простых ионов:
Пример 12. Окисляется или восстанавливается хлор при образовании хлорид-иона? Какова степень окисления этого иона? Решение: Хлор восстанавливается, поскольку к каждому атому хлора необходимо присоединить один электрон, чтобы образовался хлорид-ион. Хлорид-ион, Сl—, имеет степень окисления -1.
Пример 13. Окисляются или восстанавливаются металлы при образовании ими ионов? Какова степень окисления иона алюминия? Решение: При образовании ионов металлов последние окисляются, поскольку при этом происходит удаление электронов от атомов металла. Ион алюминия, Аl3+, имеет степень окисления +3.
Валентность химических элементов
Валентностью называют число химических связей, которые данный атом образует с другими атомами в молекуле. Однако, если говорить простыми словами, то под валентностью понимается все та же степень окисления, но в отличии от нее валентность не имеет знака и не равна нулю.
| Молекулярная формула | Валентность | Степень окисления |
| H2O | H(I), O(II) | H+1, O-2 |
| CS2 | C(IV), S(II) | C+4, S-2 |
| CH4 | C(IV), H(I) | C-4, H+1 |
Название ионов
Ионы металлов, которые имеют различные (переменные) степени окисления, записываются следующим образом:
- Fe2+ железо(II) или ион двухвалентного железа
- Fe3+ железо(III) или ион трехвалентного железа
- Сu+ медь(I) или ион одновалентной меди
- Cu2+ медь (II) или ион двухвалентной меди
- Sn2+ олово(II) или двухвалентного олова
- Sn4+ олово(IV) или ион четырехвалентного олова
Пример 2: Окисление или восстановление происходит при превращении иона трехвалентного железа в ион двухвалентного? Запишите уравнение этого процесса.
Решение: Уравнение реакции имеет следующий вид: Fe3+ + e— → Fe2+. Она представляет собой процесс восстановления, поскольку к исходному иону присоединяется электрон.
Надеюсь урок 6 «Простые ионы» оказался для вас понятным и полезным. Если у вас возникли вопросы, пишите их в комментарии.
Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов
Записать распределение электронов по энергетическим уровням можно несколькими способами.
Запись по электронным оболочкам (схема электронного строения)
Показывает заряд ядра и количество электронов на каждом энергетическом уровне.
Легче всего начинать с неё, потому что она показывает структуру атома «крупным планом».
Запись с обозначением энергетических уровней и подуровней
Каждая орбиталь обозначается квадратной ячейкой. Электрон обозначается стрелкой. Различное направление стрелок указывает на противоположные спины.Под ячейкой подписывают номер энергетического уровня, буквенное обозначение орбитали и количество электронов на ней.
Буквенно-числовое обозначение такого «адреса» электрона – это электронная формула. Электронная конфигурация – это электронная формула, которая показывает распределение электронов по энергетическим уровням.
Электронная конфигурация атомов 1 и 2 периодов
Электронная конфигурация атомов 3 периода
Строение электронных оболочек атомов элементов третьего периода
Электронная конфигурация атомов 4 периода
Заполнение орбиталей атомов 4 периода имеет свои особенности.
На движение электрона влияют поле ядра и поле других электронов. Поэтому в атомах с большим количеством электронов энергия электрона определяется главным и орбитальным квантовыми числами.
Здесь уже надо смотреть на сумму обоих квантовых чисел (n+l). Если для двух подуровней эта сумма равна: 3d, 4p, 5s (n+l=5), то сначала заполняются уровни с меньшими значениями n. То есть последовательность заполнения будет следующей: 3d – 4p – 5s.
Поэтому в 4 периоде сначала заполняется подуровень 4s, а потом подуровень 3d.
Есть ещё одна особенность, которая появляется в 4 периоде. Хром и медь имеют на 4s-орбитали по одному электрону. Всё дело в заполнении d-оболочек. Полузаполненные или заполненные d-оболочки устойчивее частично заполненных. В атоме хрома на каждой из 5 3d-орбиталей есть по одному электрону. В атоме меди на каждой на каждой 3d-орбитали есть по два электрона.
Алгоритм записи электронной конфигурации атома
- По порядковому номеру химического элемента в таблице Менделеева определяем количество электронов в атоме.
- Распределяем электроны по энергетическим уровням, то есть составляем схему электронного строения.
- Выписываем s-, p-, d-подуровни в каждом энергетическом уровне.
- Заполняем подуровни электронами: сначала по одному электрону на орбиталь, потом достраиваем электронные пары.
Электронная конфигурация ионов
Электронная конфигурация ионов составляется по тем же принципам. Нужно учитывать изменения количества электронов на внешнем энергетическом уровне.
Атом электронейтрален, то есть сколько протонов ядре, столько же электронов в атоме. Если атом принимает электроны, он становится отрицательно заряженным ионом (анионом), если отдаёт электроны – положительно заряженным ионом (катионом).
Атому легче всего отдать электроны внешнего энергетического уровня, «чужие» электроны он тоже примет на внешний энергетический уровень. На внешнем энергетическом уровне не может находиться более 8 электронов. Теория «октета» была предложена в 1916 году Гилбертом Ньютоном Льюисом и Вальтером Косселем
Атом «стремится» добрать электроны на внешний уровень или избавиться от них, поэтому и становится ионом. Полное заполнение s- и p-подуровней внешнего уровня придаёт атому стабильность. Только атом гелия имеет на единственном внешнем энергетическом уровне 2 электрона, а не 8, потому что первый энергетический уровень состоит только из одной s-орбитали.
Количество электронов на внешнем энергетическом уровне определяется по таблице Менделеева. У элементов главных подгрупп номер группы – это и есть количество электронов на внешнем уровне. У элементов побочных подгрупп количество электронов на внешнем уровне не больше двух.
Основное и возбуждённое состояния атома
На первый взгляд кажется, что атом хлора может образовывать только одну связь и соединения одного типа – например, хлориды. Но откуда берутся хлорная, хлорноватая, хлористая и хлорноватистая кислоты?
Дело в том, что атом можно перевести из основного состояния в возбуждённое.
Основное состояние – это состояние атома с наименьшей энергией. Атом обладает наименьшей энергией в основном состоянии. Но если ему передать дополнительную энергию, он перейдёт в возбуждённое состояние. Электроны перейдут на уровень или подуровень с большей энергией.
Сначала разрываются электронные пары на 3p-подуровне, электроны переходят на 3d-подуровень. Если атом хлора получит ещё больше энергии, спаренный электрон покинет даже 3s-орбиталь и перейдёт на 3d-подуровень.
Благодаря этому атом хлора может образовывать больше химических связей. Затраты энергии, потраченные на распаривание электронов, окупаются при образовании новых химических связей.
Но в возбуждённое состояние могут перейти атомы, у которых есть неспаренные электроны и свободные орбитали. Длится возбуждённое состояние недолго: атом отдаст энергию и вернётся в основное состояние. Хотя если сообщить атому слишком много энергии, электрон покинет его и атом станет ионом.
Смотри также:
Ион
Ион — это заряженная частица, образованная из молекулы или атома путём потери или приобретения одного электрона. Отсюда следует, что в ионе количество протонов не равно количеству электронов. После изучения статьи Вы узнаете, какими бывают заряженные частицы, что такое ионы, катионы и анионы, также Вы сможете по номеру элемента узнать, каким зарядом он может обладать.
Число электронов в ионе
Количество электронов в нейтральном атоме равно количеству протонов в ядре, например, у хрома (24Cr) 24 протона, соответствено, вокруг ядра вращается 24 электрона. Как было рассказано в статье «электронная конфигурация атома», каждый электрон двигается по некой орбитали, то есть обладает заданным количеством энергии.
Если ион образован из-за потери электрона, то заряд иона становится положительным (электрон имеет отрицательный заряд), схема для запоминания:
24Cr — e- = 24Cr + e+ = 24Cr+ 24Cr — 3e- = 24Cr + 3e+ = 24Cr3+
Аналогично при присоединении электрона:
24Cr + e- = 24Cr — e+ = 24Cr- 24Cr + 3e- = 24Cr — 3e+ = 24Cr3-
Энергия ионизации
Если электрону сообщить достаточное количество энергии, то электрон «оторвётся» от атома. Чем ближе электрон к ядру — тем сложнее его отрывать, а значит, больше энергии необходимо передать. Энергия, необходимая для отрыва электрона, называется энергией ионизации или ионизационный потенциал (I). Значения I затабулированы и могут быть найдены в различных справочниках.
| 1 | H | Водород | 1312 |
| 2 | He | Гелий | 2373 |
| 3 | Li | Литий | 520 |
| 4 | Be | Бериллий | 899.5 |
| 5 | B | Бор | 801 |
| 6 | C | Углерод | 1086 |
| 7 | N | Азот | 1402 |
| 8 | O | Кислород | 1314 |
| 9 | F | Фтор | 1681 |
| 10 | Ne | Неон | 2080.7 |
| 11 | Na | Натрий | 495 |
| 12 | Mg | Магний | 738 |
| 13 | Al | Алюминий | 578 |
| 14 | Si | Кремний | 787 |
| 15 | P | Фосфор | 1012 |
| 16 | S | Сера | 1000 |
| 17 | Cl | Хлор | 1251 |
| 18 | Ar | Аргон | 1520.6 |
| 19 | K | Калий | 418.8 |
| 20 | Ca | Кальций | 590 |
| 21 | Sc | Скандий | 633.1 |
| 22 | Ti | Титан | 658.8 |
| 23 | V | Ванадий | 650.9 |
| 24 | Cr | Хром | 652.9 |
| 25 | Mn | Марганец | 717.3 |
| 26 | Fe | Железо | 762.5 |
| 27 | Co | Кобальт | 760.4 |
| 28 | Ni | Никель | 737.1 |
| 29 | Cu | Медь | 745.5 |
| 30 | Zn | Цинк | 906.4 |
| 31 | Ga | Галлий | 578.8 |
| 32 | Ge | Германий | 762 |
| 33 | As | Мышьяк | 947 |
| 34 | Se | Селен | 941 |
| 35 | Br | Бром | 1142 |
| 36 | Kr | Криптон | 1350.8 |
| 37 | Rb | Рубидий | 403 |
| 38 | Sr | Стронций | 549 |
| 39 | Y | Иттрий | 600 |
| 40 | Zr | Цирконий | 640.1 |
| 41 | Nb | Ниобий | 652.1 |
| 42 | Mo | Молибден | 684.3 |
| 43 | Tc | Технеций | 702 |
| 44 | Ru | Рутений | 710.2 |
| 45 | Rh | Родий | 719.7 |
| 46 | Pd | Палладий | 804.4 |
| 47 | Ag | Серебро | 731 |
| 48 | Cd | Кадмий | 867.8 |
| 49 | In | Индий | 558.3 |
| 50 | Sn | Олово | 709 |
| 51 | Sb | Сурьма | 834 |
| 52 | Te | Теллур | 869 |
| 53 | I | Иод | 1008 |
| 54 | Xe | Ксенон | 1170.4 |
| 55 | Cs | Цезий | 375.7 |
| 56 | Ba | Барий | 503 |
| 57 | La | Лантан | 538.1 |
| 58 | Ce | Церий | 534.4 |
| 59 | Pr | Празеодим | 527 |
| 60 | Nd | Неодим | 533.1 |
| 61 | Pm | Прометий | 540 |
| 62 | Sm | Самарий | 544.5 |
| 63 | Eu | Европий | 547.1 |
| 64 | Gd | Гадолиний | 593.4 |
| 65 | Tb | Тербий | 565.8 |
| 66 | Dy | Диспрозий | 573 |
| 67 | Ho | Гольмий | 581 |
| 68 | Er | Эрбий | 589.3 |
| 69 | Tm | Тулий | 596.7 |
| 70 | Yb | Иттербий | 603.4 |
| 71 | Lu | Лютеций | 523.5 |
| 72 | Hf | Гафний | 658.5 |
| 73 | Ta | Тантал | 761 |
| 74 | W | Вольфрам | 770 |
| 75 | Re | Рений | 760 |
| 76 | Os | Осмий | 840 |
| 77 | Ir | Иридий | 880 |
| 78 | Pt | Платина | 870 |
| 79 | Au | Золото | 890.1 |
| 80 | Hg | Ртуть | 1007.1 |
| 81 | Tl | Таллий | 589.4 |
| 82 | Pb | Свинец | 715.6 |
| 83 | Bi | Висмут | 703 |
| 84 | Po | Полоний | 812.1 |
| 85 | At | Астат | 890 |
| 86 | Rn | Радон | 1037 |
| 87 | Fr | Франций | 380 |
| 88 | Ra | Радий | 509.3 |
| 89 | Ac | Актиний | 499 |
| 90 | Th | Торий | 587 |
| 91 | Pa | Протактиний | 568 |
| 92 | U | Уран | 597.6 |
| 93 | Np | Нептуний | 604.5 |
| 94 | Pu | Плутоний | 584.7 |
| 95 | Am | Америций | 578 |
| 96 | Cm | Кюрий | 581 |
| 97 | Bk | Берклий | 601 |
| 98 | Cf | Калифорний | 608 |
| 99 | Es | Эйнштейний | 619 |
| 100 | Fm | Фермий | 627 |
| 101 | Md | Менделевий | 635 |
| 102 | No | Нобелий | 642 |
| 103 | Lr | Лоуренсий | 470 |
| 104 | Rf | Резерфордий | 580 |
| Таблица 1. Энергия ионизации, справочные данные |
Энергия сродства электрону
Также электроны могут присоединяться к атому, в процессе присоединения электрон выделяет энергию, такая энергия называется энергией сродства электрону, для каждого электрона конкретного атома энергия сродства численно равна и противоположна по знаку энергии ионизации, например, 17Cl, что бы оторвать 17й электрон у атома хлора, необходимо сообщить ему 13 эВ, любой другой электрон, который присоединится на место 17го электрона также выделит 13 эВ.
Катионы и анионы
Атомы, в которых количество протонов не равно количеству электронов называются ионами, поскольку электрон имеет отрицательный заряд, то если электронов больше протонов, то суммарный заряд отрицательный: S2- означает, что в данном атоме серы количество электронов больше чем протонов на два электрона. Соответственно, если электронов меньше чем протонов, то суммарный заряд положительный и обозначается H+. Отрицательно заряженные атомы называются анионами, положительно заряженные атомы — катионами.
Какой заряд будет у атома?
Теоретически возможно отобрать все электроны у атома, но это возможно только в лабораторных условиях и за пределами лаборатории атомы в таком состоянии находиться не будут, почему?
Вернёмся к устройству электронной оболочки. Вокруг атома электроны сгруппированы по энергетическим уровням, каждый заполненный уровень экранирует ядро и является более стабильным, нежели не до конца заполненный уровень.
То есть электронная конфигурация стремиться к состоянию заполненного подуровня: если на p-оболочке находится 5 электронов, то вероятнее атом примет один электрон, нежели отдаст пять. Так, например, у атома хлора, пять электронов на 3p-подуровне, энергия сродства хлора — 3.61 эВ, энергия ионизации — 13 эВ.
У натрия на последнем подуровне один электрон, энергия сродства — 0,78 эВ, потенциал ионизации — 0,49 эВ, поэтому вероятнее натрий отдаст один электрон, нежели примет его.
Зная потенциал ионизации и энергию сродства мы можем сделать предположение о взаимодействии веществ. Если смешать натрий и хлор, и сообщить им энергию, то вероятнее всего Na будет отдавать один электрон Cl и в результате получится смесь ионов Na+ и Cl-.
Пример
Так можно по номеру элемента предположить, какой заряд он будет иметь, например, 19й элемент, электронная конфигурация — 1s 22s 22p 63s 23p64s 1, вероятнее всего, такой элемент может либо отдать, либо принять один электрон.
У 27го элемента электронная конфигурация выглядит так: 1s 22s 22p 63s 23p64s 23d7, у d-подуровня всего может быть 10 атомов, т.е. либо атом примет 1,2 или 3 электрона, либо отдаст 1,2,3…7 электронов, так, вероятнее, он примет 3, т.е.
возможные состояния — это +1, +2 и +3,
Теперь Вы знаете, что такое ионы, осталось изучить химическую связи и Вы сможете составлять окислительно-восстановительные реакции!






