- Периодическая таблица и металлы
- Какие металлы бывают?
- Черные и цветные металлы
- Металлическая связь
- Кристаллическое строение металлов. Типы кристаллических решеток
- Решетки ГЦК, ОЦК, ГПУ
- Понятие об индексах Миллера
- Дефекты в металлах
- Влияние дефектов на свойства
- Реальный кристалл металла
- Строение металлов
- Кристаллическое строение металлов – кратко о типах
- Общее строение
- Кристаллизация сплавов
- Не самопроизвольная кристаллизация (гетерогенная)
- Формирование кристаллов
- Виды решёток
- Кристаллические решетки
- Молекулярная кристаллическая решетка
- Ионная кристаллическая решетка
- Металлическая кристаллическая решетка
- Атомная кристаллическая решетка
- Характеристика решётки
- Общее понятие о металлах
- Кристаллические решетки: виды, свойства, определение простым языком
- Определение кристаллической решетки
- Общие сведения
- Виды кристаллических решеток
- Дефекты кристаллического строения металлов
- Атомная кристаллическая решетка
- Металлы и металлосодержащие вещества
- Металлическая кристаллическая решетка
- Общее понятие о металлах
- Кристаллические решетки, видео
- Павел Чайка, главный редактор журнала Познавайка
- Свойства металлов
Из школьного курса химии известно, что все элементы, которые сгруппированы по определенным правилам в периодическую таблицу Менделеева, можно условно разделить на металлы и неметаллы. В этой статье будет рассказано о кристаллическом строении металлов, их физико-химических свойствах, а также о дефектах на атомном уровне, которые в них присутствуют.
Периодическая таблица и металлы
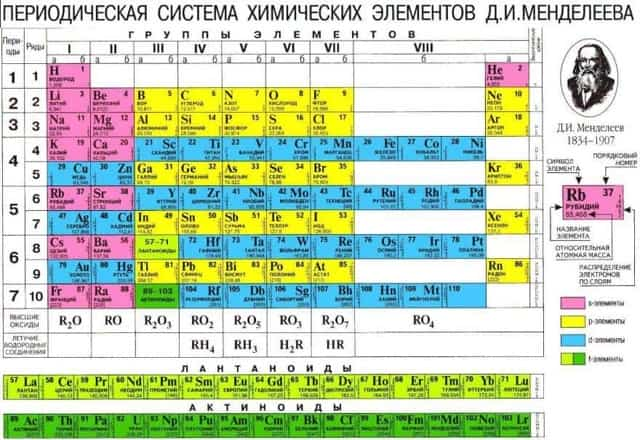
В XIX веке благодаря своему блестящему уму и многим годам труда Дмитрий Иванович Менделеев составил таблицу, собрав в нее все известные на то время химические элементы. Каждому из них в таблице отведено определенное положение в соответствии с числом протонов в атомном ядре. Вся таблица делится на 7 периодов (горизонтальные строки) и 8 групп (вертикальные строки). Чем больше период, тем больше радиус атома соответствующего элемента, и тем на более высоких орбиталях расположены его валентные электроны. Наоборот, чем старше группа (движение по таблице слева направо), тем больше валентных электронов находится на последней орбитали и тем меньше радиус атома.
Любой элемент таблицы можно условно отнести либо к металлам, либо к неметаллам. Металлы расположены по левую сторону от диагонали бор (B) — полоний (Po). Если взглянуть на таблицу, то можно сразу понять, что количество металлов в несколько раз превышает число неметаллов.
Иными словами, как можно понять, что перед нами находится металлический материал? Ответы на все эти вопросы можно получить, если рассмотреть уникальные свойства металлов. К ним относятся следующие основные:
- Наличие металлического блеска при полировке поверхности. Все металлы блестят, в своем большинстве они имеют серый цвет, однако, некоторые металлы обладают специфической окраской, например, висмут розовый, медь красноватая, а золото желтое.
- Высокая теплопроводность и электропроводность. При комнатной температуре наиболее высокие показатели для этих физических свойств характерны для меди и серебра.
- При комнатной температуре практически все металлы находятся в твердом агрегатном состоянии материи. Исключение составляет ртуть, которая плавится уже при -39 oC.
- Будучи в твердом состоянии, металлы кристаллическим строением характеризуются. Если расплав рассматриваемого материала слишком быстро охлаждать, то он приобретает аморфную структуру, в которой все же сохраняется ближний порядок.
- Температуры плавления и плотности металлов варьируются в широких пределах. Так, элемент вольфрам является самым тугоплавким (3410 oC). Самым же тяжелым считается осмий (в 22,6 раза плотнее воды), а самым легким — литий (почти в 2 раза менее плотный, чем вода).
- Все металлы химически активны. Поскольку они обладают низкой электроотрицательностью, то в химических реакциях их атомы отдают электроны и превращаются в положительно заряженные ионы (катионы).

Выше в списке были перечислены основные свойства металлов, которые их отличают от неметаллических материалов. Примерами последних являются кислород, азот, благородные газы, сера, кремний, углерод и некоторые другие. Заметим, что все живые организмы состоят в основном из неметаллов.
Какие металлы бывают?
Металлы в периодической системе Менделеева делятся на несколько групп. Перечислим и кратко охарактеризуем их:
- Щелочные. Эти металлы имеют всего 1 валентный электрон, они чрезвычайно химически активны, имеют низкую плотность и являются отличными проводниками тепла и электричества. Примерами их являются литий, натрий и калий.
- Щелочноземельные. К ним относятся кальций, магний, стронций. Эти металлы имеют 2 валентных электрона, поэтому они также являются химически активными.
- Переходные. Это металлы с переменной валентностью, которые имеют пустые или полупустые орбитали d и f типа. Это самая многочисленная группа металлов. К ним относятся титан, ванадий, хром, никель, вольфрам, осмий, золото и многие другие.
- Лантаноиды и актиноиды. Большая часть этих элементов является нестабильными и проявляет различную степень радиоактивности.
- Постпереходные. Это те элементы, после которых по периоду идут металлоиды, а затем неметаллы. Самыми известными из них являются свинец, алюминий и олово.
Черные и цветные металлы
Выше была приведена классификация рассматриваемых элементов в соответствии с их электронным строением и положением в периодической системе. Помимо нее, существует еще одно разделение, которое не связано с атомным строением — это понятие о черных и цветных металлах.
Черным является железо и все сплавы с его участием. Примеры цветных металлов — это алюминий, золото, серебро, медь и другие, а также сплавы, которые не содержат железа.
Причина такого разделения проста, черные металлы являются дешевыми и недолговечными (разрушаются в результате коррозии, ржавеют).
Наоборот, цветные металлы характеризуются способностью образовывать пленки оксидные, которые предотвращают основную массу материала от дальнейшего химического разрушения.
Металлическая связь
Изучая атомно-кристаллическое строение металлов, следует сказать несколько слов об особенностях химической связи между рассматриваемыми элементами.
Поскольку электроотрицательность металлов низкая, то, объединяясь в кристаллическую решетку, каждый атом отдает один или несколько валентных электронов.
Эти электроны слабо связаны с ядром, поэтому они легко от него отрываются уже при комнатных температурах.
Совокупность валентных электронов, которые свободно движутся в пространстве между ионными остовами в кристаллической решетке металлов, называется электронным газом. Благодаря ему кусок металла легко проводит тепло и электричество.
Электрическое поле положительно заряженных ионных остовов компенсируется отрицательным полем «размазанного» по объему металла электронного газа. Такая связь называется металлической. Она кардинальным образом отличается от других типов химической связи.
Например, в ковалентной атомы не отдают электроны в межатомное пространство, они становятся общими только для двух атомов.
Наоборот, в ионной связи один атом полностью лишает второго валентных электронов, присоединяя их к себе, и приобретая отрицательный заряд.
Кристаллическое строение металлов. Типы кристаллических решеток
Когда металл образует твердую структуру, то все его атомы стремятся занять такие положения в пространстве относительно друг друга, чтобы они соответствовали минимуму потенциальной энергии. Этому минимуму соответствует кристаллическая решетка.
Под кристаллической решеткой понимают такую пространственную атомную структуру, которая может быть получена, если известны координаты ограниченного числа ее атомов и вектора их трансляции в пространстве. Указанное число атомов называется базисом решетки, а их положения образуют так называемую элементарную ячейку.
Все металлы кристаллизуются в трех основных типах решеток:
- гранецентрированная кубическая (ГЦК);
- объемно-центрированная кубическая (ОЦК);
- гексагональная плотноупакованная (ГПУ).
Благодаря кристаллическому строению металлы обладают такими свойствами, как пластичностью, упругостью и металлическим блеском.
Решетки ГЦК, ОЦК, ГПУ
Изучая кристаллическое строение металлов, охарактеризуем подробнее каждый тип кристаллической решетки. Начнем с ГЦК. Она показана ниже на рисунке.
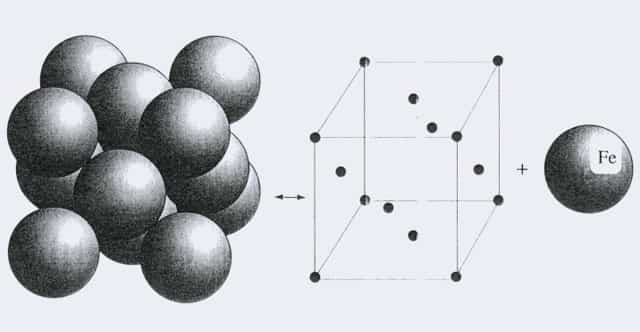
Как видно, это решетка представляет собой кубик, в котором атомы расположены в его вершинах и в центрах всех шести граней. Применяя методы кристаллографии, несложно показать, что для получения такой решетки в пространстве достаточно всего четырех атомов и векторов трансляций, совпадающих с ребрами куба.
Примерами металлов, которые кристаллизуются в ГЦК, являются алюминий, медь, золото и серебро. Железо образует ГЦК решетку только при высоких температурах.
ОЦК решетка показана ниже.
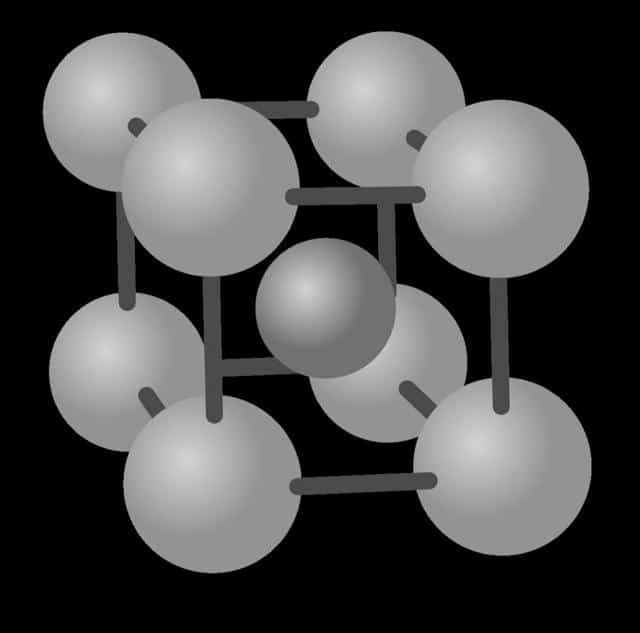
Мы видим, что она соответствует кубику, в вершинах и в центре которого находится атом. Всего два атома необходимо, чтобы в прямоугольных декартовых координатах построить ОЦК решетку. Такие металлы, как ванадий, тантал, ниобий, вольфрам имеют именно эту кристаллическую структуру.
Наконец, ГПУ решетка. Она представлена ниже на рисунке.
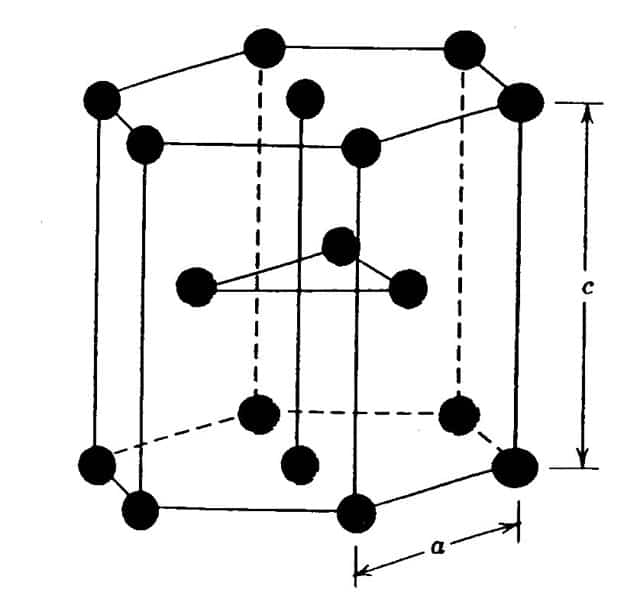
Эта кристаллическая решетка металлов отличается от двух предыдущих тем, что она в пространстве образует не куб, а правильную шестиугольную призму, которая состоит из шести атомов. В данной структуре кристаллизуются такие элементы, как титан, цирконий, магний и кобальт.
Понятие об индексах Миллера
Чтобы удобно было описывать численно показанные выше пространственные решетки, в кристаллографии используют так называемые индексы Миллера.
Они представляют собой наборы чисел, которые позволяют точно определить положение в пространстве данного атомного ряда или атомной плоскости. По этим числам судят о поверхностных энергиях, о способности металлов проявлять пластические свойства.
Например, в ГЦК решетке краевые дислокации движутся по плоскостям (1,1,1) (эти плоскости являются максимально плотноупакованными, нормалью к ним будут диагонали куба).
Дефекты в металлах
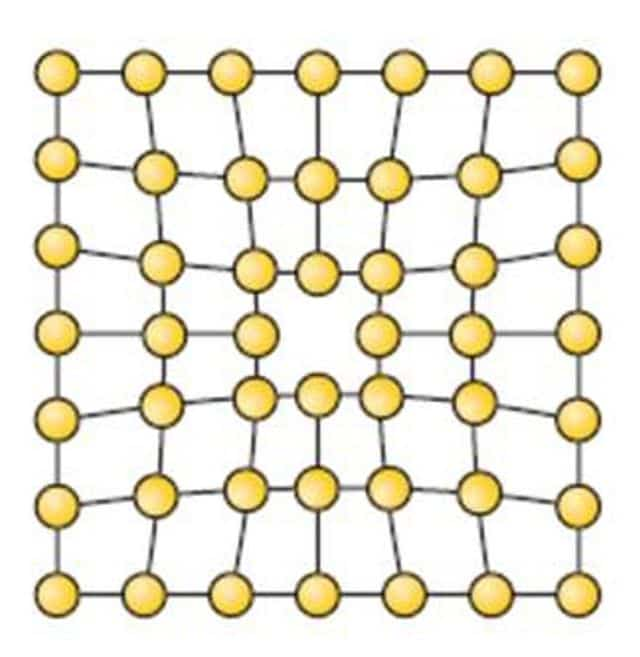
Выше мы показали идеальную ситуацию, когда все атомы находятся на своих местах, и пространственную структуру всего металлического куска можно получить с помощью простых трансляций элементарной ячейки. В действительности же существуют множество несовершенств кристаллического строения металлов. Они называются дефектами.
Все дефекты можно по геометрическому признаку отнести к одному из четырех типов:
- Точечные. Вакансии, межузельные атомы, наличие внедренных атомов других элементов, создающих микроскопические локальные напряжения.
- Линейные. Дислокации — обрывы кристаллических плоскостей, которые обеспечивают пластичность всех металлов.
- Плоские — границы зерен. Любой металл состоит из множества монокристаллов, которые друг с другом соединены в различной ориентации через межзеренные границы.
- Объемные. Поры, различные фазовые включения, которые упрочняют металл и снижают его пластичность.
Влияние дефектов на свойства
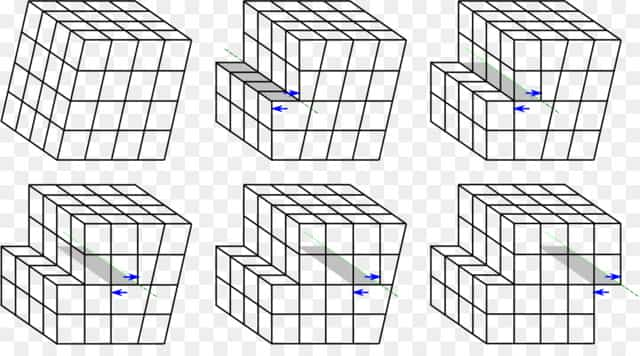
Как правило, дефекты кристаллического строения металлов приводят к снижению их теплопроводности и электропроводности, материал становится более прочным и менее пластичным. Ярким примером является сталь, которая за счет междоузельных атомов углерода и наличия разных фаз (цементита, графита) в кристаллической решетке железа, значительно прочнее, чем чистый металл.
С развитием нанотехнологий влияние дефектов на свойства металлов может быть неоднозначным. Так, с уменьшением размера зерна может наблюдаться увеличение пластичности материала, что связано с появлением совершенно иного механизма пластической деформации — зернограничного проскальзывания, которое по своей сути отличается от дислокационного.
Реальный кристалл металла
Какой бы химический металлический элемент не рассматривался, в действительности он представляет собой твердое вещество, в котором маленькие монокристаллы (зерна) соединены друг с другом в различных ориентациях. Такая структура образует поликристалл.
В нем, помимо границ зерен, присутствуют дефекты всех четырех типов, включая примеси таких неметаллов, как кислород, азот и водород.
Последний из-за своих размеров легко проникает в любую кристаллическую решетку, образует с ее ионами твердые фазы, которые приводят к охрупчиванию металла, что является одной из актуальных проблем металловедения.
Строение металлов
Введение
Металлы — простые вещества, обладающие в обычных условиях характерными свойствами: высокой электро — и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), высокой прочностью и пластичностью.
Свойства металлов могут значительно измениться при очень высоких давлениях. Многие металлы в зависимости от температуры и давления могут существовать в виде нескольких кристаллических модификаций.
Подобными металлическими свойствами обладают более 80 химических элементов и множество металлических сплавов. Число металлических сплавов, применяемых в технике, исчисляется тысячами и постоянно возрастает в соответствии с возникающими новыми и разнообразными требованиями, предъявляемыми многими отраслями промышленности.
- Свойства металлов обусловлены их кристаллическим строением и наличием в их кристаллической решетке многочисленных не связанных с атомными ядрами подвижных электронов проводимости.
- Металлические сплавы по свойствам имеют много общего с металлами, поэтому их нередко относят к металлам.
- Металлы (сплавы) в промышленности разделяют на две основные группы: черные и цветные металлы.
Черные металлы — сплав железа с углеродом, в котором могут содержаться в большем или меньшем количестве и другие химические элементы.
Кобальт, никель, а также близкий к ним по свойствам марганец нередко относят к черным металлам.
Черные металлы получили наибольшее распространение, что обусловлено относительно высоким содержанием железа в земной коре, его низкой стоимостью, высокими механическими и технологическими свойствами.
- Цветные металлы по свойствам подразделяют на следующие группы:
- легкие (Be, Mg, Al, Ti), обладающие сравнительно малой плотностью — до 5000 кг/м3;
- тугоплавкие (Ti, Сг, Zr, Nb, Mo, W, V и др.) с температурой плавления выше, чем у железа (1539°С);
- благородные (Ph, Pd, Ag, Os, Pt, Аи и др.), обладающие химическойинертностью:
- урановые (U, Th, Pa) — актиноиды, используемые в атомной технике;
- редкоземельные металлы (РЗМ), лантаноиды (Се, Рг, Nd, Sm и др.) и сходные с ними иттрий и скандий, применяемые как присадки к различным сплавам;
- щелочноземельные металлы (Li, Na, К), используемые в качестве теплоносителей в ядерных реакторах.
Классификация металлических сплавов по химическому составу, основанная на указании главного компонента сплава (железо, медь, алюминий и др.), имеет традиционный характер, и получила наибольшее распространение.
Макро-, микро- и атомную структуру металлов и сплавов изучает металлография.
Макроструктура — это строение металла, видимое невооруженным глазом или с помощью лупы в изломе или на протравленном шлифе. Микроструктура строения металла, наблюдаемое под оптическим или электронным микроскопами, позволяющими увеличить рассматриваемый участок от десяти раз до сотен тысяч раз.
Атомная структура металлов — это пространственное расположение атомов в кристаллической решетке. Этот вид структуры исследуется с помощью рентгено- графического структурного анализа.
Строение металла
Все металлы имеют кристаллическое строение. Располагаясь тем или иным способом, атомы образуют элементарную ячейку пространственной кристаллической решетки. Тип ячейки зависит от химической природы и состояния металла. Кристаллическое состояние, прежде всего, характеризуется определенным, закономерным расположением атомов в пространстве.
Это обусловливает то, что в кристалле каждый атом имеет одно и то же количество ближайших атомов — соседей, расположенных на одинаковом от него расстоянии. В процессе кристаллизации положительно заряженные ионы, располагаясь последовательно в виде элементарных кристаллических решеток, образуют кристаллы в виде зерен или дендритов.
Все металлы и сплавы имеют кристаллическое строение. Образующиеся кристаллы растут, кристаллизуются из жидкого расплава сначала свободно, не мешают один другому, потом они сталкиваются и рост кристаллов продолжается только в тех направлениях, где есть свободный доступ жидкого металла. В результате первоначальная геометрически правильная форма кристаллов нарушается.
После затвердевания зерна и дендриты имеют неправильную, геометрически искаженную форму.
Рисунок 1. Схема кристаллизации: а — в виде зерен; б — в виде дендритов.
Стремление атомов (ионов) металла расположиться, возможно, ближе друг к другу, плотнее, приводит к тому, что число встречающихся комбинаций взаимного расположения атомов металла в кристаллах невелико.
Существует ряд схем и способов описания вариантов взаимного расположения атомов в кристалле. Взаимное расположение атомов в одной из плоскостей показано на схеме размещения атомов (рисунок 2) .
Рисунок 2. Элементарная кристаллическая ячейка (простая кубическая).
Воображаемые линии, проведенные через центры атомов, образуют решетку, в узлах которой располагаются атомы (положительно заряженные ионы); это так называемая кристаллографическая плоскость.
Многократное повторение кристаллографических плоскостей, расположенных параллельно, воспроизводит пространственную кристаллическую решетку, узлы которой являются местом расположения атомов (ионов). Расстояния между центрами соседних атомов измеряются ангстремами (1 А= 1 * 10-8 см) или в килоисках — kX (1kX = 1,00202 А).
Взаимное расположение атомов в пространстве и величину между атомных расстояний определяют рентгеноструктурным анализом. Расположение атомов в кристалле весьма удобно изображать в виде пространственных схем, в виде так называемых элементарных кристаллических ячеек.
Под элементарной кристаллической ячейкой подразумевается наименьший комплекс атомов, который при многократном повторении в пространстве позволяет воспроизвести пространственную кристаллическую решетку. Простейшим типом кристаллической ячейки является кубическая решетка.
В простой кубической решетке атомы расположены (упакованы) недостаточно плотно. Стремление атомов металла занять места, наиболее близкие друг к другу, приводит к образованию решеток других типов: кубической объемноцентрированной (рисунок 3, а), кубической гранецентрированной (рисунок 3, б) и гексагональной плотноупакованной (рисунок 3, в).
Рисунок 3. Элементарные кристаллические ячейки: а — кубическая объемноцентрированная; б — кубическая гранецентрированная; в — гексагональная плотноупакованная.
металл теплопроводность электромагнитный температурный
Кружки, отображающие атомы, располагаются в центре куба и по его вершинам (куб объемноцентрированный), или в центрах граней и по вершинам куба (куб гранецентрированный), или в виде шестигранника, внутрь которого наполовину вставлен также шестигранник, три атома верхней плоскости которого находятся внутри шестигранной призмы (гексагональная решетка).
Метод изображения кристаллической решетки, приведенный на рисунке 3, является условным (как в любой другой). Может быть, более правильно изображение атомов в кристаллической решетке в виде соприкасающихся шаров (левые схемы на рисунке 3). Однако такое изображение кристаллической решетки не всегда удобно, чем принятое (правые схемы на рисунке 3).
Размеры кристаллической решетки характеризуются параметрами, или периодами решетки. Кубическую решетку определяет один параметр — длина ребра куба а (рисунок 3, а, б). Параметры имеют величины порядка атомных размеров и измеряются в ангстремах.
Так например, параметр решетки хрома, имеющего структуру объемноцентрированного куба, равен 2,878 А, а параметр решетки алюминия, имеющего структуру гранецентрированного куба, 4,041 А.
Параметр решетки — чрезвычайно важная характеристика. Современные методы рентгеновского исследования позволяют измерить параметр с точностью до четвертого или даже пятого знака после запятой, т. е. одной десятитысячной — одной стотысячной доли ангстрема.
- Из рассмотрения схем кристаллических решеток (рисунок 3), если считать, что атомы являются как бы упругими, касающимися друг друга шарами, вытекает, что параметр решетки а и атомный диаметр d связаны простыми геометрическими соотношениями.
- Для объемноцентрированного куба
- d = а v3 / 2.
- Для гранецентрированного куба
- d = а v2 / 3.
Принимая для атома форму шара, можно подсчитать, что в кубической объемноцентрированной решетке атомы занимают 68% объема, а в кубической гранецентрированной (как и в гексагональной плотноупакованной) 74%, т.е. во втором случае атомы располагаются более плотно, более компактно.
Для металлов распространена гексагональная решетка (рисунок 3, в).
Если слои атомов касаются друг друга, т. е. три атома, изображенные внутри решетки (рисунок 3, в), касаются атомов, расположенных на верхней и нижней плоскостях, то имеем так называемую гексагональную плотноупакованную решетку.
Размеры гексагональной плотноупакованной решетки характеризуются постоянным значением с/а=1,633. При иных значениях с/а получается неплотлоупакованная гексагональная решетка.
Кубическая гранецентрированная и гексагональная решетки представляют самый плотный способ укладки шаров одного диаметра.
Некоторые металлы имеют тетрагональную решетку (рисунок 4); она характеризуется тем, что ребро с не равно ребру а. Отношение этих параметров характеризует так называемую степень тетрагональности.
При с/а = 1 получается кубическая решетка.
В зависимости от пространственного расположения атомов тетрагональная решетка (как и кубическая) может быть простой, объемноцентрированной и гранецентрированной.
Рисунок 4. Тетрагональная решетка
Существенное значение для свойств данного металла или сплава имеет число атомов, находящихся во взаимном контакте. Это определяется числом атомов, равноотстоящих на ближайшем расстоянии от любого атома.
Число атомов, находящихся на наиболее близком и равном расстоянии от данного атома, называется координационным числом. Так, например, атом в простой кубической решетке имеет шесть ближайших равноотстоящих соседей, т. е. координационное число этой решетки равно 6.
Центральный атом в объемноцентрированной решетке имеет восемь ближайших равноотстоящих соседей, т. е. координационное число этой решетки равно 8.
Координационное число для гранецентрированной решетки равно 12.
В случае гексагональной плотноупакованной решетки координационное число равно 12, а в случае с/а ? 1,633 каждый атом имеет шесть атомов на одном расстоянии и шесть на другом (координационное число 6).
Для краткого обозначения кристаллической решетки с указанием в этом обозначении типа кристаллической решетки и координационного числа была принята одна из следующих систем (таблица 1).
Таблица 1
| Решетка | Обозначение | Координационное число |
| Простая кубическая | к | К6 |
| Кубическая объемно-центрированная | о. ц. к. | К8 |
| Кубическая гранецентрированная | г. ц. к. | К12 |
| Гексагональная плотноупакованная 1 | г. п. у. | Г12 |
| Гексагональная 2 | г | Г6 |
Кристаллическое строение металлов – кратко о типах
- 4.5
- Средняя оценка: 4.5
- Всего получено оценок: 174.
- 4.5
Полировальная ткань и сукно для полировки в металлографии
Средняя оценка: 4.5
Всего получено оценок: 174.
Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.
Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Кристаллизация сплавов
- Переход металла из жидкого состояния в твёрдое с образованием кристаллической структуры называется первичной кристаллизацией.
- Образования новых кристаллов в твёрдом кристаллическом веществе называется вторичной кристаллизацией (перекристаллизацией).
- Процесс кристаллизации состоит из двух одновременных процессов:
- зарождение кристаллов;
- линейный рост кристаллов;
Кристаллы могут зарождаться самопроизвольно (самопроизвольная кристаллизация) или зарождаться и расти на имеющихся готовых центрах кристаллизации (не самопроизвольная кристаллизация) (рис 33).
Рис 34 Рост зародышевых центров и рост кристаллов
Самопроизвольная кристаллизация (рис.35) обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением термодинамического потенциала G, характеристика свободной энергии системы.
Второй закон термодинамики – любая система всегда стремится занять то состояние, чтобы она обладала min свободной энергией.
Температура, при которой термодинамические потенциалы вещества, как в твёрдом, так и в жидком состояниях равны, называется равновесной температурой (термодинамической температурой) ТG.
Расшифровка маркировки и марки чугуна
- Рис.35 Самопроизвольная кристаллизация
- Термодинамический потенциал определяется:
- G = Е – ТS + РV (по Гельмгольцу)
- где G – термодинамический потенциал, свободная энергия системы,
- Е – внутренняя энергия системы,
- Т – термодинамическая температура
- S – энтропия (функция состояния: порядка и беспорядка, связанное с поступательным и колебательным движением),
- РV – работа внешних сил (давление на объём)
- G = Н – ТS (по Гиббсу)
- где Н – энтальпия (Е + РV) сумма работ внутренних и внешних сил.
Разница между равновесной (ТG.) и реальной (Тр) температурой кристаллизации называется степенью переохлаждения (Δ Т).
Образованию зародышей способствуют флуктуации энергии, т.е. отклонение энергии группировок атомов в отдельных зонах жидкого металла от некоторого среднего значения.
Появление зародышей изменяет термодинамический потенциал (свободную энергию) всей системы. С одной стороны, при переходе жидкости в кристаллическое состояние термодинамический потенциал G уменьшается, с другой стороны, он увеличивается (+) вследствие появления поверхности раздела между жидкостью и кристаллическим зародышем.
На рис.36 показано, как изменяется свободная энергия системы при кристаллизации.
Как правильно варить трубы электросваркой инвертором?
Кинетика кристаллизации.
Скорость образования зародышей, образующихся в единицу времени в единице объёма (1мм-3с-1); скорость роста – увеличением линейных размеров, растущих кристалла в единицу времени (мм/с).
Оба процесса связаны с перемещением атомов и зависят от температуры (степени переохлаждения Δ Т).
Не самопроизвольная кристаллизация (гетерогенная)
В реальных условиях процессы кристаллизации и характер образующих структур в значительной мере зависят от имеющихся готовых центров кристаллизации. Такими центрами являются:
- тугоплавкие частицы неметаллических включений;
- оксиды;
- интерметаллические соединения, образуемых примесей.
Измельчение структуры способствует улучшению механических свойств металла.
Рис.36 Изменение свободной энергии при кристаллизации
На практике для измельчения структуры металла и сплавов широко применяют технологическую операцию, называемую модифицированием.
Она состоит во введении в жидкий сплав перед заливкой специальных добавок модификаторов (бор в сталь, натрий в алюминий и его сплавы).
Подстуживание металла перед заливкой до температур, незначительно превышающих температуру плавления металла, способствует уменьшению размера зерна.
Формирование кристаллов
Форма и размер зёрен, образующихся при кристаллизации, зависят:
- скорости и направления отвода тепла:
- температуры жидкого металла;
- содержание примесей.
Структура слитка зависит от многих факторов: (рис.37)
- количество и свойства примесей в чистом металле;
- количества легирующих элементов в сплаве;
- температуры разливки сплава;
- скорость охлаждения при кристаллизации и т.д.
Рис.37 Схема строения металлического слитка, полученного при разных температурах
Типичная структура слитка сплавов состоит из трёх зон: (рис.38)
- мелкие равноосные кристаллы на поверхности слитка, из-за большой степени переохлаждения;
- столбчатые кристаллы, наиболее благоприятно ориентированные по отношению к теплоотводу, расположенные нормально к стенкам формы;
- равноосные кристаллы больших размеров в середине слитка, где наблюдается наименьшая степень переохлаждения и не ощущается направленного отвода тепла.
Структура, состоящая из одних столбчатых кристаллов, называется транскристаллитной. Встречается у слитков очень чистых металлов.
Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией. Она отрицательно влияет на механические свойства сплава. В реальных сплавах кроме зональной встречаются и другие виды ликвации.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.
Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Кристаллические решетки
Кристаллической решеткой называют пространственное расположение атомов или ионов в кристалле. Точки кристаллической решетки, в которых расположены атомы или ионы, называют узлами кристаллической решетки.
Кристаллические решетки подразделяют на молекулярные, атомные, ионные и металлические.
Очень важно не перепутать вид химической связи и кристаллической решетки. Помните, что кристаллические решетки отражают пространственное расположение атомов.
Молекулярная кристаллическая решетка
В узлах молекулярной решетки расположены молекулы. При обычных условиях молекулярную решетку имеют большинство газов и жидкостей. Связи чаще всего ковалентные полярные или неполярные.
Классическим примером вещества с молекулярной решеткой является вода, так что ассоциируйте свойства этих веществ с водой. Вещества с молекулярной решеткой непрочные, имеют небольшую твердость, летучие, легкоплавкие, способны к возгонке, для них характерны небольшие температуры кипения.
Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2. Особо хочется отметить белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы подробно изучили в статье, посвященной классификации веществ.
Ионная кристаллическая решетка
В узлах ионной решетки находятся атомы, связанные ионной связью. Этот тип решетки характерен для веществ, обладающих ионной связь: соли, оксиды и гидроксиды металлов.
Ассоциируйте этот ряд веществ с поваренной солью — NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.
Примеры: NaCl, MgCl2, NH4Br, KNO3, Li2O, Na3PO4.
Металлическая кристаллическая решетка
В узлах металлической решетки находятся атомы металла. Этот тип решетки характерен для веществ, образованных металлической связью.
Ассоциируйте свойства этих веществ с медью. Они обладают характерным металлическим блеском, ковкие и пластичные, хорошо проводят электрический ток и тепло, имеют высокие температуры плавления и кипения.
Примеры: Cu, Fe, Zn, Al, Cr, Mn.
Атомная кристаллическая решетка
В узлах атомной решетки находятся атомы, связанные ковалентной полярной или неполярной связью.
Ассоциируйте эти вещества с песком. Они очень твердые, очень тугоплавкие (высокая температура плавления), нелетучие, прочные, нерастворимы в воде.
Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), красный и черный фосфор (P).
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью.
Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию
.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
Рис. 3. Кристаллические ячейки составляют решётку.
Общее понятие о металлах
«Химия. 9 класс» — это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.
Кристаллические решетки: виды, свойства, определение простым языком
Определение кристаллической решетки
Как мы знаем, все материальные вещества могут пребывать в трех базовых состояниях: жидком, твердом, и газообразном. Правда есть еще состояние плазмы, которое ученые считают ни много ни мало четвертым состоянием вещества, но наша статья не о плазме.
Твердое состояние вещества потому твердое, так как имеет особую кристаллическую структуру, частицы которой находятся в определенном и четко заданном порядке, создавая, таким образом, кристаллическую решетку.
Строение кристаллической решетки состоит из повторяющихся одинаковых элементарных ячеек: атомов, молекул, ионов, других элементарных частиц, связанных между собой различными узлами.
Общие сведения
Твердые тела по своим свойствам и структуре обычно классифицируются на кристаллические и аморфные. Это разделение обусловлено разным положением в них ионов, атомов или молекул.
Частицы аморфных тел распределяются хаотично. Такое строение придает им изотропность и делает невозможным иметь фиксированную температуру плавления.
К аморфным материалам относятся воск, полимеры и пластики, затвердевшие смолы.
В кристаллическом веществе частицы выстраиваются в строго определенном порядке и образуют структуры, периодически повторяющиеся по всему его объему. Это придает материалу анизотропическое соответствие. Пространственное отображение такого строения — кристаллическая решетка.
Она не является статичной, ее молекулы или атомы постоянно колеблются около положений равновесия. Состоит из узлов, в которых находятся частицы вещества, и соединяющих их воображаемых линий. Узлы образуются молекулами, атомами или ионами.
Линии обозначают химические связи между этими частицами.
Как выглядит мебельный шкант, его назначение и разновидности
Существование решеток обусловлено тем, что только при условии периодичности в трехмерном пространстве достигается минимальное значение потенциальной энергии системы путем уравновешивания сил отталкивания и притяжения между атомами. Они бывают ионными, металлическими, ковалентными полярными и неполярными.
Наименьший фрагмент решетки считается элементарной ячейкой. Построить полную структуру материала можно так — перенести параллельно элементарную ячейку в любом направлении.
Компактность и заполненность такой ячейки — важная характеристика, которая определяет химические и физические свойства вещества. Описывается такими показателями: число атомов в ней, плотность упаковки и параметр, т. е.
расстоянием между ближайшими частицами. Параметр измеряется в нанометрах и вычисляется при помощи рентгеноструктурного анализа.
Простейшая элементарная ячейка состоит из восьми частиц, расположенных в вершинах куба. Другие возможные геометрические построения структур описывают модели Браве.
Виды кристаллических решеток
В зависимости от частиц кристаллической решетки существует четырнадцать типов оной, приведем наиболее популярные из них:
Металлическаякристаллическая решетка. Далее более подробно опишем все типы кристаллической решетки.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые. Ухудшают прочность и качество материала.
- Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.
Атомная кристаллическая решетка
Вещества с атомной кристаллической решеткой, как правило, имеют в своих узлах, состоящих собственно из атомов сильные ковалентные связи. Ковалентная связь происходит, когда два одинаковых атома делятся друг с другом по-братски электронами, образуя, таким образом, общую пару электронов для соседних атомов.
Из-за этого ковалентные связи сильно и равномерно связывают атомы в строгом порядке – пожалуй, это самая характерная черта строения атомной кристаллической решетки. Химические элементы с подобными связями могут похвастаться своей твердостью, высокой температурой плавления.
Атомную кристаллическую решетку имеют такие химические элементы как алмаз, кремний, германий, бор.
Металлы и металлосодержащие вещества
Химическое строение таких твердых тел определяется типом связи между его частицами, которые бывают металлическими или ионными.
Структура, состоящая из положительно заряженных ионов единственного химического элемента, между которыми находятся электроны внешнего энергетического уровня, легко теряющие связь с ядром и свободно перемещающиеся по всему металлическому телу (электронный газ), называется металлической кристаллической решеткой. В узлах располагаются ионы и атомы. Такая решетка состоит из элементарных ячеек, которые бывают следующих видов:
- Объемноцентрированный куб. Включает два атома. Ионы металла, имеющие положительный знак заряда, размещаются в узлах куба, а еще один атом — в его центре. Такую решетку имеют очень твердые и тугоплавкие металлы — вольфрам, молибден, хром, ванадий.
- Гранецентрированный куб. Содержит четыре атома, положительные ионы находятся не только в узлах, но и в центре каждой грани куба. Эта решетка характерна для свинца, меди, никеля, железа, алюминия и многих других металлов.
- Гексагональная плотно упакованная. Состоит из шести атомов и представляет собой шестигранную призму. Ионы располагаются в узлах, по центру оснований и в середине призмы. Такое строение имеют все элементы II группы таблицы Менделеева — бериллий, кальций, магний, стронций, барий, радий.
Металлический тип строения определяет наличие свойств, типичных для металлов и их сплавов — блеск, пластичность и ковкость, высокую электро- и теплопроводность.
Цепные стропы, их маркировка, классы и применение.
Если в состав кристалла входят химические элементы, состоящие из атомов с разной электроотрицательностью (способностью атома притягивать к себе общую электронную пару), то электроны от одних атомов могут полностью переходить к другим.
В результате получаются положительно и отрицательно заряженные ионы, называемые соответственно катионами и анионами. Связь между ними носит название ионной, а структура, в узлах которой находятся разнозаряженные ионы, называется ионной кристаллической решеткой.
Геометрические виды элементарных ячеек ионных структур такие же, как и у металлических, только в узлах располагаются ионы не одного, а разных химических элементов, причем одинаково заряженные находятся как можно дальше друг от друга, а разнозаряженные — как можно ближе.
Такое строение обычно бывает у соединений, образованных типичным металлом и неметаллом, при этом металл должен быть менее активным, чем неметалл.
Ионной структуре соответствуют оксиды, гидроксиды, щелочи и соли, а их составляющие бывают простыми или сложными.
Так, кристалл поваренной соли (хлорида натрия) образуется из простых ионов: катион калия K и анион хлора Cl, а в состав сернокислого калия входят простой катион калия K и сложный отрицательный сульфат-ион SO4.
Связи между ионами в структурах очень устойчивые, поэтому вещества с таким строением обладают прочностью, твердостью и тугоплавкостью и имеют небольшую летучесть.
В то же время они отличаются хрупкостью — ионные слои легко смещаются. Проводят электрический ток и тепло только в растворах или расплавах.
Металлическая кристаллическая решетка
Тип связи металлической кристаллической решетки гибче и пластичнее ионной, хотя внешне они весьма похожи. Отличительной особенностью ее является наличие положительно заряженных катионов (ионов метала) в узлах решетки.
Между узлами живут электроны, участвующие в создании электрического поля, эти электроны еще называются электрическим газом.
Наличие такой структуры металлической кристаллической решетки объясняет ее свойства: механическую прочность, тепло и электропроводность, плавкость.
Общее понятие о металлах
«Химия. 9 класс» – это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Читать также: Вездеход из бензопилы своими руками
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.
Кристаллические решетки, видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.
Адаптер для мотоблока своими руками, размеры и чертежи
Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту [email protected] или в Фейсбук, с уважением автор.
Страница про автора
Эта статья доступна на английском – Crystal Lattice in Chemistry.
Свойства металлов
К специфическим свойствам рассматриваемых веществ относят следующие.
- Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым серебристо-белым цветом. Лишь некоторые (золото, медь, сплавы) отличаются.
- Ковкость и пластичность – способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
- Электропроводность и теплопроводность – одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя. Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.






