Вычертите диаграмму состояния железо-цементит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 0,6 % С. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
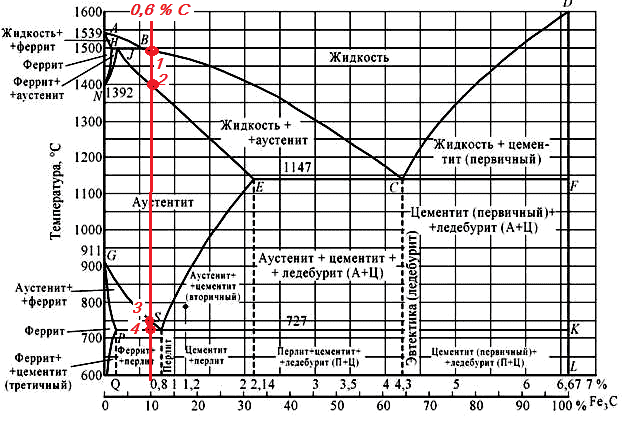
- Сплав с содержанием углерода 0,6 % называется доэвтектоидной сталью.
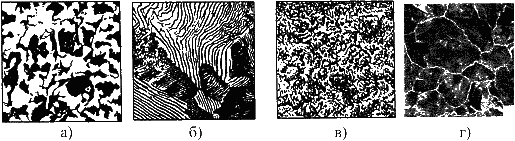
- В исходном состоянии сталь имеет структуру, состоящую из зерен феррита (твердый раствор внедрения углерода в ОЦК-решетке железа) и зерен перлита (механическая смесь из феррита и цементита).
- Микроструктура доэвтектоидной стали
- (но это не сталь с содержанием 0,6 % С, здесь примерно 0,4 %С)
Для того, чтобы проследить, какие превращения претерпевает сплав (сталь 60) при охлаждении, проведем линию сплава и пронумеруем точки пересечения линии сплава с линиями диаграммы. Это и есть критические точки.
Критическая точка – это температура, при которой начинается, заканчивается или полностью протекает фазовое или другое превращение в сплаве. На кривых охлаждения им соответствуют остановки или линии перегиба.
- 1 – температура Ликвидус (линия AВCD) – при охлаждении начинается процесс кристаллизации, из жидкого раствора выпадают кристаллы аустенита;
- 2 – температура Солидус (линия AECF ) – при охлаждении заканчивается кристаллизация аустенита;
- 3 – критическая точка А3 (линия GS) – температура начала выделения феррита из аустенита;
- 4 – критическая точка А1 (линия PSK) – превращение (распад) оставшегося аустенита в перлит – эвтектоидное превращение;
- 5 – (на диаграмме не обозначена) – магнитное превращение цементита – 210С
- Превращения, протекающие при охлаждении (цифры рядом с буквами обозначают содержание углерода в данной фазе)
- 1. Кристаллизация аустенита из жидкости Ж0,6 А0,6 (в интервале 1–2)
- 2. превращение части аустенита в феррит (путем полиморфного превращения):
- А0,6 Ф0,02 (в интервале 3–4)
- При этом оставшаяся часть аустенита обогащается по углероду до 0,8 %, согласно правилу отрезков.
- 3. Эвтектоидное превращение оставшейся части аустенита А0,8 П0,8 (Ф0,02 + Ц6,67) (на кривой охлаждения – горизонтальная линия 4–4/)
- 4. Выделение избыточного цементита третичного (ЦIII) из феррита: Ф0,02 Ц6,67
- Кривая охлаждения:
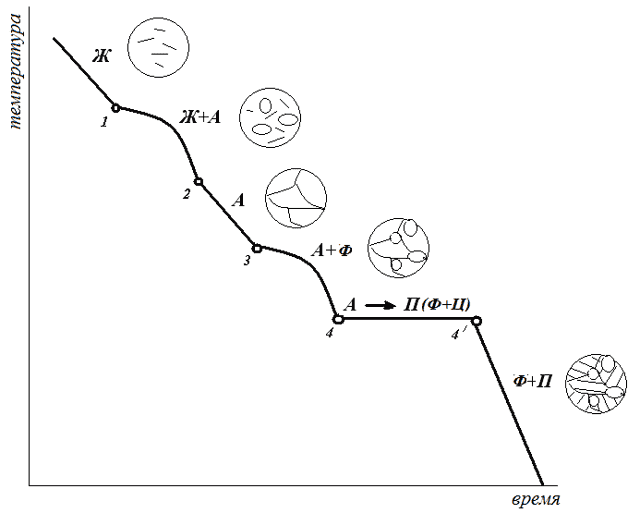
- Равновесная структура этого сплава – смесь феррита и перлита (рис. в начале)
- Количественное оотношение феррита и перлита можно определить следующим образом (и нарисовать схему структуры надо в соотвествии:
- Это только для доэвтектоидных стей
- 0,8 % С 100 % перлита
- 0,6 % С % перлита для данной марки стали
- –это столько перлита содержится в стали с 0,6 % углерода
Вычертите диаграмму состояния железо-цементит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 0,8 % С. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
Кривая охлаждения:
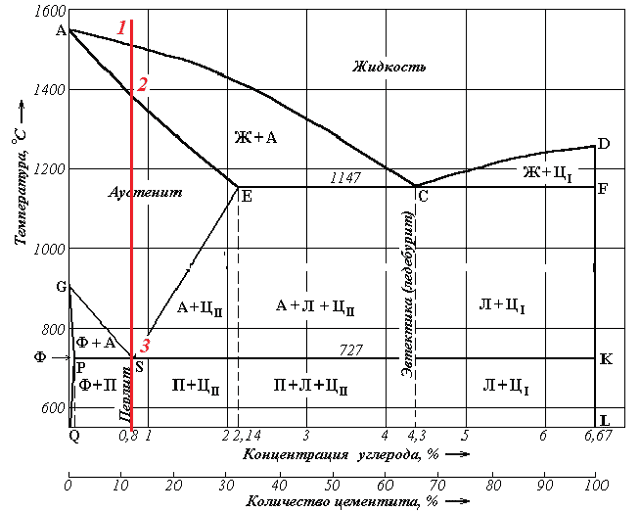
- Кривая охлаждения:
- Превращения, протекающие при охлаждении
- 1. Кристаллизация аустенита из жидкости Ж0,8 А0,8
- 2. Эвтектоидное превращение А0,8 П0,8 (Ф0,02 + Ц6,67)
- Сплав с содержанием углерода 0,8 % называется эвтектоидная сталь.
- Равновесная (окончательная) структура этого сплава – перлит (механическая смесь феррита и цементита).
Вычертите диаграмму состояния железоцементит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 1,0 % углерода. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
Кривая охлаждения
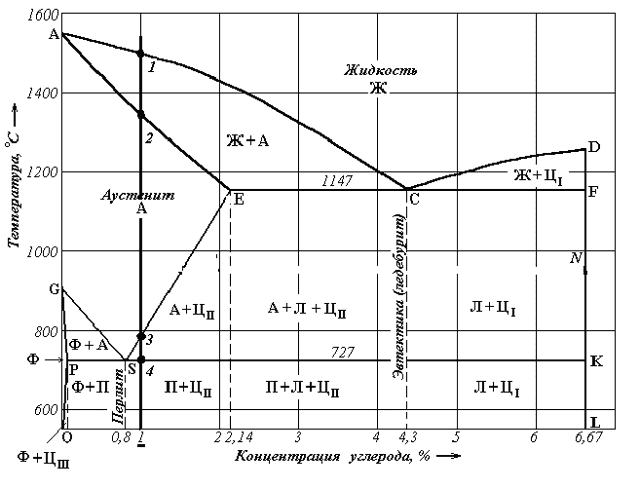
Кривая охлаждения
- Превращения, происходящие при охлаждении сплава от жидкого состояния до комнатной температуры
- 1. Кристаллизация аустенита из жидкости (от 1 до 2)
- Ж1,0 А1,0
- 2. Выделение избыточного цементита вторичного из аустенита (от 3 до 4)
- А1,0 А0,8+ Ц6,67
- 3. Эвтектоидное превращение (4–4/) А0,8 П0,8 (Ф0,02 + Ц6,67)
- Формирование структуры
- Т от 2 до 3 от3 до 4 сначала
- В интервале 4…4/ присмходит распад аустенита на (Ф-Ц)-смесь
- Сплав, содержащий 1,0% С – это заэвтектоидная сталь.
- Структура при комнатной температуре – перлит + цементит вторичный
- Структура после медленного охлаждения – перлит и цементит вторичный в виде сплошной цементитной сетки, что является брако
Здесь по правилу отрезков можно определить количественное соотношение перлита и цементита. За основу берётся отрезок РSК.
- Количество цементита =
- Здесь учтен весь цементит: в составе перлита + в виде вторичного
- Это мы рассматривали на практическом занятии
Вычертите диаграмму состояния железо-цементит, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения для сплава, содержащего 3,2 % углерода. Какова равновесная структура этого сплава при комнатной температуре и как такой сплав называется?
- Сплав, содержащий 3,2 % С называется доэвтектическим чугуном.
- Кривая охлаждения:
- Превращения, протекающие при охлаждении
- 1. Кристаллизация аустенита из жидкости Ж3,2А2,14
- 2. Кристаллизация из оставшейся жидкости эвтектики (ледебурита), состоящей из кристаллов аустенита и цементита Ж4,3 Л4,3 (А2,14 + Ц6,67)
- 3. Выделение избыточного цементита вторичного (ЦII) из аустенита
- А2,14 Ц6,67
- 4. Эвтектоидное превращение А0,8 П0,8 (Ф0,02 + Ц6,67)
- 5. Выделение избыточного цементита третичного (ЦIII) из феррита
- Ф0,02 Ц6,67
- Равновесная структура состоит из перлита (П), ледебурита (Л) и цементитаII (ЦII).
8.Строение слитков спокойной и кипящей стали.
Строение слитка зависит то t разливки стали, в линейной скорости разливки, скорости подъема, хим. состава стали.
- Слиток имеет неоднородное строение из-за большого количества зерен разных размеров и форм.
- В зависимости от степени раскисления выплавляют стали:
- а) спокойные,
- б) кипящие,
- в) полуспокойные.
Спокойная сталь получается при полном раскислении в печи и ковше. Спокойную сталь раскисляют сначала ферромарганцем, потом ферросилицием и заканчивают раскисление обычно алюминием при выпуске стали из печи. Этим достигается высокая степень раскисления, вследствие чего в течение процесса кристаллизации слитка спокойной стали не происходит бурного выделения газов.
Кипящая сталь раскислена в печи неполностью. Ее раскисление продолжается в изложнице при затвердевании слитка, благодаря взаимодействию оксида железа и углерода:
Образующийся оксид углерода выделяется из стали, способствуя удалению из стали азота и водорода, газы выделяются в виде пузырьков, вызывая её кипение. Кипящая сталь не содержит неметаллических включений, поэтому обладает хорошей пластичностью.
Легирование стали осуществляется введением ферросплавов или чистых металлов в необходимом количестве в расплав.
Легирующие элементы, у которых сродство к кислороду меньше, чем у железа ( ), при плавке и разливке не окисляются, поэтому их вводят в любое время плавки.
Легирующие элементы, у которых сродство к кислороду больше, чем у железа ( ), вводят в металл после раскисления или одновременно с ним в конце плавки, а иногда в ковш.
Дефекты и брак поковок могут быть следствием дефектов исходного металла, нагрева и дефектов, возникающих при ковке и штамповке из-за нарушения технологии и износа штампов.
Дефекты слитка. Сталь после выплавки в мартеновской печи отливается в специальные металлические формы — изложницы и в них застывает. Полученные таким образом слитки идут на дальнейшую обработку — прокатку и ковку.
Вследствие того, что условия застывания металла в разных частях слитка различные, его состав и свойства получаются неодинаковыми. В первую очередь застывает металл, который соприкасается с холодными стенками изложницы, и затем застывание идет в направлении к центральной и верхней частям слитка.
Строение металла поверхностных слоев слитка будет плотное, мелкозернистое, в центральной части кристаллы будут крупными. Сталь имеет различные составляющие, которые застывают при разной температуре.
Поэтому наибольшее количество легкоплавких составляющих, содержащих серу, фосфор, углерод и неметаллические частицы, будет находиться в центральной и верхней частях слитка.
Строение слитка зависит то t разливки стали, в линейной скорости разливки, скорости подъема, хим. состава стали.
- Слиток имеет неоднородное строение из-за большого количества зерен разных размеров и форм.
- В зависимости от степени раскисления выплавляют стали:
- а) спокойные,
- б) кипящие,
- в) полуспокойные.
Спокойная сталь получается при полном раскислении в печи и ковше. Спокойную сталь раскисляют сначала ферромарганцем, потом ферросилицием и заканчивают раскисление обычно алюминием при выпуске стали из печи. Этим достигается высокая степень раскисления, вследствие чего в течение процесса кристаллизации слитка спокойной стали не происходит бурного выделения газов.
Кипящая сталь раскислена в печи неполностью. Ее раскисление продолжается в изложнице при затвердевании слитка, благодаря взаимодействию оксида железа и углерода:
Образующийся оксид углерода выделяется из стали, способствуя удалению из стали азота и водорода, газы выделяются в виде пузырьков, вызывая её кипение. Кипящая сталь не содержит неметаллических включений, поэтому обладает хорошей пластичностью.
Легирование стали осуществляется введением ферросплавов или чистых металлов в необходимом количестве в расплав.
Легирующие элементы, у которых сродство к кислороду меньше, чем у железа ( ), при плавке и разливке не окисляются, поэтому их вводят в любое время плавки.
Легирующие элементы, у которых сродство к кислороду больше, чем у железа ( ), вводят в металл после раскисления или одновременно с ним в конце плавки, а иногда в ковш.
Дефекты и брак поковок могут быть следствием дефектов исходного металла, нагрева и дефектов, возникающих при ковке и штамповке из-за нарушения технологии и износа штампов.
Дефекты слитка. Сталь после выплавки в мартеновской печи отливается в специальные металлические формы — изложницы и в них застывает. Полученные таким образом слитки идут на дальнейшую обработку — прокатку и ковку.
Вследствие того, что условия застывания металла в разных частях слитка различные, его состав и свойства получаются неодинаковыми. В первую очередь застывает металл, который соприкасается с холодными стенками изложницы, и затем застывание идет в направлении к центральной и верхней частям слитка.
Строение металла поверхностных слоев слитка будет плотное, мелкозернистое, в центральной части кристаллы будут крупными. Сталь имеет различные составляющие, которые застывают при разной температуре.
Поэтому наибольшее количество легкоплавких составляющих, содержащих серу, фосфор, углерод и неметаллические частицы, будет находиться в центральной и верхней частях слитка.
1 — серединные кристаллы, имеющие различное направление; 2 — усадочная рыхлость и место наибольшего скопления неметаллических частиц; 3 — усадочные пустоты; 4 — мосты перемычки; 5 — усадочная раковина; 6 — кристаллы, имеющие вид мелких зерен; 7 — мелкие кристаллы, расположенные перпендикулярно к стенкам изложницы; 8 — крупные кристаллы, расположенные перпендикулярно к стенкам изложницы; 9 — крупные кристаллы, расположенные наклонно; 10 — кристаллы, имеющие вид крупных зерен
При разливке сильной струей сталь разбрызгивается, брызги попадают на холодные стенки изложницы и застывают. При прокатке или ковке застывшие брызги образуют плены, представляющие собой слои металла отделяющиеся от основной массы и не сваривающиеся с ней из-за пленки окислов.
От резкого охлаждения поверхности слитка и от подвисания слитка на поверхностях и выбоинах изложницы образуются продольные и поперечные трещины. Наличие в металле при заливке газов и неправильный режим заливки приводят к образованию в слитке подкорковых пузырей.
При отливке в металл могут попасть неметаллические включения, которые при дальнейшей обработке приводят к трещинам и волосовинам.
Рис. 87. Схема строения стального слитка.
9.Теория сплавов,понятия: система, сплав, компонент, фаза.
Сплав – вещество, полученное сплавлением нескольких элементов. Другими словами, сплав – это твердое вещество, обладающее всеми признаками металлов и состоящее из 2-х и более химических элементов.
Состоят из основы (одного или нескольких металлов), малых добавок специально вводимых в сплавлегирующих и модифицирующих элементов, а также из неудалённых примесей (природных, технологических и случайных).
Компонент – элемент или химическое соединение, входящее в состав сплава (элементы или химические соединения, образующие сплав). Компонент, преобладающий в сплаве количественно, называется основным. Компоненты, вводимые в сплав для придания ему нужных свойств, называются легирующими.
Фазовая составляющая (фаза) – однородная часть сплава, характеризующаяся определенным составом, свойствами, типом кристаллической решетки и отделенная от других частей сплава поверхностью раздела (при переходе через которую химический состав, структура, а, следовательно, свойства меняются скачкообразно).
Сплавы могут быть и однофазными и многофазными. Однофазные сплавы всегда состоят из кристаллов твердого раствора одного вида (состава).
В многофазных сплавах может одновременно присутствовать несколько структурных составляющих: 1) кристаллы твердого раствора (одного или нескольких составов), 2) кристаллы химических соединений, 3) кристаллы компонент сплава, 4) эвтектики и 5) эвтектоиды.
Основными структурами, составляющими железоуглеродистые сплавы, являются следующие.
Феррит – твердый раствор углерода в α-Fe. При температуре 723° С предельное содержание углерода 0,02 %. При отсутствии примесей не корродирует.
Цементит – карбид железа Fe3C – химическое соединение, содержащее 6,67 % углерода. Является составной частью эвтектической смеси, а также самостоятельной структурной составляющей. Способен образовывать твердые растворы путем замещения атомами других металлов, неустойчив, распадается при термической обработке. Цементит очень тверд (НВ 800) и хрупок.
Аустенит – твердый раствор углерода в γ–Fe. Атомы углерода внедряются в кристаллическую решетку, причем насыщение может быть различным в зависимости от температуры и примесей. Устойчив только при высокой температуре, а с примесями Mn, Сг – при обычных, даже низких температурах. Твердость аустенита НВ 170…220.
Перлит – эвтектоидная смесь феррита и цементита, образуется при распаде аустенита при температуре 723° С и содержании углерода 0,83 %. Примеси Si и Мn способствуют образованию перлита и при меньшем содержании углерода. Твердость перлита НВ 160…260. Структура перлита может быть пластинчатой и глобулярной (зернистой).
Ледебурит – эвтектическая смесь аустенита и цементита, образующаяся при 1130° С и содержании углерода 4,3 % Структура неустойчивая: при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит. Ледебурит очень тверд (НВ 700) и хрупок.
Графит – мягкая и хрупкая составляющая чугуна, состоящая из разновидностей углерода. Встречается в серых и ковких чугунах.
1. В жидком состоянии компоненты сплава обычно неограниченно растворяются друг в друге, образуя жидкие растворы.
Конспект урока "Кристаллизация металлов и сплавов"
Лекция
№ 3
Тема:
Кристаллизация металлов и сплавов. Кривая охлаждения «Fe».
- Цель:изучить
механизм и закономерности кристаллизации; рассмотреть строение металлического
слитка, научиться строить кривые охлаждения. - Основные
понятия: - ·
Фактическая
температура кристаллизации - ·
Кристаллизация - ·
Аллотропия - План лекции:
1. Кристаллизация
металлов и сплавов.
2. Механизм и
закономерности кристаллизации металлов.
3. Условия
получения мелкозернистой структуры.
4. Строение
металлического слитка.
5. Кривая
охлаждения железа.
6.
Вывод.
1. Кристаллизация
металлов и сплавов.
Любое
вещество может находиться в трех агрегатных состояниях: твердом, жидком,
газообразном. Возможен переход из одного состояния в другое, если новое
состояние в новых условиях является более устойчивым, обладает меньшим запасом
энергии.
С
изменением внешних условий свободная энергия изменяется по сложному закону
различно для жидкого и кристаллического состояний. Характер изменения свободной
энергии жидкого и твердого состояний с изменением температуры показан на рис.
1.
Рис.1.
Изменение свободной энергии в зависимости от температуры
В
соответствии с этой схемой выше температуры ТS вещество должно
находиться в жидком состоянии, а ниже ТS – в твердом.
При
температуре равной ТS жидкая и твердая фаза обладают одинаковой
энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы
могут существовать одновременно бесконечно долго. Температура ТS –
равновесная или теоретическая температура кристаллизации.
Для
начала процесса кристаллизации необходимо, чтобы процесс был термодинамически
выгоден системе и сопровождался уменьшением свободной энергии системы. Это
возможно при охлаждении жидкости ниже температуры ТS. Температура,
при которой практически начинается кристаллизация называется реальная
температурой кристаллизации.
- Охлаждение
жидкости ниже равновесной температуры кристаллизации называется
переохлаждением, которое характеризуется степенью переохлаждения: - Степень
переохлаждения зависит от природы металла, от степени его загрязненности (чем
чище металл, тем больше степень переохлаждения), от скорости охлаждения (чем
выше скорость охлаждения, тем больше степень переохлаждении). - Рассмотрим
переход металла из жидкого состояния в твердое.
При
нагреве всех кристаллических тел наблюдается четкая граница перехода из
твердого состояния в жидкое. Такая же граница существует при переходе из
жидкого состояния в твердое.
Кристаллизация – это
процесс образования участков кристаллической решетки в жидкой фазе и рост
кристаллов из образовавшихся центров.
Кристаллизация
протекает в условиях, когда система переходит к термодинамически более
устойчивому состоянию с минимумом свободной энергии.
Процесс
перехода металла из жидкого состояния в кристаллическое можно изобразить
кривыми в координатах время – температура. Кривая охлаждения чистого металла
представлена на рис. 2.
Рис.2.
Кривая охлаждения чистого металла
- –
теоретическая температура кристаллизации; - –
фактическая температура кристаллизации. - Процесс
кристаллизации чистого металла:
До
точки 1 охлаждается металл в жидком состоянии, процесс сопровождается плавным
понижением температуры.
На участке 1 – 2 идет процесс кристаллизации,
сопровождающийся выделением тепла, которое называется скрытой теплотой
кристаллизации. Оно компенсирует рассеивание теплоты в пространство, и поэтому
температура остается постоянной.
После окончания кристаллизации в точке 2
температура снова начинает снижаться, металл охлаждается в твердом состоянии.
2. Механизм и
закономерности кристаллизации металлов.
При
соответствующем понижении температуры в жидком металле начинают образовываться
кристаллики – центры кристаллизации или зародыши. Для начала их роста
необходимо уменьшение свободной энергии металла, в противном случае зародыш
растворяется.
Минимальный
размер способного к росту зародыша называется критическим размером,
а зародыш – устойчивым.
Переход
из жидкого состояния в кристаллическое требует затраты энергии на образование
поверхности раздела жидкость – кристалл. Процесс кристаллизации будет
осуществляться, когда выигрыш от перехода в твердое состояние больше потери
энергии на образование поверхности раздела. Зависимость энергии системы от
размера зародыша твердой фазы представлена на рис. 3.
Зародыши
с размерами равными и большими критического растут с уменьшением энергии и
поэтому способны к существованию.
Рис.3.
Зависимость энергии системы от размера зародыша твердой фазы
Механизм
кристаллизации представлен на рис.4.
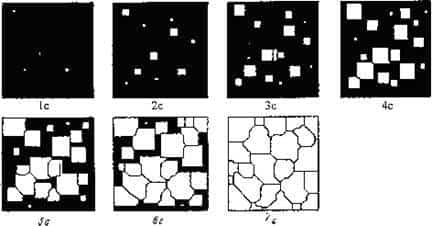
Рис.4.
Модель процесса кристаллизации
Центры
кристаллизации образуются в исходной фазе независимо друг от друга в случайных
местах. Сначала кристаллы имеют правильную форму, но по мере столкновения и срастания
с другими кристаллами форма нарушается. Рост продолжается в направлениях, где
есть свободный доступ питающей среды. После окончания кристаллизации имеем
поликристаллическое тело.
Качественная
схема процесса кристаллизации может быть представлена количественно
кинетической кривой (рис.5).
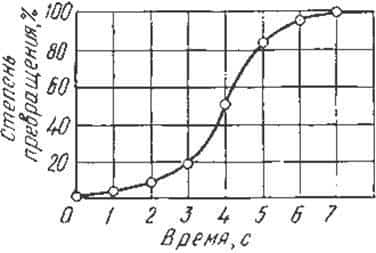
Рис.5.
Кинетическая кривая процесса кристаллизации
Процесс
вначале ускоряется, пока столкновение кристаллов не начинает препятствовать их
росту. Объем жидкой фазы, в которой образуются кристаллы, уменьшается. После
кристаллизации 50 % объема металла, скорость кристаллизации будет замедляться.
Таким
образом, процесс кристаллизации состоит из образования центров кристаллизации и
роста кристаллов из этих центров.
В
свою очередь, число центров кристаллизации (ч.ц.) и скорость роста кристаллов
(с.р.) зависят от степени переохлаждения (рис. 6).
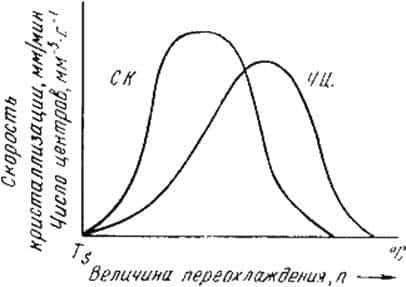
Рис.
6. Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б)
от степени переохлаждения
Размеры
образовавшихся кристаллов зависят от соотношения числа образовавшихся центров
кристаллизации и скорости роста кристаллов при температуре кристаллизации.
При
равновесной температуре кристаллизации ТS число образовавшихся
центров кристаллизации и скорость их роста равняются нулю, поэтому процесса
кристаллизации не происходит.
Если
жидкость переохладить до температуры, соответствующей т.а, то образуются
крупные зерна (число образовавшихся центров небольшое, а скорость роста –
большая).
При
переохлаждении до температуры соответствующей т.в – мелкое зерно (образуется
большое число центров кристаллизации, а скорость их роста небольшая).
Если
металл очень сильно переохладить, то число центров и скорость роста кристаллов
равны нулю, жидкость не кристаллизуется, образуется аморфное тело. Для
металлов, обладающих малой склонностью к переохлаждению, экспериментально
обнаруживаются только восходящие ветви кривых.
3. Условия
получения мелкозернистой структуры.
Стремятся
к получению мелкозернистой структуры. Оптимальными условиями для этого
являются: максимальное число центров кристаллизации и малая скорость роста
кристаллов.
- Размер
зерен при кристаллизации зависит и от числа частичек нерастворимых примесей,
которые играют роль готовых центров кристаллизации – оксиды, нитриды, сульфиды. - Чем
больше частичек, тем мельче зерна закристаллизовавшегося металла. - Стенки
изложниц имеют неровности, шероховатости, которые увеличивают скорость
кристаллизации. - Мелкозернистую
структуру можно получить в результате модифицирования, когда в жидкие металлы
добавляются посторонние вещества – модификаторы, - По
механизму воздействия различают:
1. Вещества,
не растворяющиеся в жидком металле – выступают в качестве дополнительных центров
кристаллизации.
2. Поверхностно
— активные вещества, которые растворяются в металле, и, осаждаясь на
поверхности растущих кристаллов, препятствуют их росту.
4. Строение
металлического слитка.
Схема
стального слитка, данная Черновым Д.К., представлена на рис.7.
Рис.
7. Схема стального слитка
- Слиток
состоит из трех зон: - 1. мелкокристаллическая
корковая зона; - 2. зона
столбчатых кристаллов;
3. внутренняя
зона крупных равноосных кристаллов.
Кристаллизация
корковой зоны идет в условиях максимального переохлаждения. Скорость
кристаллизации определяется большим числом центров кристаллизации. Образуется
мелко
зернистая
структура.
Жидкий
металл под корковой зоной находится в условиях меньшего переохлаждения. Число
центров ограничено и процесс кристаллизации реализуется за счет их интенсивного
роста до большого размера.
Рост
кристаллов во второй зоне имеет направленный характер. Они растут
перпендикулярно стенкам изложницы, образуются древовидные кристаллы – дендриты
(рис. 8). Растут дендриты с направлением, близким к направлению теплоотвода.
Рис.8.
Схема дендрита по Чернову Д.К.
- Так
как теплоотвод от незакристаллизовавшегося металла в середине слитка в разные
стороны выравнивается, то в центральной зоне образуются крупные дендриты со
случайной ориентацией. - Зоны
столбчатых кристаллов в процессе кристаллизации стыкуются, это явление
называется транскристаллизацией. - Для
малопластичных металлов и для сталей это явление нежелательное, так как при
последующей прокатке, ковке могут образовываться трещины в зоне стыка. - В
верхней части слитка образуется усадочная раковина, которая подлежит отрезке и
переплавке, так как металл более рыхлый (около 15…20 % от длины слитка) - Методы
исследования металлов: структурные и физические
Металлы
и сплавы обладают разнообразными свойствами. Используя один метод исследования
металлов, невозможно получить информацию о всех свойствах. Используют несколько
методов анализа.
5. Аллотропия
или полиморфные превращения.
- Способность
некоторых металлов существовать в различных кристаллических формах в
зависимости от внешних условий (давление, температура) называется аллотропией
или полиморфизмом. - Каждый
вид решетки представляет собой аллотропическое видоизменение или модификацию. - Примером
аллотропического видоизменения в зависимости от температуры является железо
(Fe). - Fe:
– ОЦК — ; - – ГЦК — ;
- – ОЦК — ;
(высокотемпературное )
Превращение
одной модификации в другую протекает при постоянной температуре и
сопровождается тепловым эффектом. Видоизменения элемента обозначается буквами
греческого алфавита в виде индекса у основного обозначения металла.
Примером
аллотропического видоизменения, обусловленного изменением давления, является
углерод: при низких давлениях образуется графит, а при высоких – алмаз.
Используя
явление полиморфизма, можно упрочнять и разупрочнять сплавы при помощи
термической обработки.
6. Кривая
охлаждения железа.
Порядковый
номер железа в таблице Менделеева – 26, атомная масса — A= 55,85 а.е.м.
(атомные единицы массы). Радиус атома — R = 1,27А. Температура плавления — Тпл
= 15390С. Плотность – 7,68 г/см3.
Железо
существует в двух аллотропических модификациях: объемноцентрированного куба (Fea) и
гранецентрированного куба (Feg). Из кривой охлаждения чистого железа
(рис.9) видно, что Fea
существует в двух интервалах температур : ниже 9110С и от 1392 до
15390С.
Достигнув при охлаждении температуры 13920С, Fea претерпевает
аллотропическое превращение, в процессе которого кристаллическая решетка
объемно-центрированного куба при постоянной температуре перестраивается в
решетку гранецентрированного куба Feg.
Второе
аллотропическое превращение в процессе охлаждения происходит при температуре
9110С, когда Feg (решетка гранецентрированного
куба) перестраивается в объемноцентрированную кубическую решетку Fea.
При температуре 7680С, называемой точкой Кюри, железо испытывает
магнитное превращение: ниже 7680С железо становится магнитным.
Магнитное превращение есть особый вид превращения и имеет ряд особенностей,
отличающих его от аллотропического превращения.
1. Вывод.
В
жидком металле атомы находятся в состоянии непрерывного движения и в их
расположении нет такого порядка, как в твердом металле.
При
переходе металла из жидкого состояния в твердое происходит кристаллизация.
Основы
теории кристаллизации разработаны основоположником науки материаловедения Д.
,К. Черновым.
ПОИСК
| Рис. 7. Кривая охлаждения металла при неизменном агрегатном состоянии и состоянии аллотропных переходов. |
| Рис. 1. Кривые охлаждения металла (I) и стекла (2) |
| Рис. 8. Кривая охлаждения металла, который переходит из расплавленного в твердое состояние. На отрезках аЬ и св, температура уменьшается монотонно на отрезке Ъс металл затвердевает, и температура остается почти постоянной. |
Диаграммы плавкости для металлов, образующих непрерывные твердые растворы, строятся по методике, разобранной для эвтектических сплавов. На кривых охлаждения в этом случае площадок не наблюдается, а существуют лишь точки перегиба для начала и конца кристаллизации. Растущий кристалл твердого раствора в среде жидкого раствора в зависимости от температуры меняет свой состав и постепенно приближается к составу твердого раствора в конце кристаллизации, что соответствует составу взятого сплава. На рис. 128 показан этот процесс, а также построение диаграммы плавкости Си—N1 по кривым охлаж- [c.248]
Кривые охлаждения сплавов, представленные на рис. 92, бив, отличаются от кривых охлаждения металла. Так, например, если сплав представляет собой твердый раствор одного компонента в другом, кривая охлаждения изменяет свой наклон в двух точках, отвечающих температурам (начало кристаллизации) и t2 (конец кристаллизации) (рис. 92, в). На протяжении всего времени кристаллизации сплава происходит медленное охлаждение его. Замедление охлаждения сплава в интервале времени от Т1 до %2 связано, как и для чистого металла, с выделением теплоты кристаллизации, а отсутствие горизонтального участка на кривой охлаждения объясняется тем, что в отличие от чистого металла состав жидкой фазы системы не совпадает с составом твердого сплава . [c.272]
Сплавы никеля и меди, широко применяемые в промышленности, — пример систем, образующих непрерывный ряд твердых растворов. На рис. УН-4 слева показаны кривые охлаждения металлов и расплавов. При охлаждении чистой расплавленной меди на кривой температура — время наблюдается пологий ход, начиная с того [c.276]
Диаграммы плавкости для металлов, о б р а-зующих непрерывные твердые раство р ы, строятся по методике, разобранной для эвтектических сплавов. На кривых охлаждения в этом случае площадок не наблюдается, а сущест- [c.274]
Кривая охлаждения представляет собой графическое изображение зависимости температуры системы от времени при охлаждении (рис. 58). Кривая I отвечает процессу затвердевания чистого металла. Из рисунка видно, что сначала температура плавно понижается, этот участок кривой соответствует жидкому состоянию металла.
Начало образования твердой фазы сопровождается появлением на кривой резкого излома (участок Ьс). При кристаллизации расплава температура остается постоянной. Затем происходит дальнейшее плавное охлаждение (участок сё).
Изменение агрегатного состояния металла (жидкое — твердое) при определенной постоянной температуре объясняется выделением скрытой теплоты плавления в процессе кристаллизации. [c.133]
Иногда остановки в падении температур[-1 наблюдаю ся и иа кривой охлаждения твердого металла, указывая иа связанные с выделением теплоты процессы, происходящие уже в твердом веществе, например, переход из одиой кристаллической формы В другую. [c.544]
Если охлаждению подвергают смесь, состоящую из 83% РЬ и 17% 5Ь (кривая охлаждения 3 на рис. 65), то состав образующейся твердой массы (точка Е) представляет собой чистую эвтектику. При других соотношениях металлов к эвтектике будут примешаны ранее выпавшие более крупные кристаллы 5Ь или РЬ. [c.217]
Для получения кривой охлаждения какого-либо сплава или чистого металла последний помещают в тигель из огнеупорного материала, засыпают порошкообразным углем (во избежание окисления поверхности расплавленного металла) и расплавляют в муфельной печи. [c.114]
На рис. 12.4 слева показано, какой вид имеет кривая охлаждения чистого расплавленного металла. Сначала понижение температуры плавно идет по кривой ак.
В точке к происходит перелом кривой, начинается образование твердой фазы (кристаллизация), сопровождающееся выделением теплоты, вследствие чего температура некоторое время остается постоянной (кривая идет параллельно оси абсцисс).
Когда вся масса расплавленного металла затвердеет, опять начинается плавное понижение температуры по кривой сЬ. [c.346]
Из сопоставления кривых охлаждения 2, 3, 5 п 6 видно, что процесс кристаллизации сплавов не происходит при какой-то одной постоянной температуре, а захватывает определенный интервал температур.
При этом начало кристаллизации сплавов различного состава наблюдается при различных температурах окончательное отвердевание их происходит при одной и той же температуре (140°С). Исключение представляет кривая охлаждения сплава 4. Она имеет такую же форму, как и у чистых металлов.
При охлаждении такого сплава вплоть до температуры 140°С кристаллизация не происходит. При 140° С из жидкой фазы в виде кристаллов одновременно начинают выпадать оба компонента, причем состав выпадающей твердой фазы одинаков с составом жидкого сплава.
По этой причине процесс кристаллизации от начала до конца происходит при постоянной температуре (как у чистых металлов). Этот сплав, обладающий наиболее низкой температурой кристаллизации, называется эвтектическим. [c.190]
Несколько иной вид имеет кривая охлаждения сплава двух металлов. Такая кривая изображена на рис. 12.4 справа. Точка к, как и на первой кривой, [c.346]
Если какое-либо чистое вещество (металл, соль, органическое соединение) нагреть до температуры в точке а, лежаш,ей выше точки его плавления, а затем записывать кривую охлаждения, то вначале падение температуры от времени будет выражаться плавной кривой аЬ (кривая 2). В некоторый момент времени в точке Ь понижение температуры прекратится. На кривой появляется го- [c.225]
Диаграммы плавкости строят при помощи кривых охлаждения. Кривая охлаждения чистого металла приведена на рис. 92, а. Гори- [c.272]
Диаграммы плавкости строят с помощью кривых охлаждения. Кривая охлаждения чистого металла приведена на рис. IX.6, а.
Горизонтальный участок прямой соответствует температуре плавления или затвердевания (кристаллизации) металла. Температура металла в процессе кристаллизации остается постоянной.
Как только исчезает жидкая фаза (т — начало кристаллизации, тг — конец кристаллизации), охлаждение продолжается с обычной скоростью. [c.249]
Кривая охлаждения расплава, состоящего из двух металлов, имеет другой вид (см. рис. 58, кривая II). В начале охлаждения кривая падает, как в случае одного металла (участок аЬ). Затем достигается температура, при которой расплав становится насыщенным относительно одного металла.
В результате этого металл начинает кристаллизоваться. Выделяющаяся скрытая теплота плавления несколько замедляет охлаждение системы.
Поэтому кривая II дает излом (участок Ьс) и дальше идет не горизонтально, а постепенно понижается, поскольку по мере выпадения кристаллов одного металла расплав обогащается другим металлом. Наконец, наступает такой момент, когда расплав делается насыщенным относительно обоих металлов, т. е.
достигает эвтектического состава. Эвтектика выделяется при постоянной температуре. На кривой II этому процессу соответствует горизонтальный участок ей. После того как весь расплав закристаллизуется, кривая падает (участок е). [c.134]
Подвергая таким образом расплав из двух металлов равномерному охлаждению в определенном температурном интервале и отображая этот процесс в прямоугольной системе координат температура — время, получают кривую охлаждения сплава. Имея ряд кривых охлаждения, можно построить диаграмму плавкости данной системы. [c.134]
Общие свойства металлов. Сплавы. Физико-химический анализ. Кривые охлаждения. Диаграмма плавкости. Эвтектика. Твердые растворы. Интерметаллические соединения. [c.167]
Используя полученные кривые охлаждения сплавов известного состава, а также кривые чистых металлов, проектируют на ось ординат температуры начала и окончания кристаллизации взятых образцов.
Таким путем на диаграмме пл — состав получают ряд точек А, 2, 3, Е, 5, 6, В. Их соединяют плавными линиями АЕ и ВЕ. Поскольку температуры окончания кристаллизации всех сплавов одинаковы, то проекции их лежат на одной прямой СО.
Эта линия, отвечающая температурам полного отвердевания, называется линией солидуса. [c.191]
Конечной целью этой работы является нахождение диаграммы состояния для пары металлов. Для этого необходимо получить кривые охлаждения ряда сплавов этих металлов различного состава, что и составляет экспериментальную часть работы. [c.67]
Затем, установив по форме кривых охлаждения сплавов, к какому типу диаграммы состояния относится исследуемая пара металлов, строят градуировочную кривую для термопары (см. выше>, находят по ней истинные значения температур, соответствующих точкам перегиба, и строят диаграмму температура — состав для данной пары металлов. [c.70]
Если расплав мышьяка и свинца эвтектического состава охлаждать, то температура снижается с постоянной скоростью до тех пор, иока не будет достигнута эвтектическая температура 290° затем жидкость кристаллизуется в твердый эвтектический сплав, причем температура остается постоянной до завершения кристаллизации. В соответствии с этим кривые охлаждения для эвтектических составов напоминают аналогичные кривые для чистых металлов. Эвтектика имеет постоянную точку плавления точно так же, как и любое из чистых элементарных веществ. [c.412]
ВНОСИТ большие затруднения и не позволяет применять к ним динамические методы. Если к металлам можно применять как метод кривых нагревания, так и метод кривых охлаждения, то в случае силикатов Егер исключает применение кривых охлаждения. Кривые же нагревания можно использовать в определенных специфических условиях. [c.370]
Хаза нов Е. И., Легкие металлы, КЬ 1, 45 (1935), Метод кривые охлаждения. Вес. %, [c.557]
Иногда остановки в падении температуры наблюдаются и на кривой охлаждения твердого металла, указывая на связанные [c.544]
Несколько иной вид имеет кривая охлаждения сплава двух металлов. Такая кривая изображена на рис. 145 справа. Точка , как н на первой кривой, отвечает началу затвердевания — началу выделения из сплава кристаллов одного из входящих в него металлов, При этом состав остающегося жидким сплава изменяется [c.544]
Диаграммы состояния получают экспериментально. Обычно для этого строят кривые охлаждения и по остановкам и перегибам на них, вызванным тепловыми эффектами превращений, определяют температуры этих преврав1ений. Для получения кривых охлаждения приготовляют из двух металлов изучаемой системы ряд смесей различного состава.
Каждую из приготовленных смесей расплавляют. Получающиеся жидкие сплавы (расплавы) медленно охлаждают, отмечая через определенные промежутки времени температуру остывающего сплава. По данным наблюдений строят кривые охлаждения, откладывая на оси абсцисс время, а на оси ординат — температуру (рис. 12.4). [c.
346]
Кривые охлаждения чистых металлов висмута и кадмия, а также их сплавов изображены на рис. 32. Кривая / характеризует охлаждение чистого висмута. Вначале температура равномерно понил< ается (происходит охлаждение расплавленного висмута).
При температуре 27ГС висмут начинает кристаллизоваться температура при этом остается постоянной (несмотря на продолжающееся охлаждение) вследствие выделения энергии кристаллической решетки. Постоянство температуры при отвердевании связано с безвариантностью системы.
В дан- [c.188]
Для получения кривой охлаждения какого-либо сплава или чистого металла последний помещают в тигель из огнеупорного материала, засыпают порошкообразным углем и расплавляют. Затем тигель с расплавом переносят в термостат и погружают в расплав термопару.
Термопара должна быть укреплена таким образом, чтобы кожух ее не касался стенок и дна тигля, так как в противном случае охлаждение не будет равномерным и на кривой могут быть обнаружены замедления и остановки, вызванные превращениями, происходящими в материале тигля.
Однако, конец кожуха термопары должен быть на 1 — 1,5 см погружен в металл, иначе прибор будет недостаточно чувствителен. После этого тигель покрйвают несколькими слоями асбеста и приступают к ежеминутной записи показаний присоединенного к термопаре милливольтметра.
После окончательного затвердевания исследуемого сплава запись прекращают, удаляют термопару (для этого необходимо расплавить металл) и проводят такой же опыт со сплавом другого состава. [c.69]
Так как в системе имеются две фазы (жидкая и твердая) и один компонент, то число степеней свободы равно нулю, т. е. температура постоянна до тех пор, пока система двухфазна.
После того как весь расплавленный висмут отвердеет, температура снова начинает понижаться — остывает отвердевший металл. Кривая охлаждения 7 чистого кадмия (темп. пл.
321° С) подобна по форме кривой охлаждения висмута. [c.192]
Из всех кривых охлаждения особого внимания заслуживает четвертая по форме она подобна кривой охлаждения чистого металла. Сплав, соответствующий этой кривой, называется эвтектическим.
Эвтектическим сплавом или эвтектикой называется сплав, обладающий самой низкой температурой отвердевания плавления) из всех сплавов, которые образуют данные металлы.
При застывании эвтектического сплава оба металла выделяются одновременно, сплав отвердевает как единое целое и состав жидкой фазы одинаков с составом твердой фазы. Эвтектический сплав огвердевает от начала до конца при постоянной температуре, т. е. как чистый металл . [c.192]
Температуру плавления платины используют для установления новой свечи, которая выбрана в качестве единицы света вместо свечи Гефнера.
Ее определяют оптическим пирометром по кривой охлаждения физически чистой платины при температуре, близкой температуре плавления.
Металл, подлежащий плавлению при высокочастотном обогреве, загружают в тигель из ТЬОг, помещенный в свою очередь в узкую трубку из ТЬОг Дно тигля, покрытое порошком ТЬОгГ визируется в качестве черного тела [233]. [c.114]
Иная картина получайся для кривой охлаждения в том случае, если сплав ишеняет свой состав при охлаждении, как это имеет место для сплавов олова и свшща, за исключением эвтектического сплава.
В этом случае температура затвердевания во время кристаллизации понижается Поэтому кристаллизация может здесь идти лишь при охлаждеййй сплава, Однако теплота, выделяющаяся при кристаллизации, уменьшает скорость охлаждения. Вследствие этого кривая охлаждения такого сплава nMeei не остановку, а лишь точку перегиба (точка К на кривой б рис. 105).
Только после того как расплав приобретет эвтектический состав, на кривой охлаждения обозначится остановка, так как кристаллизация остав- шегося еще жидкого расплава будет после этого протекать нри постоянной температуре. Длина горизонтального отрезка кривой охлаждения, т. е.
продолжительность эвтектической остановки, дает возмоншость судить о количестве эвтектики в затвердевшем сплаве. Кривая затвердевания сплава, состав которого с самого начала соответствовал эвтектике, имеет вид, подобный кривой затвердевания простого металла. [c.611]






