Цвета побежалости – спектр цветов, образующихся на поверхности железных сплавов в результате появления окисной пленки. Они образуются при нагревании поверхностей из металла до определенных температур без участия воды. Цвета побежалости являются дефектом сварного соединения.
Происхождение
В природе цвета побежалости образуются на поверхности многих минералов, включая пирит и халькопирит. Из-за окисления они покрываются тонкой оксидной пленкой, преломляющий солнечный свет. В результате интерференции поверхности металла окрашивается в разные цвета.
Яркость побежалости зависит от толщины оксидной пленки и длины волны. Наиболее яркие цвета побежалости образуются на медных минералах. Также цвет зависит от качественного состава металла. Если в элементе присутствует большое количество ионов металлов, то он окрашивается в синие цвета.
При наличии хромофоров минералы становятся красными.

Также цвета побежалости могут образовывать в естественных условиях на поверхностях старых стекол или монет. Изменение окраса может быть обусловлено длительным контактом этих материалов с землей.
Если на них присутствует жировая пленка, то они окрашиваются в радужный цвет. Побежалость скрывает настоящий цвет металла. Поэтому нельзя определять его истинный окрас на свежем изломе.
Рекомендуется определять цвет при рассмотрении оксидной пленки.
Искусственно цвета побежалости образуются на поверхности металлических заготовок при сварке или закалке. Они появляются при нагревании металлов до критических температур без участия молекул воды или иных жидкостей. Во время нагревания происходит процесс образования оксидной пленки.
Ее толщина составляет несколько молекул и уменьшается по мере нагрева. Это обусловлено явлением диффузии – процессом проникновения мельчайших частиц одного химического элемента в другой. В данном случае происходит взаимодействие атомов металла и кислорода.
На углеродистых сталях пленки из оксидов возникают быстрее, чем на легированных.
Процедура покрытия стали и железа слоем оксидной пленки называется воронением. После проведения этой процедуры повышается коррозийная стойкость изделия. Обработанные детали не покрываются ржавчиной. Процедура воронения позволяет придать изделию окрас, даже если металлическая поверхность по условиям эксплуатации не подлежит покраске.
Во время воронения заготовку протирают минеральным маслом и нагревают на железном листе. После выгорания масляной жидкости на заготовке появляются цвета побежалости. Для нужного окраса необходимо нагреть деталь до соответствующей температуры. Получившийся слой окисла является влагоустойчивым и не подвергается воздействию воздуха.
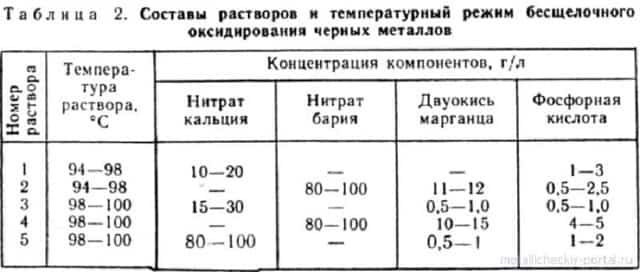
На скорость образования окисных пленок влияют следующие факторы:
- Структура поверхности: закаленные детали окисляются с большей скоростью.
- Загрязненность изделия: поверхности, покрытые маслом, при длительном нагреве обугливаются, что приводит к возникновению сажи. По этой причине образуется неровная и тонкая оксидная пленка.
- Наличие шероховатостей: если нагревается заготовка с шершавой поверхностью, то оксидная пленка получается плотной. Если перед процедурой термообработки отполировать деталь, то образуется тонкая пленка из оксидов.
- Оборудование для нагрева: если при термообработке применяются специальные нагревательные печи, способные поддерживать устойчивую температуру, то окисная пленка будет плотной. В бытовых условиях можно также использовать духовые шкафы, газовые горелки или металлургические печи (горны).
Тонкие оксидные пленки поглощают световые волны с меньшей длиной волны, но отражают – с большей. Цвет металлических деталей меняется в зависимости от температуры и плотности оксидной пленки. Чем толще оксидная пленка, тем светлее окраска. Синий или фиолетовый цвет получается, когда из спектра отражаются наиболее длинные волны.
Если пленка из оксидов отражает волны с малой длиной волны, то металлическая поверхность становится желтой. Светлые цвета соответствуют высокой температуре нагрева, светлые – более низкой.
По этой причине многие мастер часто определяют при помощи цветов побежалости степень закалки изделий, стальной стружки и режущих инструментов, применяемых во время проведения токарных работ.
Несмотря на эти факторы, при помощи цветов побежалости нельзя точно определить температуру металла, потому что на величину этого показателя оказывают влияние следующие факторы:
- время нагрева: промежуток времени, в течение которого металлическая деталь нагревается до температуры окружающей среды при отсутствии теплоотдачи.
- наличие различных примесей в составе металла;
- особенности освещения в помещении, где проводилась сварка или закалка заготовок;
- скорость разогревания: изменение температуры изделия в единицу времени при его нагревании.
В современной промышленности контроль температуры производится при помощи специальных приборов – пирометров. Они оснащены специальными датчиками, определяются степень нагрева заготовки при помощи лазера.

Цвета побежалости используются при изготовлении рабочих инструментов, лазерной маркировке и внешней обработке изделий из железа, меди, алюминия и латуни.
Если требуется изготовить инструментарии с высокой плотностью (бритвенные лезвия, предметы для проведения хирургических операций, режущие кромки резцов и грабштихели), то побежалость должна быть яркого цвета: красного, оранжевого или желтого.
До пурпурных и зеленых тонов нагревают инструменты, применяющихся в деревообрабатывающем секторе. Для достижения упругости при изготовлении пил, ножей, вил и пружин необходимо нагреть заготовки до появления синих или черных цветов.
В процессе нагревания металлическая заготовка становится гибкой, что позволяет мастеру придать ей необходимую форму. После данного процесса изделие закаляется при определенных температурах.
Согласно рекомендациям специалистов, оптимальной температурой для закалки металлов является 700–800 °C. В этом случае изделие окрашивается в разные оттенки красного или розового цветов. При превышении этих значений на 300 °C заготовка становится оранжевой или желтой.
При больших температурах происходит перекал, что негативно сказывается на прочности изделия.
Закалка улучшает следующие параметры металлической поверхности:
- Твердость: этот показатель является номинальным. Он прописан в шкале Роквелла и измеряется в HRC. Твердость определяет степень сопротивляемости металла к механическим повреждениям. На мягких изделиях при длительном соприкосновении с иными поверхностями остаются следы, что ухудшает их режущие свойства. Твердость ножей европейского образца составляет 60 HRC, азиатских – 70 HRC.
- Упругость: данный параметр определяет степень деформации металла при изгибах и ударах. Если сталь закалена, при изгибе на 10–30° она вернется в исходное положение. При перегреве снижается упругость поверхности, что приводит к поломке инструментов.
- Износостойкость: данный критерий показывает общую стойкость металла (сопротивление абразивному износу, стойкость к большим нагрузкам). При правильной закалке изделие сможет стабильно функционировать в течение более длительного срока.
После закалки заготовка приобретает высокую твердость. Для восстановления ее прочности необходимо провести процедуру отпуска, представляющую собой повторную термообработку детали.
Металлическое изделие нагревается до более низких температур и охлаждается. Между закалкой и охлаждением также осуществляется полное остывание металлической поверхности при помощи его погружения в раствор соли или в масло.
При выборе отпуска необходимо учитывать следующие особенности:
- Для изделий, подвергающимся деформациям или ударным нагрузкам, нужно использовать высокотемпературный отпуск: до 700 °C.
- Для легких клинков используется среднетемпературный отпуск: до 500 °C.
- Для обеспечения оптимальной твердости применяется низкотемпературный отпуск: до 250 °C. Но в этом случае изделие не сможет выдерживать высокие ударные нагрузки и будет легко деформироваться.

Температура цветов побежалости и каления
Во время отпуска возникают цвета каления. По ним можно определить, до какой температуры нагрелась заготовка. В отличие от побежалости, цвета каления меняются в процессе охлаждения металлической поверхности. Переход между цветами осуществляется в строгой последовательности, но с быстрой скоростью, поэтому мастер должен тщательно контролировать процесс термообработки.
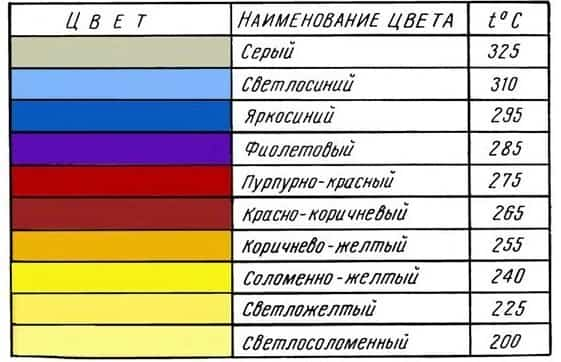
Шкала цветов побежалости стали
Окрас углеродистых деталей при соответствующих температурах указан в следующей шкале цветов побежалости стали:
| Окрас | Пределы температур, °С |
| Лимонный | 220 – 229 |
| Желтый (цвет соломы) | 230 – 245 |
| Золотой | 246 – 255 |
| Земляной или коричневый | 256 – 264 |
| Алый или красно-оранжевый | 265 — 274 |
| Пурпурный | 275 – 279 |
| Аметистовый | 280 – 289 |
| Небесный | 290 – 294 |
| Твиттера | 295 – 299 |
| Индиго Крайола | 300 – 309 |
| Светло-голубой | 310 – 329 |
| Аквамариновый | 320 — 339 |
На заготовках из нержавеющей стали12Х18Н10Т, содержащей 18% хрома, 10% никеля и 1% титана (значения определены в ГОСТ 5632-2014), цвета побежалости образуются при иных температурах.
Это обусловлено тем, что данный материал коррозийно-стойкий и жаропрочный.
Поэтому при закалке и охлаждении мельчайшие частицы металлов и кислорода взаимодействуют медленнее, что препятствует образования оксидной пленки во время закалки и каления.
В следующей таблице цветов побежалости представлены особенности изменения цвета изделий из нержавеющей стали:
| Окрас | Пределы температур,°С |
| Светло-соломенный | 300 – 399 |
| Золотистый | 400 – 499 |
| Земляной или коричневый | 500 – 599 |
| Красный или пурпурный | 600 – 699 |
| Синий или черный | 700 – 779 |

На поверхностях заготовок из нержавеющей стали могут появиться радужные полосы. Они могут появиться при нагревании изделия до температуры кипения (100 °С). Появление радужных следов обусловлено изменениями в кристаллической решетке металла. Радужный окрас на поверхности обрабатываемой заготовки не свидетельствуют о перегреве нержавеющей стали.
Коррозия алюминия, меди и латуни – изучаем причины и защитыные меры
В целом этот процесс проявляется как разрушение материала в результате его взаимодействия с внешней средой. Причем ему подвержены как металлы, так и неметаллы (керамика, дерево, полимеры и т. д.). Сюда же мы можем отнести и старение резины, и разрушение пластика. Что же насчет металлических сплавов, так в этом случае наиболее явным примером коррозии является всем известная ржавчина.
Основной причиной данного явления служит недостаточная термодинамическая устойчивость того либо иного материала к каким-либо веществам, которые мы можем обнаружить в контактирующей среде.
Так, например, резиновые покрытия портятся из-за взаимодействия с кислородом, полимеры разрушаются после многочисленных контактов с атмосферными осадками, а на большинство металлов и их сплавов губительно влияет чрезмерная влажность.
Кроме того, значительно на скорость протекания процесса влияет и температура окружающей среды, в основном, чем данный параметр выше, тем скорее осуществляется разрушение.
Вообще коррозия алюминия и многих его сплавов встречается достаточно редко, а все благодаря особенностям данного металла – он способен пассивироваться в различных агрессивных средах.
Другими словами, он переходит в пассивное состояние, так, например, при взаимодействии с воздухом на его поверхности образуется оксидная пленка, выполняющая защитные функции.
Причем в зависимости от условий толщина пассивного слоя может быть различной.
Также пленка устойчива и к воздействию влаги, а вот в кислой среде нет однозначного ответа, тут все зависит от вида кислоты.
Таким образом, изделия из алюминия практически не боятся ни азотной, ни уксусной (при нормальной температуре), а вот щавелевая, серная, муравьиная и соляная губительно влияют на металл.
Но особенно этот материал боится щелочной среды, так как при воздействии данного вещества разрушается оксидная пленка алюминия.
Теперь рассмотрим, в каких случаях встречается коррозия меди и содержащих ее сплавов. Этот металл разрушается при взаимодействии с серой и разными ее соединениями.
Также она боится окислительных и некоторых аэрированных неокислительных кислот, солей и тяжелых металлов.
Что же насчет водной среды, так в этом случае все зависит от того, насколько она насыщена кислородом, чем его содержание больше, тем скорее происходит разрушение.
Признаки коррозии латуни выражаются в основном в растрескивании (во влажной среде интенсивность повышается) и обесцинковании этого сплава, последнему же способствуют растворы, которые содержат ионы хлора.
Также происходят данные процессы при взаимодействии материала с аммиаком, растворами различных кислот-окислителей и солей. Кроме того, губительными для латуни являются ртуть, оксиды азота, трехвалентное железо и медь.
Еще одной причиной растрескивания могут послужить растягивающие напряжения.
Итак, немного узнав об особенностях разрушения цветных металлов, стоит уделить внимание вопросу, как остановить нежелательную коррозию алюминия, его сплавов и иных выше описываемых материалов. Безусловно, лучшим вариантом будет предупредить ее, но для этого необходимо знать некоторые нюансы.
Так, например, максимальной коррозионной стойкостью обладает сверхчистый алюминий, еще для работы с ним и его сплавами следует подбирать наиболее подходящую среду.
Кроме того, защита может осуществляться и такими способами, как создание на поверхности изделия лакокрасочного покрытия, металлизация, шлифовка либо дробеструйная обработка, вследствие которых возникают остаточные напряжения сжатия.
Если же металл уже поражен, тогда нужно хорошенько очистить поврежденные участки и обработать их специальными антикоррозионными растворами, купить которые можно довольно легко практически на любом строительном рынке.
Что же насчет изделий из меди и ее сплавов, так и в этом случае меры борьбы практически такие же, как и в случае с алюминием. Условия эксплуатации, а именно pH среды, тут менее значимы, разрушение будет все равно в ощутимой степени.
Действительно, произошла ли коррозия меди в сильно кислой среде или же какой-то другой, в любом случае элемент нуждается в тщательной очистке. Затем наносится защита, в качестве которой может выступать краска, лак, масло или же иной металл, такой как олово и алюминий.
Метод, когда поверхность покрывают тонким слоем расплавленного олова, называется лужение.
Дабы предотвратить коррозию латуни в результате обесцинкования, в ее состав добавляют немного мышьяка, этот процесс называется легированием. Нейтрализовать же действие аммиака способны кислотные оксиды, однако с ними также нельзя переусердствовать.
Кроме того, если речь идет об изготовлении латунных труб и иных изделий, то следует отказаться от таких операций, как безоправочное волочение, а также сборка с «натягом», дабы избежать возникновения растягивающих напряжений. Таким можно представить краткое руководство по защите от коррозии алюминия, латуни, меди и их сплавов.
Конечно, особенностей невероятное множество, но об этом лучше поговорить в отдельных статьях.
«Рыжая чума», или что мы знаем о ржавчине и коррозии — KROWN на DRIVE2
Пожалуй, каждый автомобилист согласится с тем, что именно ржавчина – одна из самых неприятных проблем, способных омрачить настроение любого автовладельца. Казалось бы, ещё вчера машина радовала взгляд безупречным глянцем лакокрасочного покрытия и вдруг – по кузову полезли «жуки», появились рыжие пятна.
На первых порах ничего, кроме эстетического неудовольствия автовладельца, ржавчина под собой не подразумевает. Да и сквозные дыры в крыльях или дверях автомобиля, возникающие в запущенных случаях, неприятны, но, практически неопасны. А вот когда процесс глубоко поразил детали силового каркаса кузова или подвеску машины, последствия могут быть весьма печальными.
«Страшилки» про сложившиеся при ДТП «домиком» кузова старых автомобилей – как раз из этой «оперы».

Полный размер
ДТП «Домиком»
Да что там машины! Ржавчина является одной из главных причин аварий таких титанических железных конструкций, как мосты. Так, 28 июня 1983 года в США произошла катастрофа с мостом через реку Мианус (Mianus). В результате падения в воду с высоты 21 метра двух автомобилей и двух тракторных прицепов погибли 3 человека и ещё 3 были серьёзно травмированы.

Участок межштатного 95-го моста длиной 100 футов через реку Мианус в Гринвиче, Коннектикут, рухнул 29 июня 1983 года. Фотография Боба Чайлда
Согласно заключению комиссии Национального совета по безопасности на транспорте, разрушение было вызвано механической поломкой наружного кронштейна, удерживающего пролёт моста, и его обоих штифтов («пальцев»). Ржавчина образовалась в подшипнике «пальца» кронштейна.
Ее объем всегда превышает объем исходной металлической детали, что приводит к неравномерному сопряжению друг с другом деталей конструкции. В случае с данным мостом, масса ржавчины отодвинула внутренний кронштейн от конца штифта, скрепляющего между собой наружный и внутренний кронштейны.
(При этом возникло усилие, превышающее допустимые проектом пределы для зажимов, удерживающих эти «пальцы»!) В результате вся масса пролета переместилась на внешний кронштейн. Такая непредвиденная нагрузка на него вызвала усталостную трещину в «пальце».
Когда два тяжелых грузовика въехали в данную секцию моста, штифты окончательно разрушились, и пролет упал в реку…

Полный размер
Вид снизу после обрушения моста через реку Мианус в США
И этот случай неединичный – 15 декабря 1967 года неожиданно рухнул в реку Огайо (Ohio) «Серебряный мост» («Silver Bridge»), соединяющий штат Западная Вирджиния (West Virginia) и штат Огайо. В момент крушения вместе с мостом в реку более чем со 100-метровой высоты упал 31 автомобиль. В результате катастрофы 46 человек погибли, и 9 получили серьёзные ранения.
Кроме того, был разрушен основной путь для транспортного сообщения между Западной Вирджинией и Огайо. Обрушение произошло из-за дефекта, возникшего в проушине № 330 одного из звеньев стержневой подвески моста. Небольшая по глубине трещина образовалась из-за фреттинг-коррозии в подшипнике.
В дальнейшем она увеличилась из-за внутренней коррозии, проблемы, известной инженерам, как коррозионное растрескивание под напряжением…
Вообще, процесс коррозии и образования ржавчины сопровождает нас с незапамятных времён. Одновременно с открытием железа и началом железного века человечество столкнулось и с возникновением ржавчины на создаваемых им орудиях труда и предметах быта.
Что такое ржавчина?
Что же такое ржавчина? В обычной жизни этим словом обозначают красные оксиды железа, образующимся в ходе его реакции с кислородом в присутствии воды или влажного воздуха.
При наличии кислорода, воды и неограниченного времени любое количество железа, в конце концов, полностью разрушается, превратившись в ржавчину.
Физически она представляет собой рыхлый порошок светло-коричневого цвета.

Полный размер
Фотография ржавчины
Процесс превращения железа в ржавчину называется коррозией – самопроизвольным разрушением металлов и их сплавов в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой. Разрушение металлов и сплавов по физическим причинам не является коррозией, а характеризуется терминами «истирание» и «износ».
С точки зрения химии коррозия металлов чаще представляет собой процесс их окисления и превращения в оксиды. Ржавление железа – также химическая коррозия. В виде упрощенных уравнений она может быть описана так:
4Fe + 3O2 + 2H2O = 2Fe2O3⋅H2O или 4Fe + 3O2 + 6H2O = 4Fe(OH)3
Т.о. ржавчина состоит из гидратированного оксида железа (III) Fe2O3⋅H2O, гидроксида железа (III) Fe(OH)3 и метагидроксида железа FeO(OH).
Интересно, что ржавчиной, как правило, называют продукты коррозии железа и его сплавов, (например, стали), хотя на самом деле целый ряд металлов также подвергается коррозии.
Однако, многие металлы (Cu, Ti, Zn, Cr, Al и др.) при коррозии покрываются плотной, хорошо скрепленной с ними оксидной пленкой (слой пассивации). Он не позволяет кислороду воздуха и воде проникнуть в более глубокие слои металла и потому предохраняет его от дальнейшего окисления (коррозии).
Взять, к примеру, алюминий – в химическом отношении это очень активный металл, хорошо реагирующий с водой с бурным выделением газа водорода:
2Al + 3H2O = Al2O3+ 3H2 ↑
Но, по причине той же высокой активности, чистый алюминий также хорошо реагирует и с кислородом воздуха. В результате этого взаимодействия поверхность металла покрывается прочной плотной плёнкой оксида Al2O3.
Оксидная плёнка защищает алюминий от дальнейшего взаимодействия с водой и кислородом. Именно по этой причине нагреваемая в алюминиевой кастрюльке вода хоть и кипит, но не вступает в реакцию с металлом.
(Потому такая посуда может служить длительное время.)

Как ни странно, химически чистое железо относительно устойчиво к воздействию чистой воды и сухого кислорода. Как и у алюминия, плотно скреплённое с поверхностью металла оксидное покрытие защищает основную массу железа от дальнейшего окисления.
Однако, надо отметить, что химически чистое железо в своей деятельности человечество практически не применяет. На практике наша цивилизация использует сталь и чугун – сплавы железа с углеродом (и другими химическими элементами), содержащие не менее 45% железа.
В реальной жизни в воздухе наших городов содержатся оксиды серы, азота, углерода и ряд других; а в воде – растворённые газы и соли.
Поэтому процесс коррозии металлов и его продукты зачастую выглядят не так просто, как в учебнике химии за 9 класс.
Так, бронзовые статуи, корродируя, покрываются слоем хорошо знакомой нам зелёной патины, представляющей собой с точки зрения химии не гидроксид, а основной сульфат меди (II) (CuOH)2SO4.
В отличие от оксида алюминия и появляющейся на бронзовой (медной) поверхности патины, ржавчина, образующаяся на сплавах железа, не создаёт никакой защиты для нижележащего металла.
Усугубляет ситуацию с коррозией железа содержание неметаллических примесей в его сплавах. Например, наличие серы в сплаве лишь способствует развитию ржавчины.
Обычно она присутствует, как сульфид FeS, но может быть и в виде других химических соединений.
В процессе коррозии сульфид железа разлагается с выделением газа сероводорода (H2S), который сам по себе является хорошим катализатором дальнейшей коррозии железа:
FeS + 2HCl = H2S ↑+ FeCl2
Нас удивляет хорошая сохранность (а значит, устойчивость к коррозии) ряда железных предметов, дошедших из глубины веков до наших дней. Одна из причин этого – низкое содержание в них серы.
В сплавы железа сера обычно попадает из каменноугольного кокса при выплавке железа из руды в доменной печи.
А вот в древние времена для производства этого металла использовался не каменный, а, практически не содержащий серы, древесный уголь…
По выраженности поражения различают сплошную и местную коррозию металлов. Как ни странно, но сплошная коррозия не представляет большой опасности для металлических конструкций и агрегатов.
Считается, что она предсказуема, а ее последствия могут быть относительно легко смоделированы.
Поэтому при проектировании металлоконструкций, эксплуатирующихся в водной среде или под открытым небом, в соответствии с технически обоснованными нормами, учитываются и будущие потери металла на коррозию.
Усугубляющие факторы
А вот местная коррозия гораздо опаснее, несмотря на то, что потери металла из-за неё могут быть вполне небольшими. Один из самых опасных видов местной коррозии – точечная.
Ведь снижая прочность на отдельных участках, она значительно уменьшает общую надёжность конструкций, сооружений и агрегатов.
Суть её заключается в формировании сквозных поражений деталей – образовании в них точечных полостей, называемых питтингами.
Развитию местной коррозии очень способствуют морская вода и растворы солей, в частности хлориды (особенно хлорид натрия – NaCl). Во многих странах его используют для плавления снега и льда, разбрасывая зимой на дорогах и тротуарах. В присутствии NaCl лёд и снег превращаются в воду, с дальнейшим образованием соляных растворов.
При этом не учитывается, что соли (и особенно хлориды) являются активаторами коррозии! Отлично диссоциируя в воде и взаимодействуя с образующейся из-за выбросов предприятий серной кислотой, хлориды образуют соляную кислоту (HCl).
А ведь она сама по себе является триггером коррозии! (Вспомним приведенную выше реакцию с входящим в состав стали сульфидом железа.
) Какие ещё нужны доказательства, что зимняя соляная «каша» приводит к ускоренному разрушению металла деталей, узлов и агрегатов транспортных средств?
Экономические потери от коррозии металлов
Экономические потери от коррозии металлов огромны. Современная цивилизация тратит значительные материальные и финансовые ресурсы на борьбу с коррозией трубопроводов, мостов и морских конструкций, судов, деталей машин, а также различного технологического оборудования.
Как уже говорилось, из-за планирования возможной коррозии приходится завышать прочность таких важных и нагруженных узлов и агрегатов, как паровые котлы, реакторы, лопатки и роторы турбин, опоры морских буровых платформ. Это автоматически увеличивает расход металла на их изготовление, а, значит, приводит к дополнительным экономическим затратам.
За два века работы металлургической промышленности в мире было выплавлено огромное количество металла. При этом, потери на коррозию составляют около 30% от его годового мирового производства! Более того – около 10% подвергшегося коррозии металла безвозвратно теряется в виде ржавчины.
По оценкам ряда экспертов, ущерб от коррозии металлов бюджету промышленно развитых стран составляет от 2 до 4 % их валового национального продукта. Так, по данным Национальной ассоциации инженеров-коррозионистов (National Association of Corrosion Engineers – NACE) в США потери от коррозии и затраты на борьбу с ней составляют 3,1 % ВВП. Для Германии это обходится в 2,8 % от ВВП.
P.S. Казалось бы, проблемы коррозии автомобильных кузовов, узлов и агрегатов меркнут на фоне вопросов защиты от коррозии таких грандиозных железных сооружений, как мосты и Эйфелева башня. Но, это только на первый взгляд.
А если учесть численность мирового автопарка? Так, по данным Международной ассоциации автопроизводителей (OICA), в 2015 году в мире эксплуатировалось 947 млн. легковых и 335 млн. коммерческих автомобилей.
Ожидается, что к 2035 году мировой автопарк достигнет 2-миллиардной отметки.
При этом, коррозией в той или иной степени, рано или поздно поражается практически 100% транспортных средств. Кроме того, надо учесть, что кузов – самая дорогая деталь автомобиля, а кузовные работы (и слесарные, и малярные) достаточно материалоёмкие и очень недешёвые.
Поэтому, проблема изыскания новых и совершенствование старых способов защиты от коррозии актуальна, как для всей тяжёлой промышленности в целом, так и для автомобильной отрасли в частности.
___________KROWN — ЗА НАМИ НЕ ЗАРЖАВЕЕТЦентр антикоррозийной защиты автомобилей
БЕЛАРУСЬ www.krown.byМинск +375 44 504-77-77
+375 (44) 504-504-1 – Солигорск
РОССИЯ www.krown.su+7 (499) 647-57-67 — Москва+7 (812) 244-98-28 — Санкт-Петербург+7 (423) 279-99-17 — Владивосток+7 (452) 39-53-28 — Саратов
+7 (3452) 564 118 — Тюмень
Коррозия цветных металлов
- Рассмотрим характеристики некоторых чистых металлов и их сплавов. С целью предупреждения коррозии цветных металлов необходимо руководствоваться следующими основными положениями:
- — не применять вместе различные материалы, поскольку возможно интенсивное развитие коррозии в результате образования макроэлементов;
- — не допускать чрезмерно высокого нагрева металлических деталей, находящихся в контакте с водой, так как это может вызвать интенсивную коррозию в результате образования пар дифференциальной аэрации; нежелательны также местные изменения температуры;
- — стараться избегать образования застойных зон, в которых происходит снижение концентрации кислорода в воде, так как это может привести к разрушению пассивирующей пленки и растворению токсичных металлов (Pb, Cu).
Коррозия алюминия
Этот металл, имеющий высокий отрицательный потенциал (—1,34 В), теоретически очень подвержен коррозии, но в действительности пассивируется в результате окисления влажным воздухом и образования защитной пленки оксида алюминия. Эту пассивацию можно вызвать искусственно анодным окислением.

Алюминий иногда применяют в морской воде при условии, что, во-первых, на нем не образуются отложения загрязнений, что приводит к возникновению катодных участков, и, во-вторых, применяется технически чистый алюминий. Алюминий можно использовать в слабо кислых водах, но его контакт со щелочными водами недопустим.
Коррозия меди
В воде, содержащей кислород, происходит естественная пассивация меди пленкой оксида меди CuO, которая имеет малую растворимость, но на практике может подвергаться сольватации в виде комплекса аммиаком или цианидами. Тем не менее эта окисная пленка в отличие от пленки, образующейся на алюминии, часто оказывается пористой, и поэтому при производстве и применении медных труб должны быть приняты меры предосторожности.

Сквозные изъязвления и питтинговая коррозия меди иногда наблюдаются в холодных минерализованных водах (питтинг типа I) и при использовании отожженных труб. Те же явления происходят в горячей воде с низким солесодержанием (питтинг типа II).
Коррозия свинца
Оксид свинца РЬО и гидроксид свинца РЬ(ОН)2 относительно растворимы.
Поэтому все воды, содержащие кислород, очень коррозионны и опасны для свинца, кроме вод, которые одновременно имеют высокую бикарбонатную щелочность (выше 2,4 мг*экв/л) и малое содержание свободного диоксида углерода (pH немного выше 7).
В этом случае может образовываться гидроксикарбонат, который характеризуется значительно меньшей растворимостью, чем гидроксид и, следовательно, защищает металл, если одновременно происходит осаждение карбоната кальция.
Однако в настоящее время рекомендуется ограничивать применение свинцовых труб для питьевого водоснабжения; и оно должно быть полностью исключено для мягкой воды.
Коррозия оцинкованной стали
Рассмотрим покрытия, полученные или электроосаждением цинка, или горячим цинкованием (погружением в ванну с цинком при температуре 450 °С или непрерывным процессом Sendzimir).
В этом случае слой n-фазы переменной толщины прочно связан со сталью, а его внешняя поверхность окисляется с образованием гидроксида цинка, оксида или гидроксикарбоната в зависимости от температуры и щелочности воды.
Пленка имеет очень сложную структуру и замедляет коррозию цинка торможением диффузии кислорода. Скорость коррозии, которая велика в мягкой воде, значительно уменьшается в водах, содержащих бикарбонат кальция.

- Значительные концентрации хлоридов, особенно в щелочной среде, могут вызывать осаждение нерастворимых оксихлоридов, что одновременно увеличивает вероятность питтинговой коррозии.
- Защитная пленка имеет более низкую электрическую проводимость, чем пленка, образующаяся на других металлах, и не изменяет потенциал цинка, поэтому действует скорее как лакокрасочное покрытие или растворимый анод, чем как пассивирующая пленка.
- При высокой коррозионной активности воды и разрушении пленки цинк, который имеет высокий отрицательный потенциал (—0,776 В), подвергается ускоренной коррозии, заканчивающейся коррозией железа с образованием ржавчины.
Влияние температуры. Скорость коррозии резко возрастает с повышением температуры, достигает максимума при 60 °С и затем снижается до начального значения при 100 °С.
При 60 °С все гидроксиды цинка превращаются в более пористый оксид, который имеет плохую адгезию с металлом и образует пленку с более положительным потенциалом, чем потенциал цинка.
В результате полярность элемента «защитная пленка — железо» изменяется на противоположную. Это вызывает ускоренную сквозную коррозию незащищенной поверхности стали.
Действие меди. Появление ионов Cu2+ в растворе (экзогенная медь, попавшая в воду в систему выше по течению) повышает электрическую проводимость пленки оксида цинка и в результате скорость коррозии стали возрастает.
Поэтому цинкование стали обеспечивает устойчивое замедление коррозии только в воде с низкой коррозионной активностью.
При использовании оцинкованных труб в воде с высокой коррозионной активностью, и особенно в морской воде, следует иметь в виду временный характер защиты, которую обеспечивает цинкование.
Коррозия латуни
Латуни — это медно-цинковые со следующими стандартными составами):
| Состав | Содержание, % | |||
| меди | цинка | алюминия | олова | |
| I | 70 | 29 | — | 1 |
| II | 60 | 40 | — | — |
| III | 76 | 22 | 2 | — |
Состав III рекомендуется использовать в морской воде.

Обесцинкование или растворение цинка с выделением остаточной Cu иногда происходит в латуни типа I и реже в других. Металл становится пористым и хрупким.
Обесцинкование усиливается в присутствии солей и вызывает образование элементов, в которых латунь служит анодом, что приводит к быстрому разрушению сплава, которое может быть предотвращено наличием в сплаве мышьяка или сурьмы.
В настоящее время имеются сорта латуни, применение которых позволяет решить эту проблему.






